TROMBOSIS VENOSA 18 PROFUNDA · Aníbal Enrique Badel Rodríguez, MD Diego Velásquez Meisel, MD...
Transcript of TROMBOSIS VENOSA 18 PROFUNDA · Aníbal Enrique Badel Rodríguez, MD Diego Velásquez Meisel, MD...
Aníbal Enrique Badel Rodríguez, MDDiego Velásquez Meisel, MD
181818TROMBOSIS VENOSA PROFUNDA
Introducción
La trombosis venosa profunda (TVP) representa una causa importante y en algunos casos prevenible de mortalidad y morbilidad cardiovascu-lar. En 1835, Rudolf Virchow describió la tríada de estasis, daño vascu-lar e hipercoagulabilidad y su relación con el desarrollo de trombosis venosa. Desde entonces, ha sido largo el camino recorrido para lograr entender, diagnosticar y tratar a esta entidad.
Epidemiología
Se estima que un 0,1% de la población mundial es afectado anualmente por una TVP, con una tasa anual ajustada por edad y género de 117/100 000 habitantes/año. Hay una clara relación con la edad, de modo que es más frecuente en los mayores de 65 años e infrecuente en niños. Hay una tendencia a un mayor compromiso del sexo masculino (130/100 000 habitantes/año vs. 110/100 000 habitantes/año). Si bien la TVP está descrita en todas las etnias, hay predominio en la raza negra, con una tendencia mayor de recurrencias en población hispana y caucásica.
Patogénesis
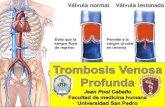
La formación de un trombo venoso en el sistema profundo está infl uen-ciada por los elementos de la tríada de Virchow, que establece una pér-dida en el balance normal de los mecanismos anticoagulantes y procoa-gulantes. Los factores de riesgo de TVP (Tabla 1) afectan a uno o más de los elementos de esta tríada. Es probable que este proceso se inicie en un porcentaje importante de casos en los recesos de las válvulas veno-sas de la pantorrilla y posteriormente se extienda de manera proximal. Si no se hace un adecuado diagnóstico y tratamiento, esta patología es potencialmente responsable de diferentes complicaciones como son el
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
398
tromboembolismo pulmonar (TEP), la TVP recurrente y el síndrome postrombótico. El TEP es la complicación más frecuente de la TVP y usualmente es secundario a TVP de las extremidades inferiores. La mor-talidad por TVP al primer mes del diagnóstico es de aproximadamente 9,4%. De un 40% a un 50% de los pacientes con TVP puede tener episo-dios silentes de TEP. Un diagnóstico y tratamiento adecuados de la TVP son importantes para lograr disminuir la mortalidad a <6%.
Tabla 1. Factores de riesgo para TVP
Factores de riesgo genéticos
Deficiencia de antitrombina, proteínas C y S
Factor V de Leiden
Mutación del gen de protrombina 20210A
Disfibrogenemia
Elevación de los factores VIII, IX y XI de la coagulación
Hiperhomocisteinemia
Factores de riesgo adquiridos
Edad mayor de 65 años y más aún >75 años
Cáncer
Síndrome antifosfolípidos
Infecciones (VIH, sepsis, entre otras)
Enfermedades inflamatorias (LES, enfermedad inflamatoria intestinal, vasculitis, entre otras)
Síndrome nefrótico
Obesidad
Tabaquismo
Factores de riesgo ambientales
Cirugía
Trauma
Inmovilización >48 horas
Presencia de catéteres venosos centrales
Embarazo y posparto
Tratamiento hormonal (contraceptivos orales, transcutáneos, inyecciones de depósito de progestágenos, reemplazo hormonal, entre otros)
Quimioterapia
Viajes prolongados (>8 horas de duración)
LES: lupus eritematoso sistémico; VIH: virus de la inmunodeficiencia humana.
399
18 · TROMBOSIS VENOSA PROFUNDA
Trombosis venosa profunda de miembros inferiores: clasificación
Tradicionalmente se habla de TVP:• Distal o aislada distal: compromiso infrapoplíteo (alta relación con
eventos quirúrgicos).• Proximal: compromiso poplíteo, femoral y/o ilíaco, con o sin com-
promiso de la vena cava inferior (VCI).
La TVP proximal es la más frecuente y corresponde aproximadamente al 84% de las TVP. La TVP aislada distal representa el 16% restante.
Adicionalmente, la enfermedad tromboembólica venosa (VTE), que incluye a la TVP y al TEP, se clasifi ca según el riesgo de recurrencias en varias fases de tratamiento luego del diagnóstico inicial así: una “fase aguda” o inicial que abarca los primeros 7 días a partir del diagnóstico y corresponde al período en que los pacientes históricamente han sido manejados con terapia parenteral; desde el día 7 hasta los 3 meses, se aplica el término de tratamiento “a largo plazo”; luego de los 3 meses comienza la “fase extendida” del tratamiento, donde la evaluación de la relación riesgo/benefi cio de continuar la anticoagulación (riesgo de recurrencia del tromboembolismo venoso (TEV) vs. riesgo de compli-caciones hemorrágicas) es crítica, y la continuidad del tratamiento se justifi ca principalmente en grupos de pacientes con un riesgo muy alto de recurrencias, como los que padecen de cáncer o episodios repetitivos de la enfermedad. Ulteriormente es importante revaluar periódicamen-te (por ejemplo, cada año) si se continúa el tratamiento con base en la relación riesgo/benefi cio.
La detección del compromiso venoso proximal de miembros inferio-res (TVP iliofemoral) es importante, ya que sus implicaciones pronós-ticas son diferentes debido a un incremento signifi cativo del riesgo de recurrencias y de la incidencia de síndrome postrombótico.
Factores de riesgo para TVP
El análisis de cada caso de TVP permite identifi car al menos uno de los tres elementos de la tríada de Virchow en un 96% de los casos. Los dos elementos principales, en la gran mayoría de los casos, son el daño vas-cular y la estasis, y la hipercoagulabilidad adquiere mayor importancia en los casos de TVP idiopática. Los factores de riesgo para TVP se clasifi -can en genéticos, adquiridos y ambientales (Tabla 1). Los factores genéticos tienen distinta fuerza de asociación con la TVP:• Fuerte: defi ciencia de antitrombina, défi cit de proteína C y S.• Moderada: factor V de Leiden, mutación de la protrombina 20210A.• Débil: variantes del fi brinógeno y de los factores XIII y XI.
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
400
Evaluación clínica
Clásicamente la TVP se manifiesta con eritema, dolor, calor y/o edema en la extremidad afectada. El dolor asociado con la TVP suele ser descrito como un calambre o dolor en la pantorrilla o el muslo y se puede o no encontrar un signo de Homans (dolor en la pantorrilla con la dorsiflexión del pie). En ocasiones se puede hacer evidente la presencia de circula-ción venosa colateral o un cordón venoso palpable. Sin embargo, no es infrecuente que la presentación clínica sea muy insidiosa e inespecífica. La severidad de la presentación estará afectada por el nivel y el grado de oclusión venosa. Aunque la sensibilidad y especificidad de los síntomas y signos clínicos es baja, lo que puede dificultar la evaluación inicial, la pre-sencia de factores de riesgo para el desarrollo de la misma es una herra-mienta fundamental a tener en cuenta cuando se sospecha la enfermedad.
Diagnóstico diferencial
Los signos y síntomas de TVP con cierta frecuencia son compartidos por otras entidades clínicas, como la insuficiencia venosa crónica, el linfede-ma, la tromboflebitis superficial, la celulitis, las patologías musculares, el quiste (poplíteo) de Baker y los hematomas, entre otras. En promedio, la prevalencia de trombosis confirmada en pacientes con sospecha de TVP es del 19%, en un rango que va desde un 5% en pacientes con baja probabilidad preprueba, hasta un 53% en pacientes con una alta proba-bilidad preprueba.
Determinación de la probabilidad preprueba de TVP
En la evaluación clínica se utilizan distintos puntajes y reglas clínicas que permiten una aproximación efectiva al paciente con sospecha de TVP; de estos, los criterios de Wells son los más utilizados (Tabla 2). En el estudio inicial de Wells, se definieron características de riesgo que permitían clasificar al paciente como de riesgo bajo (0 puntos, 3% de probabilidad de TVP), medio (1-2 puntos, 17% de probabilidad de TVP) y alto (3 o más puntos, 75% de probabilidad de TVP). Al puntaje originalmente creado en 1995 se le añadió ulteriormente el criterio de antecedente de TVP previa, con la intención de mejorar su sensibilidad. El modelo de Wells no es aplicable en embarazadas, en anticoagulados, en presencia de síntomas de más de 60 días de duración, en sospecha de TEP y en pacientes con una pierna amputada.
401
18 · TROMBOSIS VENOSA PROFUNDA
Tabla 2. Puntaje de Wells para TVP
Elemento clínico Puntaje
Cáncer activo o tratamiento para cáncer en los últimos 6 meses 1
Parálisis o paresia o inmovilización con yeso reciente de un miembro inferior
1
Reposo en cama reciente de más de 3 días o cirugía mayor en las últimas 12 semanas
1
Tumefacción localizada a lo largo del recorrido del sistema venoso profundo de la extremidad inferior
1
Edema de toda la pierna 1
Aumento del perímetro de la extremidad afecta >3 cm respecto a la asintomática (medido 10 cm bajo la tuberosidad tibial)
1
Edema con fóvea en la extremidad sintomática 1
Presencia de circulación venosa colateral superficial (no várices preexistentes)
1
Documentación previa de TVP 1
Diagnóstico alternativo al menos tan probable como la TVP -2
TVP: trombosis venosa profunda.Probabilidad alta: 3 o más puntos; probabilidad moderada: 1 o 2 puntos; probabilidad baja: 0 puntos-
Pruebas diagnósticas complementarias
Dímero D
El dímero D es un producto de degradación de la fi brina que se libe-ra en el torrente sanguíneo cuando la fi brina es lisada por la plasmina. Típicamente está elevado en los pacientes con TEV, aunque también se aumenta en otras condiciones (cáncer, coagulación intravascular dise-minada, infección, embarazo, edad avanzada, postoperatorio temprano, fi brilación atrial, enfermedad cerebrovascular, entre otras), de modo que es una prueba muy sensible, pero poco específi ca. Esto se traduce en que un resultado negativo excluye casi por completo un TEV (valor predicti-vo negativo [VPN] del 98%), aunque un dímero D positivo no es diagnós-tico, principalmente si coexisten otras condiciones que puedan elevarlo. Hay varios métodos de laboratorio para la cuantifi cación del dímero D: los de alta sensibilidad (93%-94%) son menos específi cos (ELISA, látex cuantitativo o inmunoturbidimetría) y los de sensibilidad intermedia (71%) (aglutinación de glóbulos rojos de sangre entera o látex semi-cuantitativo), que son más específi cos para el diagnóstico del TEV. La variabilidad de la prueba de laboratorio implica que el resultado del examen debe ser interpretado en el contexto del tipo de sensibilidad de la prueba y de la probabilidad preprueba por puntaje de Wells. De esta
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
402
forma, un resultado negativo que utiliza una prueba de sensibilidad moderada puede ser suficiente para descartar con bastante certeza una TVP en un paciente con una probabilidad preprueba baja; sin embargo, un paciente con probabilidad preprueba moderada necesita al menos un dímero D negativo de alta sensibilidad para completar de manera segura el algoritmo diagnóstico sin necesidad de un estudio de imagen. Por otra parte, no hay suficiente evidencia para apoyar la seguridad de utilizar solamente el dímero D para descartar TVP en pacientes de alto riesgo. El punto de corte tradicional para el dímero D es mayor de 500 µg/L FEU (equivalente en unidades de fibrinógeno) para que la prueba sea positiva. Estudios recientes sugieren ajustar el umbral del dímero D en los pacientes mayores de 50 años de edad, en quienes se recomienda multiplicar la edad del paciente por 10 y el resultado tomarlo como um-bral para positividad o negatividad.
Ultrasonido de compresión
La ultrasonografía dúplex del sistema venoso profundo proximal es la modalidad diagnóstica más utilizada para evaluar la presencia de TVP, debido a que es económica, no invasiva y segura (sin exposición a radiación ni a material de contraste). Combina la imagen en escala de grises en 2 dimensiones (modo B) con el flujo Doppler color o ima-gen espectral. La imagen se obtiene desde la trifurcación poplítea hasta la vena femoral común. La documentación de una compresión venosa anormal en modo B (normalmente la vena debe colapsarse fácilmente con la compresión), la presencia de un trombo ecogénico a nivel de la luz de la vena, la visualización de defectos de llenado con Doppler co-lor y un flujo Doppler color o flujo Doppler espectral anormales hacen el diagnóstico de TVP. El ultrasonido de compresión (USC) tiene una sensibilidad del 96,5% y una especificidad del 94% para el diagnóstico de TVP proximal. Sus limitaciones incluyen una evaluación restringida del sistema venoso profundo proximal a la vena femoral común (venas ilíacas), su incapacidad para evaluar el sistema venoso a nivel del canal de los aductores y su limitación en la evaluación del sistema venoso por debajo de la rodilla. Debido a que el riesgo de extensión proximal de una TVP aislada o infrapoplítea no diagnosticada es relativamente bajo (15%-25%), se ha recomendado repetir el estudio en 1 semana. Si a los 7 días no hay extensión proximal de la TVP, es muy poco probable que suceda subsecuentemente, y si existe una TVP aislada distal (y no se extendió), generalmente termina resolviéndose de manera espontánea. Datos recientes han encontrado que solo el 1,3% de las TVP aisladas dis-tales se propaga proximalmente en el USC repetido en el seguimiento, de manera que si se utiliza adecuadamente la estratificación de riesgo con la escala de Wells y el dímero D, en algunos casos se puede omitir el
403
18 · TROMBOSIS VENOSA PROFUNDA
USC de control a la semana. El ultrasonido de toda la extremidad puede realizarse como un estudio complementario al USC, con la intención de buscar TVP aislada o distal. Sin embargo, la sensibilidad de este estudio para el diagnóstico de TVP distal es de solo un 63%; adicionalmente, esto incrementa la complejidad técnica y el tiempo del examen y fre-cuentemente se puede terminar dando sobretratamiento a una trombo-sis aislada que en la mayoría de las veces no hubiera presentado exten-sión proximal. De hecho, varios estudios que han comparado el USC con el ultrasonido de la extremidad entera han demostrado que ambas estrategias tienen una incidencia similar de VTE a 3 meses.
Venografía por tomografía axial computarizada
La venografía por tomografía axial computarizada (TAC) comparte con la venografía invasiva la necesidad del uso de medio de contraste y la exposición a radiación ionizante. Sin embargo, no requiere la canulación de una vena dorsal del pie (las inyecciones se ponen en el brazo), y en el mismo estudio se puede evaluar la circulación pulmonar, para defi nir la presencia de embolia pulmonar, además de valorar la presencia de trombosis pélvica o ilíaca. Este estudio tiene una sensibilidad y una es-pecifi cidad cercanas al 95% para el diagnóstico de TVP. De esta manera, es una alternativa principalmente en pacientes en los que no se logra realizar adecuadamente un USC.
Venografía por resonancia magnética nuclear
Se puede realizar una venografía por resonancia magnética nuclear (RNM) sin utilizar medio de contraste (secuencias de tiempo de vuelo o contraste de fase), aunque las mejores imágenes se obtienen utilizando gadolinio. Tiene una sensibilidad diagnóstica alta, especialmente en la pelvis, la región infrapoplítea y los miembros superiores, pero es costo-sa, requiere más tiempo para su realización y personal altamente entre-nado para su interpretación. Sin embargo, tiene la ventaja de no exponer al paciente a radiación ionizante.
Venografía invasiva
Consiste en la inyección de contraste yodado a nivel de una vena dorsal del pie, para delinear todo el sistema venoso profundo de la extremidad inferior. El diagnóstico es hecho cuando se documenta la presencia de defectos de llenado, la terminación abrupta de la columna de contraste, la ausencia de llenado del sistema venoso o la diversión del fl ujo. Esta es la prueba de referencia para el diagnóstico de TVP, y en un paciente con una prueba negativa, la probabilidad de aparición de TEV a 3 me-ses es menor del 1,3%. Sin embargo, su realización es cada día menos
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
404
frecuente puesto que implica la exposición a radiación ionizante (incre-mento del riesgo de aparición de neoplasias), la exposición a medios de contraste (limitación en pacientes con daño renal y riesgo de reacciones adversas al contraste), es invasiva (riesgo de daño vascular y de lesiones en la piel) e incrementa los costos. Por otra parte, hasta en un 20% de los casos, las imágenes no tendrán la calidad necesaria para el diagnós-tico (inadecuada visualización de un segmento venoso), en un 5% de los pacientes no se consigue el acceso venoso dorsal y actualmente el rendimiento diagnóstico del VTE ha mejorado mucho con las pruebas de imagen no invasivas, que incluyen en primera instancia el USC. Por todo lo anterior, la venografía invasiva no se considera un examen de rutina en el diagnóstico de TVP.
Enfoque diagnóstico en la TVP de extremidades inferiores
Las guías de terapia antitrombótica y prevención de la trombosis del Colegio Americano de Médicos del Tórax (ACCP) proponen el enfoque diagnóstico teniendo en cuenta que “no se debe aplicar la misma secuencia de exámenes diagnósticos en todos los pacientes y que estos deben dirigirse de acuerdo con la probabilidad preprueba” (Figura 1):
Pacientes con baja probabilidad preprueba de un primer episodio de TVP: el estudio inicial es el dímero D de alta o moderada sensibilidad, dependiendo de la disponibilidad de la institución. Si el dímero D es negativo, se descarta TVP, pero si el resultado es positivo, el siguiente estudio es un USC. Si este es normal, se descarta TVP, y si se documenta TVP, se da tratamiento.
Pacientes con probabilidad preprueba intermedia o moderada de TVP: si solo hay disponibilidad de dímero D de sensibilidad moderada, la recomendación es omitir el dímero D y pasar directamente a la reali-zación de un USC. Si hay disponibilidad de dímero D de alta sensibili-dad y el resultado es negativo, se descarta TVP, pero si el resultado es positivo, el siguiente estudio es un USC (proximal). Si el USC es positivo para TVP, el paciente va a tratamiento, pero si el resultado es negativo, el estudio se debe repetir en 1 semana. Si la modalidad de US que se escogió fue de toda la extremidad y el resultado es positivo para TVP, el paciente va a tratamiento y si el resultado fue negativo, se descarta TVP.
Pacientes con probabilidad preprueba alta de TVP: en este grupo se recomienda omitir el dímero D y realizar directamente un USC o un US de toda la extremidad. Cuando el USC proximal inicial es negativo, se recomienda repetirlo en 1 semana, pero si es positivo, se debe dar trata-miento. Si se realizó US de toda la extremidad y el resultado es positivo para TVP, el paciente va a tratamiento; si el resultado es negativo, se descarta TVP.
405
18 · TROMBOSIS VENOSA PROFUNDA
En los casos en los que no se realizó estratifi cación del riesgo (no recomen-dado), se sugiere iniciar el estudio con un USC proximal. En caso de que sea negativo, se puede repetir el examen en 1 semana, realizar un dímero D (en ausencia de comorbilidades que lo contraindiquen) o llevar a cabo un US de toda la pierna o una venografía invasiva.
La evaluación con ecografía de todo el miembro inferior se sugiere en el pa-ciente que tendrá un seguimiento difícil (razones geográfi cas o de soporte fami-liar o social o motivos de índole personal). Permite el diagnóstico de TVP distal aislada que no se relaciona de forma importante con síndrome postrombótico o con TEP, lo que implica la posibilidad de realizar tratamiento o seguimiento según el riesgo potencial de sangrado de cada paciente.
La realización de venografía invasiva, o no invasiva por TAC o por RMN, no debe considerarse un elemento de rutina en la evaluación del paciente con TVP, y siempre deben tenerse en cuenta los riesgos y los costos frente al posible benefi cio. Cuando se decida realizar ultrasonido, se debe considerar la presen-cia de edema o de mucho tejido celular subcutáneo que difi culte la realización del examen; en esta última situación, se recomienda la venografía invasiva, por TAC o por RMN.
Recomendaciones de tratamiento de la trombosis venosa profunda de las extremidades inferiores
Una vez establecido el diagnostico de TVP, se debe defi nir la estrategia de manejo a seguir. El elemento fundamental de la misma será la anti-coagulación sistémica y se considerará en cada caso la pertinencia de otras estrategias para disminuir la carga trombótica o la posibilidad de embolia pulmonar.
Los pacientes con TVP proximal tienen indicación de manejo anticoagulante para disminuir la posibilidad de eventos embólicos, de síndrome postrombótico y de recurrencia de la TVP. El proceso de estudio de los pacientes con sospecha de TVP puede completarse usualmente en 12 a 24 horas, dependiendo de la disponibilidad de los recursos y de la complejidad de cada caso. Este tiempo de espera implica un riesgo potencial de complicaciones embólicas y de morta-lidad, especialmente en pacientes con TVP proximal o con una menor reserva cardiopulmonar, al igual que un incremento del riesgo de sangrado en los pa-cientes que se anticoagulen de forma innecesaria.
Se recomienda el inicio de un anticoagulante parenteral (de preferen-cia los esquemas de administración en infusión o subcutáneos [SC] cada 12 horas sobre los de 24 horas) en las siguientes situaciones:• Alta probabilidad preprueba de TVP, mientras se termina el estudio
de TVP.• Probabilidad intermedia de TVP, si el estudio de TVP no se termina-
rá en las 4 horas siguientes.
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
406
Dím
ero
D A
S o
MS
Dím
ero
D A
S
Dím
ero
D n
orm
alD
ímer
o D
ano
rmal
Si d
ímer
o M
S, p
roce
da U
S
Alto
Sosp
echa
de
TVP
Punt
aje
de W
ells
Mod
erad
oBa
jo
Dím
ero
D n
orm
alD
ímer
o D
ano
rmal
US
dúpl
ex
Ano
rmal
Trat
e TV
P
Nor
mal
Neg
ativ
oN
egat
ivo
Neg
ativ
oN
egat
ivo
Posi
tivo
Posi
tivo
Trat
e TV
PSi
n TV
PTr
ate
TVP
Dúp
lex
TLP
Dúp
lex
TLP
Dúp
lex
prox
imal
Dúp
lex
prox
imal
Repi
ta U
SPr
ox. 7
día
sRe
pita
US
Prox
. 7 d
ías
Sin
TVP
Sin
TVP
Om
ita
dím
ero
Dy
proc
eda
a im
agen
Figu
ra 1
. Alg
oritm
o di
agnó
stic
o de
TVP
de
extre
mid
ades
infe
riore
s.AS
: alta
sen
sibili
dad;
MS:
mod
erad
a se
nsib
ilida
d; T
LP: t
oda
la p
iern
a; T
VP: t
rom
bosis
ven
osa
prof
unda
; US:
ultr
ason
ido
407
18 · TROMBOSIS VENOSA PROFUNDA
No se recomienda iniciar anticoagulación parenteral hasta completar los estudios en:• Baja probabilidad preprueba para TVP.• Alto riesgo de sangrado (véase la Tabla 3 para los esquemas de dosi-
fi cación de los anticoagulantes parenterales).
Tabla 3. Esquemas de tratamiento de anticoagulantes parenterales en TVP
Medicamento Dosis inicial Dosis mantenimiento
HNF 80 UI/kg 18 UI/kg/h; modifique para TPT entre 50 a70 segundos
Enoxaparina 1 mg/kg/12 h 1 mg/kg/12 h o 1,5 mg/kg/24 h si la depuración de creatinina es mayor de 30 mL/min y la edad <75años1 mg/kg/24 h o 0,5 mg/kg/12 h si la depuración de creatinina es menor de 30 mL/min, independientemente de la edad0,75 mg/kg/12 h si la depuración de creatinina es mayor de 30 mL/min en edad >75 años
Dalteparina 200 UI/kg/24 h 150 UI/kg/24 h
Tinzaparina 175 UI/kg/24 h 175 UI/kg/24 h
Fondaparinux 5 mg/24 h <50 kg7,5 mg/24 h 50-100 kg10 mg/24 h >100 kg
5 mg/24 h <50 kg7,5 mg/24 h 50-100 kg10 mg/24 h >100 kg
HNF: heparina no fraccionada; TPT: tiempo parcial de tromboplastina; TVP: trombosis venosa profunda; UI: unidades internacionales.
Todos los pacientes con TVP de extremidades inferiores deben reci-bir, como mínimo, tratamiento anticoagulante de largo plazo (3 meses) con alguno de los nuevos anticoagulantes (NOAC) o también llamados anticoagulantes directos (dabigatrán, edoxabán, rivaroxabán y apixabán) o con antagonistas de la vitamina K (VKA). Se recomienda cualquiera de los NOAC sobre los VKA (grado 2B), ya que en los estudios aleato-rizados, los NOAC demostraron ser al menos igual de efectivos que los VKA, pero con menores eventos de sangrados.
En los pacientes con TVP de extremidades inferiores asociada con cáncer, el anticoagulante de primera elección son las heparinas de bajo peso molecular (HBPM) sobre los NOAC o los VKA, ya que en este es-cenario, las HBPM han demostrado menos recurrencias de eventos que otro tipo de anticoagulantes (grado 2C).
Si la TVP fue provocada por una cirugía o por un factor de riesgo tran-sitorio no quirúrgico, son sufi cientes 3 meses de tratamiento anticoagu-
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
408
lante, ya que en estos casos, dar más de 3 meses de anticoagulación au-menta los riesgos de sangrado sin beneficio en las recurrencias (grado 1B).
Si la TVP está asociada con cáncer o con un factor de riesgo no tran-sitorio o es un segundo episodio, la duración de la anticoagulación está sujeta a la evaluación del riesgo de sangrado, así: si el riesgo de sangra-do no es alto, la recomendación es dar anticoagulación indefinida, dado que el riesgo de recurrencias en estos casos es alto, con reevaluación de la justificación de la continuidad de la terapia cada cierto tiempo (al me-nos cada año). El grado de recomendación en TVP asociada con cáncer o con un factor de riesgo no transitorio es grado 2B, y para TVP recurren-te, grado 1B. Si el riesgo de sangrado es alto, se recomiendan 3 meses de terapia anticoagulante.
Las escalas de estimación del riesgo de sangrado siempre son una herra-mienta de ayuda en la toma de decisiones y para definir qué paciente tiene riesgo alto de sangrado (Tabla 4). Sin embargo, el juicio clínico prima al momento de definir qué paciente se considera con alto riesgo de sangrado o qué paciente se beneficiará de la terapia anticoagulante extendida.
Tabla 4. Estimación del riesgo de sangrado en pacientes con TVP que reciben terapia anticoagulante
Factores de riesgo
Edad mayor de 75 años
Sangrado previo
Cáncer metastásico
Falla renal o hepática
Trombocitopenia
ACV previo
Diabetes
Terapia antiplaquetaria concomitante
Cirugía reciente
Abuso de alcohol
Pobre control de la anticoagulación
Caídas frecuentes
ACV: accidente cerebrovascular.Con 2 o más factores de riesgo se considera que el paciente es de alto riesgo.
Si el anticoagulante oral escogido fue un VKA, se recomienda conti-nuar la terapia anticoagulante parenteral inicial hasta que el índice in-ternacional normalizado (INR) llegue a rangos terapéuticos (2,0 a 3,0); en este momento debe suspenderse el anticoagulante parenteral.
409
18 · TROMBOSIS VENOSA PROFUNDA
Si el anticoagulante escogido fue dabigatrán (150 mg cada 12 horas) o edoxabán (60 mg/día, a excepción de los pacientes con peso <60 kg o depuración de creatinina entre 30-50 mL/min, en quienes la dosis es de 30 mg cada 24 horas), se recomienda un período inicial (promedio de 5 días) de anticoagulación parenteral. Si el anticoagulante parenteral de inicio fue una HBPM, la primera dosis del NOAC se administra 2 horas antes de la hora a la que correspondía la siguiente dosis SC de la HBPM y se suspende la última. Si el anticoagulante parenteral de inicio fue he-parina no fraccionada (HNF), en el momento en que el paciente reciba la primera dosis del NOAC se suspende la infusión de HNF.
Si el anticoagulante oral elegido fue rivaroxabán o apixabán, no se requiere anticoagulación parenteral antes del inicio del anticoagulante oral. Si se escogió rivaroxabán los primeros 21 días, la dosis es de 15 mg c/12 horas y ulteriormente de 20 mg c /24 horas. Si se escogió apixabán, los primeros 7 días se administrarán 10 mg cada 12 horas, seguidos de 5 mg cada 12 horas.
No se recomienda cambiar el anticoagulante, a menos que la situación específi ca lo amerite.
En la TVP infrapoplítea o aislada distal, usualmente no se recomien-da la anticoagulación (grado 2C), ya que la probabilidad de extensión proximal es baja y, por ende, el riesgo de complicaciones. Usualmente estas trombosis terminan resolviéndose de forma espontánea. Sin em-bargo, se recomienda un USC de control a los 7-14 días, y en caso de do-cumentarse extensión proximal, se debe anticoagular al paciente. Solo en TVP infrapoplíteas muy sintomáticas o en presencia de factores de riesgo para extensión proximal (Tabla 5) se recomienda anticoagulación de entrada. Cuando se decide anticoagulación, se utilizarán los mismos esquemas recomendados para la TVP proximal.
Tabla 5. Factores de riesgo para extensión proximal de la TVP
Dímero D persistentemente positivo
Trombosis con cercanía al sistema venoso proximal <5 cm
Compromiso de múltiples venas
Diámetro máximo de la vena comprometida >7 mm
Longitud del trombo mayor de 5 cm
Factor desencadenante irreversible o no secundaria
Paciente hospitalizado
Cáncer activo
Antecedente de VTE
VTE: enfermedad tromboembólica venosa.A mayor número de factores de riesgo, mayor justificación para anticoagulación.
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
410
En TVP aguda con una carga trombótica muy alta, como es el caso de las TVP multisegmentarias, del compromiso extenso iliofemoral, del compromiso de la vena cava inferior o de las condiciones clínicas que impliquen un riesgo en la viabilidad de la extremidad (flegmasia alba dolens o cerúlea dolens), no es infrecuente que la anticoagulación sola no sea suficiente para resolver la trombosis y el riesgo de desarrollo de síndrome postrombótico o inclusive de pérdida de la extremidad no es despreciable. Si el riesgo de sangrado no es alto y la TVP tiene menos de 14 días, la trombólisis selectiva dirigida con catéter es recomendada en estos casos por encima de la trombólisis sistémica (grado 2C).
La trombectomía quirúrgica es una alternativa a la trombolisis dirigi-da con catéter y comparte sus indicaciones, pero por tratarse de un pro-cedimiento más invasivo, ha venido siendo reemplazada en los últimos años por el tratamiento endovascular.
La angioplastia venosa y el implante de stent están recomendados en las lesiones obstructivas ilíacas residuales luego de procedimientos de trombolisis dirigida y de trombectomía endovascular o quirúrgica.
En pacientes con TVP no provocada, que por algún motivo deciden suspender el tratamiento anticoagulante, la aspirina (siempre que no esté contraindicada) es una alternativa a no dar ningún tipo de manejo médico, aunque es muy claro que los beneficios de la terapia antiagre-gante nunca superan a los de la anticoagulación en TVP (grado 2B).
En pacientes con TVP y presencia o sospecha de trombocitopenia inducida por heparina (HIT), debe iniciarse un inhibidor directo de la trombina (grado 1B).
Dónde iniciar la terapia
Si bien no existe un estudio aleatorio controlado que resuelva esta pre-gunta, la evidencia disponible sugiere que en muchos casos no se in-crementa el riesgo de sangrado o la recurrencia de la TVP al iniciar el manejo en la casa y esto puede disminuir los costos del tratamiento de manera significativa. Se recomienda el manejo en casa sobre el manejo hospitalario, si las condiciones médicas, sociales y económicas del pa-ciente lo permiten (nivel 1B).
Cuándo iniciar la deambulación
Los estudios iniciales de TVP exigían un período de reposo en cama ini-cial mientras se recibían los anticoagulantes parenterales. Sin embargo, la evidencia actual sugiere que la deambulación temprana, si el dolor y el edema lo permiten, disminuye el riesgo de síndrome postrombótico y mejora la calidad de vida.
411
18 · TROMBOSIS VENOSA PROFUNDA
Terapia compresiva
La utilización de distintos dispositivos de compresión ha sido estudiada en momentos diferentes de la enfermedad, desde la profi laxis hasta el manejo de las complicaciones, específi camente del síndrome postrom-bótico. Las medias de compresión dan un soporte mecánico al sistema venoso y principalmente a las válvulas, lo que ayuda a prevenir el de-terioro estructural y funcional del mismo (que es la base para que se desarrolle el síndrome postrombótico) mientras se va resolviendo en el tiempo la TVP con el manejo médico y con la ayuda del mismo sistema fi brinolítico endógeno. Actualmente se recomienda el uso de medias de compresión graduadas hasta la rodilla, personalizadas (hechas sobre medida) y con gradientes de 30-40 mm Hg, de la siguiente manera:• Los pacientes con TVP proximal sintomática deben utilizar medias
de compresión con gradiente de 30-40 mm Hg hasta la rodilla diaria-mente durante 2 años, para la prevención del síndrome postrombóti-co (clase I, nivel de evidencia: B).
• En pacientes con TVP proximal y síndrome postrombótico, es razo-nable un ensayo de medias de compresión con gradiente de 30-40 mm Hg hasta la rodilla, diariamente y de manera indefi nida (clase IIa, nivel evidencia: B).
Filtros de vena cava inferior
Los fi ltros de vena cava inferior (FVCI) no están dirigidos al tratamiento de la trombosis, sino, más bien, a la prevención de su principal consecuencia: la embolia pulmonar. En ningún caso reemplazan la anticoagulación y están indi-cados básicamente en las situaciones en las que por causa médica o quirúrgica es imposible la misma en forma inmediata o crónica. Se dispone de FVCI per-manentes y transitorios.
Recomendaciones para FVCI clase I
• Los pacientes adultos con diagnóstico de TVP proximal aguda y con contraindicación para anticoagulación o con sangrado activo deben recibir un FVCI (nivel de evidencia: B).
• Se debe iniciar la anticoagulación en el paciente con FVCI, una vez se resuelvan las contraindicaciones para la misma o se haya resuelto el sangrado activo (nivel de evidencia: B).
• Los pacientes que reciben un FVCI transitorio deben ser revaluados periódicamente para defi nir su retiro, dependiendo de la ventana de retiro de cada dispositivo (evaluación cada 1-3 semanas) (nivel de evidencia: B).
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
412
Recomendaciones para FVCI clase II
• En pacientes con TEP recurrente a pesar de una anticoagulación ade-cuada, es razonable implantar un FVCI (nivel de evidencia: C).
• Si hay contraindicaciones para la anticoagulación a largo plazo, se debe implantar un FVCI, con preferencia por un dispositivo de dise-ño permanente (nivel de evidencia: C).
• Si hay contraindicaciones transitorias para la anticoagulación, se debe implantar un FVCI, con preferencia por un dispositivo de dise-ño transitorio (nivel de evidencia: C).
Recomendaciones para FVCI clase III
• No se recomienda el uso rutinario de un FVCI en TVP proximal (ni-vel de evidencia: B).
TVP recurrente de miembros inferiores
No hay estudios aleatorizados o prospectivos de cohortes que hayan evaluado el enfoque diagnóstico y la anticoagulación en pacientes con TVP recurrente, por lo que la calidad de la evidencia es baja. La evalua-ción debe estar orientada inicialmente a definir si realmente se trata de una recurrencia de la entidad, ya que no es infrecuente que después de un episodio inicial de TVP los pacientes refieran dolor o edema a nivel del miembro afectado, y las causas pueden ser una recurrencia de la TVP, un síndrome postrombótico e inclusive causas no trombóticas. Es importante definir si existe realmente un nuevo episodio de TVP, pues esto determinará si el paciente se mantiene de forma indefinida con an-ticoagulación. Por otra parte, pasar por alto el diagnóstico de una recu-rrencia implicaría un riesgo alto de TEP potencialmente fatal. Además, es importante definir la causa de la recurrencia de la TVP. Estas pueden clasificarse en dos grupos: las relacionadas con el tratamiento anticoagulan-te y las relacionadas con los factores intrínsecos del paciente. Dependiendo de la causa de la recurrencia, deberá orientarse el tratamiento.
Causas relacionadas con el tratamiento
El riesgo de recurrencia de una TVP disminuye rápidamente después del inicio de la terapia anticoagulante, que es más alto en la primera semana de tratamiento que en la segunda. Una recurrencia muy cercana al inicio del tratamiento (por ejemplo, primer mes) puede generalmente ser manejada con un período más agresivo de terapia anticoagulante, por ejemplo, regresarse de un agente anticoagulante oral a HBPM o au-mentar la dosis de la HBPM. Otros factores relacionados con la recu-rrencia podrían sugerir la aproximación al manejo específico; por ejem-plo: ¿se utilizó adecuadamente la dosis de la HBPM? ¿Fue el paciente
413
18 · TROMBOSIS VENOSA PROFUNDA
adherente al tratamiento? ¿Si recibió un VKA, estuvo en rangos de INR terapéuticos? ¿El paciente consumió medicamentos concomitantes a los anticoagulantes que pudieran interferir con la efi cacia de los anticoa-gulantes? En los pacientes que vienen con dosis de enoxaparina de 1,5 mg/kg SC cada 24 horas, se recomienda cambiar la dosis a 1 mg/kg SC cada 12 horas; en pacientes que vienen con dosis plenas de la HBPM (1 mg/kg SC cada 12 horas) se puede aumentar la dosis total en un 25%; en pacientes que vienen con un VKA con INR subterapéuticos, se debe insistir en la importancia de lograr metas de INR o aumentar el INR ob-jetivo de 2,0-3,0 a 2,5-3,5, con la intención de disminuir la probabilidad de INR menores de 2,0, o cambiar al paciente a HBPM o fondaparinux; en pacientes que vienen recibiendo tratamiento con un NOAC con una dosis y adherencia adecuadas, se recomienda cambiar a VKA o a HBPM.
Causas relacionadas con los factores intrínsecos
El factor de riesgo principal para recurrencia de TVP mientras el pa-ciente viene recibiendo terapia anticoagulante es el cáncer activo. El síndrome antifosfolípidos, la disfi brinogenemia, la trombocitopenia inducida por heparinas y la hemoglobinuria paroxística nocturna son otras entidades que pueden estar asociadas con la recurrencia de la TVP y requieren manejo médico específi co. Las alteraciones anatómicas como el síndrome de May-Thurner son también causas de recurrencias y requieren manejo específi co endovascular o quirúrgico adicional a la anticoagulación.
Evaluación de la probabilidad preprueba
No se han validado los criterios de Wells (véase Tabla 2) en esta subpo-blación de pacientes, pero al puntaje de Wells original se ha agregado el criterio de antecedente de TVP con la intención de poder utilizarlo como una ayuda diagnóstica.
Dímero D
Los niveles del dímero D en sangre se normalizan hacia el tercer mes del tratamiento anticoagulante, lo que lo hace una herramienta valiosa en el estudio de pacientes ambulatorios con sospecha de TVP recurrente, con un porcentaje de falsos negativos del 3% al 5%. Una estrategia recien-temente evaluada es defi nir los pacientes clasifi cados como improbables por escala de Wells y con dímero D negativo, en los que la frecuencia de TVP recurrente es de solo un 0,9%.
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
414
Venografía invasiva
Su valor en los casos de TVP recurrente es limitado, pues frecuentemente no permite diferenciar los episodios nuevos del proceso residual previo, y hasta un 33% de los pacientes tendrá una venografía técnicamente insuficiente por múltiples defectos de llenado.
Ultrasonido de compresión
Se requiere el USC previo para poder evaluar el nuevo estudio. Los ca-sos ipsilaterales enfrentan problemas similares a los de la venografía invasiva, como son el definir qué parte del compromiso es reciente y cuál corresponde al evento previo. Se sugiere un incremento de 4 mm o más en el diámetro del trombo como marcador de alta especificidad (95%) para recurrencia, o el compromiso de otros territorios vasculares previamente no implicados; los otros marcadores tienen una importante variabilidad interobservador y no apoyan el diagnóstico.
Venografía por TAC y por RMN
No hay estudios que evalúen estas técnicas en este grupo de pacientes, por lo cual no se da una recomendación para su utilización.
Enfoque diagnóstico en la TVP recurrente
El estudio se debe iniciar con la realización de una ecografía proximal (si se tiene el estudio previo) o con un dímero D de alta sensibilidad (si no se dispone de la ecografía previa). Si el dímero D es negativo, se excluye el diagnóstico, y si es positivo, se debe repetir la ecografía proximal en un máximo de 7 días. De no ser concluyente la ecografía, se recomienda la realización de una venografía invasiva.
TVP en miembros superiores
El compromiso de los miembros superiores es infrecuente y general-mente pasa desapercibido. Se estima una incidencia de 3/100 000 ha-bitantes y corresponde al 2%-4% de todas la TVP. Tradicionalmente se ha considerado que tiene un curso más benigno que la TVP de extremi-dades inferiores. Sin embargo, esta entidad clínica es causante de TEP entre un 11% y un 33% y de síndrome postrombótico en un 13% de los casos. La TVP de las extremidades superiores es frecuentemente asocia-da con un factor desencadenante intrínseco o extrínseco. El factor ex-trínseco precipitante más frecuente es la presencia de catéteres venosos centrales (CVC), marcapasos (MP), cardiodesfibriladores implantables (CDI) o intervenciones venosas. En estos casos, la trombosis se localiza
415
18 · TROMBOSIS VENOSA PROFUNDA
vecina al dispositivo, y en caso de que la trombosis esté distante al dis-positivo, se deben buscar otras causas para la misma. Usualmente las TVP asociadas con CVC se manejan con anticoagulación sola sin necesi-dad de retirar el CVC, excepto cuando los síntomas relacionados con la TVP persistan a pesar de la anticoagulación, caso en el cual es necesario su retiro. Idealmente se debe esperar 1 semana con el tratamiento an-ticoagulante antes de retirar el dispositivo para disminuir el riesgo de TEP. Si el paciente no es candidato a anticoagulación, es mejor retirar inmediatamente el catéter que colocar un fi ltro de vena cava superior, ya que es mayor el riesgo asociado con la colocación de un fi ltro que el riesgo de TEP asociado con el retiro del CVC. El tiempo de duración recomendado del tratamiento anticoagulante es de 3 meses, a menos que exista indicación de continuar más tiempo con el CVC. En TVP asociada con CVC en pacientes con diagnóstico de cáncer, se sugiere mantener la anticoagulación durante todo el tiempo que el catéter esté implantado y durante los 3 meses ulteriores a su retiro. En pacientes con TVP asociada con MP o con CDI, la recomendación inicial es 3 meses de anticoagulación sin retirar el dispositivo. En pacientes en quienes a pesar de la anticoagulación se extienda la trombosis por toda la vena subclavia, en pacientes muy sintomáticos o cuando se trate de un acceso vascular muy importante (único), estaría indicada la terapia fi brinolítica dirigida con catéter, si el riesgo de sangrado es bajo y la evolución de la trombosis es menor de 14 días (grado 2C).
En cuanto a los factores intrínsecos, el síndrome de opérculo torá-cico y el síndrome de trombosis inducida por esfuerzos (Paget-von Schroetter) son las principales patologías que deben ser investigadas. La trombosis inducida por esfuerzos es una entidad rara y vista más fre-cuentemente en hombres jóvenes. Los síntomas incluyen dolor, edema y fatiga de la extremidad superior afectada, característicamente después de ejercicio intenso. La etiología es explicada por una compresión de la vena subclavia entre la primera costilla y el músculo escaleno. General-mente la anticoagulación no es sufi ciente para resolver el problema y la terapia fi brinolítica dirigida con catéter seguida de angioplastia venosa, angioplastia con stent o cirugía son necesarias. En más de la mitad de los casos hay compromiso de la otra extremidad. En pacientes con síndro-me del opérculo torácico, muchas veces se requiere la combinación de anticoagulación con cirugía.
La anatomía del sistema venoso de los miembros superiores difi ere de la de los miembros inferiores, lo que difi culta la extrapolación del enfoque diagnóstico que se ha discutido previamente para los miem-bros inferiores. A continuación se dan algunas recomendaciones a tener en cuenta al abordar el diagnóstico de una TVP de las extremidades superiores.
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
416
Ultrasonido
Una vez que el sistema venoso ingresa al tórax, se hace imposible la eva-luación por compresión del mismo, pero se puede utilizar un enfoque de multimodalidad (compresión, imagen bidimensional y Doppler). La evidencia que soporta el uso de la ecografía es de baja calidad y no hay ningún estudio de seguimiento y/o tratamiento hasta la fecha.
Valoración de la probabilidad preprueba
Se ha propuesto un esquema de puntuación para definir un posible diagnóstico, con una sensibilidad del 78% y una especificidad del 64%, pero aún no se ha evaluado de manera prospectiva (Tabla 6).
Tabla 6. Puntaje de probabilidad de TVP de miembros superiores
Criterio Puntos
Presencia de marcapasos o de catéter central 1
Dolor localizado 1
Edema ipsilateral 1
¿Existe otro diagnóstico posible? -1
Interpretación:
• -1 o 0 puntos: baja probabilidad.• 1 punto: probabilidad intermedia.• 2 o 3 puntos: alta probabilidad.
Dímero D
Solo se ha evaluado en 1 estudio de 52 pacientes y se encontró una sen-sibilidad del 100% con una muy baja especificidad del 17%.
Venografía por RMN
Tiene importantes limitaciones. Incluso la adquisición de imágenes con contraste tiene una sensibilidad baja (aproximadamente del 50%), con una especificidad del 80%.
Enfoque diagnóstico
Se recomienda iniciar el estudio con una imagen ecográfica que utilice múl-tiples modalidades, y de ser negativa, realizar un dímero D en quienes per-sista la sospecha clínica de TVP. Si este también es negativo, pero persiste
417
18 · TROMBOSIS VENOSA PROFUNDA
la sospecha clínica, se debe proceder a una venografía, con excepción de los casos en los que por otra causa se expliquen claramente los síntomas.
TVP asintomática
Grupo de pacientes en los que durante una evaluación clínica se les des-cubre de manera incidental una TVP, o que la misma se les diagnostica dentro del estudio de un TEP. Estos pacientes tienen el mismo riesgo de complicaciones. Se recomienda el mismo enfoque de tratamiento inicial y a largo plazo que en los pacientes sintomáticos.
Prevención de tromboembolismo venoso en pacientes quirúrgicos
Se estima que cada año, se presentan en Estados Unidos entre 150 000 y 200 000 muertes asociadas con el TEV. Una tercera parte de estos casos se presenta en el período postoperatorio, por lo que es necesario hacer una adecuada planifi cación de la profi laxis antitrombótica en todos los pacien-tes llevados a cirugía. La evidencia clínica y los análisis de costo-efectividad son contundentes en el valor de esta estrategia en la prevención de la mor-bilidad y la mortalidad y en el ahorro de costos para los sistemas de salud.
Si bien existen múltiples estrategias para la prevención del TEV (HBPM, HNF, métodos de compresión mecánica [Tabla 7]), los niveles de evidencia son variables y no se puede aplicar una estrategia única en todos los pacientes. Las guías actuales de manejo se basan en una indivi-dualización del riesgo de acuerdo con el tipo de paciente, el tipo de ciru-gía a realizarse y las posibles complicaciones asociadas con la profi laxis. Para una aproximación racional, propondremos una estrategia de pasos que permita llegar al esquema de profi laxis adecuado en cada caso:• Paso 1: defi nir el nivel de riesgo de TVP asociado con el tipo de inter-
vención quirúrgica: riesgo bajo, intermedio o alto (Tabla 8).• Paso 2: defi nir el riesgo individual del paciente. Existen distintos
puntajes para establecer el riesgo de TVP en cada paciente indivi-dualmente, adicional al riesgo asociado con el tipo de cirugía, pero solo el puntaje de Caprini está validado de manera retrospectiva y es el recomendado por las últimas guías del ACCP (Tabla 9). Con este puntaje se clasifi ca el riesgo de TVP en: muy bajo (0-1 punto), bajo (2 puntos), intermedio (3-4 puntos) y alto (≥5 puntos).
• Paso 3: defi nir el riesgo de sangrado. No hay una herramienta o pun-taje que permita defi nir claramente el riesgo de sangrado en esta po-blación quirúrgica por ausencia de estudios controlados. En general, a mayor riesgo de sangrado, mayor será la tendencia al uso de medi-
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
418
das mecánicas de profilaxis, y en riesgo bajo de sangrado, mayor será la tendencia al uso de profilaxis farmacológica. Es importante recal-car que la profilaxis antitrombótica debe iniciarse 12 horas antes o 12 horas después de cualquier intervención quirúrgica, recomendación que busca disminuir la posibilidad de sangrado en el perioperatorio.
Tabla 7. Esquemas de profilaxis antitrombótica en pacientes quirúrgicos
Medicamento Dosis-posología
Enoxaparina 40 mg SC c/24 h
Dalteparina 5000 UI SC c/24 h
Heparina no fraccionada 5000 UI SC c/8 h
Fondaparinux 2,5 mg SC c/24 h
Rivaroxabán 10 mg VO c/24 h
Dabigatrán 150 mg VO c/12 h
Warfarina 5 mg VO c/24 h (meta del INR: 2,0-3,0)
Medidas de compresión externa (neumática)
La compresión debe mantenerse 18 h/día
INR: índice internacional normalizado; SC: subcutáneo; UI: unidades internacionales; VO: vía oral.
Tabla 8. Nivel de riesgo de TVP por tipo de procedimiento quirúrgico
Nivel de riesgo Intervención
Bajo Cirugía abdominopélvica laparoscópica, apendicectomía, RTU
Intermedio Cirugía ab dominopélvica abierta
Alto Cirugía abdominopélvica oncológica
RTU: resección transuretral de la próstata.
419
18 · TROMBOSIS VENOSA PROFUNDA
Tabl
a 9.
Pun
taje
de
Cap
rini
1 pu
nto
2 pu
ntos
3 pu
ntos
5 pu
ntos
Edad
41-
60 a
ños
Edad
61-
74 a
ños
Edad
>75
año
sAC
V <
1 m
es
Ciru
gía
men
orC
irugí
a ar
t ros
cópi
caH
istor
ia d
e TV
PAr
tropl
astia
ele
ctiv
a
IMC
>25
C
irugí
a m
ayor
abi
erta
Hist
oria
fam
iliar
de
TVP
Frac
tura
de
pelv
is, c
ader
a o
pier
na
Edem
a de
mie
mbr
os in
ferio
res
Ciru
gía
lapa
rosc
ópic
a >
45 m
inut
osFa
ctor
V d
e Le
iden
Lesió
n m
edul
ar a
guda
<1
mes
Emba
razo
o p
uerp
erio
Cán
cer
Prot
rom
bina
202
10A
Hist
oria
de
abor
to re
curr
ente
in
expl
icad
oRe
poso
en
cam
a >
72 h
Antic
oagu
lant
e lú
pico
Antic
once
ptiv
os o
rale
sC
atét
er v
enos
o ce
ntra
lAn
ticue
rpos
ant
icar
diol
ipin
as
Seps
is <
1 m
esPr
esen
cia
de in
mov
iliza
dore
sH
omoc
istei
nem
ia
Enfe
rmed
ad p
ulm
onar
sev
era
(incl
uye
neum
onía
)H
istor
ia d
e tro
mbo
cito
peni
a po
r hep
arin
a (H
IT)
Prue
bas
de fu
nció
n pu
lmon
ar a
ltera
das
Otra
trom
bofil
ia a
dqui
rida
o co
ngén
ita
Infa
rto a
gudo
de
mio
card
io
Falla
car
díac
a
Enfe
rmed
ad in
flam
ator
ia in
test
inal
Repo
so e
n ca
ma
por o
rden
méd
ica
ACV:
acc
iden
te c
ereb
rova
scul
ar; I
MC
: índ
ice
de m
asa
corp
oral
; TVP
: tro
mbo
sis v
enos
a pr
ofun
da.
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
420
Recomendaciones en cirugía general, abdominopélvica, cirugía urológica, cirugía vascular, cirugía bariátrica y cirugía estética y reconstructiva
• En los pacientes con riesgo muy bajo de TVP (puntaje de Caprini de 0), no se recomienda el uso de tromboprofilaxis diferente a la deam-bulación temprana.
• En los pacientes con riesgo bajo de TVP (puntaje de Caprini de 1-2), se recomienda el uso de medidas de compresión extrínseca (MCE).
• En los pacientes con riesgo intermedio de TVP (puntaje de Caprini de 3-4) y riesgo bajo de sangrado, se recomienda el uso de HBPM, HNF o MCE.
• En los pacientes con riesgo intermedio de TVP (puntaje de Caprini de 3-4) y riesgo alto de sangrado, se recomienda el uso de MCE.
• En los pacientes con riesgo alto de TVP (puntaje de Caprini ≥5) y riesgo bajo de sangrado, se recomienda el uso de HBPM o HNF y se sugiere adicionar MCE.
• En los pacientes con riesgo alto de TVP (puntaje de Caprini ≥5) y riesgo alto de sangrado, se recomienda el uso de MCE hasta que se pueda utilizar HBPM o HNF.
• En los pacientes con cáncer y riesgo alto de TVP (puntaje de Caprini ≥5) y riesgo bajo de sangrado, se recomienda el uso de HBPM de forma prolongada (4 semanas).
• En los pacientes con riesgo alto de TVP (puntaje de Caprini ≥5), ries-go bajo de sangrado y con contraindicación para el uso de HBPM y HNF, se sugiere el uso de ASA en dosis bajas, fondaparinux o MCE.
Recomendaciones en cirugía cardíaca
Se considera que este grupo de pacientes tiene un riesgo moderado de TVP, con un incremento importante en el riesgo de sangrado:• En los pacientes sometidos a cirugía cardíaca que tienen un postope-
ratorio no complicado, se recomienda el uso de MCE como profilaxis para TVP.
• En los pacientes sometidos a cirugía cardíaca que tienen un posto-peratorio prolongado sin complicaciones hemorrágicas, se sugiere la utilización de HBPM o HNF como profilaxis para TVP.
Recomendaciones en cirugía de tórax
La mayoría de los pacientes en este grupo es considerada de riesgo intermedio para TVP. Solo se consideran de alto riesgo los pacientes sometidos a resección pulmonar extensa, neumonectomía, neumonec-tomía extrapleural, esofagectomía o cirugía oncológica:
421
18 · TROMBOSIS VENOSA PROFUNDA
• En los pacientes con riesgo moderado de TVP y riesgo bajo de san-grado, se recomienda el uso de HNF, HBPM o MCE.
• En los pacientes con riesgo alto de TVP y riesgo bajo de sangrado, se recomienda el uso de HNF o HBPM, con adición de MCE a la terapia farmacológica.
• En los pacientes con riesgo alto de TVP y riesgo alto de sangrado, se recomienda el uso de MCE hasta que se pueda iniciar el uso de HNF o HBPM.
Recomendaciones en neurocirugía
Craneotomía
Representa dos grandes problemas. Por una parte, este subgrupo siem-pre es de alto riesgo para TVP y si la cirugía craneal es oncológica, el riesgo será muy alto (10% de probabilidad de TVP). Por otra parte, las consecuencias del sangrado serían potencialmente muy severas. El ba-lance entre estas dos circunstancias varía en el tiempo, lo que hace diná-micas las recomendaciones para profi laxis:• En los pacientes con riesgo alto de TVP, se recomienda el uso de
MCE.• En los pacientes con muy alto riesgo de TVP, se recomienda el uso
de MCE, e iniciar HBPM o HNF una vez se consiga una hemostasia adecuada.
Cirugía espinal
El perfi l de riesgo de TVP no es tan alto como el de los pacientes lle-vados a craneotomía, pero las consecuencias del sangrado pueden ser igual de devastadoras. Los factores que determinan un mayor riesgo de TVP son un abordaje conjunto anterior y posterior, coexistencia de cáncer e historia previa de TVP:• En los pacientes llevados a cirugía espinal, se recomienda el uso de
MCE como profi laxis de TVP.• En los pacientes con riesgo alto de TVP, se recomienda el uso de
MCE, con adición de HBPM o HNF una vez se logre una hemostasia adecuada.
Recomendaciones en trauma mayor, incluido el trauma craneoencefálico y el trauma raquimedular
Las características fi siopatológicas y la población afectada por trauma son muy heterogéneas, por lo que se deben individualizar en cada caso espe-cífi co el riesgo de TVP y las consecuencias de un posible sangrado. Los pacientes que sufren de trauma raquimedular agudo o trauma craneo-encefálico moderado a severo tendrán un riesgo mucho mayor de TVP:
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
422
• En los pacientes con trauma mayor, se recomienda el uso de HBPM, HNF o MCE como tromboprofilaxis.
• En los pacientes con trauma mayor y riesgo alto de TVP, se sugiere adicionar MCE a la tromboprofilaxis, si no existen contraindicación por trauma de miembros inferiores.
• En los pacientes con trauma mayor y contraindicación para el uso de HBPM o HNF, se debe utilizar MCE, con adición de heparinas una vez sea posible.
• En los pacientes con trauma raquimedular con paraplejia, se reco-mienda mantener la profilaxis para TVP por 3 meses.
Recomendaciones en cirugía ortopédica
La cirugía ortopédica ha cambiado de forma radical a lo largo de los úl-timos 50 años. Si bien se ha incrementado la complejidad de los procedi-mientos, cada día se hacen menos agresivos y limitan la invasión al míni-mo posible, lo que ha implicado cambios en el perfil trombogénico de los mismos. Aun así, el riesgo de TVP en el paciente ortopédico se mantiene como uno de los más altos en todas las especialidades quirúrgicas.
Cirugía ortopédica mayor: artroplastia total de cadera, artroplastia total de rodilla y osteosíntesis de cadera
• En los pacientes sometidos a artroplastia total de rodilla (ATR) o ar-troplastia total de cadera (ATC) se recomienda el uso de cualquiera de los siguientes agentes para tromboprofilaxis, por un mínimo de 10 a 14 días: HBPM, fondaparinux, apixabán, dabigatrán, rivaroxabán, dosis bajas de HNF, dosis ajustadas de warfarina, ASA o MCE.
• En los pacientes sometidos a osteosíntesis de cadera (OC), se reco-mienda el uso de cualquiera de los siguientes agentes para trombo-profilaxis, por un mínimo de 10 a 14 días: HBPM, fondaparinux, do-sis bajas de HNF, dosis ajustadas de warfarina, ASA o MCE.
• Si bien existen múltiples opciones para el manejo de la tromboprofi-laxis en el paciente de cirugía ortopédica mayor, los mejores niveles de evidencia de seguridad y eficacia son con las HBPM. La selección de otro agente antitrombótico debe fundamentarse en la imposibili-dad de la utilización de las mismas o en ciertas características farma-cológicas específicas para cada caso.
• Se recomienda continuar la tromboprofilaxis en el período ambula-torio, hasta el día 35 del postoperatorio.
• Se recomienda la utilización conjunta de un sistema de compresión extrínseca (MCE) asociado con la tromboprofilaxis farmacológica durante el período intrahospitalario.
• En los pacientes con muy alto riesgo de sangrado, se recomienda el uso de MCE o no utilizar tromboprofilaxis.
423
18 · TROMBOSIS VENOSA PROFUNDA
• En los pacientes llevados a cirugía que se niegan o son incapaces de mantener un esquema inyectable o las medidas de compresión externa, se recomienda como opción la utilización de apixabán, dabi-gatrán, rivaroxabán o dosis ajustadas de warfarina.
• No se recomienda el uso de FVCI como elemento profi láctico en pa-cientes con alto riesgo de sangrado, si se tienen en cuenta las posibles complicaciones asociadas con su utilización.
• No es necesario estudiar con ecografía a los pacientes sometidos a cirugía ortopédica mayor antes del alta en busca de TVP.
Lesiones aisladas por debajo de la rodilla
No se sugiere la utilización de tromboprofi laxis en lesiones que requie-ren la inmovilización de la pierna por debajo de la rodilla.
Artroscopia de rodilla
No se recomienda el uso de tromboprofi laxis, excepto en los pacientes que han tenido una TVP previa.
Lecturas recomendadas
• Falck-Ytter Y, Francis CW, Johanson NA, et al. Prevention of VTE in orthope-dic surgery patients: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest. 2012;141(2 Suppl):e278S-e325S.
• Gould MK, Garcia D, Wren S, et al. Prevention of VTE in nonorthopedic sur-gical patients: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guide-lines. Chest. 2012;141(2 Suppl):e227S-e277S.
• Jaff MR, McMurtry S, Archer S, et al. Management of massive and submassive pulmonary embolism, iliofemoral deep vein thrombosis, and chronic throm-boembolic pulmonary hypertension a scientifi c statement from the american heart association. Circulation 2011;123(16):1788-830.
• Kearon C, Aki EA, Ornelas J, et al. Antithrombotic therapy for VTE disease: CHEST Guideline and Expert Panel Report. Chest. 2016;149(2):315-52.
• Kearon C, Akl EA, Comerota A, et al. Antithrombotic Therapy for VTE disease: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American Co-llege of Chest PhysiciansEvidence-Based Clinical Practice Guidelines. Chest. 2012;141(2 Suppl):e419S-e494S.
• Kesieme E, Kesieme C, Jebbin N, et al. Deep vein thrombosis: a clinical review. J Blood Med. 2011;2:59-69.
• Montoya R, Gajra A. Current status of new anticoagulants in the management of venous thromboembolism. Adv Hematol. 2012;2012:856341.
GUÍAS DE MANEJO EN ENFERMEDADES CARDÍACAS Y VASCULARES. ESTADO ACTUAL 2017
424
• Sharifi M. Modern management of deep venous thrombosis. Vasc Dis Man. 2014;11(1):e2-e11.
• Streiff MB, Agnelli G, Connors JM, et al. Guidance for the treatment of deep vein thrombosis and pulmonary embolism. J Thromb Thrombolysis. 2016;41(1):32-67.
• Wells PS, Forgie MA, Rodger MA, et al. Treatment of venous thromboembo-lism. JAMA. 2014;311(7):717-28.
• Woo KC, Goertz JK. Diagnosis and management of deep venous thrombosis in the emergency department. Emerg Med Pract. 2015;17(3):1-24.