QUINOLONAS
-
Upload
jasmin-rojas -
Category
Documents
-
view
1.343 -
download
1
Transcript of QUINOLONAS

QUINOLONAS
IntroducciónLas quinolonas integran una familia de antibióticos, conocida desde la década del 60, derivados de síntesis obtenidos a partir de un antimalárico: la cloroquina; siendo el ácido nalidíxico la primer quinolona usada en clínica (1962); y que junto con el ácido pipemídico, obtenido en 1973, integran la primera generación de quinolonas. El segundo tiene un espectro de acción más amplio y mejores propiedades farmacocinéticas.
Las quinolonas de segunda generación son derivados fluorados o fluoroquinolonas (FQ); las de tercera generación integrada por derivados bi y trifluorados y actualmente están en desarrollo las de cuarta generación.
La primer FQ en aparecer fue norfloxacina (1978), lo que significó un importante adelanto por su mayor potencia y espectro antibacteriano. Con posterioridad surgieron: ciprofloxacina (1987), ofloxacina (1991), enoxacina, lomefloxacina y temafloxacina (1992), levofloxacina y esparfloxacina (1997), trovafloxacina y grepafloxacina (1998), gatifloxacina y moxifloxacina (1999). Algunas de ellas fueron retiradas del mercado, después de aprobada su comercialización, por sus efectos tóxicos (sparfloxacina, trovafloxacina, grepafloxacina).
Aunque las primeras quinolonas tenían actividad sólo contra bacterias aerobias gramnegativas y eran eficaces para tratar infecciones gastrointestinales y urinarias, las nuevas quinolonas se han convertido en un armamento muy importante contra mayor número de infecciones. Ello deriva del mayor espectro de actividad, su buena biodisponibilidad y penetración tisular.
Como consecuencia de su uso extensivo en los últimos años, se ha observado un incremento progresivo de cepas resistentes.
Estructura química
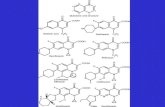
Las quinolonas, tienen una estructura química formada por dos anillos con un nitrógeno en la posición 1, un grupo carboxilo en la posición 3 y un grupo carbonilo en la posición 4. Estos antibióticos cuando tienen un átomo de flúor en la posición 6, aumentan su potencia antibacteriana. Ver Figura 1.
LAS
QUINOLONAS
Las quinolonas son antibióticos obtenidos por síntesis; en su estructura básica las FQ se distinguen de su predecesora, el ácido nalidíxico, en agregar uno (en posición 6) o más átomos de fluor en la posición 1, 5, 7 y 8; con lo que modifican sus propiedades farmacocinéticas y farmacodinámicas y ha llevado a clasificar las quinolonas en primera, segunda, tercera y cuarta generación.
Mecanismo de acción
Las quinolonas actúan en el interior de la bacteria, penetrando a través del canal acuoso de las porinas. Son los únicos agentes antibacterianos que ejercen su actividad bactericida uniéndose e inhibiéndolas a las topoisomerasas bacterianas; aunque éste no sería el único mecanismo de acción.
Las topoisomerasas son enzimas que controlan el superenrollamiento y desenrollamiento del ADN bacteriano. El superenrollamiento permite a la larga molécula de ADN empaquetarse dentro de célula bacteriana. Esta estructura debe ser desenrollada para permitir diferentes funciones como replicación, transcripción y reparación del ADN. La inhibición de la actividad de estas enzimas impide a la célula bacteriana producir las proteínas necesarias para su reparación, crecimiento y reproducción. Una inhibición prolongada conduciría así a la muerte de la célula.

Existen 4 tipos de topoisomerasas. Las quinolonas actuarían a nivel de ADN-girasa (también llamada topoisomerasa tipo II) y de la topoisomerasa tipo IV. No actúan a nivel de las topoisomerasas I y III.
La compleja interacción de las quinolonas con las topoisomerasas es la base del diferente espectro antibacteriano de las quinolonas y también de la selección de cepas resistentes. La actividad de las quinolonas contra las bacterias grampositivas se debe a su acción "blanco" en las topoisomerasas IV, en cambio la actividad contra las bacterias gramnegativas es por su acción "blanco" en las topoisomerasa II o ADN-girasa.
Actividad antibacteriana
Las FQ son antibióticos bactericidas, de penetración intracelular.
Las quinolonas de primera generación son activas frente a microorganismos gramnegativos: E. coli, Proteus, Klebsiella, Enterobacter, Citrobacter, Salmonella, Shigella; con excepción de Pseudomonas spp., y nula para cocos grampositivos y anaerobios. Se usan como antisépticos urinarios.
Las quinolonas de segunda generación tienen el mismo espectro anterior, presentan una buena cobertura en contra de bacilos Gram negativos aerobios y enterobacterias como: E coli, salmonella, S tiphy, shigella, enterobacter, klebsiella, proteus spp, campilobacter, Y. enterocolitica y vibrios. Su espectro incluye a P. aeruginosa, N. gonorrhoeae, S. aureus, S. epidermitis (incluyendo meticilino resistentes), H. influenzae, M. Catarrhalis, gérmenes multirresistentes a cefalosporinas, penicilinas y aminoglucósidos, micobacterias y algunos patógenos atípicos. Ciprofloxacino es la mejor quinolona contra Ps. aeruginosa. Estas fluoroquinolonas tienen escasa
actividad frente a Streptococcus pneumoniae y otras especies de Streptococcus. Su actividad es escasa contra Enterococcus spp. Tienen baja actividad contra anaerobios.
Las de tercera generación mantienen la buena actividad de las de segunda generación frente a gramnegativos y micobacterias, pero presentan mejor actividad frente a bacterias grampositivas (Streptococcus pyogenes y neumococo penicilina sensible y penicilina resistentes), anaerobios y patógenos "atípicos".
Las de cuarta generación tienen una actividad similar a la anterior expandiéndose a bacterias anaerobias (Clostridium y bacteroides).
La actividad contra Mycobacterium tuberculosis y M. avium es variable, siendo los más eficaces: Moxifloxacina, ciprofloxacina y ofloxacina. Ofloxacina y pefloxacina son activos contra M. leprae.
Los patógenos "atípicos" (Chlamydia spp, Mycoplasma spp. y Legionella spp., Gardnerella vaginalis) son muy sensibles a las nuevas quinolonas.
Ninguna de las quinolonas es activa frente a Treponema spp. ni Nocardia spp.
Este amplio espectro de actividad de las fluoroquinolonas permite su uso en una variedad de infecciones de: aparato urinario, piel, partes blandas, hueso, aparato respiratorio.
Mecanismo de resistencia
El número de bacterias resistentes a las quinolonas ha ido aumentando, lo que se relaciona a la presión selectiva de su extenso uso.
Los mecanismos de resistencia a las fluoroquinolonas son tres:
1. Mutación de la enzima. Se produce por producción de mutaciones cromosómicas que alteran la topoisomerasa del ADN bacteriano, a la que no podría unirse las quinolonas.
2. Alteración de la permeabilidad. Se presenta como una disminución de la permeabilidad bacteriana por alteración de las porinas. Esto impide la entrada de estos antibióticos a la bacteria, y afecta únicamente a las bacterias gramnegativas.223. Bomba de eflujo. Por un mecanismo de eflujo, mediante el cual se excreta de manera activa a las quinolonas hacia el exterior bacteriano.
La resistencia es cruzada entre las distintas FQ, pero no es del mismo grado para todas.

FarmacocinéticaLas quinolonas se absorben bien del tracto gastrointestinal superior después de su administración oral. Las FQ tienen una biodisponibilidad que supera el 50% en todos los compuestos y se aproxima a 100 % en algunos. Así norfloxacina sólo se absorbe 50%, ciprofloxacina 70%, el resto de FQ presentan una absorción casi completa entre 97 y 100%.
Esta alta biodisponibilidad permite el tratamiento por vía oral o el rápido pasaje de vía parenteral a oral cuando las condiciones del paciente lo permiten. Por lo general se alcanzan concentraciones séricas pico dentro de 1 a 3 horas de administrada una dosis. Los alimentos no reducen de manera sustancial la absorción de las quinolonas, pero pueden prolongar el tiempo en que se alcanza la concentración sérica máxima.
Las FQ se difunden ampliamente debido a su baja unión a las proteínas plasmáticas, a su solubilidad y al grado de ionización.
Alcanzan concentraciones elevadas en tejidos y a nivel intracelular, atraviesan barreras, sobre todo si están inflamadas (meninges, placenta, próstata) y penetran bien en el interior de las células, sobre todo en los macrófagos y polimorfonucleares, por lo que son antibióticos adecuados para tratar infecciones producidas por gérmenes intracelulares. Las concentraciones en orina, tejido renal, prostático, materia fecal, bilis, pulmón, macrófagos y neutrófilos suelen superar las concentraciones séricas. Por lo general las concentraciones de las quinolonas en saliva, líquido prostático, hueso y líquido céfalo raquídeo son más bajas que en el suero. Se ha observado penetración de pefloxacina (72% de la concentración sérica) y de ofloxacina (120%) en el líquido de ascitis.
Estos antibióticos atraviesan la barrera placentaria y se acumulan en el líquido amniótico, se excretan por la leche materna alcanzando un 75% de las concentraciones plasmáticas.
Los niveles séricos pueden ser mayores en el anciano, porque la absorción es mayor y el aclaramiento renal menor. Como norfloxacina no alcanza concentraciones séricas suficientes para algunas bacterias, raramente se indica para infecciones fuera del tracto gastrointestinal o genitourinario.
Existen diferencias notables en el grado de metabolismo hepático que sufren las fluoroquinolonas. La biotransformación ocurre fundamentalmente en el hígado por reacciones de oxidación en las que intervienen enzimas del sistema citocromo P450.
Las principales vías de eliminación difieren entre las quinolonas. La eliminación se produce principalmente por vía renal (por filtración glomerular y secreción tubular) como fármaco inalterado, en el caso de norfloxacina, ciprofloxacina, ofloxacina y lomefloxacina. La eliminación biliointestinal es predominante en el caso de pefloxacina. Algunos de los metabolitos pueden sufrir circulación entero-hepática. Ciprofloxacina, enoxacina, fleroxacina y norfloxacina presentan una eliminación mixta, renal y biliar. Como consecuencia todas las quinolonas excepto pefloxacina, alcanzan altos niveles urinarios.
La vida media de los fármacos que se excretan por vía renal (ofloxacina), aumenta cuando hay insuficiencia renal severa. Por eso hay que adaptar las dosis con relación a la vía de eliminación del fármaco administrado y al aclaramiento de creatinina: cuando es menor de 50 ml/min., para ofloxacina, e inferior a 30 ml/min., para norfloxacina, ciprofloxacina, lomefloxacina y enoxacina. No está indicado disminuir la dosis de ácido nalidíxico ni de pefloxacina.
Si el paciente padece disfunción hepática habrá que reducir la posología de pefloxacina y únicamente habrá que ajustar la dosis del resto de quinolonas cuando se asocien disfunción de ambos órganos o cuando alguna de ellas sea grave.
Interacciones farmacocinéticas
Las quinolonas muestran marcada reducción de la biodisponibilidad cuando se las coadministra por vía oral con antiácidos que contienen aluminio, magnesio o calcio, con sales de hierro o zinc, presumiblemente debido a la formación de complejos catión-quinolona que se absorben escasamente. El sucralfato, contiene grandes cantidades de iones aluminio, reduce de manera similar la absorción de las quinolonas. Si bien, al distanciar la toma de antiácidos y quinolonas, puede reducir esa interacción, esta conducta pueda ser no totalmente segura en algún paciente individual. En pacientes que toman quinolonas y que necesitan disminuir su acidez gástrica, se prefiere usar los antagonistas de receptores de histamina (cimetidina y ranitidina) que sólo pueden retrasar la absorción.

Algunas quinolonas (ciprofloxacina), reducen el aclaramiento de teofilina y cafeína entre el 20 y el 50%, aumentando sus niveles plasmáticos y su toxicidad. En los pacientes medicados con quinolonas y teofilina se debe reducir las dosis de teofilina. Norfloxacina, ofloxacino, y el ácido nalidíxico no producen este efecto.
Los antiinflamatorios no esteroideos pueden incidir en los efectos estimulantes de las quinolonas sobre el SNC. Se comunicaron convulsiones en enfermos que recibían enoxacina y fenbufen.
Con algunas quinolonas se ha observado un aumento del efecto anticoagulante de la warfarina.
El incremento en los niveles plasmáticos de estos fármacos puede explicarse por una inhibición de tipo competitivo, sobre el sistema citocromo P-450 en el hígado.
Efectos adversos
Las quinolonas en general son bien toleradas, con un perfil de seguridad similar para todos los componentes del grupo. Los efectos adversos a las quinolonas en su mayoría son leves y retroceden al suspender la droga.
Los efectos adversos más frecuentes son alteraciones gastrointestinales, seguidos de síntomas neurosiquiátricos y de
reacciones cutáneas de hipersensibilidad.
Gastrointestinales: pueden observarse náuseas, vómitos, diarrea, dolor abdominal, pérdida del apetito y malestar abdominal. La colitis por Clostridium difficile no es común.
Neurosiquiátricos: las manifestaciones adversas neurológicas más frecuentes son: mareo, cefalea, insomnio, alucinaciones. Se destacan, por su gravedad, las convulsiones y las reacciones maníacas o psicóticas, especialmente en personas con enfermedades previas del SNC: epilepsia, tumores cerebrales, arterioesclerosis, hipoxemia cerebral o alteraciones metabólicas, por lo que se recomienda evitar estos antibióticos en estos enfermos. El riesgo de convulsiones aumenta con la administración concomitante de algunos fármacos como: antiinflamatorios, teofilina o foscarnet.
Hipersensibilidad: En general son leves o moderadas. Pueden observarse reacciones cutáneas como rash y prurito. Se han descrito formas más graves, pero con una baja incidencia. La hipersensibilidad es cruzada entre las diferentes quinolonas. Fueron descritas reacciones de fotosensibilidad, a tomarse en consideración en zonas tropicales.
Articulaciones: En menores de 18 años causan erosión del cartílago articular en crecimiento, en articulaciones que soportan peso, por ello están contraindicadas en los niños, adolescentes (menores de 18 años), embarazadas y durante la lactancia.
Cardiacas: Las FQ causan prolongación del intervalo QT, por lo que no deben usarse en pacientes con síndromes congénitos o adquiridos de prolongación de QT.
Hematológicas: En la esfera hematológica pueden producir: leucopenia, eosinofilia o trombocitopenia. Con el ácido nalidíxico se han descrito casos de depresión medular. En pacientes con déficit de glucosa-6-fosfato-deshidrogenasa (G-6-PD) pueden producir hemólisis y anemia.
Hepáticas: Que se refleja en un aumento de transaminasas, fosfatasa alcalina y bilirrubina.
Renal: hiperazoemia, cristaluria y nefritis intersticial.
Otros: Otro efecto adverso es la tendinitis y rotura del tendón de Aquiles.
Indicaciones clínicas
Su uso debe restringirse para los casos específicos y no indicarlas en forma indiscriminada, para evitar la creciente resistencia de los microorganismos, lo que lleva a una pérdida de su utilidad clínica.
- Infecciones urinarias
Las quinolonas de primera generación se las utiliza como antisépticos urinarios estrictos.

Las quinolonas de segunda generación son útiles para tratar infecciones urinarias complicadas o no, sobre todo en las que afectan parénquima renal y en prostatitis. Esto se basa en su excelente actividad contra los uropatógenos más habituales, la alta concentración que adquieren en orina y su buena penetración en el tejido prostático. Cuando las orinas son alcalinas, estos antibióticos pueden perder eficacia.
Son de elección para iniciar un tratamiento empírico, el que luego debe adaptarse al resultado del estudio bacteriológico. En infecciones urinarias no complicadas de la mujer, si el germen es sensible a trimetoprim-sulfametoxazol, se lo prefiere por su menor costo ya que es igualmente activo, reservando las FQ para las infecciones urinarias complicadas y para pacientes alérgicos a las sulfas.
Las quinolonas, al igual que trimetoprim-sulfametoxazol, eliminan los gérmenes de los reservorios (vaginal, perirrectal y perineal), sin alterar la flora normal del intestino y vagina, por lo que disminuye la frecuencia de las recidivas de las infecciones urinarias.
De las nuevas quinolonas, levofloxacina está aprobada para el tratamiento de infecciones urinarias altas y bajas.
ESQUEMAS TERAPÉUTICOS PARA ADULTOS CON INFECCIÓN URINARIA
SÍNDROME DURACIÓN FÁRMACOS DOSIS * (mg) INTERVALO
Cistitis, mujeres no complicadas
Tres días(3 días)
Norfloxacino2Ciprofloxacino2Levofloxacino3
400250250
c/12hc/12hc/24h
Cistitis complicada 10-14 días(Diez a catorce días)
NorfloxacinoCiprofloxacinoLevofloxacino
400250250
c/12hc/12hc/24h
Prostatitis aguda 4 semanas(Cuatro semanas)
CiprofloxacinoLevofloxacino
500250
c/12hc/24h
Prostatitis crónica 6-12 semanas(Seis a doce
semanas)
CiprofloxacinoLevofloxacino
500250
c/12hc/24h
Pielonefritis, ambulatoria
14 días(Catorce días)
CiprofloxacinoLevofloxacino
500250
c/12hc/24h
2 = quinolonas de segunda generación.3 = quinolonas de tercera generación.
Quinolonas disponibles en nuestro medio:
NOMBRE PRESENTACIÓN FARMACÉUTICATabletas/Comprimidos Ampollas
Ácido nalidíxico1 Tabletas: 500 mgÁcido pipemídico1 Comprimidos: 200 y 400 mgCiprofloxacino2 Comprimidos: 250 y 500 mg Ampollas para uso I. V.:
200 y 400 mgNorfloxacino2 Comprimidos: 400 mgLevofloxacino3 Comprimidos: 500 mg Ampollas para uso I. V.: de 500 mgMoxifloxacino4 Comprimidos: 400 mg1, 2, 3, 4: Generación de las quinolonas.
- Infecciones gastrointestinales
Todos los patógenos bacterianos que provocan gastroenteritis suelen ser susceptibles in vitro a las quinolonas. Alcanzan altas concentraciones en materia fecal, aunque ésta puede reducir su actividad. La eficacia contra infecciones sistémicas por especies de Salmonella está favorecida por la penetración de las FQ en los macrófagos, siendo éstos patógenos intracelulares. Por otra parte se ha demostrado que el uso de quinolonas en diarrea causada por Salmonella spp., determina un prolongado estado de portador, por lo que el tratamiento en este caso debe ser sintomático, reservándose los antibióticos para enfermedad severa, pacientes inmunodeprimidos o edades extremas.
Las FQ de segunda generación (ciprofloxacina o norfloxacina) son de elección para el tratamiento de la diarrea del viajero, pues son activas contra las etiologías más frecuentes: Salmonella, Shigella, E. coli enteropatógeno, Campylobacter spp., Vibrio spp., Yersinia enterocolitica, Aeromonas hydrophila. Tienen poca actividad contra Helicobacter pylori y no son activas contra Clostridium difficile. Para la diarrea del viajero se indican ciprofloxacina, norfloxacina u ofloxacina por 3 días. Las nuevas quinolonas aun no fueron suficientemente estudiadas para esta aplicación.
- Infecciones respiratorias

Las quinolonas de segunda generación no deben indicarse para el tratamiento empírico de neumopatías agudas comunitarias, donde S. pneumoniae es la causa más frecuente, ya que son poco activas contra este germen. Pueden ser útiles en el tratamiento de neumopatías hospitalarias cuando se sospecha o se conoce que el agente es un bacilo gramnegativo.
En algunos países, las más nuevas quinolonas con actividad antineumococo (esparfloxacina, trovafloxacina, levofloxacina o moxifloxacina) fueron incluidas en los planes de tratamiento empírico inicial de neumopatías agudas comunitarias. Ello se basa en que son activas contra prácticamente todos los gérmenes que causan neumopatías agudas (incluyendo gérmenes "atípicos", anaerobios y S. pneumoniae resistente) y son fáciles de administrar. Esta indicación debiera reservarse para comunidades con tasa elevada de S. pneumoniae con resistencia de alto nivel a betalactámicos.
Con el fin de evitar el surgimiento de cepas resistentes se aconseja usar estas quinolonas con prudencia, reservándolas para casos especiales: fracaso de tratamiento, alergia a betalactámicos, alta resistencia del neumococo comprobada (CIM no menor de 4 mg/l).
The Food and Drug Administration (FDA) Anti-Infectives Subcomite recientemente aprobó la levofloxacina para el tratamiento de la neumonia causada por S. pneumoniae resistente a la penicilina.
La FDA también aprobó el uso de ciprofloxacina, levofloxacina y moxifloxacina para tratar las exacerbaciones de bronquitis crónicas, aunque es importante volver a recordar la escasa actividad de ciprofloxacina frente a S. pneumoniae y lo ya aconsejado en cuanto a la prudencia en el uso de las FQ de última generación.
- Infecciones óseas y articulares
S. aureus continúa siendo el microorganismo más prevalentemente aislado en las osteomielitis hematógenas, especialmente de huesos largos, en jóvenes sanos. También los bacilos gramnegativos están frecuentemente en la causa de la espondilodiscitis de los adultos. Cuando la osteomielitis es secundaria a un foco contiguo suelen aislarse diferentes microorganismos del hueso infectado: S. aureus, bacilos gramnegativos y anaerobios.
Debido a que los planes terapéuticos deben ser prolongados, los agentes orales facilitan el tratamiento. Las quinolonas pueden cumplir este rol en razón a su espectro de actividad, eficacia y buena penetración en hueso. Además suelen ser bien tolerados, aun en tratamientos prolongados. Los fracasos en el tratamiento se relacionan con: debridamiento incompleto, presencia de cuerpos extraños, desarrollo de resistencia, especialmente de S. aureus, P. aeruginosa o Serratia marcescens. Como las más recientes quinolonas tienen mayor actividad contra Staphylococcus, es de esperar mejores resultados.
- Infecciones de piel y de tejidos blandos
Aunque los agentes etiológicos más comunes de la celulitis y la piodermitis son Streptococcus pyogenes y S. aureus, los pacientes diabéticos, con enfermedad vascular, éscaras de decúbito y heridas quirúrgicas, pueden presentar infecciones de tejidos blandos por una asociación bacteriana donde además participan: aerobias gramnegativas y anaerobias. En estos grupos de pacientes, las quinolonas, solas o asociadas, resultan eficaces.
- Infecciones sexualmente transmitidas.
Ciprofloxacina es adecuada para el tratamiento de enfermedad gonocócica no complicada (uretritis, cervicitis, proctitis, faringitis), aunque ya se han descrito cepas resistentes. También es activa frente a Haemophilus ducrey, agente de chancroide, infección rara en nuestro medio.
Ofloxacina es la única quinolona fluorada con buena actividad frente a Chlamydia trachomatis y se utiliza para el tratamiento de infecciones, incluso enfermedad inflamatoria pélvica. No se dispone de la misma en nuestro medio.
- Otros usos
Infecciones ginecológicas (anexitis, endometritis y salpingitis); en estos casos deben asociarse a metronidazol dada su poca actividad frente a anaerobios, sobre todo Bacteroides fragilis.
El uso de quinolonas para el tratamiento de la endocarditis es limitado. Ciprofloxacina asociada a rifampicina, ambas por vía oral, son una alternativa para el tratamiento de endocarditis infecciosa derecha por S. aureus en usuarios de drogas i. v., cuando su capital venoso es insuficiente o no toleran una permanencia prolongada en el hospital, debiendo tratarse en domicilio.
Ciprofloxacina 500 mg en dosis única puede ser empleada para la profilaxis de los contactos de meningitis meningocóccica.
Las quionolonas son activas contra algunas ETS producidas por Neisseria gonorrhoeae, Chlamydia trachomatis y Haemophilus ducrey, pero no contra Treponema pallidum.
Cervicitis, uretritis, faringitis e infecciones perirrectales gonocóccicas no complicadas pueden tratarse con una única dosis de 250 a 500 mg de ciprofloxacina, 400 mg de ofloxacina o 800 mg de norfloxacina. Pero no se recomiendan en adolescentes.

Para tratar infecciones por Chlamydia trachomatis, la única quinolona aprobada por el CDC es la ofloxacina, en un curso de 7 días.
TRIMETOPRIM –SULFAMETOXAZOL (TMP-SMX)
El trimetoprim es un derivado diaminopirimidínico, utilizado inicialmente para combatir plasmodios, que revitalizó a las sulfas, al demostrarse que administrados conjuntamente tenían eficaz acción bactericida sobre un número considerable de cepas bacterianas. La introducción del trimetoprim en combinación con el sulfametoxazol constituyó un progreso importante y representó la aplicación práctica de una consideración teórica, es decir, si dos fármacos actúan en fases seriadas en la vía de una reacción enzimática obligada en bacterias, el resultado de la combinación sería la sinergia. En muchos países, se conoce dicha combinación como cotrimoxazol.
Espectro antibacteriano. El espectro antibacteriano del trimetoprim es semejante al del sulfametoxazol, aunque el primero tiene una potencia de 20 a 100 veces mayor que el segundo. Casi todos los microorganismos gramnegativos y grampositivos son sensibles al trimetoprim, pero puede surgir resistencia si se utiliza cada uno en forma independiente.
Pseudomonas aeruginosa, Bacteroides fragilis, T. pallidum, M. tuberculosis, M. leprae, ricketssias y enterococos por lo común son resistentes.
Son sensibles al trimetoprim-sulfametoxazol: estafilococos, estreptococos, diplococos, klebsiella, proteus, salmonella, shigella, brucella, neiseria, E. coli, H. influenza y otros.
Microorganismos sensibles al TMP-SMX Patógenos respiratorios Streptococcus pneumoniae
Haemophilus influenzaeMoraxella catarrhalisPneumocystis carinii
Patógenos del tracto urinario Escherichia coliMorganella morgagniProteus mirabilisKlebsiella pneumoniaeEnterobacter spp.
Patógenos del tracto gastrointestinal Escherichia coli enterotoxigénicoSalmonella typhiShigella spp.Vibrio choleraeYersinia enterocoliticaIsospora belliCyclospora
Otros patógenos ListeriaNocardiaMycobacterium marinum
Mecanismo de acción. Esta combinación, sulfametoxazol (sulfonamida) y trimetoprim, atacan a los gérmenes sensibles, afectando la síntesis de ácido fólico de la bacteria que es vital para su crecimiento. En la síntesis, se utiliza como sustrato el ácido para-aminobenzoico (PABA), el que por acción de la sintetasa de dihidropteroato se une a la pteridina para formar el ácido didropteroico un sustrato previo en la síntesis del folato. El sulfametoxazol, específicamente compite con el PABA e inhibe dicha sintetetasa dando origen a análogos no funcionales que entorpecen el crecimiento ulterior de la bacteria. El trimetoprim afecta a las bacterias en otro momento progresivo de su actividad biológica: inhibe la enzima dihidrofólico reductasa e impide la síntesis de tetrahidrofolato, sustrato indispensable para la síntesis de las purinas y en último término de los ácidos nucleicos bacterianos (DNA).
Este particular mecanismo de acción de las combinaciones sulfonamida-trimetoprim, no solo amplia el espectro bacteriano ejercido por cada componente individual, sino que ejercita actividad bactericida. Además cabe advertir que trimetoprim puede activar también a la enzima dihidrofólico reductasa humana ocasionando severos efectos indeseables, ventajosamente ello no ocurre, ya que se requieren concentraciones 100.000 veces superiores para inhibir la enzima humana, respecto a la necesaria para inhibir la bacteriana.
Cuadro sobre el mecanismo de acción:
Resistencia bacteriana. La resistencia bacteriana al trimetoprim-sulfametoxazol es un problema que está aumentando con rapidez, aunque es menor en relación con la administración de uno u otro de los fármacos solos.
Los mecanismos implicados que se han descrito son:
1. Sobreproducción de dihidrofolato-reductasa.

2. Reducción de la permeabilidad bacteriana al TMP.
3. Producción de dihidrofolato reductasa sin afinidad al TMP (por mutación genética plasmídica). Este mecanismo confiere alto nivel de resistencia.
El mecanismo de resistencia más importante por su frecuencia y consecuencias es este último. La prevalencia global de resistencia bacteriana al TMP-SMX se ha venido incrementando desde los años 80, observándose altos porcentajes de resistencias (40%) entre las cepas aisladas de Escherichia coli en países desarrollados. Este hecho ha determinado una disminución notable del uso de esta asociación.
La aparición de resistencia es un problema para el tratamiento de muchas infecciones bacterianas, como ocurre en pacientes con SIDA que reciben el fármaco para profilaxia de neumonía por Pneumocystis carinii.
Absorción, distribución y excreción. Después de ingerir una sola dosis de la combinación TMP-SMX, el trimetoprim se absorbe con mayor rapidez que el sulfametoxazol, al parecer el primero torna lenta la absorción del sulfametoxazol. Por lo común, en término de 2 h se alcanzan cifras máximas de trimetoprim en sangre en casi todos los enfermos, en tanto que las de sulfametoxazol se logran unas 4 h después de una sola dosis oral. Las vidas medias son de alrededor de 11 y 10 horas, respectivamente. Las concentraciones en sangre de SMX-TMP alcanzan una proporción constante de 20:1. Cuando se administran 800 mg de sulfametoxazol con 160 mg de trimetoprim (la proporción habitual de 5:1) dos veces al día, las concentraciones máximas de ambos en plasma son de 40 y 2 g/ml, que son lasμ óptimas.
El trimetoprim se distribuye y concentra rápidamente en tejidos y, en promedio, 40% queda ligado a proteínas plasmáticas en presencia de sulfametoxazol. El fármaco penetra fácilmente en líquido cefalorraquídeo y esputo; en bilis también se identifican concentraciones grandes de cada componente. En promedio, 65% del sulfametoxazo1 está ligado a proteínas plasmáticas.
Aproximadamente 60% del trimetoprim y 25 a 50% del sulfametoxazol administrados se excretan por la orina en término de 24 h. Se ha observado que 66% de la sulfonamida no está conjugada. También se excretan metabolitos del trimetoprim. Las velocidades de excreción y las concentraciones de ambos compuestos en orina disminuyen de manera significativa en personas con uremia.
Efectos adversos. No hay datos de que la administración de trimetoprim-sulfametoxazol a las dosis recomendadas induzca deficiencia de folato en personas normales; salvo cuando las células del paciente muestran deficiencia de folato.
Reacciones hematológicas: En los déficits de folato, puede causar megaloblastosis, leucopenia o trombocitopenia.
Además de las mencionadas, se incluyen varios tipos de anemia (aplásica, hemolítica y macrocítica); trastornos de la coagulación, granulocitopenia, agranulocitosis, púrpura de Henoch-Schonlein y sulfahemoglobinemia.
Reacciones dermatológicas e hipersensibilidad: En promedio, 75% de los efectos adversos se manifiesta en piel; como ya se describió, estos son los datos característicos generados por sulfonamidas. Sin embargo, se ha señalado que trimetoprim-sulfametoxazol causa incluso tres veces más reacciones dermatológicas que el sulfisoxazol solo (5.9% en comparación con 1.7%). La dermatitis exfoliativa, el síndrome de Stevens-Johnson y la necrólisis epidérmica tóxica (síndrome de Lyell) son reacciones infrecuentes y afectan más bien a personas de edad avanzada.
Gastrointestinales: La náusea y el vómito son las reacciones gastrointestinales más habituales y la diarrea es infrecuente. La glositis y estomatitis son relativamente comunes. A veces surge ictericia leve y transitoria y al parecer posee las características histológicas de la hepatitis colestásica alérgica.
Neurológicas: Las reacciones del sistema nervioso central consisten en cefalea, depresión y alucinaciones que se sabe son producidas por sulfonamidas.
Renales: Puede haber perturbación permanente de la función renal con el uso de trimetoprim-sulfametoxazol en personas con ne-fropatía, y en individuos con función renal normal se ha observado una disminución reversible en la depuración de creatinina.
Aplicaciones terapéuticas
Infecciones de vías urinarias. Una sola dosis (320 mg de trimetoprim y 1600 mg de sulfametoxazol en adultos) ha sido eficaz en algunos casos de infecciones agudas no complicadas de vías urinarias, pero probablemente se necesita un mínimo de tres días de administración para lograr eficacia.
La combinación al parecer muestra eficacia especial en infecciones crónicas y recurrentes de vías urinarias. Quizá resulten eficaces dosis pequeñas (200 mg de sulfametoxazol y 40 mg de trimetoprim diariamente, o dos a cuatro veces dichas dosis, una o dos veces por semana) para disminuir el número de infecciones recurrentes en vías urinarias en adultos. También se han observado niveles

terapéuticos de trimetoprim en las secreciones prostáticas y la combinación con sulfametoxazol es eficaz para combatir la prostatitis bacteriana.
ESQUEMAS TERAPÉUTICOS PARA ADULTOS CON INFECCIÓN URINARIA
SÍNDROME DURACIÓN VIA DE ADMINISTRAC.
FÁRMACOS DOSIS * (mg)
INTERVALO
Cistitis, mujeres no complicadas
Tres días(3 días)
VO TMP-SMX 160/800 c/12h
Cistitis complicada
10-14 días(Diez a
catorce días)
VO TMP-SMX 160/800 c/12h
Prostatitis aguda
4 semanas(Cuatro
semanas)
VO TMP-SMX 160/800 c/12h
Prostatitis crónica
6-12 semanas(Seis a doce
semanas)
VO TMP-SMX 160/800 c/12h
Pielonefritis, ambulatoria
14 días(Catorce días)
VO TMP-SMX 160/800 c/12h
Infecciones bacterianas de vías respiratorias. El trimetoprim-sulfametoxazol es eficaz en exacerbaciones agudas de bronquitis crónica; no debe utilizarse para tratar la faringitis por estreptococos porque no los erradica, pero es eficaz en otitis media aguda en niños; y, sinusitis maxilar superior aguda en adultos, causada por cepas sensibles de H. influenzae y S. pneumoniae.
Infecciones de tubo digestivo. La combinación que se señaló puede administrarse para combatir la shigelosis. También es un fármaco de segunda elección (los medicamentos preferidos son ceftriaxona o una fluoroquinolona) contra la tifoidea en adultos (a dosis de 800 mg sulfometoxazol, y de 160 mg de trimetoprim cada 12 h, durante 15 días).
La combinación mencionada al parecer es eficaz en el tratamiento de portadores de cepas sensibles de Salmonella typhi y otras especies de Salmonella, en igual dosis a la señalada pero, durante tres días; sin embargo, hay datos de su ineficacia. La diarrea aguda por cepas sensibles de E. coli enteropatógena puede evitarse o tratarse con la combinación de los dos fármaco. Sin embargo, la antibioterapia (con trimetoprim-sulfametoxazol o con cefalosporina) de la enfermedad diarreica debida a E. coli O157:H7 enterohemorrágica puede au-mentar el riesgo de síndrome hemolítico-urémico, quizá al incrementar la liberación de toxinas de Shiga por las bacterias.
Infección por Pneumocystis carinii. La combinación de dosis altas de los dos fármacos (trimetoprim, 20 mg/kg de peso/día y sul-fametoxazol, 100 mg/kg de peso/día en tres o cuatro dosis) es eficaz contra la infección grave por el microorganismo mencionado en sujetos con síndrome de inmunodeficiencia adquirida. El tiempo de la terapéutica o la profilaxia depende de la gravedad del síndrome.
Profilaxia en enfermos neutropénicos. Se observó protección notable contra la sepsis por bacterias gramnegativas al usar la com-binación (800 mg de sulfametoxazol más 160 mg de trimetoprim) dos veces al día, en individuos fuertemente neutropénicos. La apa-rición de bacterias resistentes puede limitar el uso de la mezcla como profiláctico en la proporción mencionada.
Presentaciones del Trimetoprim-Sulfametoxazol
SUSPENSIÓN TMP-SMX TABLETAS TMP-SMX5 mL: 40/200 mg 80/400 mg
160/800 mg
ANTISÉPTICO Y ANALGÉSICO EN INFECCIONES DE VÍAS URINARIAS
Los antisépticos de vías urinarias inhiben la proliferación de muchas especies de bacterias; no se utilizan para tratar otras infecciones porque con las dosis comunes no se alcanzan concentraciones eficaces en plasma. Sin embargo, dado que estas sustancias se con-centran en túbulos renales alcanzando concentraciones terapéuticas adecuadas en vías urinarias, se usan por vía oral para combatir infecciones de vías urinarias. Nitrofurantoína. La nitrofurantoína (FURADANTIN, MACROBID, UVAMIN, otros) es un nitrofurano sintético que se utiliza para evitar y tratar infecciones de vías urinarias exclusivamente, con poco o nulo efecto antibacteriano sistémico.
Mecanismo de acción: No se conoce exactamente. La presencia de enzimas bacterianas (reductasas), son de gran importancia para su activación, generando productos fuertemente reactivos de la nitrofurantoína que lesionan el ADN de los gérmenes susceptibles que inhiben de esta manera la síntesis proteica en estos. Existe una relación inversamente proporcional entre los niveles de estas reductasas de los gérmenes susceptibles y la concentración inhibitoria mínima del fármaco (CMI).
CMI = 1/Niveles de reductasas
A mayor nivel de reductasas menor concentración inhibitoria mínima y viceversa.

Actividad antimicrobiana. La nitrofurantoína es activa contra muchas cepas de E. coli y enterococos. Sin embargo, casi todas las especies de Proteus y Pseudomonas y muchas de Enterobacter y Klebsiella son resistentes. Este medicamento es bacteriostático contra casi todos los microorganismos sensibles, a concentraciones de 32 g/ml o menos y es bactericida a concentraciones > 100 g/ml. Laμ μ actividad antibacteriana es mayor en orina ácida.
Farmacología y toxicidad. La nitrofurantoína oral se absorbe en forma rápida y completa en vías gastrointestinales. La variante macrocristalina se absorbe y excreta con mayor lentitud. No se alcanzan concentraciones plasmáticas antibacterianas después de ingerir las dosis recomendadas porque el medicamento se elimina con rapidez. La vida media plasmática es de 0.3 a 1 hora, y en promedio 40% del producto se excreta por la orina sin modificaciones. La dosis promedio de nitrofurantoína genera una concentración en orina de 200
g/ml, aproximadamente, y tal cantidad es soluble a pH mayor de 5, pero la orina no debe alcalinizarse porque disminuye la actividadμ del antimicrobiano. La actividad de la nitrofurantoína es nula a un pH de 8 o mayor. La velocidad de excreción guarda relación directa con la eliminación de creatinina, de manera que en individuos con función glomerular deficiente puede disminuir la eficacia del fármaco y aumentar la toxicidad sistémica. La nitrofurantoína da a la orina un color pardo, que debe advertírsele al paciente.
Los efectos adversos más frecuentes son náusea, vómito y diarrea; la preparación macrocristalina es mejor tolerada. A veces se observan diversas reacciones de hipersensibilidad que incluyen escalofríos, fiebre, leucopenia, granulocitopenia, anemia hemolítica [relacionada con deficiencia de deshidrogenasa de glucosa-6-fosfato], ictericia colestática y daño hepatocelular. La hepatitis crónica activa es un efecto adverso infrecuente pero grave. La neumonía aguda con fiebre, escalofríos, tos, disnea, dolor retro esternal, infiltración de campos pulmonares y eosinofilia pueden surgir en término de horas o días de haber emprendido el tratamiento, aunque este cuadro muestra involución horas después de interrumpir el uso del fármaco. A veces, también ocurren reacciones subagudas más insidiosas y, en individuos que emplean el medicamento por tiempo prolongado, llega a presentarse fibrosis pulmonar intersticial que al parecer se debe a la generación de radicales de oxígeno como consecuencia del ciclo redox del medicamento en pulmón. Los ancianos son especialmente sensibles a la toxicidad de la nitrofurantoína en pulmones. La anemia megaloblástica es infrecuente. Se han observado diversos cuadros neurológicos de modo ocasional. Cefalalgia, vértigo, somnolencia, mialgias y nistagmo suelen ser fácilmente reversibles, pero se han señalado casos de polineuropatías graves con desmielinización y degeneración de nervios sensitivos y motores; el resultado comprende signos de desnervación y atrofia muscular. Hay mayor posibilidad de que surjan las neuropatías en personas con deficiente función renal y en quienes reciben el fármaco por mucho tiempo. Algunas reacciones adversas pueden ser causadas por metabolitos reactivos tóxicos.
La dosis de nitrofurantoína oral en adultos es de 50 a 100 mg cuatro veces al día, con los alimentos y a la hora de acostarse. Otro régimen diario sería 5 a 7 mg del fármaco/kg de peso en cuatro fracciones (que no rebase 400 mg). A veces basta una sola dosis de 50 a 100 mg a la hora de acostarse para evitar recidivas. La dosis diaria para niños es de 5 a 7 mg/kg de peso, pero puede llegar a 1 mg/kg de peso en la terapéutica a largo plazo.
El ciclo terapéutico no debe exceder de 14 días y la repetición de los ciclos ha de estar separada por periodos sin uso del medicamento. No deben recibir nitrofurantoína las personas con deficiencia de la función renal (depuración de creatinina menor de 40 ml/min) y niños menores de un mes de edad.
La nitrofurantoína ha recibido aprobación únicamente para el tratamiento de infecciones de vías urinarias causadas por microor-ganismos con sensibilidad probada a ella. En la actualidad, la resistencia bacteriana a nitrofurantoína es más frecuente que la resistencia a las fluoroquinolonas o al trimetoprim-sulfametoxazol, lo que la hace un fármaco de segunda línea para la terapéutica de infecciones de las vías urinarias. La nitrofurantoína tampoco se recomienda para el tratamiento de pielonefritis o prostatitis; sin embargo, es eficaz para la profilaxia de infecciones recurrentes de las vías urinarias.
Presentación:
Genérico ComercialNitrofurantoínaTabletas o cápsulas de 50 y 100 mg
Uvamin retardCápsulas de 100 mg
Para tratar las infecciones recurrentes asociadas a malformaciones de las vías urinarias, se han empleado los siguientes esquemas:
FÁRMACO DOSIS
Trimetoprim-Sulfametoxazol 1-10 mg/kg/día
Nitrofurantoína 1-2 mg/kg/día
Aplicar por periodos de 6-12 meses hasta desaparecer la recidiva
Fenazopiridina. El clorhidrato de fenazopiridina (PIRUDIUM, otros) no es un antiséptico urinario ni un antibiótico; sin embargo, posee una acción analgésica en vías urinarias y alivia síntomas de disuria, polaquiuria, ardor y urgencia para la micción. La dosis usual es de 200 mg tres veces al día. Es un compuesto de colorantes azoicos y da a la orina un color naranja o rojo, de manera que resulta prudente anunciárselo al paciente. Hasta en 10% de los enfermos se presentan alteraciones en vías gastrointestinales y pueden

reducirse al administrar el fármaco con los alimentos; la dosis excesiva ocasiona metahemoglobinemia. La fenazopiridina también se combina con sulfisoxazol y sulfametoxazol, ampicilina, etc.
Precauciones: Su uso se debe evitar durante el embarazo y probablemente también en las madres lactantes.
Diccionario MOSBY
Patogenia
Inglés: pathogenesisDefinición:
Fuente o causa de una enfermedad o trastorno.
Colonización Inglés: colonizationDefinición:
Presencia y multiplicación de microorganismos sin lesión o invasión tisular.
Epidemiología Inglés: epidemiologyDefinición:
Estudio de la presentación, distribución y causas de las enfermedades humanas.
Anatomía patológica Inglés: pathologic anatomyDefinición:
(en anatomía aplicada) estudio de la estructura y morfología de los tejidos y de las células del cuerpo en relación con la enfermedad.
Dispareunia Inglés: dyspareuniaDefinición:
Trastorno de la mujer, en el que la relación sexual se acompaña de dolor. El dolor puede ser el resultado de anomalías genitales, reacciones psicofisiológicas disfuncionales ante la unión sexual, coito forzado o excitación sexual incompleta.
Etiología Inglés: etiologyDefinición:
1. estudio de todos los factores implicados en el desarrollo de una enfermedad, incluyendo la susceptibilidad del paciente y la naturaleza de la enfermedad. 2. causa de una enfermedad.
Vejiga neurógena Inglés: neurogenic bladderDefinición:
Vejiga urinaria disfuncionante por causa de una lesión del sistema nervioso central. Su tratamiento está dirigido a permitir que la vejiga se vacíe por completo y de forma regular, evitando la infección, controlando la incontinencia y conservando la función renal. Algunos tipos de vejiga neurógena son: vejiga espástica, vejiga flácida y vejiga refleja.
Caseoso Inglés: caseousDefinición:
Semejante al queso; término que describe la mezcla de grasas y proteínas que aparece en algunos tejidos corporales que experimentan necrosis.
BIBLIOGRAFÍA:
Medicina Interna de Farreras-Rozman. 14ª edición.

Enfermedades Infecciosas de Reese-Beets
Dra. Mariela Vacarezza
Uso Racional de Antibióticos. Guía 5-8
Las Bases Farmacológicas de la Terapéutica. Goodman&Gilman. Décima Edición.
Farmacología Humana. Director: Jesús Flores. 3ª edición.
Diccionario de Especialidades Farmacéuticas. Thomson. PLM.
Diccionario Mosby
Farmacología Médica. LA. Malgor. M. E. Valsecia.
Temas de Medicina Interna. Reinaldo Roca Goderich. 4ª edición.