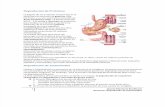
Aminoacidos
-
Upload
claudia-l-perez -
Category
Documents
-
view
96 -
download
3
description
Transcript of Aminoacidos
-
AMINOCIDOS
DRA. SANDRA LUZ CABRERA HILERIO
-
DefinicinSon las unidades estructurales bsicas de las protenas
Son compuestos orgnicos formados por Carbono, Nitrgeno, Oxgeno eHidrgeno (algunos poseen Azufre).
Los aminocidos reciben este nombre porque presentan los gruposfuncionales Amino (NH3+) y carboxilo (COO-); algunos autores los definen
como derivados aminados de cidos carboxlicos.
Con esta definicin podemos encontrar cientos de compuestos, sin embargonos limitaremos a estudiar a los llamados -aminocidos, denominados as
porque el amino y el carboxilo estn unidos al mismo carbono.
-
Funciones
A)Monmeros proteicos
Las funciones que cumplen los aminocidos
en un organismo son variadas siendo la ms
importante la de formar protenas.
Aminocidos para sntesis de protenas Precursores de otras molculas no proteicas
de importancia biolgica
Como los Neurotransmisores Donadores de Nitrgeno para otras
molculas no proticas
Fuente de energa cuando los combustibles usuales (carbohidratos y lpidos) no estn
disponibles
-
FUNCIONES
Las funciones que cumplen los aminocidos en un organismo son
variadas siendo la ms importante la de formar protenas.
Aminocidos para sntesis de protenas Precursores de otras molculas no proteicas de
importancia biolgica
Donadores de Nitrgeno para otras molculas noproticas
Fuente de energa cuando los combustibles usuales(carbohidratos y lpidos) no estn disponibles
-
Estereoqumica
Con la excepcin de la glicina, en los 19 aminocidos restantes
tienen el carbono- asimtrico, lo que les confiere actividadptica; esto es, sus disoluciones desvan el plano de polarizacin
cuando un rayo de luz polarizada las atraviesa.
Un aminocido puede en principio existir en sus dos formas
enantiomricas (una dextrgira y otra levgira), pero en lanaturaleza lo habitual es encontrar slo una de ellas.
-
Los aminocidos presentan una disposicin espacial especfica y es la
denominada L (en orgnica S) para entender esta forma tomaremos como
ejemplo a un aminocido, la Serina
(a) A cada grupo unido al
carbono (quiral) se le asigna
un valor considerando su peso
atmico, siendo 4 el ms alto
(b) Se orienta la molcula con el grupo de
mayor prioridad -4- hacia atrs del carbono
quiral y se traza un crculo del ms pequeo
al ms grande; si seguimos el sentido de las
manecillas del reloj se dice que el compuesto
es D (en orgnica R) si va en el sentido
contrario de las manecillas se dice que es L.
-
FORMA INICA
Dada la proximidad de los grupos amino y carboxilo se influyen
mutuamente haciendo que se ionicen y as los aminocidos se
encuentran en forma de Zwitterin.
-
Clasificacin
Por ser formadores de
Protenas
Protenas No protecos Poco frecuentes
Por su funcin que realizan
en la protena
Esenciales No esenciales
Por su sntesis en los
organismos
Dispensables Indispensables
Por la polaridad del radical (R) a ph=7.0
No Polares
sin carga
Polares carga positiva (bsicos)con carga
carga negativa (cidos)
-
Aminocidos NO polares
-
Aminocidos polares sin carga
-
Aminocidos con carga negativa (cidos)
-
Aminocidos polares con carga positiva (bsicos)
-
AMINOCIDOS POCO FRECUENTES
(Slo se encuentran en algunas protenas)
-
(No se encuentran en protenas, pero cumplen funciones
especficas en el organismo)
AMINOCIDOS NO PROTEICOS
-
Segn su capacidad de sntesis
Aminocidos esenciales o indispensables: los organismos
superiores no los sintetizan, es necesario incluirlos en la
dieta.
Valina (Val)Leucina (Leu)Metionina (Met)Triptfano (Trp)Histidina (His)*Treonina (Thr)Lisina (Lys)Isoleucina (Ile)Arginina (Arg)*Fenilalanina (Phe)
-
Alanina (Ala)Prolina (Pro)Glicina (Gly)Serina (Ser)Cistena (Cys)Asparagina (Asn)Glutamina (Gln)Tirosina (Tyr)cido asprtico (Asp)cido glutmico (Glu)
A los aminocidos que pueden ser sintetizados por el
cuerpo se los conoce como no esenciales y son:
-
Propiedades cido - Bsicas de los aminocidos
A pH neutro: iones dipolares (zwitterion)
El grupo amino: NH3+
El grupo cido: COO-
Son anfteras
Comportamiento anfotrico
-
PUNTO ISOELCTRICOpH para el cual el 100% del aminocido se
encuentra en estado de zwitterion (sin carga neta)
pH para el cual el 50% del aminocido se encuentra en forma de
zwitterion y el 50% con carga (-)
pH para el cual el 50% del aminocido se encuentra en forma de
zwitterion y el 50% con carga (+)
-
Ka indicar cuan fcilmente se disocia el cido, esto es, su fuerza, pero al serestos valores muy pequeos, se emplea la escala logartmica, con lo que se
obtiene el valor del exponente de la base 10,pero cambiado de signo, esto es
la pKa y se define como -log de Ka.
Por tanto indica lo mismo,la fuerza del cido, pero de un modo ms sencillo.
Por ejemplo si Ka = 10 ^-1,pKa = 1.
http://www.ehu.es/biomoleculas/buffers/buffer3.htm
-
Valores de pK de los aminocidos formadores de protenas