Tema 15 INHIBICIÓN ENZIMÁTICA I
description
Transcript of Tema 15 INHIBICIÓN ENZIMÁTICA I

Tema 15 INHIBICIÓN ENZIMÁTICA I
1. Introducción
2. Inhibición reversible2.1 Inhibición competitiva (inhibición específica)2.2 Inhibición no-competitiva2.3 Inhibición incompetitiva o acompetitiva2.4. Representación de Dixon2.5 Inhibición por sustrato

Las sustancias que disminuyen la velocidad de reacción, química o enzimática, se denominan inhibidores.
Los inhibidores se pueden dividir en tres grandes grupos:
- Inhibidores reversibles, - Inhibidores pseudorreversibles- Inhibidores irreversibles
1. IntroducciónDesde el principio de la Enzimología se sabia de sustancias que
disminuían la velocidad de la reacción catalizada por los catalizadores, “envenenando” o dificultando la actuación de
éstos.

INHIBIDORES REVERSIBLES la unión del inhibidor a la enzima es débil.
INHIBIDORES PSEUDOIRREVERSIBLES la unión del inhibidor a la enzima es fuerte.
INHIBIDORES IRREVERSIBLES la unión del inhibidor a la enzima es prácticamente irreversible, generalmente covalente (inhibidores suicidas).

2. INHIBICIÓN REVERSIBLE
Los inhibidores reversibles son sustancias que forman complejos “dinámicos” o reversibles con la enzima ( interacciones de tipo débil) y que presentan propiedades
catalíticas diferentes a las de la enzima libre.
Cumplen las condiciones impuestas al Substrato para la deducción de la ecuación cinética de M&M:
La concentración inicial de inhibidor [Io] >> [Eo]

que para resolver la ecuación de velocidad en presencia de inhibidor,
[EI] o [ESI] es despreciable frente a la de [Io].
Por lo tanto, en todo momento, [I] = [Io]Por otra parte, la formación de los complejos EI o ESI es muy
rápida, de forma que se alcanza rápidamente el siguiente equilibrio:
E + I <=====> EIy podemos definir la constante de disociación del complejo EI:
[E] [I] Ki = ------------ [EI]

Donde. [E] concentración de enzima libre
[I] concentración de inhibidor libre [EI] concentración del complejo EI
-Así mismo, debemos tener en cuenta:
i) que la actividad de la enzima se afecta por la presencia del inhibidor
ii) que las velocidades medidas son velocidades iniciales
iii) que estamos en una situación de estado estacionario
Consecuentemente, la concentración de las diferentes especies químicas en que puede encontrarse la enzima: [E],
[ES], [EI] y en su caso [ESI] son constantes respecto del tiempo, d[EX]/dt = 0.

Si la enzima, a concentraciones saturante de inhibidor, no presenta actividad catalítica alguna (v = 0) se dice que la
inhibición es completa o total.
Sin embargo, frecuentemente nos referimos a este tipo de inhibición como inhibición lineal, ya que la representación de Kmap/Vmaxap o de 1/Vmaxap frente a [I] nos da una linea recta.
Con menor frecuencia está el caso en que el complejo EI sí presenta cierta actividad catalítica residual (v 0) a
concentraciones saturantes de inhibidor.
Este tipo de inhibición se conoce como inhibición parcial, o inhibición hiperbólica, ya que la curva resultante al representar
Kmap/Vmaxap o 1/Vmaxap frente a la [I], nos da una curva hiperbólica.

* Ambos tipos de inhibición, lineal e hiperbólica, pueden a su vez subclasificarse de acuerdo con los parámetros cinéticos
aparentes de Michaelis-Menten que se vean afectados, si bien, en lo que sigue, nos referiremos principalmente a la inhibición lineal.
* La inhibición por inhibidores reversibles lineales, tradicionalmente, y de acuerdo con el mecanismo de reacción,
se suele clasificar en tres grupos:
- Inhibición competitiva --> Inhibidores competitivos
- Inhibición no-competitiva --> Inhibidores no-competitivos
- Inhibición acompetitiva --> Inhibidores acompetitivos

2.1. Inhibición competitiva2.1. Inhibición competitiva
En la inhibición competitiva o inhibición específica, el inhibidor compite con el sustrato por el mismomismo centro activo
de la enzima. La molécula del inhibidor es, generalmente, en todo o en parte, un isóstero del sustrato, excluyendose mutuamente del centro
activo de la enzima.Isóstero --> Moléculas que tienen formas y tamaños similares


Km kcat
E + S <====> ES ----------> E + P
EI -------->
<==
===>
I Kic
- Así pues, la enzima total, Eo, puede estar como enzima libre, E, unida al sustrato formando el complejo-ES, ES o como enzima
unida al inhibidor formando el complejo-EI, (EI).
- Y de acuerdo con la ecuación de conservación de masas podemos escribir:
Pero solamente el complejo ES puede dar producto.

[Eo] = [E] + [ES] + [EI]
El valor de la [ES] lo podemos obtener a partir de la cte de Michaelis:
[E] [S] Km = ------------
[ES]
[E] [S] [ES] = ----------- Km
Y análogamente, el valor de la [EI] lo podemos obtener a partir de la definición de la constante de disociación del complejo EI:
Kic
Vic = kcat [ES]Velocidad inicial en presencia de inhibidor competitivo

[E] [I] Kic = ------------
[EI]
[E] [I] [EI] = ------------
Kic Sustituyendo estos valores en la ec. de balance de masas,
tenemos:
Eo = E + ES + EI
[E] [S] [E] [I] [Eo] = [E] + ------------ + ------------ Km Kic

Valor de la Enzima libre
KmS
KmS
KiIEoES
1
1
KmS
KiIEoE
1
1
SKiIKmKm
SVKmS
KmS
KiIkcatEovic
max
1
1
[E] [S] [ES] = ----------- Km Vic=Kcat [ES]
SKiIKm
SVvic
1
max
Ecuación representa el comportamiento cinético de un inhibidor competitivo puro

Así pues, la velocidad de reacción inicial, en presencia de inhibidor competitivo vendrá dada por la ecuación:
[S] vic = Vmax ----------------- [S] + Kmap - Ecuación semejante a la ec. de M&M, pero donde el valor de
Kmap depende de la concentración del inhibidor (I) y de la cte de inhibición Kic.
* En este tipo de inhibición reversible, los valores de las ctes de inhibición, Kic, suelen ser del mismo orden que las Km. Oscilando
entre 10-3 y 10-6 M.
KicIKmKmap 1

- Algunos inhibidores de este tipo suelen tener aplicaciones medico-farmacéuticas.
¿Cuáles serán los mejores? aquellos que tengan un valor de Ki pequeño
* En estos casos, además de interesante, es necesario determinar el valor IC50 o concentración de inhibidor que en unas
condiciones dadas produce una inhibición del 50%.
Cálculo del grado de inhibición, i:
KmSKicI
Ii
1
Grado de inhibición es un valor entre 0-1Razón entre la velocidad en presencia de I y en ausencia.
aVVica
ic
1
a
Tarea Calcúlalo

- El análisis de la ec. anterior nos indica que el valor del grado de inhibición, i, depende:
i) de la concentración de inhibidor, [I];
ii) del valor de la Kic;
iii) de la concentración de sustrato, [S]
iv) de la constante de Michaelis, Km
- A concentraciones altas de sustrato, [S], el valor de inhibición puede ser no significativo.
- Cuando i = 0,5, es decir cuando hay una inhibición del 50% , el valor de IC50 viene dado por la ec. que hemos indicado
anteriormente.

Así pues, el valor IC50 para una inhibición competitiva no puede considerarse como un valor característico del inhibidor, ya que depende de la concentración actual de sustrato, [S] y de la Km
de la enzima para dicho sustrato.
Pero realmente lo que es útil es calcular la concentración de inhibidor, [I], que causa un determinado grado de inhibición.
Calculemos la concentración de un inhibidor competitivo que causa una inhibición del 60% de la enzima E; sabiendo que la [S]
= 2 10-3 M, Km = 10-3 M y que la Kic = 5 10-3 M

Determinación gráfica de los parámetros cinéticos en una inhibición competitiva
Podemos utilizar las mismas linealizaciones que para la ecuación de Michaelis-Menten; por ejemplo:
* 1/vic vs 1/[S] --> Representación de Linenweaver-Burk
* vic vs vic/[S] --> Representación de Eadie-Hoftee
* [S]/vic vs [S] --> Representación de Hanes
* vic vs [S] --> Representación directa o de Eisenthal- Cornish

1/v
1/[S]
1/Vmax
- 1/Km
[I] = 0[I] > 0
-1/Kmap
Representación de Linenweaver-Burk


v
v/[S]
Vmax
Vmax/Km
m = tg = -Km
Representación de Eadie-Hoftee
Vmax/Kmap
´m = tg´ = -Kmap
[I] > 0

[S]/v
[S]
Km/Vmax
- Km
Representación de Hanes
m = tg = 1/Vmax
-Kmap
Kmap/Vmax
I = 0
[I] > 0

Representación directa o de Eisenthal-Cornish
v0
Vmax
I = 0
S0-S2-S1 Km
[I] > 0
Kmap

2.2. Inhibición no-competitiva2.2. Inhibición no-competitivaEn una inhibición no-competitiva el inhibidor se une a la enzima
en un centro de unión diferente al centro activo de la enzima.

Consecuentemente, las especies químicas en las que puede encontrarse la enzima serán:
- la enzima libre, E,- la enzima unida al sustrato, ES (complejo-ES)- la enzima unida al inhibidor, EI (complejo-EI)- la enzima unida al sustrato y al inhibidor, ESI o EIS (complejo- ESI o EIS)
En el caso de la inhibición no-competitiva pura suponemos que tanto la enzima libre, E, como el complejo-ES pueden unirse al
inhibidor, y que la constante de disociación, Ki, es igual en ambos casos.
- En este caso, también, sólo el complejo-ES evoluciona dando producto
E y EI unen al sustrato sin que afecten a las constantes de disociación (Km)

Los inhibidores no-competitivos, generalmente no presentan
relación estructural con el sustrato, y se unen a la enzima en un sitio
distinto del centro activo.

Cuando [S] no desaparece la inhibición.

Km kcat
E + S <====> ES ----------> E + P
Km EI <=====>
<==
===>
I Ki
ESI ---------->
<==
===>
I Ki
* La deducción de la velocidad de reacción, en este caso, es análoga a la realizada en el caso de la inhibición competitiva:
vinc = kcat (ES)
[Eo] = [E] + [ES] + [EI]+ [ESI]

- Así pues, en una inhibición no-competitiva pura, la Km de la enzima por el sustrato no se modifica, sin embargo, la Vmax sí se
modifica, transformándose en una Vmaxap.
[S] vinc = Vmaxap -------------------- [S] + Km
KiI
VV ap
1
maxmax

* * Determinación gráfica de los parámetros cinéticos en una inhibición no-competitiva
- Podemos utilizar las mismas linealizaciones que para la ecuación de Michaelis-Menten, por ejemplo:
*1/vinc vs 1/[S] --> Representacion de Linenweaver-Burk
vinc vs vinc/[S] --> Representación de Eadie-Hoffte
vinc vs [S] --> Representación directa o de Eisenthal-Cornish

1/vinc
1/S
(I) > 0
- (1/Km)
1/Vmaxap
1/Vmax
(I) = 0
Representación de Linenweaver-Burk

I > 0
I = 0
vinc/S
vinc
Vmax
Vmaxap
m = -(1/Km)
Vmax/Km
Vmaxap/Km
Representación de Eadie-Hoffte

Representación directa o de Eisenthal-Cornish
v0 Vmax
(I) = 0
S0-S2-S1 Km
(I) > 0
Vmaxap

[I] i = -------------------
[I] + Ki
Cálculo del grado de inhibición, i:
Valor de la IC50 característica propia del inhibidor
No depende de la [S] ni de la Km
Valor IC50 es igual a la Ki

2.3. Inhibición acompetitiva2.3. Inhibición acompetitiva* El tercer tipo de inhibición reversible es la inhibición
acompetitiva, en la que el inhibidor sólo puede unirse al complejo-ES, formando un complejo-ESI, que no da producto.
* En este caso como en los dos anteriores, únicamente el complejo-ES da producto de reacción.

- De acuerdo con el siguiente esquema:
Km kcat
E + S <====> ES ----------> E + P
ESI ---------->
<==
===>
I Ki
* Al igual que los otros dos casos, en este la velocidad de reacción viene dada por:
viac = kcat (ES)
Y por tanto su deducción se realizará de manera análoga.
[Eo] = [E] + [ES] + [ESI]

* Así pues, en una inhibición acompetitiva se modifica tanto Vmax como Km, y ambas se ven afectadas por el mismo factor multiplicativo
[S] viac = Vmaxap ---------------- Kmap + [S]
Donde:
S
KI
KS
KI
Vv
iac
m
iac
iac
11
max
iac
map
KI
VV1
max
iac
mmap
KI
KK1


•Del análisis de la anterior figura así como de la ecuación que nos da viac podemos observar que tanto la Vmax como la Km están disminuidas por un
mismo factor:
¿No les parece paradójico que un inhibidor disminuya la Km de una enzima por el sustrato?
Es decir, ¡que aumente la afinidad de la enzima por el sustrato!
- La respuesta la podríamos tener en el mecanismo de inhibición
* Al unirse el inhibidor al complejo-ES desplaza el equilibrio y, aparentemente, por lo tanto, la constante de disociación Kmap
disminuye.
KiI1

Representacion de Linenweaver-Burk
Determinación gráfica de los parámetros cinéticos en una inhibición Determinación gráfica de los parámetros cinéticos en una inhibición acompetitivaacompetitiva
1/viac
1/S
(I) > 0
- (1/Km)
1/Vmaxap
1/Vmax
(I) = 0
- (1/Kmap)
Tarea. Realiza representaciones gráficas con las
otras representaciones

2.4. Representación de Dixon-Webb
Dixon y Webb propusieron una representación gráfica alternativa de la ecuación de inhibición competitiva y no-competitiva
Representando 1/vi frente a [I], manteniendo constante la (S).
(I)
1/viS1
S2
S2 > S1
-Ki

En el caso de una inhibición competitiva, para dos concentraciones de sustrato fijas, (S1) y (S2), tendremos:
1 1 Km 1 Km ----- = --------- + ---------- ------ + ---------------------- [I] vic1 Vmax Vmax [S1] Vmax Ki [S1]
1 1 Km 1 Km ----- = ---------- + --------- ------ + ---------------------- [I] vic2 Vmax Vmax [S2] Vmax Ki [S2]
S1
S2

- Estas dos rectas se cortarán en el único punto común que tienen, el correspondiente a 1/Vmax.
La condición de corte de estas dos rectas es que 1/vic1 = 1/vic2
- Así pues, igualando ambas ecuaciones, simplificando y reordenando, llegamos a la siguiente ecuación:
ii KI
SKI
S1111
21

- Por definición
Luego, la solución a la anterior ecuación será:
- De donde:
* La representación gráfica de estas dos rectas:
(I)
1/vicS1
S2
S2 > S1
-Ki
1/Vmax
21
11SS
01 iKI
iKI

* En el caso de una inhibición no-competitiva:
1 1 Km 1 ----- = --------- (1+[I]/Ki) + -------- ------ (1+[I]/Ki) vinc2 Vmax Vmax (S2)
1 1 Km 1 ----- = --------- (1+[I]/Ki) + -------- ------ (1+[I]/Ki) vinc1 Vmax Vmax (S1)
- Estas dos rectas se cortarán cuando 1/vinc1 = 1/vinc2.
* Operando de manera análoga al caso de la inhibición competitiva, obtenemos:
- Como por definición:
S1
S2
21
11SS
ii KI
SKI
S1111
21

=> 1 + (I)/Ki = 0 Luego: (I) = -Ki-Sustituyendo este valor en la ecuación que define 1/vinc, obtenemos: 1/vinc1 = 1/vinc2 = 0- Luego las rectas se cortan en un punto, sobre el eje (I), tal que (I) = -Ki
[I]
S1
S2
S2 > S1
-Ki
1/vinc1

2.5. Inhibición por exceso de sustrato* Este es otro tipo de inhibición reversible en el que un exceso de sustrato provoca una pérdida de actividad de la enzima.
* En este caso, el modelo cinético presupone que una segunda molécula de substrato puede unirse al complejo-ES dando lugar a la formación del complejo-ES2 que no da producto:
Km kcat
E + S <====> ES ----------> E + P
ES2 ---------->
<==
===>
S Ks´
- La ecuación de velocidad, como siempre, la podemos deducir a partir de: v = kcat (ES)
Suponemos que la constante de disociación del segundo complejo
[ES2] es diferente a la Km
Se denomina Ks´

Eo = E + ES + ES2
v = kcat [ES] [E] [S] [ES] = ----------- Km
Ecuación de conservación de la enzima
`
2
KmKsES
KmSEEEo
2
`ESSEKs
ESSEKm
´1
12
KmKsS
KmS
EoE
KmS
KmKsS
KmS
Vv
KmS
KmKsS
KmS
kcatEov
´1
1max
´1
1
2
2

La representación de v frente a (S) muestra una curva que presenta un máximo:
(S)(S)op
v
Vmax
Igualando a cero la primera derivada
con respecto a la [S]
La concentración de sustrato a la cual se obtiene el máximo el óptimo de
velocidad
´KmKsSop

- La representación de 1/v frente a 1/S es una hipérbola cuadrática, que tiene un mínimo correspondiente al inverso de
(S)op.
1/[S]1/[S]op
-1/Km1/Vmax
1/v

Succinato produce inhibición por substrato de la succinato deshidrogenasa.
Comenta cual podría ser el mecanismo de inhibición
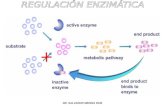
Un mecanismo de inhibición podría:
Una molécula de sustrato se une a la enzima, después una segunda molécula del S se une formando un complejo inactivo.
¿qué tipo de inhibición de los que hemos estudiado se ajusta a la inhibición por sustrato?
E
-OOC I
CH2
I CH2
I-OOC
E
-OOC I
CH II CH
I-OOC

S
KI
K
S
KI
Vv
iac
miac
iac
1
1
max
S
KS
K
S
KS
Vv
iac
miac
iac
1
1
max
Sustituyendo [I] por [S]
iacm
iac
KSSK
SVv1
max
A bajos valores de [S] S/Kiac tiende a cero M-M
A altos valores de [S] Km se desprecia
iac
iac
KS
Vv1
max
(S)
vVmax

RESUMEN
Inhibidores aquellos compuestos disminuyen la actividad de una enzima. Se agrupan en tres clases: Reversibles, Pseudoirreversibles y suicidas.
Inhibidores reversibles cumplen las condiciones de Michaelis, la [Io] es muy superior a la [Eo] siendo el complejo enzima-inhibidor [EI] despreciable frente a [I]
Tres tipos de inhibición reversible: a)Inhibición competitiva el inhibidor compite por el mismo lugar que el substrato. La
velocidad máxima queda inafectada por el inhibidor que aumenta la Kmap al multiplicarse la Km de la enzima por el factor (1+ I/Ki). El grado de inhibición depende
de las concentraciones de I y S, así como de la Km y Ki.
b)Inhibición no competitva el inhibidor se une a la enzima en un lugar diferente al de la unión al substrato. La inhibición afecta a la velocidad máxima disminuyendo su .
valor al ser dividida por (1+ I/Ki). El grado de inhibición depende solamente de la [I] y de la constante Ki.
c)Inhibición acompetitiva el inhibidor se une solamente al complejo Enzima-Substrato, disminuye la velocidad máxima por el factor (1+ I/Ki) y, paradójicamente,
disminuye la Km por el mismo valor obteniéndose una Kmap menor.
Inhibición por exceso de substrato puede ocurrir. La curva de velocidad en función de diferentes concentraciones de substrato presenta un máximo. En general se da este tipo
de inhibición cuando el substrato a grandes concentraciones puede reaccionar con la proteína enzimática en lugar diferente al de la unión enzima substrato

Imaginemos que estamos estudiando una reacción S P catalizada por una enzima E, y que obtenemos los siguientes resultados:
[S] (mmol L-1) v(mol L-1 min-1) v´(mol L-1 min-1) [I] = 0 [I] = 2 10-3 M
0,30 0,57 0.360,50 0,85 0.550,75 1,18 0.751,50 1,82 1.333,00 2,50 2.22
7,50 3,23 3.13 A partir de estos datos calcular, mediante la representación
adecuada: Vmax, Kmap, Kic y grado de inhibición (i) para [S] = 0,65 mM. ¿Qué concentración de inhibidor habría que utilizar para
inhibir la enzima un 25% a la misma concentración de sustrato?