Propiedades periódicas...
Transcript of Propiedades periódicas...

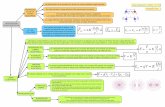
Propiedades periódicas atómicas
Antecedentes…
UNIDAD 2

Figure 08.05

CARGA NUCLEAR EFECTIVA (Zef) • Carga positiva neta que experimenta un electrón en un
átomo polielectrónico. • No es la carga nuclear total, ya que los electrones
internos del átomo escudan o apantallan parcialmente al núcleo.
• Los electrones del kernel (internos) apantallan a los electrones de valencia (externos) mucho más que lo que los electrones de valencia se apantallan entre sí.
Zef = Z real - • La cte de apantallamiento () generalmente es un nº
cercano al nº de e- internos en un átomo, y su valor es: Z > > 0

CARGA NUCLEAR EFECTIVA

Figure 07.03 Átomo de sodio

Variación periódica de Zef

RADIO ATÓMICO
Es la mitad de la distancia que hay entre los núcleos de dos átomos adyacentes.

Figure 07.07

Variación periódica del RADIO ATÓMICO

Figure 07.08

ENERGÍA DE IONIZACIÓN
• Energía mínima necesaria para remover un electrón del estado basal de un átomo en estado gaseoso.
• En consecuencia se forman iones con carga positiva.
• A mayor energía de ionización (EI), mayor dificultad (mayor gasto energético) para quitar a ese electrón, por lo que:
EI1 < EI2 < EI3 < EI4 …

ENERGÍAS DE IONIZACIÓN SUCESIVAS

Figure 07.12

AFINIDAD ELECTRÓNICA (AE)
• Cambio de energía que ocurre cuando se añade un electrón a un átomo o a un ión en estado gaseoso.
• En la mayoría de los átomos, se libera energía cuando se les añade un e-.
• A mayor valor de AE, el ión es más estable.
• Es más difícil adicionar un e- a un átomo cuyo núcleo no lo puede retener con fuerza.

Figure 07.14 VALORES DE AFINIDAD ELECTRÓNICA

Variación periódica de la AFINIDAD ELECTRÓNICA

Electronegatividad
Linus Carl Pauling (1901-1994), premio Nóbel de Química en 1954 y premio Nóbel de la paz en 1962.
17

Electronegatividad
• La electronegatividad representa una medida del grado de atracción de un par de electrones en un enlace covalente.
• Pauling obtuvo los valores de electronegatividad empíricamente, a través de la medición de las energías de los enlaces.
18

Electronegatividad
• La escala de electronegatividades de Pauling sigue siendo la más usada en nuestros días y presenta valores que siempre son positivos.
• En esta escala el F es el elemento más electronegativo (4.0) y el Cs el menos electronegativo (0.7).
19

Electronegatividad
• Los elementos que presentan valores grandes de electronegatividad son elementos que tienen gran tendencia a atraer electrones y se dice que son los elementos más electronegativos.
• Aquellos elementos con valores de
electronegatividad pequeños tenderán a ceder electrones y se dirá que son los elementos menos electronegativos.
20

Figure 08.06