minerales, materiales y medio ambienteproductividad.cimav.edu.mx/productividad/adjuntos...8 sobre...
Transcript of minerales, materiales y medio ambienteproductividad.cimav.edu.mx/productividad/adjuntos...8 sobre...



minerales, materiales y medio ambiente

Este libro se editó gracias al apoyo PIFI de la Universidad Autónoma de
Zacatecas «Francisco García Salinas». La investigación, arbitrada por
pares académicos, se privilegia con el aval de la institución editora.
Primera edición 2014
Derechos reservados
© Patricia de Lira Gómez
Uriel Ramírez-García Correa
Eduardo García Sánchez
(coordinadores)
© Taberna Libraria Editores
Jazmín 106-A, Col. Las margaritas.
980017, Zacatecas, Zacatecas.
Tel. (01492) 154 2969; cel. 0444921031935
Edición Friné González Herrera
Diseño: Juan José Macías
ISBN: 978-607-9165-82-6
Queda rigurosamente prohibida, sin autorización de los titulares del
copyright, bajo las sanciones establecidas por las leyes, la reproduc-
ción total o parcial de esta obra por cualquier medio o procedimiento.
Impreso y hecho en México / Printed and made in Mexico

Patricia de Lira GómezUriel Ramírez-García Correa
Eduardo García Sánchez (Coordinadores)
MINERALES, MATERIALES y MEDIo AMBIENTE
Alejandro Uribe SalasRoberto Pérez Garibay
Sergio Gabriel Flores GallardoClara Hilda Ríos Reyes
Luis Humberto Mendoza HuizarErasmo orantia Borunda
Universidad Autónoma de Zacatecas


7
PRESENTACIÓN
En nuestra actualidad, la tendencia global mundial ha sido el impulso
hacia el avance científico y tecnológico de los países. Estos esfuerzos
en pro del desarrollo y crecimiento económico están tan diversificados
y cultivados por los diferentes sectores productivos que, respecto al
industrial y al educativo particularmente, se busca lograr el máximo
aprovechamiento de las capacidades económicas y de infraestructura
disponibles, y de este modo propiciar la generación de recursos hu-
manos de alta calidad, a fin de conformar sistemas productivos más
eficientes y eficaces, ad hoc a las necesidades de cada región. Para lo-
grar esto se requiere de un permanente e incesante trabajo de inves-
tigación científica, la que a través de diversos mecanismos le provea
al investigador la posibilidad de explorar, desde su génesis, algunas
condiciones o comportamientos dentro de los procesos que pudieran
verse reflejados al innovar la formulación de nuevos y mejores mate-
riales funcionales, y hacer a los sistemas más rentables.
Minerales, Materiales y Medio Ambiente es el resultado de la cola-
boración entre Profesores Investigadores de diversas Instituciones
de Educación Superior y Centros de Investigación de nuestro país,
convocados por el Cuerpo Académico UAZ-CA-178 a participar en las
«1ª, 2ª y 3ª Reunión de Materiales», organizadas en las ciudades de
Zacatecas y Durango a finales del 2009, 2010 y 2011; en este último
año se logra una comunión de ideas y cristaliza la colaboración entre
quienes en ellas participamos. El objetivo de la presente obra es pre-
sentar algunos de los trabajos de investigación actuales y de vanguar-
dia en los diferentes campos a los que hace alusión el título del libro.
Así, pues, los autores tratan una diversidad de temas que van
desde el análisis de algunos factores que intervienen en el proceso
del beneficio de minerales; la caracterización de materiales polimé-
ricos modificados con nanoarcilllas; el empleo de técnicas voltampe-
rométricas sobre materiales electrodepositados de Fe sobre Carbón
Vítreo; el estudio electrocinético de la electrodepositación de cobalto

8
sobre carbón vítreo, cerrando con el análisis de cómo la nanotecnolo-
gía influye en el medio ambiente y la salud humana.
Los trabajos aquí presentados cultivan líneas articuladoras de
generación y aplicación del conocimiento del UAZ-CA-178, pretendi-
damente de carácter multidisciplinario en las áreas de ciencia y tec-
nología, resultado que nos brindó la plena confianza para fomentar y
promover la colaboración entre las Instituciones de Educación Supe-
rior, Centros de Investigación y/o del Sector Productivo concerniente.
Patricia de Lira GómezZacatecas, Zac., agosto 2014

9
Héctor Hugo Lerma Triana, Alejandro Uribe Salas, Roberto Pérez Garibay
EVALUACIÓN DE SURFACTANTES USADoS EN LA FLoTACIÓN DE SULFURoS EN TéRMINoS
DEL TAMAño PRoMEDIo DE BURBUJA
RESUMEN
Se realizaron experimentos enfocados a la caracterización de los ta-
maños de burbuja que se generan en una celda de flotación marca
Denver, de escala laboratorio de 5 litros de capacidad. Se evalúo el
efecto que ejercen las principales variables de operación de la celda
sobre el tamaño de las burbujas (representado por el diámetro Sauter
(d32) en mm) y sobre la dispersión de los datos alrededor de la media
de las distribuciones de tamaños de burbujas —representado por el
coeficiente de variación (Cv)—. La técnica empleada se fundamenta
en colectar burbujas y fotografiarlas, para después procesar median-
te software especializado las imágenes obtenidas.
Asimismo, se estudió el efecto del caudal de aire suministrado
(representado por la velocidad superficial de aire Jg en cm/s), la velo-
cidad de los impulsores, la concentración y el tipo de espumante, las
características fisicoquímicas del agua empleada y la presencia de só-
lidos hidrofóbicos en el sistema. Se utilizaron dos espumantes usados
típicamente en la industria, como lo son el MIBC (metil isobutil car-
binol) y el α-Terpinol, además de un tercero (1-octanol) para compa-
ración, todos grado reactivo, de la marca Sigma Aldrich y a diferentes
concentraciones. Se prepararon varios sistemas: con agua disponible
de la red municipal, con agua purificada, con una solución 0.4M de
NaCl (sal comestible), y un sistema con pulpa mineral de sílice con
35 % en peso de sólidos de tamaños de partícula menores a 60 µm,
empleando 5 x10-5 M de dodecilamina como colector, y manteniendo
un pH de 9.5 con hidróxido de sodio.

Lerma Triana,Uribe Salas, Pérez Garibay
10
Los resultados experimentales muestran que el MIBC tiene la ca-
pacidad de disminuir con mayor eficiencia el tamaño de las burbujas
y que en un sistema con agua de la red municipal se generan las
burbujas más pequeñas, independientemente del tipo de espumante;
mientras que en un sistema con pulpa mineral de sílice, se gene-
ran las poblaciones de burbujas de tamaños más grandes y distri-
buciones más homogéneas. Los resultados arrojan también la muy
evidente disminución del tamaño de las burbujas a medida que se
incrementa la concentración de espumante, así como que la veloci-
dad superficial de aire afecta de manera contraria; además de que, en
el caso de celdas que operan con aire forzado, se debe mantener una
relación óptima entre la velocidad de los impulsores y el flujo de aire
suministrado, a fin de que la dispersión del aire sea eficiente.
Palabras clave: espumante, celda de flotación, velocidad superfi-
cial de aire, diámetro Sauter.
1. INTRODUCCIÓN
La flotación es un proceso metalúrgico cuyo objetivo es la recupera-
ción de las especies mineralógicas de interés contenidas en un mine-
ral. Este proceso consiste en separar las especies que tienen valor co-
mercial (principalmente sulfuros) del material no deseado (arcillas y
arenas de sílice, de forma primordial). Dicha separación se fundamen-
ta en el hecho de que los sulfuros metálicos desarrollan propiedades
hidrofóbicas mediante un acondicionamiento químico adecuado, uti-
lizando diversos reactivos químicos, tales como espumantes, colecto-
res, activadores, depresores, etc., mismos que se suministran en algu-
na de las etapas del proceso, en cantidades suficientes para que cada
uno cumpla un objetivo en particular. La eficiencia en la concentra-
ción de los minerales se debe en gran medida a la correcta acción de
dichos reactivos. Los espumantes son uno de los insumos más impor-
tantes, debido a que su objetivo es generar burbujas de tamaños rela-
tivamente pequeños, además de promover la formación de una cama
de espuma homogénea y estable; ambas características afectan di-
rectamente el rendimiento metalúrgico de los procesos (Finch, 2005).

Evaluación dE surfactantEs usados En la flotación dE sulfuros
11
1.1. Acción de los espumantes
La acción de los espumantes se debe a que son agentes tensoactivos,
lo cual quiere decir que poseen la propiedad de disminuir la tensión
superficial del sistema, a medida que se incrementa la concentración
del espumante en la solución; también disminuyen la coalescencia
entre las burbujas cuando están presentes en la concentración crítica
de coalescencia (CCC), en la cual el tamaño de las burbujas generadas
no cambia. Se ha encontrado que la CCC es diferente para cada tipo
de espumante, por lo que ha sido un parámetro para su clasificación
(Laskowski y col., 2006). otras maneras de clasificar los espumantes
es de acuerdo con la estructura de su cadena hidrocarbonada (lineal,
ramificada o aromática), o con un balance hidrofílico-lipofílico (HLB)
de su estructura (Guo y col., 2006). Los espumantes utilizados de for-
ma común en la industria del procesamiento de minerales median-
te flotación, en concentraciones no mayores a 30 partes por millón,
son principalmente alcoholes alifáticos, tales como el 4-metil-2-pen-
tanol (MIBC por metil isobutil carbinol); alcoholes cíclicos, como el
α-terpinol; o del tipo de poliglicoles, como el DowFroth 250, entre
otros.
1.2. Caracterización de tamaños de burbujas
En los últimos años, se han venido desarrollando técnicas de caracte-
rización de la distribución de tamaños de burbujas generadas en cel-
das y columnas de flotación a nivel laboratorio. Algunas técnicas se
basan en la utilización de ecuaciones empíricas que toman en cuenta
propiedades fisicoquímicas del sistema, como la tensión superficial,
la viscosidad y la densidad; además de la aplicación de software para
análisis de imágenes de las burbujas, tomadas con cámaras fotográ-
ficas o de video directamente sobre paredes transparentes de colum-
nas de flotación (Subatra, 2006). Se ha encontrado que en una celda
de flotación se generan burbujas de menor tamaño en sistemas de
baja tensión superficial, definida por la concentración de espuman-
te (Girgin y col., 2006), del mismo modo que diferentes patrones de
mezclado, dependiendo del tipo y diseño del impulsor (Gorain, 1997).
También se ha observado que el tamaño de las burbujas depende del

Lerma Triana,Uribe Salas, Pérez Garibay
12
caudal de aire y del diseño de la celda (Nesset y col., 2006), sumado
a que en soluciones electrolíticas, a medida que se incrementa su
fuerza iónica, se generan burbujas de tamaños más pequeños sin ne-
cesidad de utilizar espumantes (Quinn y col., 2007).
2. PARTE EXPERIMENTAL
2.1. Aparato para la colección de burbujas
Se utilizó un equipo denominado cámara de visualización de burbu-
jas (McGill bubble size analizer), que consta de un recipiente de sección
cilíndrica de 7 litros de capacidad, con paredes de vidrio transparente
e inclinada 15° respecto a su eje vertical. En la parte superior cuenta
con una tapa roscada, provista de una válvula; dicha tapa se abre
para permitir el llenado de la cámara con agua. En la parte inferior
se encuentra una unión roscada de alrededor de 4 cm de diámetro,
donde se inserta un tubo de PVC de aproximadamente 2” de diámetro,
roscado en el exterior en el extremo superior, en el cual se introduce
un tubo PVC de 1.27 cm de diámetro por 85 cm de largo (es posible
utilizar distintas longitudes), denominado tubo de muestreo, por don-
de ascienden las burbujas recolectadas para ser desplegadas en la cá-
mara de visualización. En la parte posterior de la cámara se coloca un
foco de 150 W de potencia para una adecuada iluminación del equipo.
Se utiliza una cámara digital Nikon D100 para la toma de imágenes,
equipada con un lente macro de 108 mm y disparador automático,
mismo que regula la velocidad y cantidad de fotos deseadas. En la
figura 1 se representa un esquema del equipo utilizado.

Evaluación dE surfactantEs usados En la flotación dE sulfuros
13
Figura 1. Esquema de la cámara de visualización de burbujas utilizada.
La recolección de las burbujas a través del tubo de muestreo se lleva
a cabo gracias al fenómeno de desplazamiento volumétrico, es decir,
las burbujas tienden a subir por efectos de boyancia y, a medida que
lo hacen, van desplazando el líquido contenido dentro de la cámara
de visualización hacia la celda. Conforme las burbujas de aire ascien-
den a lo largo del tubo de muestreo, es muy probable que su tamaño
se vea afectado debido a la diferencia de presión que existe entre el
punto de muestreo y el punto en que se fotografían las burbujas en
la cámara de visualización, como se observa en parte derecha de la
figura 1; por lo tanto, es importante introducir un factor de corrección
en el tamaño de las burbujas obtenido de las imágenes.

Lerma Triana,Uribe Salas, Pérez Garibay
14
El factor de corrección se propone planteando un balance de pre-
siones hidrostáticas en el punto de muestreo, donde la presión exter-
na e interna del tubo de muestreo deben de ser iguales, obteniéndose
la ecuación siguiente:
Pvacío+gρAgua H1+H2+H3( )=PAtm+P1 (1)
Pvacío es la presión en la parte superior dentro de la cámara (Pascales),
g es la constante de aceleración de la gravedad (9.81 m/s2), ρAgua es la
densidad del agua con la que se llena la cámara (kg/m3), H1 es la longi-
tud del tubo de muestreo (m), H2 y H3 son distancias conocidas dentro
de la cámara (m), PAtm es la presión atmosférica (Pascales) y P1 es la
presión en el punto de muestreo (Pascales), definida por:
P1 = ρsistema H4 g (2)
ρsistema es la densidad del sistema dentro de la celda (kg/m3), H4 es la
profundidad que se sumerge el tubo de muestreo dentro de la celda
(m).
Al reacomodar la ecuación (1) se obtiene la expresión para calcu-
lar la presión en el interior de la cámara de visualización.
( )3211 HHHgPPP AguaAtmVacío ++−+= ρ
(3)
Al aplicar la ley de Boyle en los puntos de muestreo y de toma de
imágenes, se obtiene la siguiente expresión:
2211 VPVP = (4)
en la cual P y V son la presión y el volumen de las burbujas, mientras
que los subíndices 1 y 2 son las posiciones de muestreo, y el punto en
que se lleva a cabo la captura de las imágenes, respectivamente. Con-
siderando las burbujas como esferas, en la ecuación (4) se sustituye
el volumen de éstas para obtener la expresión siguiente:
⎟⎠
⎞⎜⎝
⎛=⎟⎠
⎞⎜⎝
⎛ 322
311 66
dPdP ππ
(5)

Evaluación dE surfactantEs usados En la flotación dE sulfuros
15
Tras eliminar el término π/6 de la ecuación (5) y reacomodándola,
se obtiene la relación del diámetro de las burbujas en el punto de
muestreo (d1), en función del diámetro en el punto de la toma de las
imágenes (d2):
( )( )
3
4
323
1
221 ⎟⎟
⎠
⎞⎜⎜⎝
⎛
+
+=⎟⎟
⎠
⎞⎜⎜⎝
⎛=
HgPHgP
dPPdd
sistemaAtm
Aguavacío
ρ
ρ
(6)
definiendo al factor de corrección de tamaño, Fc, como:
( )( )
3
4
3⎟⎟⎠
⎞⎜⎜⎝
⎛
+
+=
HgPHgP
FsistemaAtm
Aguavacíoc ρ
ρ
(7)
cFdd 21 =
(8)
donde d1 es el diámetro de burbuja en el punto de muestreo y d2 es el
diámetro de la burbuja en el punto donde es fotografiada, el cual es
proporcionado por el software (mm).
Al realizar una prueba experimental se mide la presión atmosfé-
rica con un barómetro, lo que permite calcular el factor de corrección
de tamaño de burbuja (parámetro adimensional), aplicable a las con-
diciones particulares del experimento. Para el cálculo de la presión
en el punto de muestreo P1 —ecuación (2)—, se requiere conocer la
densidad del sistema dentro de la celda (agua o pulpa aireada, según
sea el caso), datos que pueden calcularse tomando en cuenta que en
las celdas de flotación se genera de un 15 a un 20% de aire retenido
(Girgin y col., 2006).
2.2. Celda de flotación
Se utilizó una celda de flotación marca Denver, de escala de labora-
torio de 5 litros de capacidad y sección cuadrada de 240 cm2 de área
transversal. La celda cuenta con un sistema mecánico de agitación
con un impulsor tipo turbina, cuya velocidad se puede regular; se le

Lerma Triana,Uribe Salas, Pérez Garibay
16
acopló una línea de suministro de aire proveniente de un compresor, a
la cual se le instaló un regulador de presión y un rotámetro calibrado.
En la Figura 2 se presenta un esquema gráfico de la instalación uti-
lizada.
Figura 2. Esquema del sistema experimental empleado en el presente trabajo.
2.3. Técnica de análisis de imágenes
Para el análisis de las imágenes tomadas por la cámara, se utilizó el
software Northern Eclipse 7.0â, diseñado por Empix Imaging Inc., con
el cual se procesan de manera automática las imágenes, en forma
de archivos con extensión TIFF (Tagged Image File Format, formato de
archivo de imágenes con etiquetas), pues dicho formato permite con-
vertir las imágenes —originalmente a color— a escala de grises, a fin
de ser procesadas por el software.
Northern EclipseÒ analiza la imagen y, de acuerdo al nivel de la
intensidad de grises, distingue entre el fondo de la foto y los objetos
encontrados en ella (burbujas), identificándolos con números, pro-
porcionando algunos parámetros morfológicos, como son:
Área: representada por el número total de pixeles que ocupa el objeto.
Perímetro: distancia en pixeles del contorno que genera el objeto.
Diámetro equivalente: es el diámetro en pixeles de un círculo que tiene la
misma área que el objeto analizado y está dado por la ecuación siguiente:

Evaluación dE surfactantEs usados En la flotación dE sulfuros
17
páreadeq 2. = (9)
Factor de forma: parámetro indicativo de la esfericidad del objeto, de-
finida por:
( )( )24perímetro
áreaformadeFactor π=
(10)
El factor de forma representa el área del objeto, dividido entre el área
de un círculo que tiene el mismo perímetro que dicho objeto. Cabe
mencionarse que para un círculo perfecto el valor del factor de forma
es la unidad; sin embargo, en el caso de imágenes digitales todos los
objetos consisten de pixeles, por lo que un círculo “perfecto” tendrá
un factor de forma menor a la unidad (ver figura 3). Por lo general los
objetos circulares tienen factores de forma de aproximadamente 0.85.
Este parámetro es importante porque permite cuantificar sólo
burbujas individuales, ya que con frecuencia se fotografían burbujas
que se traslapan o están pegadas unas con otras y el programa las
reconoce como un objeto único, al cual le asigna un factor de forma
muy pequeño. También se descartan las burbujas que no son circu-
lares, debido a que se encuentran en el borde de la fotografía. En la
figura 3 se aprecia dicho fenómeno.
Figura 3. Imagen de una burbuja aislada, ampliada 800 veces, donde se aprecian los pixeles
que forman su contorno, fenómeno generado por la variación de la intensidad de luz traducida
a la escala de grises (izquierda). Imagen característica, en la que se observan dos burbujas
pegadas y tres burbujas que tocan los bordes de la fotografía (derecha).

Lerma Triana,Uribe Salas, Pérez Garibay
18
Una vez analizadas las imágenes necesarias para obtener por lo me-
nos 2500 objetos o burbujas, los valores de sus diámetros equivalen-
tes se almacenan en hojas de cálculo para obtener distrbuciones de
tamaños de burbuja y sus parámetros estadísticos, diámetro prome-
dio y desviación estándar.
2.4. Variables experimentales
Se estudiaron las principales variables que, en investigaciones recien-
tes, se ha demostrado que influyen en el tamaño de las burbujas que
se generan dentro de los equipos de flotación. El diseño de experi-
mentos propuesto involucró el análisis de los tamaños de burbuja
que se generan para distintos sistemas (agua de la red municipal-aire,
agua purificada-aire, solución 0.4 M de NaCl y pulpa mineral-aire),
usando diferentes concentraciones de espumante (1, 2, 3, 4, 5, 10, 15 y
20 ppm), así como velocidades superficiales de aire de 0.2, 0.4, 0.6, 0.8,
1.0, 1.2, 1.4, 1.6, 1.8 y 2 cm/s. En la tabla I se reportan las característi-
cas físicas de los espumantes utilizados.
Tabla I. Características de los espumantes utilizados.
Nombre Fórmula Peso molecular
(g / mol)
Pureza (%) *Densidad
(g /cm3)
MIBC C6H16o 104 98 0.7536
α-Terpinol C10H18o 154 90 0.8663
1-octanol C8H18o 130 99 0.8118
* Los valores de las densidades se obtuvieron mediante técnicas gravimétricas, usando una
balanza analítica calibrada, pesando 1 mL de espumante a condiciones atmosféricas y en
repetidas ocasiones.
Se preparó una pulpa con 35% en peso de finos de sílice malla -270
(menor de 60 µm, ver figura 4), la cual puede considerarse como de
densidad similar a las pulpas que se procesan industrialmente en
la etapa de flotación primaria. El procedimiento de preparación
de la pulpa de flotación fue el siguiente: se pesaron 6.67 kg de síli-
ce y se añadieron a un recipiente con 12.4 kg de agua purificada y
20 ppm de MIBC como espumante. El recipiente se sometió a agi-

Evaluación dE surfactantEs usados En la flotación dE sulfuros
19
tación durante 10 minutos aproximadamente para homogeneizar el
sistema, añadiendo 0.139 g de colector (dodecilamina) para obtener
una concentración de 5x10-5 M y se mantuvo a pH de 9.5 añadiendo
hidróxido de sodio. El experimento consistió en llevar a cabo pruebas
de flotación intermitente (e.g., batch) de la sílice.
Figura 4. Función de distribución de tamaños de partícula de los finos de sílice empleados,
obtenida mediante difracción de rayos láser (Coulter LS 100Q).
3. RESULTADOS Y DISCUSIÓN
3.1. Efecto de las condiciones de agitación
Se realizaron mediciones de velocidad superficial de aire (Jg) a dife-
rentes velocidades de agitación de la celda, operando ésta mediante
succión natural, con el objetivo de encontrar la relación entre estas
dos variables. Las mediciones se llevaron a cabo bajo el principio del
desplazamiento volumétrico, empleando una probeta invertida origi-
nalmente llena de agua, la cual se tapó y fue sumergida dentro de la
celda. La medición consiste en monitorear el tiempo que tarda el aire
en desplazar un volumen determinado de agua de la probeta. En la
figura 5 se muestran los resultados obtenidos.

Lerma Triana,Uribe Salas, Pérez Garibay
20
Figura 5. Velocidad superficial de aire generada y flujo de aire succionado por el agitador de la
celda a diferentes velocidades de agitación, medidos por el desplazamiento de 200 cm3 de agua,
contenida en una probeta invertida de 9.66 cm2 de sección transversal. Las barras de error
delimitan el intervalo de confianza de 95%.
Una vez encontrada la relación entre la velocidad superficial de aire
y el giro del impulsor, se llevaron a cabo experimentos en un siste-
ma agua-aire, usando α-Terpinol a diferentes concentraciones. En un
caso manteniendo esta relación y en otro a velocidad de agitación
constante (1500 rpm).
Figura 6. Efecto en el diámetro Sauter de burbujas generadas dentro de la celda, en función
de la concentración de espumante y de la velocidad superficial de aire (Jg), a diferentes
condiciones de agitación.

Evaluación dE surfactantEs usados En la flotación dE sulfuros
21
Generalmente los parámetros de operación de los equipos de flota-
ción los proporcionan los proveedores, de acuerdo a las necesidades
del proceso. Con los resultados presentados en la figura 6 queda de-
mostrado que la técnica implementada es una herramienta intere-
sante para evaluar el estado de operación de los equipos, en términos
de los tamaños de burbuja que en ellos se generan. Es muy eviden-
te que el diámetro Sauter disminuye a medida que se incrementa
la concentración de espumante, mientras que para el caso del Jg, el
efecto es contrario. Las condiciones de dispersión del aire dentro de
la celda son mejores cuando se incrementa la velocidad de agitación
del impulsor, conforme aumenta el caudal de aire suministrado (fi-
gura 6, derecha), debido a que la mayor eficiencia de la acción de
dispersión del aire se refleja en la generación de burbujas de menor
tamaño. También se observa que si se mantiene la velocidad de agita-
ción constante a 1500 rpm, a valores bajos de caudal de aire, éste se
dispersa de manera adecuada, pero que a valores superiores ya no es
suficiente la energía de corte causada por la agitación para dispersar
el aire de manera eficiente, dando lugar a la formación de burbujas
más grandes (figura 6, izquierda).
3.2. Efecto del tipo de espumante
Una vez definidas las mejores condiciones de dispersión del aire en la
celda, reflejadas éstas por el tamaño promedio generado de burbuja,
se realizaron experimentos con los espumantes mencionados para
determinar el efecto de la naturaleza química del espumante sobre
el diámetro Sauter de las burbujas. Para preparar los sistemas de
prueba se utilizó agua de la red municipal y se añadieron diferentes
concentraciones de los tres espumantes a evaluar.

Lerma Triana,Uribe Salas, Pérez Garibay
22
Figura 7. Efecto del tipo de espumante sobre el diámetro Sauter en un sistema con agua de la
red municipal de Ramos Arizpe, Coahuila, a las mismas condiciones experimentales.
En la figura 7 se presenta la evolución del diámetro Sauter, a medida
que se incrementa la concentración de los diferentes espumantes y
el Jg. Puede observarse que el efecto sobre el tamaño de las burbujas,
debido la velocidad superficial de aire, es menor que el atribuido a
la concentración de espumante en los tres casos. El MIBC tiende a
disminuir con mayor facilidad el tamaño de las burbujas y sólo se
requiere una concentración de 10 ppm para mantener un tamaño de
burbuja constante. Los otros dos espumantes disminuyen el diámetro

Evaluación dE surfactantEs usados En la flotación dE sulfuros
23
promedio de las burbujas en menor proporción, siendo el 1-octanol el
menos eficaz en este sentido.
Figura 8. Efecto del tipo de espumante sobre la función de densidad de volumen y el grado
de dispersión de la distribución de tamaños de burbuja, representado por el coeficiente de
variación (Cv) en experimentos con 5 ppm de espumante, a una velocidad superficial de aire
de 1 cm/s. El área bajo la curva representa el 100% del volumen de aire, ocupado por 2528
burbujas analizadas.
La homogeneidad de las distribuciones de tamaños de burbuja se re-
presentan cuantitativamente, mediante el coeficiente de variación
Cv (cociente entre la desviación estándar y el diámetro promedio), el
cual indica el grado de dispersión de los valores sobre la media po-
blacional. En un experimento típico efectuado con MIBC, se generan
distribuciones de burbujas más uniformes que las generadas con los
otros espumantes, como se observa en la figura 8.
3.3. Efecto de las características del sistema
Se encontró que el tamaño de las burbujas en el sistema con agua
purificada es, en todos los casos, ligeramente mayor que el de las
generadas con agua de la red municipal (ver figura 9). Este fenómeno
se puede atribuir a la presencia de sales disueltas en el agua de la red

Lerma Triana,Uribe Salas, Pérez Garibay
24
municipal, las cuales coadyuvan en la disminución del tamaño de las
burbujas.
Figura 9. Diámetro Sauter de las burbujas que se obtienen con los diferentes tipos de agua, en
función de la velocidad de aire, usando 20 ppm de MIBC.
Aunque en el sistema de pulpa mineral se generaron las poblacio-
nes de burbujas de tamaños más grandes, éstas son de distribuciones
más uniformes ya que los valores de coeficiente de variación son más
bajos, como se muestra en la figura 10.
Figura 10. Evolución del grado de dispersión de las distribuciones de tamaños de burbuja en
función de la velocidad superficial de aire, para los cuatro sistemas en estudio, cuando se
emplean 20 ppm de MIBC.

Evaluación dE surfactantEs usados En la flotación dE sulfuros
25
En el sistema de pulpa mineral se generan las burbujas de tamaños
más grandes, probablemente debido a que los sólidos hidrofóbicos
depositados en sus superficies promueven la coalescencia, le siguen
en menor tamaño las burbujas generadas en el sistema con agua pu-
rificada, luego las de la solución de NaCl y, por último, las burbujas
más pequeñas son las del sistema con agua de la red municipal. En
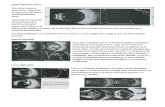
las fotografías de la figura 11 se muestra este fenómeno.
Sistema pulpa mineral-aire
Sistema agua purificada-aire
Sistema 0.4M de NaCl
Sistema agua de la red municipal-aire
Figura 11. Series de fotografías que muestran poblaciones típicas de burbujas en los diferentes
sistemas de estudio, usando 20 ppm de MIBC y un Jg de 1 cm/s.

Lerma Triana,Uribe Salas, Pérez Garibay
26
4. CONCLUSIONES
Las condiciones que favorecen la dispersión ineficiente del aire en
las celdas mecánicas promueven la generación de burbujas relativa-
mente grandes. Una buena dispersión del aire depende, en principio,
de la velocidad de los impulsores y el empleo de un caudal de aire
que pueda ser dispersado de manera adecuada. La metodología ex-
perimental implementada en el presente trabajo de investigación es
una herramienta importante que puede utilizarse a nivel industrial
para evidenciar el estado de aireación que prevalece en los equipos
de flotación, en términos de las características de la distribución de
tamaños de burbuja.
En todos los casos estudiados se observó un efecto evidente de
la velocidad superficial del aire sobre el diámetro promedio de las
burbujas, así como sobre la distribución de tamaños generados en la
celda. Las burbujas tienden a incrementar su tamaño a medida que la
velocidad superficial del aire aumenta, mientras que la distribución
de tamaños se hace más amplia.
Conforme aumenta la concentración del espumante en el siste-
ma, independientemente de su naturaleza química, el tamaño de las
burbujas disminuye y su distribución se hace más estrecha, siendo
el MIBC el espumante más eficaz, pues al compararse con los otros,
en las mismas concentraciones, se obtienen burbujas más pequeñas.
Este hecho corrobora el motivo por el cual, de los tres espumantes
probados, el MIBC es el que más se utiliza en la industria para la con-
centración de sulfuros.
Asimismo, se observa que los sólidos disueltos en el agua afec-
tan la generación de burbujas. Utilizando agua disponible de la red
municipal de Ramos Arizpe, Coahuila, de conductividad 2.5 mS/cm,
se generan las poblaciones de burbujas más pequeñas, comparadas
con las encontradas en el sistema con agua purificada (0.08 mS/cm)
y la solución 4 M de cloruro de sodio (~40 mS/cm). El hecho puede
deberse a que las sales inorgánicas realizan un efecto similar al de
los espumantes, por lo tanto, resulta razonable considerar que las
burbujas son más pequeñas gracias al efecto sumado del espumante
y las sales disueltas que contiene el agua.

Evaluación dE surfactantEs usados En la flotación dE sulfuros
27
En el sistema con agua purificada se generan burbujas más gran-
des en todos los casos, este fenómeno se atribuye a su baja fuerza
iónica, por lo que el efecto tensoactivo de los espumantes es menos
fuerte. A valores bajos de velocidad superficial de aire (menores de
0.6 cm/s), las burbujas generadas en el sistema acuoso con 0.4 M de
NaCl son más pequeñas que las generadas en el sistema con agua
de la red municipal, pero ligeramente mayores a velocidades de aire
más altas, pese a que la fuerza iónica de la solución salina es mucho
mayor, comparada con la del agua de la red.
Una pulpa mineral de sílice hidrofóbica con una alta concentra-
ción de sólidos (35% en peso) promueve la formación de burbujas de
tamaños ligeramente mayores a las obtenidas en un sistema agua-
aire, es probable que esto se deba a que las partículas adheridas a las
burbujas provocan la coalescencia de éstas.
Bibliografía
Finch J. A., S. Gelinas, P. Moyo (2005), “Frother-related research at McGill University”,
Minerals Engineering, Vol. 19, pp. 726-733.
Girgin E. H., S. Do, C. o. Gomez, J. A. Finch (2006), “Bubble size as a function of im-
peller speed in a self-aeration laboratory flotation cell”, Minerals Engineering,
Vol. 19, pp. 201-203.
Gorain B. K., J. P. Franzidist and E. V. Manlapig (1997), “Studies on impeller type, im-
peller speed and air flow rate in an industrial scale flotation cell. part 4: effect
of bubble surface area flux on flotation performance”, Minerals Engineerig, Vol.
10, no. 4, pp. 367-379.
Guo X., Z. Rong, X. ying (2006), “Calculation of hydrophile–lipophile balance for
polyethoxylated surfactants by group contribution method”, Journal of Colloid
and Interface Science, vol. 298, pp. 441-450.
Laskowski J. S., F. Melo (2006), “Fundamentals properties of flotation frothers and
their effect on flotation”, Minerals Engineering, Vol. 19, pp. 767-730.
Nesset J. E., J. R. Hernandez Aguilar, C. Acuna, C. o. Gomez, J. A. Finch (2006), “Some
gas dispersion characteristics of mechanical flotation machines”, Minerals En-
gineering, vol. 19, pp. 808-815.

Lerma Triana,Uribe Salas, Pérez Garibay
28
Quinn J. J., W. Kracht, C. o. Gomez, C. Gagnon, J. A. Finch (2007), “Comparing the ef-
fect of salts and frother (MIBC) on gas dispersion and froth properties”, Miner-
als Engineering, vol. 20, pp. 1296-1302.
Subatra, K. M., K. Gautam, M. Dibyendu (2006), “Bubble size distribution and gas–
liquid interfacial area in a modified downflow bubble column”, Chemical Engi-
neering Journal, vol. 122, pp. 1–10.

29
Luz Cecilia Pérez Velásquez,1 Sergio Gabriel Flores Gallardo2 Patricia de Lira Gómez3, Tomás Lozano Ramírez4
ESTUDIo DE NANoCoMPUESToS MoNTMoRILLoNITA/PLA
1. INTRODUCCIÓN
Hoy en día la incorporación de rellenos en la escala nanométrica en
los polímeros ha atraído gran interés, como uno de los caminos más
efectivos para desarrollar nuevos materiales con funcionalidades
adaptadas a aplicaciones específicas o para cubrir las desventajas que
presentan los polímeros5 (Dong y Byoung, 2007). Los nanocompuestos
son materiales conformados por dos o más componentes, se denomina
matriz al que se encuentra en mayor porcentaje y carga al de menor,
esta última tiene que estar en tamaño nanométrico, típicamente en
el rango de 1-20 nm.
La creciente atracción por dicho tipo de sistemas (materiales
orgánicos-inorgánicos) se debe al factor de que la ultra fina, o nano-
dispersión de los rellenos, así como las interacciones locales entre
el relleno y la matriz, conducen a un nivel más alto de propiedades
1 Luz Cecilia Pérez Velásquez. Estudiante de Doctorado en Materiales del Área de Integri-dad y Diseño de Materiales Compuestos del Centro de Investigación en Materiales Avan-zados (CIMAV), Ingeniero Químico y MC. en Alimentos. [email protected]
2 Sergio Gabriel Flores Gallardo. Profesor investigador de Asociado A del Área de Integri-dad y Diseño de Materiales Compuestos del Centro de Investigación en Materiales Avan-zados (CIMAV). Ingeniero Químico y Doctor en Polímeros. [email protected]
3 Patricia de Lira Gómez. Profesora Investigadora de TC de la Unidad Académica de Cien-cias de la Tierra de la Universidad Autónoma de Zacatecas. Ingeniero Minero Metalurgista, Maestra en Ciencias en la especialidad de Metalurgia Extractiva y Doctora en Ciencia de Materiales. [email protected]
4 Tomás Lozano Ramírez. Profesor Investigador del Departamento de Ingeniería Química División de Estudios de Posgrado e Investigación. Coordinador de la Maestría en Ciencias en Ingeniería Química del Instituto Tecnológico de Ciudad Madero. Ingeniero Químico y Doc-torado en Ingeniería Química con especialidad en polímeros. [email protected]
5 Brody, L. A. (2007) Nanocomposite technology in food packaging. FoodTechnology, 61, 10, pp. 80–83.

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
30
que para sus equivalentes micro o macro compuestos, aun con una
disminución de la cantidad de relleno. El potencial interés en estos
materiales es el resultado del mejoramiento en sus comportamientos
de retraso al fuego y estabilidad térmica, propiedades barrera contra
transmisión de gas y vapor, y sus propiedades mecánicas.6
Los efectos del reforzamiento dependen en gran medida de la
nanoestructura representada por la forma de relleno, tamaño, con-
centración y homogeneidad de la distribución de la partícula7. Tí-
picamente, las cargas más adicionadas a matrices poliméricas son:
partículas esféricas (silica, metal y otras partículas orgánicas e ino-
rgánicas), partículas fibrosas (nanofibras y nanotubos) y partículas
laminares (carbono grafito, silicatos y aluminosilicatos laminados, así
como otros materiales laminados). El cambio en el diámetro de la
esfera, diámetro de la fibra y espesor de la lámina, del tamaño mi-
crométrico (compositos) al tamaño nanométrico (nanocompositos),
presenta dramáticas modificaciones en el incremento del área inter-
facial y, con ello, de las propiedades del material compuesto.
Se ha demostrado que el uso de la tecnología de nanocompositos
de polímero/arcilla es una forma útil de producir materiales con un
amplio rango de propiedades ingenieriles. Dichos mejoramientos son
llevados a cabo por la expansión de las capas de arcilla y la dispersión
de las capas de arcillas separadas de manera individual en el políme-
ro.8 Los factores más importantes para esta área de investigación son:
1) dispersión de las nanopartículas inorgánicas en el polímero matriz,
y 2) compatibilidad entre el relleno inorgánico y el polímero orgáni-
co.9 Las propiedades de los nanocompositos de polímero/arcilla se op-
timizan adaptando la morfología (intercalado o exfoliado) del sistema
y la interacción del polímero matriz con las partículas inorgánicas.
6 Duquesne S., C. Jama, M. Le B., R. Delobel, P. Recourt, J. M. Gloagen (2003) Elaboration of EVA-nanoclay systems characterization, termal behavior and fire performance, pp. 1141-1147.
7 Lin J. (2006) “Compression and wear behavior of composites filled with various nanoparticles”, pp. 79-85.
8 Sozer, N. and J. L. Kokini (2008) Nanotechnology and its applications in the food sector. Trends in Biotechnology, 27: (2), pp. 82–89.
9 Lee H., S. Mall, P. He, D. Shi, S. Narasimhadevara, y. yeo-Heung, V. Shanov, M. J. Schulz (2006) Characterization of carbon nanotube/nanofiber-reinforced polymer composites using an instrumented indentation technique, pp. 58-65.

31
Estudio dE nanocompuEstos montmorillonita/pla
Estructura y propiedades de los filosilicatos
De acuerdo con su distribución estructural, los minerales arcillosos
se pueden dividir en las siguientes familias o grupos: filosilicatos bila-
minares, filosilicatos trilaminares y cloritas. A su vez, los filosilicatos
trilaminares comprenden tres familias: esmectitas, micas y minera-
les fibrosos o atapulgita. La familia de las esmectitas, o minerales
expandibles, incluye especies dioctaédricas como la montmorillonita,
nontronita, beidelita, y trioctaédricas como la saponita, sauconita y
hectorita; también se les da el nombre de bentonitas. En los filosilica-
tos trilaminares (Fig.1.1) cada lámina está formada por dos capas de
tetraedros de sílice, que encierran una capa de octaedros de alúmina
o de magnesia, por esta razón se les denomina “trilaminares”, 2:1.
Debido a sustituciones isomórficas de la alúmina dentro de las capas
de sílice (Al +3 por Si+4) o magnesio por aluminio (Mg+2 por Al+3), cada
celda unidad tiene una carga negativa de entre 0.5 y 1.3. Las capas
se retienen junto con una capa de cationes compensantes de carga,
tales como Li+, Na+, K+ y Ca+, que proveen una ruta para enriquecer la
química de intercalación y la modificación de la superficie requerida
para dispersar las arcillas en la nanoescala de los polímeros. La ca-
pacidad de intercambio catiónico (CEC) define el número de cationes
intercapa intercambiables y usualmente se describe como mEq/100g.
El rango de valores va de 60 a 120 para arcillas esmectitas. Las capas
son de 20-200 nm de diámetro y se encuentran en agregados conoci-
dos como tactoides, los cuales puede ser 1 nm o más. La separación
entre láminas es del orden de 10Å.10
10 Bernal, I., H. Cabezas, C. Espitia, J. Mojica & J. Quintero (2003) “Análisis próximo de arcillas para cerámica”. Rev. Acad. Colomb. Cienc. 27, pp. 569-578.

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
32
Figura 1.1. Estructura de los filosilicatos 2:.1
La montorillonita (MMT) es una arcilla natural, perteneciente al gru-
po de las esmectitas, se usa con frecuencia como un relleno nanomé-
trico para nancompositos de polímero, tiene una alta capacidad de
hinchamiento, la cual resulta esencial para un intercalación eficiente
del polímero, y las hojas de silicato apiladas proveen buenas propie-
dades térmicas, tensiles y de barrera molecular.11
Modificación de las arcillas
En estado puro, los filosilicatos son sólo miscibles con polímeros hi-
drofílicos. Para dar miscibilidad con otras matrices de polímero, los
cationes inorgánicos entre las capas de la arcillas —como Na+, Ca+2,
K+, etc.— son reemplazados por cationes orgánicos, produciendo or-
ganoarcillas. El reemplazo de los cationes intercambiables inorgáni-
cos por iones orgánicos de las galerías de las superficies de las arcillas
ayuda a igualar la polaridad de la superficie de la arcilla con la polari-
dad del polímero y a expandir las galerías de la arcilla, esto facilita la
penetración de los espacios de las galerías (intercalación) por las ca-
11 Chang J. y Mu K. M. (2006) “Nanocomposite fibers of poly (ethyleneterephthalate) with montmorillonite and mica: thermomechanical properties and morphology”, pp. 57-69.

33
Estudio dE nanocompuEstos montmorillonita/pla
denas de polímeros. Fukushima y sus colaboradores12, en sus detalla-
dos estudios de compositos polímero/silicato en capas, demostraron
que la lipofilización causada por el reemplazamiento de los cationes
inorgánicos en las galerías de la arcilla natural con surfactantes de
alquilamonio exitosamente las hace compatibles con las matrices de
polímero hidrofóbicos. La arcilla modificada fue así llamada arcilla li-
pofilizada, arcilla organofilica, o simplemente organoarcilla; además,
encontraron que la lipofilización hace posible la expansión de las ga-
lerías de la arcilla y la exfoliación de las capas de silicato en capas
individuales de 1 nm de espesor.
Una de las organoarcillas más empleadas es la arcilla montmori-
llonita modificada con una sal de amonio cuaternaria, cuyo nombre
comercial es Cloisite 10ª, misma que se utiliza de manera principal
como aditivo para plásticos, a fin de mejorar varias propiedades físi-
cas de estos, entre ellas el reforzamiento, HDT y barrera. En la figu-
ra 1.2 se muestran cuatro tipos de MMT orgánicamente modificada,
con sus nombres comerciales: Cloisite 30B (metil-T-bis-2-hidroxietil
amonio) (MT2EtoH), Cloisite 10A (dimetil-bencil- sebo hidrogena-
do-amonio cuaternario) (2MBHT), Cloisite 25A (dimetilhidrogenado
T-2-etilhexil amonio) (2MHTL8), y Cloisite 20A (dimetil-dihidrogenado
T amonio) (2M2HT).13
12 Fukushima, K., Tabuani, D. and Camino, G. (2009b) “Nanocomposites of PLA and PCL based on montmorillonite and sepioliteK”, Materials Science and Engineering C 29, pp. 1433–1441.
13 okamoto (2006), “Recent advances in polymer/layered silicate nanocomposites”, Materials Science and Technology, Vol. 22, No. 7, pp. 756-779.
(A) (B)

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
34
Figura 1.2. Estructura química de los cationes en (A) Cloisite 30B, (B) Cloisite 10A,
(C) Cloisite 25A, y (D) Cloisite 20A (T es sebo conteniendo ≈ 65% C18, ≈30% C16, y ≈ 5% C14)
(okamoto, 2006).
La tabla 1 muestra el rango de la polaridad para Cloisite Na+, Cloisite
30B, Cloisite 10A, Cloisite 25A, Cloisite 93A, Cloisite 20A y Cloisite 15A.
La Cloiste Na+ es la MMT sin modificar, presentando el mayor grado
de polaridad.
Tabla 1. Rango de polaridad de las diferentes cloisites
(C) (D)

35
Estudio dE nanocompuEstos montmorillonita/pla
2. HIPÓTESIS
Las propiedades mecánicas, térmicas y barrera de nanocompuestos
PLA-arcilla pueden mejorarse mediante la incorporación de un agen-
te compatibilizante acrílico, con la finalidad de ampliar su uso en la
industria de alimentos.
3. OBJETIVO
El objetivo de este trabajo fue estudiar el efecto de la adición de un
terpolímero acrílico, como agente compatibilizante, sobre las propie-
dades mecánicas y térmicas en materiales compuestos a partir de
ácido poliláctico y nanoarcillas.
4. MATERIALES Y MÉTODOS
4.1. Materiales
Se uso ácido poliláctico, adquirido en PRoMAPLAST RESINAS, S.A.
DE C.V. (Estado de México); del mismo modo, se utilizaron dos arci-
llas comerciales: montmorillonita Cloisite 30B y Cloisite 10A, dichas
nanoarcillas son arcillas naturales modificadas con cationes orgáni-
cos. El agente compatibilizante fue un terpolímero acrílico P(MMA-c-
BuA-MAA), que se obtuvo por polimerización radical. Las principales
características de los materiales utilizados se presentan en la tabla 2.
Tabla 2. Principales características de los materiales utilizados
Material Estructura química Principales características
PLA
Ácido poliláctico (PLA 2002D NatureWorks®)
Densidad relativa 1.24

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
36
Cloisite 30B*
Southem Clay Products Ing
Sal de amonio cuaternaria de metil bis-2 hidroxietil
Cloisite 10A**Southem Clay Products Ing.
Sal de amonio cuaternaria
Terpolímero Acrílico
Terpolímero acrílico P(MMA-c-BuA-MAA)
(Metil metacrilato-Butil acrilato-Ácido matacrilico)
(Relación en % en peso 87.5 – 10 – 2.5)
* Herrera-Kao and Aguilar-Vega, 2008.
4.2. Etapas experimentales
La parte experimental se llevó a cabo en dos etapas, que se distin-
guieron por el procesamiento mediante el cual se obtuvieron los dife-
rentes nanocompuestos. La primera etapa se realizó en una cámara
de mezclado, en un procesamiento por lotes, mientras que la segunda
etapa fue a través de un procesamiento continuo por medio de un
estruxor. La finalidad de ambas etapas fue analizar el efecto del pro-
cesamiento sobre la exfoliación de los nanocompuestos.
4.3. Preparación de nanocompuestos
4.3.1. Mezclado mecánico
Las arcillas fueron secadas, al igual que el PLA, 24 horas antes de ser usa-
das en la elaboración de los nanocompuestos, a una temperatura cons-
tante de 90ºC. Las distintas mezclas del PLA y arcilla constaron del polí-
mero, 5% de una de las arcillas y 3, 6 ó 9% del terpolímero, y se realizaron
en la cámara de mezclado de un equipo Brabander plasti-corder, modelo
DDRV752, con un juego de rotores roller. La mezcla se hizo con la rampa
de velocidades de acuerdo a la tabla 3, a temperatura constante de 200ºC.

37
Estudio dE nanocompuEstos montmorillonita/pla
Tabla 3. Rampa de velocidades durante el mezclado en la cámara
Velocidad (rpm) Tiempo (min) Etapa
80 6 Introducción del polímero a la cámara
30 5 Adición de la arcilla
80 19Periodo de mezclado
Las mezclas, una vez enfriadas, fueron trituradas en un molino de cuchillas.
4.3.2. Mezclado por extrusión
Al igual que para el mezclado mecánico, las arcillas y los polímeros
fueron secados 24 horas, a temperatura constante de 90ºC, antes de
ser usados en la elaboración de los nanocompuestos. Las distintas
mezclas del PLA y arcilla constaron del polímero, 5% de una de las
arcillas y 9% de terpolímero, y se realizaron en un extrusor mono hu-
sillo Brabander plasti-corder, modelo DDRV752. La mezcla se llevó a
cabo con el programa de temperaturas según la tabla 4.
Tabla 4. Programa de temperaturas (ºC)
Segmento Temperatura
Alimentación 180
Compresión 180
Dosificación 170
Dado 160
Dado 150
Los materiales se pararon por el extrusor a una velocidad de 10rpm,
posteriormente la mezcla se trituró en un molino de cuchillas y vol-
vió a pasarse por el extrusor, luego se trituraron de nuevo las mezclas
y pasaron una vez más por el extrusor, en esta ocasión pasando por
un dado capilar de 2:40; para finalizar, el hilo de las mezclas fue cor-
tado con pinzas.

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
38
4.3.3. Elaboración de películas
Para la elaboración de las películas se tomaron 3.5 g de cada una de
las mezclas de blancos y nanocompuestos, se elaboraron películas en
una prensa Carver, a temperatura de 200ºC aproximadamente y pre-
sión de 10 Ton, usando hojas de teflón para facilitar el desmoldado.
4.4. Caracterización
4.4.1. Difracción de rayos
Las pruebas de difracción de rayos X se realizaron para detectar el
grado de intercalación o exfoliación de cada nanocompuesto, en un
difractometro X’Pert Pro of PANalytical. Las condiciones del análisis de
difracción de rayos X fueron: 40 mA, 40 kV; rango de barrido: 1.00 –
10º, tamaño del paso: 0.02º, tiempo del paso: 4 seg, modo de barrido:
continuo
4.4.2. Calorimetría diferencial de barrido
Las mediciones de la calorimetría diferencial de barrido (DSC) fue-
ron conducidas en la unidad TA instruments, modelo DSC 2920. Cada
muestra (2-13mg) fue corrida con un barrido de temperatura en una
atmósfera de aire. Las muestras fueron calentadas de temperatura
ambiente hasta 200ºC, a velocidad de 10 ºC/min y enfriadas a 35º.
El historial térmico de las muestras fue borrado por un ciclo previo
de calentamiento-enfriamiento a 10ºC/min. El porcentaje de crista-
linidad (Xc) de los polímeros y de los nanocompuestos fue evaluado
tomando en cuenta la cantidad de arcilla presente en las mezclas,
usando la siguiente ecuación (Fukushima, et al., 2009b):
ec- (1)
Donde ΔHm es la entalpía de fusión específica de la muestra, ΔHom es
la entalpía de fusión de la matriz polimérica 100% cristalina —93.0
J/g para el PLA (Kalb and Pennings, 1980; Sánchez, et al., 2005; Ahmed

39
Estudio dE nanocompuEstos montmorillonita/pla
et al., 2009; Bang and Kim, 2011)— y %wtclay es el porcentaje en peso
de la arcilla.
4.4.3. Análisis termogravimétrico
El análisis termogravimétrico (TGA) se hizo en un equipo marca TA
instruments, modelo SDT 2960. El porcentaje de pérdida de peso es
reportado en función de la temperatura, a velocidad de calentamien-
to de 10ºC/min, desde la temperatura ambiente hasta 700ºC, en una
atmósfera de aire.
5. RESULTADOS
5.1 Difracción de rayos X (XRD)
El grado de difracción de rayos X es el método utilizado para la deter-
minación de la altura de las galerías (distancia interplanar, d-spacing)
de las partículas de arcilla.14 En la figura 7 se muestran los resultados
de XRD de las películas de PLA y el compatibilizante acrílico. Como
se observa en dicha figura, los polímeros analizados no presentan pi-
cos de difracción en relación a una fase cristalina, probando que los
polímeros se obtienen inicialmente de manera amorfa. Vale la pena
señalar que el PLA presentó una curva bien definida para todas las
películas en el rango 2θ de 9° a 30°, que es la contribución de la fase
amorfa del PLA. La bibliografía reporta que el PLA es caracterizado
por un pico ancho, con un máximo aproximado de 2θ = 17°, indicando
una estructura completamente amorfa, y que la XRD del PLA no es
influenciada por la presencia de las laminas de nanoarcillas.15
14 Di, y., S. Iannace, E. Di Miao, L. Nicolais (2003) “Nanocomposites by melt intercalation based on polycaprolactone and organoclay”, Journal of Polymer Science Part B: Polymer Physics 41, 7, pp. 670–678.
15 Pluta, M. (2004) “Morphology and properties of polylactide modified by thermal treat-ment, filling with layered silicates and plasticization”, Polymer, 45, pp. 8239-8251.

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
40
2 3 4 5 6 7 8 9 1
4
9
16
25
36
PLA Terpolym
Intensity
2
Figura 7. Curvas de XRD del PLA y del terpolímero.
La figura 8 representa los patrones XRD de los nanocompuestos del PLA con CLo30B y CLo10A,
sin presencia del terpolímero, comparados con los de las arcillas vírgenes. Es evidente que
un cambio de los picos hacia valores más bajos de 2θ se observa en las películas de los
nanocompuestos, lo que indica una intercalación de las arcillas con la matriz polimérica.16
Figura 8. Comparativo de XRD de las CLo10A y CLo30B y sus nanocompuestos con PLA.
16 Pavlidou, S. and C. D. Papaspyrides (2008) “A review on polymer–layered silicate nano-composites. Progress in Polymer Science”, 33, pp. 1119 – 1198.

41
Estudio dE nanocompuEstos montmorillonita/pla
La CLo 30B se caracteriza por un pico de difracción en 2θ = 4.79°, que
corresponde a la reflexión basal (001), lo que representa una distan-
cia interplanar de 1.8 nm, esto se debe a los dos grupos funcionales
hidroxilo (bis-2-hidroxietil) en su galería. Por su parte, la CLo10A está
caracterizada por dos picos de difracción a 2θ = 4.59° y 1.51°, corres-
pondientes a distancias interplanares de 1.9 nm y 4.9 nm, respectiva-
mente. La Cloisite 10A se caracteriza por un grupo funcional aromá-
tico (benceno) unido a ella.
Se analizaron los espacios interplanares correspondientes a las
arcillas de los nanocompuestos PLA/CLo. Para las muestras PLA/CLo
30B y PLA/CLo10A, los primeros picos de difracción se observaron
con un desplazamiento a ángulos más bajos en comparación con los
de las organoarcillas originales, lo cual indica la intercalación de PLA
en las capas de las organoarcilla (figura 8). Los picos de las organoar-
cillas CLo30 (2θ=4.79º) y CLo10A (2θ=4.59º) pasaron a 2,35° y 2,59°
para el nanocompuesto PLA/CLo30B y PLA/CLo10A, respectivamente
(figura 8). El espaciamiento interplanar de los nanocompuesto PLA/
CLo30B fue de 3.7 nm, lo que representa un aumento de 1.9 nm, en
comparación con la organoarcilla original, contrastada a su vez con
el aumento de la distancia interplanar de los nanocompuestos PLA/
CLo10A, que fue sólo 1.5 nm, ya que las películas PLA/CLo10A pre-
sentaron un espaciamiento de 3.4 nm.
Dados los resultados anteriores, es evidente que la intercalación
de la CLo30B en el PLA es mayor que el de la CLo10A. Esto se atri-
buye a la fuerte interacción o miscibilidad entre el PLA y la CLo30B,
lo cual da origen a enlaces de hidrógeno entre el grupo carboxilo de
PLA y el grupo hidroxilo en la galería de CLo30B, y genera también
una disminución significativa de la intensidad máxima, que se pue-
de explicar por la formación de una estructura desordenada en las
galerías de la arcilla. La interacción entre el PLA y la CLo10A no es
tan fuerte, debido a la polaridad débil de cationes de amonio en las
capas de silicato de la CLo10A, por lo que el grado de intercalación es
menor bajo las mismas condiciones de mezclado. otros investigado-
res encontraron resultados similares en la preparación de nanocom-
puestos polímero/arcilla, en los que las fuertes interacciones de tipo
polar favorecieron la intercalación de las arcillas en el polímero. Cabe

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
42
señalarse que el espectro del nanocompuesto PLA/CLo10A presentó
tres picos.
Estos resultados sugieren que la morfología del compuesto es
compleja. El primer pico de difracción que se produjo a 2θ = 2,59° se
ha observado como un cambio a un ángulo menor, en comparación
con el de organoarcilla virgen. Todo ello indica que, durante el proceso
de fusión, las cadena de PLA entran en las galerías de arcilla forzando
las plaquetas, lo que resulta en un aumento de la distancia interpla-
nar. Dicho resultado se atribuyó a la compatibilidad entre el modifi-
cador de la arcilla y la matriz de PLA. El segundo pico de difracción
no cambió mucho, siendo de 2θ = 5,19°, pico de intensidad más baja
que sugiere una menor distribución de arcilla en la matriz del PLA.
El origen de otros picos más pequeños, alrededor de 2θ = 5,85° y 2
θ = 7,73° para PLA/CLo30B y PLA/CLo10A, respectivamente, apuntan
a que una pequeña fracción del la arcilla presenta hojas de aglome-
rados que han contribuido a la formación de una estructura tactoid.17
Una situación similar fue observada también por Kalambur y Rizvi.18
Todo lo cual indica que las arcillas no permiten una intercalación de
macromoléculas en todos los espacios, lo que algunos autores atri-
buyeron a la degradación térmica y pérdida de algunas partes del
tensioactivo de las galerías de la organobentonita, durante el proceso
que causa el colapso de las galerías de la arcilla.19
Los patrones de difracción de rayos X de las arcillas puras
(CLo30B, CLo10A), los nanocompuestos PLA/CLo30B y PLA/CLo10A y
los nanocompuestos con diferente porcentaje en peso del terpolíme-
ro acrílico (3, 6 y 9% en peso) se muestran en las figuras 9 y 10.
17 Rhim, J. W., S. I. Hong and C. S. Ha (2009) “Tensile, water vapor barrier and antimicrobial properties of PLA/nanoclay composite films”, LWT - Food Science and Technology, 42, pp.612 – 617.
18 Kalambur, S. and S. S. H. Rizvi (2005) “An overview of starch-based plastics blends from reactive extrusion”, Journal of Plastic film and Sheeting, 22, pp. 39 – 58.
19 Sinha Ray, S. and M. Bousmina (2005) “Biodegradable polymers and their layered sili-cate nanocomposites: in greening the 21st century materialsworld”, Progress in Materials Science, 50, pp. 962–1079.

43
Estudio dE nanocompuEstos montmorillonita/pla
Figura 9. Curvas de XRD de la CLo30B sus nanocompuestos PLA/terpolímero.
En el caso de los nanocompuestos PLA/CLo30B, a los que se les adi-
cionó el terpolímero acrílico mostraron que éste tiene un ligero efecto
negativo sobre la dispersión y la interacción de la CLo30B en el PLA.
Por su parte, el pico de la CLo30B, en las muestras con 5% en peso
de la organoarcilla y 3% del compatibilizador, presenta un desplaza-
miento menor (3.45º) en comparación con la mezcla sin terpolíme-
ro (3.35º), como se aprecia en la figura 9; diversos autores sugieren
que aunque esta arcilla tiene un tensioactivo con más grupos polares
en relación a otras, el grado de saturación de los cationes intercam-
biables y el espaciamiento inicial menor dentro de las galerías (1,83
nm) son factores importantes que dificultan la exfoliación de estas
nanoarcillas.20 Con un espaciamiento intergalería inicial bajo de la
arcilla 30B, sería más difícil que el polímero se intercalara y su exfo-
liación. Sin embargo, cabe señalarse que las muestras con 6 y 9% en
peso de compatibilizante terpolímero acrílico muestran un cambio
del pico de difracción a ángulos más bajos. Creemos que el cambio
considerable de esta propiedad podría deberse a una alta dispersión
20 Ali Dadfar, S. M., I. Alemzadeh, S. M. Reza Dadfar and M. Vosoughi (2011) “Studies on the oxygen barrier and mechanical properties of low density polyethylene/organoclay nanocomposite films in the presence of ethylene vinyl acetate copolymer as a new type of compatibilizer”, Materials and Design 32, pp. 1806–1813.

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
44
y la compatibilidad de compatibilizador y PLA con el utilizado Cloisi-
te 30B, especialmente en el caso de compatibilizador. Por lo tanto, la
presencia de terpolímero acrílico (3% en peso) disminuye la intercala-
ción de organoarcilla, debido a la competencia en la interacción entre
la PLA, compatibilizador y organoarcilla. Esto podría contribuir a la
aglomeración de las hojas, formando una estructura a tactoid.
Figura 10. Curvas de XRD de la CLo10A sus nanocompuestos PLA/terpolímero.
Por otro lado, todas las muestras con 5% en peso de la Cloisite 10A y
diferentes porcentajes en peso del compatibilizante (figura 10) mues-
tran un cambio del pico de difracción a ángulos más bajos y mayores
espaciamientos interplanares, que van de 1,92 nm para la CLo10A
original a 3,39 nm para el nanocompuesto PLA/CLo10A; mientras que
los picos de reflexión de las muestras con 3, 6 y 9% en peso del ter-
polímero acrílico manifestaron una mayor aumento de las distancias
interplanares, lo cual indica que la estructura ordenada de la arcilla
mineral se intercala con eficacia. Este hecho revela que la arcilla se
dispersa de manera más eficiente (intercalada-compatibilidad) en la
matriz de PLA cuando se utiliza este compatibilizante, en especial
cuando se usa un mayor porcentaje en peso del compatibilizante
acrílico. Se ha informado de la capacidad del PLA para dispersar e

45
Estudio dE nanocompuEstos montmorillonita/pla
intercalar la CLo10A durante la composición fundida21; asimismo,
hemos observado que el grado de dispersión de la arcilla varía con el
contenido compatibilizante.
Los resultados obtenidos en el presente trabajo han demostrado
que terpolímero acrílico tiene una capacidad excepcional para dis-
persar e intercalar este contenido de arcilla. Esto puede atribuirse a
una fuerte interacción entre los grupos polares extremos del derivado
de ácido metacrílico del compatibilizante acrílico y la superficie anió-
nica de la arcilla, bajando su energía superficial y aumentando su
dispersión en la matriz polimérica, todo lo cual indica la posibilidad
de obtener una estructura más dispersa y exfoliada en las muestras
con terpolímero acrílico. Sin embargo, estos supuestos deben ser con-
firmados por otros análisis.
El ANoVA que se presenta en la tabla 5 muestra que las variables,
tipo de arcilla y concentración de terpolímero producen efecto alta-
mente significativo (a nivel de significancia de 0.01) sobre los espacios
interplanares de las arcillas, además se observa un efecto que se debe
a la interacción de dichas variables.
Tabla 5. ANOVA para los espacios interplanares de las arcillas
FV Gl SC CM F P
A 1 0.116204167 0.116204167 228.5983607 6.78338E-11 **
B 3 0.019279167 0.006426389 12.6420765 0.000172004 **
A*B 3 0.032545833 0.010848611 21.34153005 7.73032E-06 **
Error 16 0.008133333 0.000508333
Total 23 0.1761625
Nivel de significancia *p<0.05, **p<0.01, ns no significativo, A = tipo de arcilla, B =
concentración de terpolímero.
21 Chang, J. H., y. U. An, G. S. Sur (2003) “Poly (lactic acid) nanocomposites with various organoclays. I. Thermomechanical properties, morphology, and gas permeability”, Journal of Polymer Science, Part B: Polymer Physics, 41, pp. 94–103.

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
46
Los análisis de diferencias mínimas significativas entre los tratamien-
tos mostraron que, para la concentración de terpolímero, los mayores
espacios interplanares se generaron a una concentración del 9%. En
el caso de tipo de arcilla la 30B implicó las mayores distancias.
5.2. Calorimetría diferencial de barrido (DSC)
El análisis de calorimetría diferencial de barrido (DSC) fue usado para
investigar la transición vítrea (Tg) y los fenómenos de cristalización
y fundido, tanto del PLA como de los nanocompuestos. La Tg, tem-
peratura de fundido (Tm) y entalpias de cristalización y de fundido
(ΔHc, ΔHm) del segundo calentamiento se resumen en la tabla 6. La
Tg se relaciona con la movilidad de las cadenas de la zona amorfa de
las muestras poliméricas, mientras que las temperaturas de fundido
están relacionadas con las zonas cristalinas. El tamaño de los picos
de cristalización y de fundido en los termogramas del DSC es propor-
cional al grado de cristalización de las muestras.
Tabla 6. Principales resultados del DSC
Muestras
Propiedades térmicas
Segundo calentamiento
Matriz Arcilla % de TerpolímeroTg
ºC
Tm
ºC
ΔHc
(J/g)
ΔHm
(J/g)
cc
%
PLA - 0 56.92 150.91 7.93 8.07 9.13
PLA - 3 59.72 153.86 7.63 9.73 11.01
PLA - 6 59.09 154.42 4.72 7.31 8.27
PLA - 9 57.55 153.01 17.17 17.22 19.49
PLA 10A 0 55.73 150.80 8.28 7.61 8.613
PLA 10A 3 60.19 154.41 19.35 17.60 19.92
PLA 10A 6 59.93 154.29 9.69 12.54 14.19
PLA 10A 9 59.36 154.28 17.60 19.67 22.26
PLA 30B 0 56.46 149.31 24.84 25.54 28.91
PLA 30B 3 60.47 155.14 9.35 8.27 9.36
PLA 30B 6 58.76 153.72 13.78 11.87 13.43
PLA 30B 9 49.48 153.96 9.242 8.57 9.70

47
Estudio dE nanocompuEstos montmorillonita/pla
La Tg del PLA, seguida de la cristalización del polímero y la fusión del
polímero, se puede observar en los termogramas de todas las mues-
tras (figuras 11-13). Como puede verse, el PLA tiene una Tg de 56,9° C
y Tm de 150,9° C. Los nanocompuestos PLA/CLo30B y PLA/CLo10A
muestran una Tg de 56,5° C y 55,7° C y Tm de 149,3° C y 150,8° C, res-
pectivamente, las cuales fueron muy similares a la Tg y Tm del PLA.
Estos resultados indican que no hay influencia importante sobre la
transición vítrea y la temperatura de fusión del PLA por la presencia
de las organoarcillas (figura 11). Sin embargo, se advierten algunas
diferencias, como función de la composición de las mezclas. El por-
centaje de cristalinidad Xc en los diferentes materiales compuestos
se presenta en la tabla 6. Mientras Xc del PLA no se vio afectada por
la presencia de CLo10A, el porcentaje de cristalinidad de PLA aumen-
tó de forma notoria por la presencia de CLo30B, pasando de 9 a 29%,
respectivamente. Dicho aumento puede atribuirse a que las capas de
la CLo30B están totalmente dispersas dentro de la matriz de PLA (de
acuerdo a datos de rayos X), esta dispersión completa es posible que
se deba a la interacción de las plaquetas de la arcilla con la colum-
na vertebral del PLA, lo cual permite que la arcilla actúe como un
agente de nucleación. Estos resultados están de acuerdo con los de
otras investigaciones, que señalan el efecto nucleante de la nanoar-
cillas es más pronunciado en los niveles de cargas bajas, 1 a 5% en
peso. Por encima de estos niveles las nanoarcillas puede dificultar el
movimiento de los polímeros, retardando así la cristalización de los
polímeros.22
22 Tjong, S. C. (2006) “Structural and mechanical properties of polymer nanocomposites”, Materials Science and Engineering, 53, 73–197.

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
48
0 50
100
150
200
250
0.0
0.1
0.2
Terpolymer
PLA PLA –
CLO10A PLA –
CLO30B
Figura 11. Termograma del segundo calentamiento del PLA y sus nanocompuestos PLA/CLo30B
y PLA/CLo10A, así como del terpolímero acrílico.
La tabla 6 muestra que la incorporación del compatibilizante a la
mezcla PLA-CLo genera cambios significativos en las propiedades tér-
micas de los nanocompuestos estudiados. En particular, la adición de
diferentes porcentajes en peso del terpolímero acrílico conduce a un
aumento de la Tg y Tm de los nanocompuestos PLA/CLo30B y PLA/
CLo10A, que correspondían aproximadamente a 3° y 5° C, respectiva-
mente. Esto podría deberse a las fuertes interacciones entra las super-
ficies de las plaquetas de las arcillas CLo30B y CLo10A, y los grupos
funcionales sobre el PLA y las cadenas del compatibilizante, el cual
causó reducciones en la movilidad de las moléculas, lo que sugiere
algún tipo de refuerzo de la matriz nanocompuesto por el compatibi-
lizador. Asimismo, en dicha tabla también se advierte que el compati-
bilizante tiene un fuerte efecto sobre el porcentaje de cristalinidad del
PLA en las mezclas PLA/terpolímero, en las cuales se observa que: en
contenidos bajo del compatibilizante (3, 6%) se presentó una cristali-
nidad similar a la del; mientras que en contenidos elevados del terpo-
límero acrílico esta tendencia se invirtió y el Xc aumentó de 9,13 (PLA)
a 19,49 (PLA/Terpolimero 9% en peso). Estas observaciones confirman
una interacción entre el compatibilizante y la matriz de PLA.

49
Estudio dE nanocompuEstos montmorillonita/pla
Ex 5
1 1 2
PLA-
PLA-CLO30B
PLA-CLO30B
PLA-CLO30B
2
5
Temperat
Heatflow
(
P
Figura 12. Termograma del segundo calentamiento del PLA/CLo30B y diferentes porcentajes
de terpolímero.
Del mismo modo, como se aprecia en la tabla 6, la adición de dife-
rentes porcentajes en peso del terpolímero acrílico (3, 6 y 9% en peso)
a los nanocompuestos PLA/CLo30B y PLA/CLo10A genera cambios
significativos en la cristalinidad.
Para los nanocompuestos PLA/CLo30B, con diferentes contenidos
de compatibilizante, se observa una cristalinidad reducida respecto al
PLA/Cloisite 30B, de 28,91% a 9,36%. Esto sugiere que la incorporación
simultánea de arcilla y compatibilizante en el PLA disminuyó la dis-
persión de arcilla y agregados de ésta aparecieron, de acuerdo con los
resultados obtenidos por DRX, debido a la formación de una estructu-
ra de ramificación de cadena larga en el compatibilizante-Cloisite 30B
mezcla,23 que no se incorpora fácilmente en la red cristalina. Dichos
cambios podrían ser entendidos en relación con la competencia entre
el efecto de nucleación de la organoarcilla (como queda demostrado
por el aumento de Tc y Xc para el nanocompuesto) y la inmoviliza-
23 Pluta, M. (2004) “Morphology and properties of polylactide modified by thermal treat-ment, filling with layered silicates and plasticization”, Polymer, 45, pp. 8239-8251.

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
50
ción/restricción de las cadenas poliméricas de las capas de silicato
durante la reordenación para el proceso de cristalización, así como
la restricción física para el crecimiento de las regiones de polímeros
cristalinos.
Ex
5
1 1 2
PLA-
PLA-CLO10A
PLA-CLO10A
PLA-CLO10A
2.
5
Temperatur
Heatflow
P
Figura 13. Termograma del segundo calentamiento del PLA-CLo10A y diferentes porcentajes
de terpolímero.
Los nanocompuestos PLA/CLo10A, con diferentes concentracio-
nes del compatibilizante, (tabla 6) manifiestan un comportamiento
completamente diferente a los que contienen Cloisite 30B. Para los
nanocompuestos con compatibilizante, una cristalinidad mayor se
observa respecto a nanocompuesto sin compatibilizante, que va de
8.61 a 22.26%. Estas observaciones sugieren que el compatibilizante
promovió tanto la intercalación de arcilla, como la distribución uni-
forme y/o exfoliación de la organoarcilla en la matriz del polímero.24
La dispersión de las organoarcillas mejora el efecto de nucleación en
24 Gorrasi, G., V. Vittoria, M. Murariu, A. Da Silva Ferreira, M. Alexandre, Ph. Dubois (2008) “Effect of filler content and size on transport properties of water vapor in PLA/calcium sulphate composites”, Biomacromolecules, 9, pp. 984–990.

51
Estudio dE nanocompuEstos montmorillonita/pla
la matriz PLA. Por su parte, la temperatura de transición vítrea (Tg) de
estos materiales se incrementa 4ºC aprox., confirmando así la apari-
ción de movimientos restringidos de las cadenas del polímero, luego
de la adición de estas partículas de sílice. Además, la formación de un
único pico de fusión a temperatura más alta indica que las partículas
de sílice pueden promover la formación de una estructura cristali-
na estable.25 En todos los casos las entalpías de cristalización fueron
iguales a las entalpías de fusión, lo cual pone de manifiesto que las
películas de referencia son totalmente amorfas; las diferencias apa-
rentes entre estas dos variables entran dentro del error estadístico.
La significancia estadística de resultados del análisis térmico se
presenta en el resumen de los ANoVAS de las diferentes variables de
repuesta de la tabla 7.
Tabla 7. Resumen de los ANOVAS del análisis térmico
FV Tg Tm Hc Hm
A ** Ns ** **
B Ns ** * *
A*B Ns ** ****
Nivel de significancia *p<0.05, **p<0.01, ns no significativo
A = tipo de arcilla, B = concentración de terpolímero
5.3. Análisis termogravimétrico (TGA)
La estabilidad térmica de los materiales poliméricos es estudiada co-
múnmente por análisis termogravimétrico (TGA), en el cual la pérdida
de peso de la muestra, debido a la volatización de productos de la
degradación, se monitorea en función de la temperatura (Alexandre
and Dubois 2000). En la figura 14 se advierte la degradación del PLA y
de los nanocompuestos PLA/CLo, con respecto a la temperatura, y es
posible distinguir dos etapas de reacción durante la degradación del
25 Fukushima, K., D. Tabuani, C. Abbate, M. Arena and P. Rizzarelli (2011) “Preparation, characterization and biodegradation of biopolymer nanocomposites based on fumed sili-ca”, European Polymer Journal, 47, pp. 139–152.

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
52
PLA. La primera etapa representa la descomposición de los finales de
cadena del PLA (antes 300º C). La segunda etapa, entre 300º C y 400º C,
representa el rompimiento aleatorio de las cadenas poliméricas.26 Asi-
mismo, se muestran estas dos etapas de reacción para el PLA, mien-
tras que los nanocompuestos manifiestan sólo la segunda etapa y un
cambio hacia una temperatura más alta (T5%), lo que indica la estabi-
lidad térmica mejorada para los nanocompuestos sobre el polímero
puro. Autores de varios artículos han reportado mejoras similares en
la estabilidad térmica de los nanocompuestos con base en el PLA27.
Figura 14. Curvas de TGA de pérdida de masa para PLA y los nanocompuestos PLA/CLo30B y
PLA/CLo10A.
Las temperaturas de degradación tomadas en cuenta para el análisis
estadístico fueron la temperatura a 5% de pérdida en peso (T5%) y la
temperatura de la tasa máxima de pérdida (Tmax), presentadas en
la tabla 8. La degradación T5% de vírgen PLA y del compatibilizante
se inició a 312,69° C y 283,42° C, respectivamente, así como que la
temperatura de máxima degradación (Tmax) se presentó a 362,29° C
26 Zhang, J., J. Lou, S. Ilias, P. Krishnamachari and J. yan (2008) “Thermal properties of poly (lactic acid) fumed silica nanocomposites: Experiments and molecular dynamics simula-tions”, Polymer 49, pp. 2381– 2386.
27 McLauchlin, A. R. and N. L. Thomas (2009) “Preparation and thermal characterisation of poly (lactic acid) nanocomposites prepared from organoclays based on an amphoteric surfactant”, Polymer degradation and stability, pp. 1-5.

53
Estudio dE nanocompuEstos montmorillonita/pla
y 355,76° C, como se muestra en la tabla 6. Como se esperaba, la es-
tabilidad térmica de la matriz PLA mejora por la presencia de ambas
arcillas, con una mención especial para Cloisite 10A, que confirma su
efecto significativo en la estabilización de la matriz del poliéster, de
hecho, un aumento de la T5% 5.2° y 17.7° C se observó con la CLo30B
y la CLo 10ª, respectivamente, en comparación con PLA puro (tabla 8).
Tabla 8. Resultados de análisis termogravimétrico.
MuestraUnder air
T5% (°C) Tmax (°C)
PLA 312.7 362.3
Terpolímero 283.4 305.7, 355.8
PLA/T3 329.8 358.4
PLA/T6 321.0 363.2
PLA/T9 324.1 362.8
PLA/C30B 317.9 359.6
PLA/C30B/T3 330.9 371.8
PLA/C30B/T6 328.3 375.0
PLA/C30B/T9 328.5 375.4
PLA/10A 330.4 364.1
PLA/10A/T3 332.4 361.1
PLA/10A/T6 331.0 361.7
PLA/10A/T9 327.2 367.4
En lo que se refiere a la Tmax, el comportamiento es diferente en am-
bas arcillas. La CLo 10 presentó un aumento de 2° C; sin embargo, la
CLo30B generó una disminución de este parámetro en el PLA. otros
autores han atribuido consecuencias resultados similares debido al
efecto catalizador de las arcillas, el cual puede catalizar oxígeno que
inicia la degradación térmica de PLA, probablemente a través de un
mecanismo de radicales, porque el oxígeno reacciona con sus dos
electrones no apareados, activando abstracción radical hidrógeno.
Este efecto químico se debe a que la presencia de oxígeno supera el
efecto estabilizador barrera física de las partículas de sílice, disminu-
yendo Tmax de nanocompuestos por debajo del de PLA puro.

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
54
Figura15. Curvas de TGA de pérdida de masa para los nanocompuestos PLA-CLo30B y
diferentes porcentajes de terpolímero.
Por otro lado, se analizaron los resultados obtenidos para las mezclas
PLA/CLo, en presencia de diferentes concentraciones del compati-
bilizante. La estabilidad térmica de la matriz de PLA mejora signifi-
cativamente gracias a la presencia de todas las concentraciones del
terpolímero, en especial con una de 3% en peso (figuras 15-17). De
este modo, los nanocompuestos PLA/CLo10A y PLA/CLo30B, con 3%
en peso, muestran mejoras en T5% de alrededor de 19,7° y 18,2° C,
respectivamente.
Estos comportamientos de estabilidad se atribuyen por lo general
al efecto de las capas de las arcillas dentro de la matriz del polímero,
las cuales actúan como una barrera para el transporte de masa de los
productos volátiles, generados durante la descomposición térmica.
En nuestros resultados, el aumento de la estabilidad térmica puede
explicarse, por un lado, debido al aumento de la dispersión de los na-
noplatelets de la CLo10A, confirmado por rayos-X —superior disper-
sión de los silicatos crea un obstáculo más eficiente en el proceso de
degradación—; sin embargo, en lo que respecta a la CLo30B, creemos

55
Estudio dE nanocompuEstos montmorillonita/pla
que se debe principalmente a las interacciones que se logran con el
agente compatibilizante y, por otro lado, a la disminución de la distri-
bución de la CLo 30B.
Figura16. Curvas de TGA de pérdida de masa para los nanocompuestos PLA-CLo10A y
diferentes porcentajes de terpolímero.
Figura17. Curvas comparativas de TGA de los nanocompuestos con 3% en peso del agente
compatibilizante.

Pérez Velásquez, Flores Gallardo, de Lira Gómez, Lozano Ramírez
56
La significación estadística de la estabilidad térmica de los nanocom-
puestos se presenta en el resumen de los ANoVAS de las diferentes
variables de respuesta (tabla 9).
Tabla 9. Resumen de los ANoVAS de estabilidad térmica
FV %W300º T5% TMax
A Ns ** **
B ** ** *
A*B * * *
Nivel de significancia *p<0.05, **p<0.01, nsno significativo
A = tipo de arcilla, B = concentración de terpolímero.
6. CONCLUSIONES GENERALES
El terpolímero acrílico demostró ser un buen compatibilizante en las
mezclas de PLA y organoarcillas CLo30B y CLo10A obtenidas, tan-
to en cámara de mezclado, como por extrusor, dado que facilita la
intercalación de las arcillas y la matriz polimérica, al tiempo que
promueve mejoras en las propiedades termo–mecánicas de los nano-
compuestos de ambas arcillas.
Las mejoras en las propiedades termo–mecánicas que mostraron
los nanocompuestos con el terpolímero es probable que se debieran
a la gran interacción de las arcillas con los polímeros. Creemos que
un agente compatibilizante como el terpolímero acrílico P (MMA-c-
BuA-MAA) puede considerarse potencialmente interesante para opti-
mizar las propiedades de los polímeros.

57
Clara Hilda Ríos Reyes, Luis Humberto Mendoza Huizar,
Víctor Esteban Reyes Cruz, María Aurora Veloz Rodríguez
ESTUDIo VoLTAMPERoMéTRICo y EFECTo DEL pH EN LoS DEPÓSIToS DE Fe SoBRE
CARBÓN VíTREo
INTRODUCCIÓN
La electrodepositación es un método viable para la obtención de pe-
lículas delgadas metálicas (Schlesinger, 2000), cuyas propiedades son
de gran importancia en la industria electrónica. Además de las pe-
lículas delgadas, se ha incrementado el interés en la obtención de
cúmulos nanométricos, debido a que estos llegan a presentar un in-
cremento en sus propiedades físicas, que los hace buenos candidatos
en aplicaciones del campo de la nanotecnología. En este trabajo pre-
sentamos los resultados obtenidos de cúmulos y películas delgadas
de Fe, obtenidos por métodos electroquímicos, ya que éste presen-
ta propiedades ferromagnéticas (Grujicic y Pesic, 2005). A pesar de
que se han estudiado diversas aleaciones de Fe (Levy, 1969; Venka-
tasetty, 1970; Sarojamma y Rama, 1972; Gowri y Shenoi, 1972; y Aus-
ten, 1970), hay pocos estudios donde se considere al Fe puro (Grujicic,
2005; Sánchez, 2010). De ahí el interés por estudiar depósitos de Fe.
Se encontraron las condiciones adecuadas para el electrodepósito de
hierro, mediante el análisis de los diagramas de zonas de predominio
y de pourbaix correspondientes a un medio acuoso de 0.01 M de FeSo4
y 0.1 M de Na2So4, a una temperatura de 25º C y pH = 2.5 y pH = 5. Se
utilizó la técnica por voltametría cíclica para determinar los poten-
ciales de electrocristalización y se realizaron los depósitos por medio
de técnicas cronoamperométricas y de voltametría lineal. Se estudió
la morfología de los depósitos mediante MEB (microscopía electróni-
ca de barrido) y se analizaron las películas delgadas y los cúmulos

Ríos Reyes, Mendoza Huizar, Reyes Cruz, Veloz Rodríguez
58
por EDS. A partir de lo anterior, pudo observarse que se obtuvieron
cúmulos con un tamaño promedio de 250 nm.
MATERIALES Y MÉTODOS
Estudio electroquímico del depósito de hierro sobre carbón vítreo
Los depósitos de hierro se efectuaron sobre un electrodo de carbón
vítreo (CV), a partir de una solución acuosa 10-2 M de FeSo4 + 0.1M
Na2So4, a un pH = 2.5 (ajustada con una solución 1 M de H2So4) y pH
= 5 (pH natural de la solución), a una temperatura de 25º C. Bajo estas
condiciones, la especie química principal del ion de Fe (II) fue el com-
plejo [Fe(H2o)6]2+, de acuerdo al diagrama realizado con el software
HyDRA, con la respectiva interfase gráfica Medusa (Puigdomenech,
2009; Puigdomenech, 2010). El potencial de equilibrio en el sistema
redox [Fe(H2o)6]2+/Fe0 fue determinado como -0.568 V vs SHE, (-0.810 V
vs Calomel). Todas las soluciones fueron preparadas usando reactivos
grado analítico con agua ultra pura (sistema Millipore-Q). El electrodo
de trabajo fue de carbón vítreo, marca BAS, con un área de 0.071 cm2.
El área expuesta del electrodo fue pulida acabado espejo, con alúmi-
na Alfa Aesar (menor a 0.05 µm) y limpiada ultrasónicamente. Como
contraelectrodo se utilizó una barra de grafito. Como electrodo de re-
ferencia se usó un electrodo saturado de calomel. Los experimentos
electroquímicos se llevaron a cabo en un potenciostato/galvanostato
Princeton Applied Research, modelo 263A, conectado a una computa-
dora personal con el programa PowerSuite, a fin de controlar los expe-
rimentos y adquisición de datos. Se realizó un estudio de voltametría
cíclica en el intervalo de potencial de 0.250 V a –1.100 V para el baño
con el pH = 5 (Sistema I) y otro en el intervalo de 0.250 V a -1400 V
para el baño con el pH = 2.5 (Sistema II); todos los voltamperogramas
se obtuvieron a una velocidad de barrido de 20 mV/s.

Estudio voltampErométrico y EfEcto dEl pH En los dEpósitos dE fE sobrE carbón vítrEo
59
Estudios por SEM y EDS
Las microestructuras de los depósitos se examinaron mediante un
microscopio electrónico de barrido, JEoL JSM 6300, equipado con un
espectrómetro de energía dispersiva de rayos X (EDS). Los depósitos
observados se lograron por medio de la técnica cronoamperométrica
de un paso de potencial. El paso de potencial se aplicó en los valores de
-1.100 V para el Sistema I y de -1.400 V para el Sistema II, durante 120
segundos, iniciando en un potencial de 0.1 V. Además, se realizó un de-
pósito a un potencial de -0.900 V para el Sistema I, aplicando la técnica
de voltametría lineal en el intervalo de 0.1 V a -0.9 V, hacia la dirección
catódica, a una velocidad de barrido de 20 mV/s, 10 veces. Luego de ob-
tener los depósitos, los electrodos se enjuagaron con agua desionizada
para eliminar impurezas producto de las sales de la solución.
RESULTADOS
Estudio termodinámico
Con la finalidad de diseñar un baño de electrodepósito adecuado para
la obtención de los depósitos de hierro, se partió de la construcción
de un diagrama tipo Pourbaix, para el sistema 10-2 M de FeSo4 + 0.1
M Na2So4. En la figura 1 se muestra el diagrama para el Sistema I, en
dicho gráfico es posible observar que la especie predominante en el
sistema, bajo las condiciones experimentales utilizadas, es el sulfato
de Fe (II), el cual pasa por una reacción de hidrólisis y forma la espe-
cie hexaacuo complejo de hierro (II) (Cotton, 1980), que se reduce a Fe
(0) mediante la siguiente reacción:
[Fe(H2o)6]2+ + 2e- ↔ Fe0 + 6H2o Eo=-810 mV vs. Calomel (1)

Ríos Reyes, Mendoza Huizar, Reyes Cruz, Veloz Rodríguez
60
Figura 1. Diagrama tipo Pourbaix para el sistema Fe(II)/Fe(0) con pFe(II) = 2, pSo4 = 0.96 y pNa = 0.7.
En el caso del Sistema II, se observó el mismo comportamiento que el
diagrama de la figura 1. Por otra parte, se realizó un diagrama de solu-
bilidad con el objetivo de observar las especies solubles en la solución
y se pudo constatar que la especie de Fe(II) se encuentra totalmente
soluble en el baño a un pH de 2.5, como se muestra en la figura 2.
Para el baño a un pH = 5 se observó que esta especie no es soluble;
sin embargo, la rapidez con la que se forma el precipitado, debido a la
insolubilidad de la especie (hidróxido ferroso, que es color amarillo),
es lo suficientemente lenta para realizar los depósitos y el estudio
voltamperométrico en el pH natural de la solución.
Figura 2. Diagrama de solubilidad para el sistema Fe(II)/ Fe(0) con pFe(II) = 2, pSo4 = 0.96 y pNa = 0.7.

Estudio voltampErométrico y EfEcto dEl pH En los dEpósitos dE fE sobrE carbón vítrEo
61
Estudio voltamperométrico
La figura 3 muestra el comportamiento voltamperométrico de los sis-
temas I (línea continua) y II (línea discontinua), a una velocidad de
barrido de 20 mVs-1. El barrido se inició en un potencial de corriente
nula de 250 mV, y se continúo hacia la zona catódica. Durante el ba-
rrido directo para el Sistema I, se observó la formación de los picos A
(ver recuadro de la figura 3) y B, a los potenciales de -534 mV y -993
mV, respectivamente. En la inversión del barrido del potencial se ob-
servaron dos cruces, Ec1 y Ec2, en los potenciales de -963 mV y -814
mV, los cuales son típicos de la formación de una nueva fase que in-
volucra un proceso de nucleación (Greef et al., 1985) y el potencial de
equilibrio aparente, respectivamente. En la zona anódica se observó
un pico D en -612 mV, precedido por un pico más pequeño C, ambos
relacionados con la disolución de un depósito de Fe y la oxidación de
hidrógeno; de lo cual se ha reportado que cuando ocurre el depósito
de Fe, hay un proceso simultáneo de reducción de hidrógeno (Díaz et
al.,2008; Greef et al., 1985). Es posible observar que el proceso de elec-
trocristalización de hierro comienza a un potencial de -930 mV (Ep).
Además, el pico A se ha asociado en algunos casos a la presencia de
oxígeno. Sin embargo, se ha apuntado en otros trabajos que el pico
se observa aun cuando la solución sea burbujeada con nitrógeno o
no, por lo que puede deberse a otro proceso (como una adsorción,
por ejemplo). No obstante, con la finalidad de descartar un proce-
so secundario, se realizó un estudio de potencial de inversión y se
encontró que la formación del pico A se debe tanto a un proceso de
adsorción del electrolito soporte, como a un proceso de reducción de
un metal; como pudo constatarse al realizar el mismo estudio con el
electrolito soporte (recuadro de la figura 3 y figura 4). Por otra parte,
el pico B está relacionado con la reducción de hierro (Grujicic, 2005;
Sánchez, 2010). Cercano al valor de potencial de -1200 mV, se observó
la evolución de hidrógeno.

Ríos Reyes, Mendoza Huizar, Reyes Cruz, Veloz Rodríguez
62
Figura 3. Voltamperograma obtenido para el Sistema I (línea continua) y el Sistema II (línea
discontinua), sobre un electrodo de carbón vítreo. El recuadro muestra el Sistema I (línea
continua) junto con el voltamperograma correspondiente al electrolito soporte (línea
punteada).
Por otro lado, para el Sistema II se observó la formación del pico B’, a
un potencial de -1396 mV. En la inversión del barrido del potencial se
vislumbraron dos cruces, Ec1’ y Ec2’, en los potenciales de -1320 mV
y -866 mV, los cuales son típicos de la formación de una nueva fase
que involucra un proceso de nucleación (Greef, 1985) y el potencial de
equilibrio aparente, respectivamente. En la zona anódica se observó
un pico C’ en -636 mV, mismo que está relacionado con la disolución
de un depósito de Fe, junto con un proceso simultáneo de oxidación
de hidrógeno, ya que se ha observado su presencia en sistemas si-
milares (Díaz, 2008). Es posible ver que el proceso de electrocrista-
lización de hierro comienza a un potencial de -1257 mV (Ep’). En el
potencial de -1500 mV fue posible notar la evolución de hidrógeno.

Estudio voltampErométrico y EfEcto dEl pH En los dEpósitos dE fE sobrE carbón vítrEo
63
Figura 4. Voltamperograma obtenido para el Sistema I a un potencial de inversión de -900 mV
(línea continua delgada), a un potencial de inversión de -970 mV (línea continua gruesa) y el
electrolito soporte (línea punteada).
Estudio MEB y EDS
Los depósitos de hierro se consiguieron mediante la técnica cronoam-
perométrica, de un solo pulso, en la que se mantiene el potencial
de corriente nula durante unos pocos segundos antes de realizar el
depósito y, posteriormente, se aplica el potencial en el cual se desea
realizar el electrodepósito. A partir del estudio voltamperométrico, se
observó que el potencial de equilibrio aparente de la reducción de
Fe(II) y la aparición del pico catódico para los sistemas I y II fue de
-814 mV y -963 mV, y de -866 mV y -1320 mV, respectivamente, por lo
que se decidió realizar los depósitos a los potenciales de -900 y -1100
mV para el Sistema I y en -1400 para el Sistema II. La figura 5 muestra
una comparación de cada depósito en los diferentes potenciales.

Ríos Reyes, Mendoza Huizar, Reyes Cruz, Veloz Rodríguez
64
a) b)
c)
Figura 5. Comparación de los depósitos de Fe observados por microscopía electrónica de
barrido, obtenidos a los potenciales de a) -1.100 V y b) -0.900 V para el Sistema I y a un
potencial de c) -1.400 V para el Sistema II, respectivamente.
En la figura 5 es posible observar que existe una marcada diferencia
en la microestructura del depósito dependiente del pH (figura 5a y
5c). En el caso del Sistema I (figura 5a), el depósito que se observa
es homogéneo, con un tamaño de partícula de 250 nm en promedio,
el grano es esférico y tiene una distribución uniforme; en el Sistema
II (figura 5c), se observó un depósito irregular y disperso. Se midió
el tamaño de partícula, que resultó de 250 nm, en promedio. Sin
embargo, al igual que el Sistema I, el depósito fue disperso y no se
observó homogeneidad. En la figura 5b puede verse un depósito a
un potencial de -900 mV para el Sistema I, en dicho caso se realizó
a este potencial pues interesaba constatar la composición química

Estudio voltampErométrico y EfEcto dEl pH En los dEpósitos dE fE sobrE carbón vítrEo
65
del depósito del pico A, presente en el recuadro de la figura 3 y la
figura 4. El depósito observado fue un depósito disperso, con un
tamaño de grano en el intervalo de [300 a 1200] nm y tendencia a
formar bordes en ángulo.
Figura 6. Análisis EDS del depósito de Fe sobre el electrodo de carbón vítreo, obtenido a un
potencial de -0.900 V para el Sistema I.
En la figura 6 se muestra el análisis por EDS realizado a la superficie
del electrodo en el que se hicieron los depósitos y se encontraron pre-
sentes hierro y carbono. El hierro se debe al depósito llevado a cabo,
la presencia de carbono es posible debido al electrodo de trabajo, que
fue de carbón vítreo. Para todos los depósitos mostrados en la figura
5 se realizó un análisis EDS, en todos los casos se apuntó un espectro
similar al mostrado en la figura 6, por lo cual no se incluyen.
De acuerdo al EDS realizado, se observó que la cantidad de hierro
para cada uno de los depósitos fue menor al 1% en peso, respecto a la
superficie de carbón vítreo para el Sistema II, a un potencial de -1400
mV, de 3.18 % y de 4.80 % para el Sistema I, a los potenciales de -1100
mV y -900 mV, respectivamente.

Ríos Reyes, Mendoza Huizar, Reyes Cruz, Veloz Rodríguez
66
DISCUSIÓN
A partir de los resultados anteriores, es posible notar que los pará-
metros electroquímicos encontrados son los adecuados para obtener
tanto películas delgadas, como cúmulos de hierro. Se observó que es
importante tener en cuenta el pH del baño electrolítico, pues aunque
a un pH = 2.5 se tiene sólo la especie de Fe2+ soluble en el baño, la can-
tidad de iones H+ presentes interfiere en el depósito, presentado un
proceso competitivo y la reducción de los iones a hidrógeno gaseoso;
por lo cual el tipo de depósito no es homogéneo, aunque el tamaño de
grano del depósito es muy parecido al del Sistema I, a un potencial de
-1100 mV (figura 5a).
Por otra parte, es evidente en la figura 3 que en los potenciales
a los cuales inicia la electrocristalización de los depósitos de Fe, Ep
y Ep’, para los Sistemas I y II respectivamente, hay un corrimiento
aproximado de 327 mV hacia potenciales más catódicos, lo cual se
ha observado para otros sistemas de Fe en la literatura [2], en los que
se ha estudiado la influencia del pH. De ahí el interés por analizar el
tipo de depósito en los potenciales de -1100mV y -1400 mV, cuando
ya se ha obtenido el depósito de Fe. Como existe un corrimiento del
potencial de electrocristalización, era de esperarse que el depósito
no fuera similar para ambos potenciales, ya que la presencia de la
reducción de los iones hidrógeno tuvo una influencia marcada en la
microestructura del depósito a -1400 mV del Sistema II.
En la figura 3 pudo notarse el influjo del pH en el comportamien-
to electroquímico del baño diseñado, para el cual la especie predo-
minante en ambos pHs fue el ion Fe2+; sin embargo, la solubilidad de
esta especie fue diferente para ambos sistemas (ver figura 2). Se notó
para el Sistema I, pese a que la especie predominante que se observa
de acuerdo al diagrama de pourbaix es el FeSo4, que corresponde a
una especie de Fe2+, la presencia de un precipitado en el baño de elec-
trodepósito después de un día de preparada la solución, por lo que se
sospechó de la presencia de otra especie. Revisando en la literatura,
se encontró que una especie que forma un precipitado a partir de so-
luciones acuosas de hierro es el hidróxido de hierro (II) y el hidróxido
de hierro (III) (Grujicic, 2005), aun en pHs ácidos (Díaz, Calderón, Bar-

Estudio voltampErométrico y EfEcto dEl pH En los dEpósitos dE fE sobrE carbón vítrEo
67
cia y Mattos, 2008). Para saber de qué especie se trataba se realizó un
estudio de voltametría cíclica de disco rotatorio de platino, ya que Xin
Jin et al. (Jin, Gerardine, Botte, 2009) desarrollaron una técnica para la
cuantificación simultánea de Fe2+ y Fe3+ en solución, y se observó sólo
la presencia de Fe2+ (estudio no mostrado). Además, por las caracte-
rísticas del precipitado, que era color amarillo claro, se precisó que se
trataba de la especie Fe(oH)2, y no el Fe2(oH)3, ya que este último no
se avistó en el estudio de disco rotatorio, puesto que forma un preci-
pitado color rojizo, el cual no se observó. Asimismo, fue posible notar
que el pico A de la figura 3 no aparece cuando la solución tiene un
pH de 2.5, debido a que la especie de Fe2+ es totalmente soluble en el
baño, lo cual se comprobó pues, al dejar la solución varios días des-
pués de preparada, no se observó ningún precipitado y no cambió el
comportamiento electroquímico del baño. De acuerdo a la discusión
anterior se planteó que el pico A se debe a la reducción de la especie
de Fe(oH)2 (Jones, 1992) como se muestra en la ecuación (2):
Fe(oH)2 + 2H+ + 2e- = Fe + H2o EFe/Fe(oH)2= -0.576 V vs Calomel (2)
Con la finalidad de verificar que el depósito observado en el pico A no
se debiera sólo a la presencia de otra especie diferente a la de hierro
(una impureza o una adsorción por el electrolito soporte), se realizó
un estudio de potencial de inversión, en el que se determinó que has-
ta -970 mV inicia el depósito de Fe2+ mediante la ecuación (1), por lo
que el depósito se realizó a -900 mV y únicamente se observó un pico
en la zona anódica, debido a la oxidación del depósito previamen-
te obtenido, mismo que está relacionado con el pico A (figura 4). Se
realizó un voltamperograma del electrolito soporte, bajo las mismas
condiciones que en el baño de Fe2+ para descartar algún proceso de
adsorción. En la figura 5b pudo verse que, en efecto, existe un recubri-
miento metálico a este potencial, con el cual está relacionado el pico
A pero, además, que se trata de Fe, como se constató por medio del
análisis de EDS para esa muestra (figura 6).

Ríos Reyes, Mendoza Huizar, Reyes Cruz, Veloz Rodríguez
68
CONCLUSIONES
Se obtuvieron los depósitos tanto de películas delgadas de hierro,
como de nanocúmulos de hierro, en el orden de los 250 nm. Es im-
portante considerar la composición química de los baños. En nues-
tro caso, las mejores condiciones de depósito fueron con el sistema
CV/10-2 M de FeSo4 + 0.1M Na2So4, a un pH de 5. Bajo estas circuns-
tancias la especie predominante fue el [Fe(H2o)6]2+ con un potencial
de reducción de Eo=-810 mV vs. Calomel. Los depósitos fueron unifor-
mes y esféricos. A este mismo pH, se encontró un depósito también
de Fe, pero debido a la especie [Fe(oH)2], para el cual el depósito fue
bastante irregular. Para el Sistema II, a un pH=2.5, se observó que
aunque la única especie predominante es [Fe(H2o)6]2+, el depósito se
ve fuertemente afectado por la reducción simultánea de hidrógeno,
obteniéndose una microestructura irregular y dispersa por el proceso
competitivo.
AGRADECIMIENTOS
C. H. R. R. agradece la beca de estancia posdoctoral otorgada por Co-
NACyT, así como el apoyo en infraestructura para la realización de
este trabajo, por parte de la UAEH. Todos los autores agradecen al Dr.
Juan Hernández (UAEH) la asistencia técnica en la obtención de las
imágenes de SEM y el análisis EDS.
Bibliografía
Cotton F. A., G. Wilkison (1980), Advanced Inorganic Chemistry, 4th ed., New york, Wi-
ley/Interscience.
D. Grujicic y B. Pesic (2005), Electrochimica Acta, 50, p. 4405.
Denny A. Jones (1992), Principles and Prevention of Corrosion, New york, Macmillan
Publishing Company, p. 58.

Estudio voltampErométrico y EfEcto dEl pH En los dEpósitos dE fE sobrE carbón vítrEo
69
Díaz, S. L., J. A. Calderón, o. E. Barcia, o. R. Mattos (2008), “Electrochimica”, Acta 53,
p. 7426.
Díaz, S. L., o. R. Mattos, o. E. Barcia y F. J. Fabri Miranda (2008), Journal of Electro-
analytical Chemistry 617, p. 194.
E. M. Levy (1969), Plating 56 p. 903.
Greef R., R. Peat, L. M. Peter, D. Pletcher & J. Robinson (1985) “Instrumental Methods
in Electrochemistry”, Ch. 9, Chichester, U. K., Ed. Ellis Horwood, Southampton
Electrochemistry Group.
H. E. Austen (1970), J. Electrochem. Soc. 117, p. 403.
H. V. Venkatasetty (1970), J. Electrochem. Soc. 117, p. 403.
Ignasi Puigdomenech (aug. 2009), Hidrochemical Equilibrium-Constant Database, Ver-
sión 18, Inorganic Chemistry, Stockholm, Sweden, Royal Institute of Technology
100 44.
Ignasi Puigdomenech (dec. 2010), Make Equilibrium Diagrams Using Sophisticated Al-
gorithms, 32 bits, Versión 6, Inorganic Chemistry, Stockholm, Sweden , Royal In-
stitute of Technology 100 44.
M. Aguilar Sánchez (2010), “Formación y crecimiento electroquímico de núcleos
nanométricos de metales y aleaciones. Fundamentos, aplicaciones y control
estructural”, tesis doctoral, México, D. F., UAM-Azcapotzalco.
M. Sarojamma y T. L. Rama Char (1972), Met. Finish. 70 (9), p. 36.
M. Schlesinger y M. Paunovic (2000), Modern Electroplating, 4th ed., Wiley, New york,
Ny, pp. ix, 461.
S. Gowri y B. A. Shenoi (1972), Met. Finish. 70 (6), p. 30.
Xin Jin Æ, G. Gerardine, J. Botte (2009), “Appl Electrochem 39”, p. 1709.


71
Nancy Ramos Lora, Luis Humberto Mendoza Huizar, Clara Hilda Ríos Reyes, Eduardo García Sánchez, Patricia de Lira Gómez3
ESTUDIo ELECTRoCINéTICo DEL PRoCESoDE ELECTRoDEPoSITACIÓN DE CoBALTo
SoBRE CARBÓN VíTREo
INTRODUCCIÓN
Los materiales construidos a base de cobalto han suscitado un gran
interés, debido a sus potenciales aplicaciones en campos tanto cien-
tíficos como tecnológicos. Hasta donde sabemos, la electrodeposita-
ción de cobalto a partir de soluciones amoniacales ha recibido poca
atención, aun cuando las propiedades complejantes del ión amonio
pueden utilizarse para modular las propiedades del cobalto deposi-
tado a través de una especiación química.[23] Soto et al.[4] y Palomar-
Pardavé et al.[5] investigaron la electrodepositación de cobalto a partir
de soluciones amoniacales a base de cloruro sobre carbón vítreo (CV)
y encontraron que el proceso de nucleación es del tipo progresivo,
seguido de un crecimiento tridimensional. En otro estudio, Mendoza-
Huizar et al.[6] encontraron evidencias de la existencia de un proceso
de depósito a subpotencial de cobalto sobre carbón vítreo a partir de
soluciones amoniacales.
A pesar de las ventajas que exhiben los baños amoniacales para
controlar el proceso de deposito de cobalto, es importante mencio-
nar que los iones (NH4)+ en la solución se adsorben sobre el electro-
do polarizado y los núcleos de cobalto recién formados, esto último
ocasiona un proceso competitivo entre los iones H+ y el (NH4)+, lo cual
provoca una modificación del ambiente de nucleación del cobalto so-
bre el electrodo.[7] Adicionalmente, los iones (NH4)+ pueden adsorberse
de forma preferencial en ciertas orientaciones de la superficie, retar-
dando la velocidad de crecimiento del cobalto.[7] Asimismo, es bien

Ramos Lora, Mendoza Huizar, Ríos Reyes, García Sánchez, de Lira Gómez
72
sabido que los iones (NH4)+ presentes en la solución electrolítica for-
man complejos con los iones metálicos del baño electrolítico, lo que
retarda su velocidad de oxidación.[8]
Por otro lado, son pocos los estudios que han considerado la in-
fluencia del anión So4-2 durante el proceso de electrodepositación de
cobalto.[9, 10] Se ha reportado que el So4-2 induce un proceso de ab-
sorción competitiva sobre la superficie del electrodo. En adición, el
ión sulfato causa un cambio en la forma de la curva voltamperomé-
trica, produciendo nuevos picos que parecen ser causados por una
coadsorción inducida por adátomos.[11] Dado lo anterior, en el presen-
te trabajo se llevó a cabo un estudio cinético del proceso de electro-
depositación de cobalto sobre GCE, considerando la influencia de los
iones (NH4)+ y So4
-2, con la intención de aumentar el conocimiento
disponible sobre este sistema.
METODOLOGÍA
Los depósitos de cobalto sobre carbón vítreo se obtuvieron a partir
de una solución que contenía 10-1 M of CoSo4 + 1M (NH4)2So4. Todas
las soluciones se prepararon utilizando reactivos grado analítico con
agua ultrapura (Millipore-Q system) y fueron desoxigenadas burbu-
jeando nitrógeno por quince minutos antes de cada experimento. El
electrodo de trabajo fue una punta de CV provista por BAS™ con una
área de 0.071 cm2. La superficie expuesta fue pulida a acabado espejo,
utilizando alúmina nanométrica. Se empleó una barra de grafito con
área expuesta mucho mayor que la del electrodo de trabajo como
contraelectrodo. Un electrodo de Ag/AgCl fue usado como electrodo
de referencia y todos los potenciales medidos se refieren a esta escala.
Los experimentos electroquímicos se realizaron en un potenciostato
BAS conectado a una computadora personal, a través del software
BAS100W. Para verificar el comportamiento electroquímico del elec-
trodo en el baño electrolítico, se realizó un estudio voltamperométrico
en la ventana de potencial de 0.600 a -1.300 V. El mecanismo cinético
del cobalto depositado sobre CV se estudió bajo condiciones poten-
ciostáticas, mediante el análisis de los transitorios experimentales.

73
Estudio ElEctrocinético dEl procEso dE ElEctrodEpositación dE cobalto sobrE carbón vítrEo
RESULTADOS Y DISCUSIÓN
Estudio voltamperométrico
Por medio de la técnica de voltamperometría cíclica, se determinaron
los potenciales de inicio de cristalización y de disolución del depósi-
to de cobalto sobre la superficie del electrodo de trabajo. La figura 1
muestra un voltamperograma típico para el sistema CV/10-1 M CoSo4
+ 1.0 M (NH4)2So4 cuando se somete a un barrido de potencial de 0.6
a -1.2 V, a una velocidad de barrido de 5 mVs-1. El barrido se inició en
600 mV, en la región de corriente nula donde no se registran procesos
electroquímicos en la superficie del electrodo; se continúa el barrido
en dirección catódica y aproximadamente en -1094 mV se observa
el inicio de la disminución de corriente (Ecrist.), lo cual se debe a un
proceso de electrocristalización simultáneo con la evolución de hi-
drógeno. En -1200 mV (Ec, Jc), se invierte el sentido del barrido hacia
la región anódica y se detecta un potencial de cruce (-1043 mV Ecruce),
mismo que se ha relacionado con un efecto autocatalítico del siste-
ma.[12] El proceso continúa hacia la región anódica, donde se deter-
mina un segundo potencial de cruce (Eequia), que puede atribuirse al
potencial de equilibrio aparente del sistema Co/Co2+. Continuando en
esta dirección, se registró un pico en -671 mV (Ea1), el cual es asocia-
do a la formación de una fase de cobalto, mientras que los otros dos
picos (-399 mV_Ea2 y 235 mV_Ea3) se asocian a la disolución de cobalto
previamente depositado durante el barrido catódico.

Ramos Lora, Mendoza Huizar, Ríos Reyes, García Sánchez, de Lira Gómez
74
-20
-10
0
10
20
-1400 -900 -400 100 600
-7
-5
-3
-1
-1000 -800 -600 -400
E (mV) vs Ag/AgCl
j (m
Acm
-2)
Ecrist
Ec , Jc
Ecruce
Ea1
Eequia
Ea2 Ea3
j (m
Acm
-2)
E (mV) vs Ag/AgCl
Ea1
Figura 1. Voltamperograma cíclico típico obtenido en CV/10-1 M CoSo4 + 1.0 M (NH4)2So4 a una
velocidad de barrido de 5 mVs-1.
Una vez determinados los potenciales de electrocristalización, se rea-
lizaron voltamperogramas cíclicos a diferentes velocidades de barri-
do, para identificar el comportamiento del depósito sobre el electrodo
de trabajo. La figura 2 muestra que, conforme aumenta la velocidad
de barrido, el potencial de cristalización (Ecrist) se desplaza hacia va-
lores catódicos; esto indica que se necesita un mayor requerimiento
energético para depositar el ión metálico sobre la superficie del elec-
trodo a altas velocidades de barrido.

75
Estudio ElEctrocinético dEl procEso dE ElEctrodEpositación dE cobalto sobrE carbón vítrEo
-50
-30
-10
10
-1200 -1000 -800
-80
-60
-40
-20
0
20
40
-1300 -800 -300 200E (mV) vs Ag/AgCl
j (m
Acm
-2)
j (m
Acm
-2)
E (mV) vs Ag/AgCl
5 mVs-1
1020
-jP
Ecrist
5 mVs-1
1020304050
304050
Ea3
Ea2
Ea1
Figura 2. Voltamperogramas cíclicos típicos obtenidos a diferentes velocidades de barrido en
CV/10-1 M CoSo4 + 1.0 M (NH4)2So4
El potencial de pico asociado con la reducción de una fase de cobalto
(Ea1) se localiza en -671 mV y no mostró un desplazamiento aprecia-
ble en función de la velocidad de barrido. El proceso de disolución de
cobalto (Ea2 y Ea3) presenta un desplazamiento hacia la región anódi-
ca, indicando que a altas velocidades de barrido la energía necesaria
para disolver el depósito es menor. Los cambios en los valores de los
potenciales de electrocristalización, de equilibrio aparente y de cruce,
fueron proporcionales al cambio de la velocidad de barrido, mientras
que los potenciales de equilibrio aparente y cruce disminuyeron con
el aumento de la velocidad de barrido. A partir de los voltamperogra-
mas cíclicos mostrados en la figura 2, se determinó el tipo de control
en el proceso de depósito, a través del trazado de la densidad de co-
rriente máxima del pico de reducción (-jP), en función de la velocidad
de barrido (v1/2) y de acuerdo con la ecuación de Berzins–Delahay (ec.
(1))[13]:

Ramos Lora, Mendoza Huizar, Ríos Reyes, García Sánchez, de Lira Gómez
76
(1)
donde jP es la corriente máxima (Amperes), n es el número de elec-
trones transferidos, A es el área (cm2), C0 es la concentración en la
solución (M), D es el coeficiente de difusión (cm2s-1) y v es la velocidad
de barrido (volts s-1). El comportamiento lineal (ver figura 3) sugiere
que se tiene un proceso controlado por difusión.
v1/2 (mV1/2s-1/2)
-jP
(mA
cm-2
)
10
20
30
40
2 3 4 5 6 7 8
Figura 3. –jP vs velocidad de barrido (v1/2) para CV/10-1 M CoSo4 + 1.0 M (NH4)2So4.
Estudio cronoamperométrico
Es bien sabido que la formación de una nueva fase requiere de un
proceso de nucleación y crecimiento.[14, 15] Los estudios experimenta-
les de la formación electroquímica de fases pueden llevarse a cabo,
bien sea por observación directa de la superficie del electrodo, de-
terminando la variación con el tiempo del número de cristales en
la superficie del electrodo;[16, 17] o por el procedimiento indirecto de
21
21
023
367 vDACnjP =

77
Estudio ElEctrocinético dEl procEso dE ElEctrodEpositación dE cobalto sobrE carbón vítrEo
relacionar la corriente con el número de núcleos,[18, 19] para lo cual es
necesario conocer la velocidad de crecimiento del depósito. La figura
4 muestra una familia de transitorios de corriente–tiempo, obteni-
dos durante la electrodepositación de cobalto sobre carbón vítreo al
aplicar diferentes pulsos de potencial en la superficie del electrodo, a
partir de una solución de 10-1 M CoSo4 en 1.0 M (NH4)2So4.
0
5
10
15
20
25
30
0 20 40 60 80 100
j (m
Acm
-2)
t (s)
-910-900
-990-1000 mV
-980-970-960-950-940-930-920
Figura 4. Transitorios de corriente registrados durante la electrodepositación de cobalto sobre
CV/10-1 M CoSo4 + 1.0 M (NH4)2So4.
Para determinar el mecanismo de nucleación y crecimiento, cada
transitorio experimental mostrado en la figura 4 se comparó con su
respectiva curva adimensional, cada una de las cuales fue construida
sustituyendo las coordenadas de sus máximos localizados (tmáx, jmáx)
con el modelo del nucleación propuesto por Scharifker y Hills,[20] que
permite clasificar el mecanismo de nucleación y crecimiento como
instantáneo —ec. (2)—: [20]

Ramos Lora, Mendoza Huizar, Ríos Reyes, García Sánchez, de Lira Gómez
78
(2)
o progresivo —ec. (3)—: [20]
22
2
2
3367.2exp1225.1
⎪⎭
⎪⎬⎫
⎪⎩
⎪⎨⎧
⎥⎥⎦
⎤
⎢⎢⎣
⎡⎟⎟⎠
⎞⎜⎜⎝
⎛−−=
máx
máx
tt
ttJm
J (3)
La figura 5 muestra la comparación del transitorio experimental, ob-
tenido a -970 mV con las curvas teóricas adimensionales generadas
por las ecuaciones (2) y (3). observe que para un t/tmax<3 hay una
respuesta a una nucleación progresiva 3D, pero a tiempos mayores
el comportamiento general del transitorio no es bien descrito por las
ecuaciones (2) y (3). Este hecho sugiere que hay una contribución adi-
cional al proceso de nucleación y crecimiento.
Palomar–Pardavé et al.[21] propusieron que durante la electrodeposi-
tación de cobalto ocurre simultáneamente la reducción de hidrógeno
en un crecimiento 3D, controlado por difusión, por lo que la densidad
de corriente total está dada por la ecuación (4):
(4)
donde:
Constante de reducción de hidrógeno: FzPKprPR
1= (5)
Número de sitios activos de nucleación: (6)
Velocidad de nucleación: 3PA = (7)
21
0
*1
1
2⎟⎟⎠
⎞⎜⎜⎝
⎛
=
πρMC
PP
2
2
2
2564.1exp19542.1⎪⎭
⎪⎬⎫
⎪⎩
⎪⎨⎧
⎥⎦
⎤⎢⎣
⎡⎟⎟⎠
⎞⎜⎜⎝
⎛−−=
máx
máx
tt
ttJm
J
( ) ( ) ( )( )⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
⎭⎬⎫
⎩⎨⎧
⎥⎦
⎤⎢⎣
⎡ −−−−−−−×⎟
⎠⎞
⎜⎝⎛ −+= −
3
322
1
4*1
exp1exp1)(
PntP
ntPntPPtjtotal
N0 =P2
π *KD
21
08* ⎟⎟
⎠
⎞⎜⎜⎝
⎛=
ρπC
K

79
Estudio ElEctrocinético dEl procEso dE ElEctrodEpositación dE cobalto sobrE carbón vítrEo
Coeficiente de difusión
(8)
= 0.1 M, MCo =58.933 (gmol-1), p = 3.1416, ρCo = 8.9 gmol-1, F= 96.6 kJVolt-1, ZPR = 1, * K = 0.53140475, n = tiempo de inducción del
proceso de nucleación y crecimiento, -E = pulso de potencial, KPR =
constante de reducción de hidrógeno, D = coeficiente de difusión, N0 =
número de sitios activos de nucleación, A = velocidad de nucleación,
n = tiempo de inducción.
La ecuación (4) considera la corriente asociada con la contribu-
ción, debido al proceso de reducción de cobalto (j3d - dc) y la corriente
asociada a la reducción de hidrógeno (jPR). Esta última contribución
es la que ocasiona que los adimensionales —ecuaciones (2) y (3)— no
sean capaces de describir el comportamiento total de los transitorios
mostrados en la figura 4.
La figura 6 muestra la comparación del transitorio experimental
obtenido a -970 mV, con la curva teórica generada a partir de un ajus-
te no lineal de los datos experimentales a la ecuación (4).
Figura 6. Comparación entre un transitorio experimental ( —), durante la electrodepositación
de cobalto sobre la superficie de carbón vítreo a un pulso de potencial de -970 mV, con la curva
teórica (o) generada a partir de un ajuste no lineal de los datos experimentales a la ecuación (4).
0
21
4
2FCPD π
=
02468
1012141618
0 20 40 60 80 100
j (m
Acm
-2)
t (s)
Data: Data1_B Model: Nucleación
Chi^2/DoF = 0.03507 R^2 = 0.99881
P1 0.00389 P2 138.58598 P3 0.00113 P4 49.89520 n 0.01198
+20Co
C

Ramos Lora, Mendoza Huizar, Ríos Reyes, García Sánchez, de Lira Gómez
80
Es claro que el modelo expresado por la ecuación (4) predice satisfac-
toriamente el comportamiento del transitorio experimental, para un
proceso de nucleación y crecimiento 3D. Las constantes físicas obte-
nidas a partir de los mejores parámetros del ajuste no lineal de los
datos experimentales a la ecuación (4) se resumen en la tabla 1.
Tabla 1. Parámetros y datos cinéticos del análisis experimental de los transitorios
corriente–tiempo, de acuerdo a la ecuación (4).
-E
/ mV
P1*
(x10-3)P2 (x102) P3 P4(x10-3) nx10-3 (s-1)
KPR x 10-5
(mol cm-2 s-1)
Dx10-3
(cm-2 s-1)
N0x105
(cm-2)
A
(s-1)
900 7x10-6 18.81 0.90 38.46 4.23x10-4 1.11x10-5 1.87 0.59 0.90
910 3x10-3 10.84 1.67 46.68 1.30x10-11 4.78x10-3 2.07 0.31 1.67
920 3.25 56.48 2.73 2.37 115.99 5.18 46.62 7.25 2.73
930 4.59 142.20 5.04 1.88 113.86 7.31 41.53 2.04 5.04
940 3.09 78.79 10.46 2.70 27.41 4.92 49.76 9.47 10.46
950 4.72 40.19 15.41 2.29 11.93 7.52 45.83 5.25 15.41
960 3.89 139.20 29.13 2.71 11.93 6.20 49.86 16.31 29.13
970 3.9 138.58 49.89 2.71 11.98 6.20 49.86 16.63 49.89
980 5.30 209.15 95.13 2.35 9.55 8.45 46.43 26.96 95.13
990 6.40 160.50 134.85 1.96 7.97 0.10 42.40 22.66 134.85
1000 7.87 356.97 182.23 1.68 8.22 0.12 39.25 54.43 182.23
La contribución de la evolución de hidrógeno, a partir de los transito-
rios mostrados en la figura 4, se puede estimar a partir de la ecuación
(9), considerando sólo la contribución de la densidad de corriente de
reducción de hidrógeno: [21]
( ) ( )tSPtjPR 1= (9)
( ) ( )⎪⎭
⎪⎬⎫
⎪⎩
⎪⎨⎧
⎭⎬⎫
⎩⎨⎧
⎥⎦
⎤⎢⎣
⎡ −−−−−×⎟⎟
⎠
⎞⎜⎜⎝
⎛=
3
32
21
0 exp1exp1
2P
tPtP
MCtS
πρ
(10)
El la figura 7 se muestra la comparación entre un transitorio experi-
mental (-970 mV) ajustado a la ecuación (4), las contribuciones indi-

81
Estudio ElEctrocinético dEl procEso dE ElEctrodEpositación dE cobalto sobrE carbón vítrEo
viduales del proceso de nucleación (j3D–dc) y la reducción de hidrógeno
(jPR). [21] En promedio, la contribución del proceso de evolución de hi-
drógeno a la corriente total fue del 10%.
-5
0
5
10
15
20
0 20 40 60 80 100
j (m
Acm
-2)
t (s)
jPR
j3D-dc
Figura 7. Comparación entre el transitorio experimental -970 mV (o), ajustado con la
ecuación (4), las contribuciones individuales del proceso de nucleación (j3D–dc) y la reducción
de hidrógeno (jPR).
A partir de la teoría atomística es posible obtener el tamaño del nú-
cleo crítico [23] de cobalto de la dependencia potencial de A con la
ecuación (11): [23]
(11)
donde k es la constante de Boltmann (1.381x10-23 JK-1), T la tempera-
tura absoluta (273.15 ºK), e0 la carga del electrón (1.60x10-19 C), z la
carga, D el coeficiente de difusión (cm2 s-1) y v la velocidad de barrido
(volt s-1). Al sustituir en la ecuación (11) el valor de α = 0.5 y el valor
α−⎟⎠
⎞⎜⎝
⎛⎟⎠
⎞⎜⎝
⎛=dEAd
zekTnc
ln0

Ramos Lora, Mendoza Huizar, Ríos Reyes, García Sánchez, de Lira Gómez
82
dlnA/dE = 0.0549, como resultado de la dependencia experimental del
ln A dentro del intervalo potencial de 0.90 – 1 V (figura 8), se obtiene
nc = 0. Dicho resultado implica que cada sitio activo en la superficie
del electrodo de carbón vítreo actúa como núcleo crítico.[24] El núcleo
crítico es estable y está compuesto por un átomo adsorbido sobre un
sitio activo. [25]
-E (mV)
lnA
(s-1
)
-2
0
2
4
6
880 930 980 1030
Figura 8. ln A vs –E (mV). Los valores de A (o) fueron determinados a partir de la ecuación (4).
CONCLUSIONES
Al estudiar el proceso de depósito de cobalto a partir de una solución
10-1 M CoSo4 en 1.0 M (NH4)2So4 a pH = 5.01, sobre el substrato de car-
bón vítreo, utilizando la voltamperometría cíclica a diferentes veloci-
dades de barrido, se encontró que el proceso de deposición de cobalto
es controlado por difusión. También se observó que a mayor veloci-
dad de barrido, mayor es el requerimiento energético para depositar

83
Estudio ElEctrocinético dEl procEso dE ElEctrodEpositación dE cobalto sobrE carbón vítrEo
el ion metálico sobre la superficie del electrodo. Los transitorios expe-
rimentales presentan una forma de crecimiento 3D progresivo y evo-
lución de hidrógeno durante la deposición de cobalto. Al determinar
los parámetros cinéticos de los depósitos, se apreció que cuando se
aumenta el valor del sobrepotencial aplicado, hay un incremento en
el valor de la densidad numérica de sitios activos de nucleación y de
la velocidad de nucleación. En promedio, la evolución de hidrogeno
corresponde al 10% de la corriente registrada en los transitorios ex-
perimentales.
Bibliografía
Arbib M., Zhang B., Lazarov V., Stoychev D., Milchev A., Buess-Herman C., J. Electroa-
nal. Chem., 510 (2001), 67.
Bao, Z. L., Kavanagh, K. L. Journal of Crystal Growth, 287 (2006), 514.
Berzins, T. and Delahay, P. J. Am. Chem. Soc., 75 (1953) 555.
Bubendoeff, J. L., Mény, C., Beaurepaire, E., Panissod, P., Bucher, J. P., Eur. Phys. J., B–17
(2000), 635.
Fleischmann M., Thirst H. R., Trans.Faraday Soc., 51 (1955), 71.
Fleischmann M., Thrisk H. R., Electrochim. Acta, 2 (1960), 22.
Floate, S., Hyde, M., Compton R.G., J. Electroanal. Chem., 523 (2002), 49.
Gómez, E., Marin, M., Sanz, F. and Valles, E., J. Electroanal. Chem., 422, (1997), 139.
Greef, R., Peat, R., Peter, L.M., Pletch er D., and Robinson J., 1985, Instrumental.
Grujicic, D., Pesic, B. Electrochimica Acta, 49 (2004) 4719.
Hamada, H., Haneda, M., Kakuta, N., Miura, H., Inomi, K., Nanba, T., Qi Hua, W.,
Veno, A., ohfune, H., Udagawa, y Chem. Lett., 26 (1997), 887.
Hills G, J., Schiffrin D. J., Thompson J., Electrochim. Acta, 19 (1974), 657.
Jiménez, V.M., Fernández, A., Espinos, J.P., González-Elipe, A.R, J. Electron Spectrosc.
Relat. Phenom., 71 (1995) 61.
Kaischew R., Mutaftchiew B., Electrochim. Acta, 10 (1965), 643.
Mendoza-Huizar, L.H., Rios-Reyes, C.H., Rivera, M., Galán-Vidal, C. A. Advances in
Technology of Materials and Materials Processing, 8 [2] (2006), 152.
Methods in Electrochemistry, Ellis Horwood, Chichester, Ch. 9.
Milchev A., Contemp. Phys., 32 (1991), 321.

Ramos Lora, Mendoza Huizar, Ríos Reyes, García Sánchez, de Lira Gómez
84
Milchev A., Electrocrystallization, Fundamentals of Nucleation and Growth, Kluwer Aca-
demic Publishers, Boston, 2002.
Palomar P. M., Scharifker B. R., Arce E. M., Romero R. M., Electrochim. Acta, 50 (2005),
4736.
Palomar-Pardavé, M., González, I., Soto, A.B., Arce, E.M., J. Electroanal. Chem., 443
(1998), 125.
Scharifker B., Hills G., Electrochimica Acta, 28 (1983), 879.
Soto, A.B., Arce, E.M., Palomar-Pardavé, M., González, I., Electrochim. Acta, 41 (1996),
2647.
Tanaka, M., Mukaia, M., Fujimuri, y., Kondoh, M., Tasaka, y., Baba, H., Usami, S Thin
Solid Films, 281-282 (1996), 453.
Toshev S., Milchev A., Popova K., Markov I., C. R. Acad. Bulg. Sci., 22 (1969), 1413.
Wheeler, D.R., Wang, J.X., Adzic, R.R. J. Electroanal. Chem. 387 (1995) 115.

85
Erasmo orrantia Borunda, Hilda Amelia Piñón Castillo, Sandra Ixmucamé Concha Guerrero, Blanca Sánchez
Ramírez, Silvia Lorena Montes Fonseca, Carlos Arzate Quintana, Vicente Rodríguez González, José Alberto
Duarte Möller y María Antonia Luna Velasco
IMPACToS DE LA NANoTECNoLoGíA ENEL MEDIo AMBIENTE y LA SALUD HUMANA
Los productos de la nanotecnología se diseminan rápidamente, por ello
ejercerán influencia en el medio ambiente y la salud humana, es impor-
tante evaluar su impacto en ambas áreas mediante estudios técnicos y
científicos que nos permitan averiguar sus efectos para darlos a conocer
a la comunidad científica, sector productivo, gobierno y sociedad en su
conjunto; se espera que los resultados obtenidos hasta el momento se
traduzcan en las acciones gubernamentales necesarias para regular su
utilización, dentro de un marco normativo y legal que garantice que los
impactos negativos sean menores con respecto a los positivos y, de ma-
nera especial, que la percepción pública sea la adecuada, en relación a
los riesgos y ventajas que conlleva su utilización.
Es evidente que el panorama mostrado a continuación es sólo una pe-
queña parte de lo que puede encontrarse en la literatura científica y tec-
nológica. El propósito fundamental es generar el interés de la comunidad
científica de nuestro país para emprender acciones y comprender cómo
los productos de la nanotecnología nos afectarán.
INTRODUCCIÓN
La nanotecnología se ha incorporado de manera definitiva a la vida
cotidiana a través de bienes y servicios, y al quehacer científico y tec-
nológico por medio de la generación de nuevas disciplinas como la
nanotoxicología y la nanomedicina, dedicadas a estudiar el impacto

Orrantia, Piñón, Concha, Sánchez, Montes, Arzate, Rodríguez, Duarte, Luna
86
de los nanomateriales en la salud humana y en el medio ambiente.
Debemos encontrar un balance para lograr el mayor número de be-
neficios sociales con el mínimo de riesgos ambientales o de salud,
tomando en cuenta las propuestas que nos permitan llegar a este
equilibrio, incluyendo innovación en técnicas toxicológicas, modela-
ción de análisis de riesgo, así como las herramientas que porporciona
el análisis de decisión multicriterio, entre otras (Linkov y cols., 2008).
La nanotecnología tiene múltiples aplicaciones a nivel comercial:
cosméticos, pantallas, pinturas, recubrimientos, catalizadores, lubri-
cantes, tratamiento de aguas, impresiones, textiles, artículos deporti-
vos, medicina y salud, empaques para alimentos, electrónica, celdas
de combustible, baterías, aditivos, manufactura de papel, armas y ex-
plosivos (PEN, 2005).
Un estudio reciente (Research & Markets, 2010) muestra que los
nanopolvos de óxidos metálicos típicamente contienen alúmina, tita-
nia, óxido de fierro, óxido de zinc, cerio, y se aplican en compósitos,
los cuales se utilizan de forma amplia en la industria automotriz, cui-
dado personal y equipos electrónicos —como parte de catalizadores,
recubrimientos, pinturas y pantallas solares—. De manera específica,
las nanopartículas de fierro ostentan un potencial sorprendente en el
tratamiento de cáncer e imágenes de resonancia magnética, puesto
que óxidos de tierras raras están empezando a utilizarse para la re-
moción de fosfato en pacientes con hipofosfatemia. También es posi-
ble usar los óxidos metálicos en telecomunicación de alta velocidad
por computadora, incluyendo sensores optoelectrónicos y remedia-
ción ambiental.
Dentro de los nanomateriales con mayor número de aplicaciones
destacan los nanotubos de carbono en sus diferentes versiones y apli-
caciones, mismas que incluyen compósitos metálicos y cerámicos,
aplicaciones en polímeros y membranas, microscopía electrónica,
diagnóstico médico, cosméticos, sensores químicos, microelectróni-
ca, celdas solares y de combustible (Köhler y cols., 2008); sin embargo,
la velocidad de sus aplicaciones presentes y futuras no va asociada
al estudio de los efectos en el medio ambiente, ésta es quizá una de
las prioridades, desde un orden ecotoxicológico, que debe ser incluida
dentro de un análisis de ciclo de vida.
El mercado de los nanopolvos de óxidos metálicos alcanzó, en

87
Impactos de la nanotecnología en el medIo ambIente y la salud humana
2009, 6,150 millones de euros y se estima que rebasará los 14,550
millones en 2017, gracias a su utilización en la electrónica, medicina,
cuidado personal y militar. La compañía Nanoposts.com (2010), en su
último reporte, estima que el mercado actual de nanotubos de carbo-
no es de 247 millones de euros y que las nuevas aplicaciones de nano-
tubos funcionalizados alcanzarán 2.7 billones en 2015. La demanda
obedecerá fundamentalmente a industrias como la militar, energé-
tica, aeroespacial y automotriz, así como almacenamiento de datos
y usos en electrónica. Cabe mencionarse como dato adicional que
compañías grandes y pequeñas están interesadas en estos produc-
tos y servicios, entre las cuales se encuentran Bayer MaterialScience,
BASF, Thomas Swan, Nanocomp, Nanocyl, Arkema, Mitsui, Toray, IBM,
Surrey Nanosystems, Nanotero, Natural Nano, Unidym and Eikos.
El acelerado crecimiento de la nanotecnología se relaciona de for-
ma directa con la habilidad para diseñar nuevos materiales a nivel de
nanoescala, su dispersión posterior. La disposición de estos nanomate-
riales, una vez concluido su ciclo de vida, demanda esfuerzo por parte
de los sistemas científicos y tecnológicos de cualquier país. El reto más
importante a que nos enfrentamos es la implementación y validación
de técnicas analíticas químicas, físicas, de biología molecular y médi-
cas para evaluar los riesgos asociados a su uso. (Ju-Nam y Lead, 2008).
Pese a que los nanomateriales tienen una larga tradición en sus
formas actuales, su manipulación y la cuantificación a nivel de na-
noescala es relativamente nueva. El entendimiento de sus impactos
en la salud y medio ambiente son temas que recién inician e involu-
cran una gran cantidad de disciplinas científicas y tecnológicas, requi-
riendo el saber de la ciencia ambiental, biología molecular, ingeniería
genética, química analítica, fisicoquímica, física, ciencia de materia-
les, toxicología, entre otras (Baalousha & Lead, 2009). La estructura,
forma, función y composición de los nanomateriales, los métodos de
producción, sus aplicaciones y comportamiento químico son cuestio-
nes indispensables para conocer y determinar sus niveles de toxici-
dad, incluido el tamaño, procesos redox y de absorción/adsorción, así
como cinéticas de difusión y disolución. obviamente, para evaluar el
impacto de los nanomateriales en el medio ambiente y la salud, todos
los entornos —terrestre, acuático, aire, etcétera— deben ser incluidos.

Orrantia, Piñón, Concha, Sánchez, Montes, Arzate, Rodríguez, Duarte, Luna
88
Dentro de las técnicas o procedimientos más importantes para
estudiar el comportamiento de las nanopartículas, y desde luego para
evaluarlas, se encuentra el Análisis de Ciclo de Vida, proceso que per-
mite entender las implicaciones positivas y negativas a través de toda
la cadena productiva (Lee y cols, 1995).
¿Qué conceptos debemos incluir en el ciclo de vida de los nanomate-
riales?
Translocación, comportamiento ambiental y toxicológico, monitoreo, efecto de la
exposición, incluyendo salud ocupacional, fabricación, intermediarios y destino
final, así como análisis de flujo (Som y cols., 2010).
La descarga de los nanomateriales en sistemas de drenaje o trata-
miento de aguas es una situación a considerar. Un estudio reciente
sobre nanotubos de carbono presenta evidencias de un incremento en
la producción de sustancias poliméricas extracelulares, generadas por
los microorganismos para protegerse de los nanotubos, lo cual tiene
como consecuencia una inhibición en la respiración de los microorga-
nismos, con la consiguiente carga metabólica (Luongo y Zhang, 2010).
BENEFICIOS POTENCIALES DE LA NANOTECNOLOGÍA
Medio ambiente
Los nanomateriales tienen potencial para mejorar el ambiente a
través de nuevas soluciones como la detección, remoción y preven-
ción de contaminantes, por medio del diseño de procesos indus-
triales más limpios y la creación de productos amigables con el
entorno ecológico. Las nanopartículas pueden utilizarse para con-
vertir contaminantes químicos en compuestos menos peligrosos,
gracias a su gran área superficial, alta reactividad e incremento en
su transportación; por ejemplo, nanopartículas de fierro elemental
se han usado para remediar agua contaminada con tricloroetileno
(Zang, 2003) y para la remoción de arsénico de agua subterránea
anóxica (Kanel y cols., 2005), asimismo, cerámica nanoporosa com-
binada con monocapas autoensambladas con grupos funcionales

89
Impactos de la nanotecnología en el medIo ambIente y la salud humana
se ha empleado para remover metales pesados de agua de desecho
(Mattigod y cols., 2006).
Algunos nanocompósitos de sílica y titania se han utilizado tam-
bién para la remoción de vapor de mercurio elemental, como una
alternativa al método convencional de inyección en carbón activado
(Pitoniak y cols., 2005) y la sílica nanoestructurada ha resultado efi-
caz para capturar cadmio de un ambiente contaminado con gases
de combustión (Lee y cols. 2005). Nanosensores base óxido de zinc y
oxido de estaño pueden utilizarse como detectores de contaminantes
químicos y biológicos en el ambiente (Vaseashta & Dimova-Malinovs-
ka, 2005). Uno de los ejemplos más dramáticos de esto es la destruc-
ción de compuestos aromáticos en agua, utilizando una combinación
de nanoclusters de oxido de zinc semiconductor, acoplados con luz
UV (Kamat y cols., 2002).
La nanotecnología es capaz de ayudar a reducir la demanda de
energía, mediante el uso más eficiente y efectivo de los materiales,
mismos que pueden ser más ligeros, con geometrías que muestren
mejor control de temperatura, con transmisión eléctrica incremen-
tada y menor disipación, un ejemplo de ello es que nanopartículas
de óxido de cerio se han utilizado para disminuir la emisión de diesel
(Jung y cols., 2005). Quantum dots y nanopartículas de semiconduc-
tores pueden hacer más eficientes las celdas solares (Nozik, 2002), su
uso en pinturas ofrece la posibilidad de recubrimientos más delga-
dos para aviones y vehículos terrestres, con el consiguiente ahorro
de energía debido a la disminución en peso, aunado al reducción de
emisiones de Co2.
Salud humana
Dentro de los usos de los nanomateriales, la incorporación de nano-
partículas de plata (figura 1) en cosméticos se contempla como un
efecto promisorio, gracias a sus efectos antibacteriales y fúngicos
(Kokura, S. y cols, 2010).

Orrantia, Piñón, Concha, Sánchez, Montes, Arzate, Rodríguez, Duarte, Luna
90
Figura 1. Nanopartículas de plata elemental preparadas mediante técnicas químicas,
utilizando precursores inorgánicos.
Nanopartículas de óxido de fierro superparamagnéticas han sido
propuestas como pruebas de diagnóstico para evaluar toxicidad en
pulmones, usando como técnica imagenología óptica (Cho y cols.,
2009). Shlyakhtenko y sus colaboradores (2007) plantearon un mé-
todo, empleando AFM, para la recuperación y selección de anticuer-
pos específicos, dada su relevancia como nanosensores para terapia
y diagnóstico.
En un trabajo reciente, los nanotubos de carbono (figura 2) pro-
meten ser vehículos para llevar y depostiar drogas en células cancerí-
genas, debido a la interacción de los mismos con células endoteliales
(Albini y cols., 2010) y a su capacidad de atravesar membranas bioló-
gicas, dado su carácter hidrofóbico y lipofílico.

91
Impactos de la nanotecnología en el medIo ambIente y la salud humana
Figura 2. Bosque de nanotubos de carbono.
Es posible percibir algunas de las ventajas de los distintos nanoma-
teriales en diversas actividades, en las cuales estos funcionan como
acarreadores de medicamentos, biomarcadores, sensores magnéticos
de DNA, detectores de tumores y nódulos, sensores o como agentes
de contraste en medicina; también se encuentran en la termotera-
pia, imagenología, deposición de medicamentos y genes, y actividad
antimicrobiana. Con seguridad más cualidades están en proceso de
incorporarse o de ser descubiertas (Sekhon y Kamboj, 2010).
Los nanotubos han resultado implicados también en el trata-
miento de enfermedades como la de Alzheimer —de tanto interés en
el campo de la medicina—, en el cual el hallazgo más importante,
desde un punto de vista clínico, fue que bajo las condiciones estu-

Orrantia, Piñón, Concha, Sánchez, Montes, Arzate, Rodríguez, Duarte, Luna
92
diadas, los nanotubos, funcionalizados con acetilcolina, colapsan el
potencial de membrana mitocondrial, interfiriendo con la producción
de ATP (yang y cols., 2010).
La inserción de nanopartículas como acarreadores de medica-
mentos a órganos como el cerebro, hígado, corazón, riñón, bazo y pul-
mones es quizá uno de los aspectos más prometedores de la nanotec-
nología como una aplicación médica (Semete y cols., 2010), algunos
estudios con nanopartículas de PLGA han demostrando que las célu-
las mantienen su viabilidad. Del mismo modo, es interesante que las
nanopartículas de oro, consideradas básicamente como un detector
de cáncer (figura 3), en algunas líneas celulares cancerígenas pulmo-
nares actúan como un agente tóxico (Patra y cols., 2007).
Figura 3. Nanopartículas de oro elemental, obtenidas a través de sales, mediante procesos de
precipitación.

93
Impactos de la nanotecnología en el medIo ambIente y la salud humana
La nanotecnología tiene el potencial suficiente para mejorar nues-
tras vidas, específicamente las de aquellas personas que se hallan en
condiciones médicas complicadas o con lesiones severas. La siguiente
es una lista que contempla algunas de sus aplicaciones actuales y
futuras (Rocco, 2003):
• Desarollo de nuevas vacunas (Cui & Mumper, 2003).
• Reparación y sustitución de órganos y nervios enfermos o da-
ñados (yang y cols., 2004).
• Diagnóstico temprano, tratamiento y prevencion de cáncer, así
como de otras enfermedades (Cuenca y cols., 2006).
• Nuevas formulaciones y rutas para suministrar fármacos en
órganos como el cerebro (yih & Al-Fandi, 2006).
• Equipos artificiales a nivel nanoescala pueden ser introducidos
dentro de las células para diagnosticar y eventualmente llevar
componentes activos (Freitas, 1998).
• La movilización del cuerpo por sí mismo puede crear habilida-
des para regenerar células dañadas y motivar el crecimiento di
novo de neuronas (yang, et al., 2004).
• Combinando nano con biotecnología se puede alcanzar la ca-
pacidad de reparar o reemplazar componentes celulares de-
fectuosos como receptores de membrana (Rocco & Brainbrid-
ge, 2003).
• El establecimiento de enlaces directos entre el tejido neuronal
y las máquinas posibilitaría que éstas fueran extensiones del
cuerpo (Rocco & Brainbridge, 2003).
• El monitoreo y/o tratamiento continuo de la salud por medio
de nanoaparatos (Rocco & Brainbridge, 2003).
EFECTOS ADVERSOS POTENCIALES DE LA NANOTECNOLOGÍA
La nanotecnología puede utilizarse lo mismo para propósitos benéfi-
cos que para dañinos, entre estos últimos se encuentra la fabricación
de armas nucleares (Glenn, 2006). Independientemente de su uso, el
rápido crecimiento de la industria nanotecnológica traerá como con-

Orrantia, Piñón, Concha, Sánchez, Montes, Arzate, Rodríguez, Duarte, Luna
94
secuencia una mayor concentración de nanomateriales en el ambien-
te, con la consiguiente exposición para el hombre y los sistemas o
nichos ecológicos. Por desgracia existen pocos estudios sobre el efecto
de los materiales con nivel de nanoescala en el entorno ecológico y
la salud, debido sobre todo a nuestra incapacidad para cuantificarlos.
La brecha entre conocimento y toxicidad de los nanomateriales aún
es grande, dado que nuestras investigaciones sobre sus implicaciones
en la salud y en el medio ambiente recién inician.
En una muy reciente revisión sobre los posibles riesgos asociados
a los nanomateriales, Savolainen y sus colaboradores (2010) exponen
los tópicos que consideran principales para ser estudiados: medición
y standards para aerosoles, exposición incluyendo datos y modelos,
datos biomédicos y estrategias de evaluación, traslocación en el cuer-
po humano, considerando los datos asociados a los riesgos probables
de los químicos empleados en la fabricación de nanomateriales.
Medio ambiente
Potencialmente los nanomateriales tendrían impacto sobre el medio
ambiente en cuatro posibles vías:
I) Efecto directo sobre microorganismos, organismos inverte-
brados, peces y otros.
II) Interacción con los contaminantes que cambiarían la biodis-
ponibilidad de compuestos tóxicos y nutrientes.
III) Cambios en compuestos inorgánicos (Baalousha & Lead, 2009).
IV) Conversión de compuestos peligrosos con rutas establecidas
para su control y disposición en refractarios.
El estudio del impacto ambiental y salud involucra, por supuesto,
áreas tan diversas como la ecotoxicología, medicina ocupacional,
química, física, biología molecular, etc. En Europa ya existen esfuer-
zos tendientes a la regulación del uso de los nanomateriales, cuatro
áreas parecen esenciales: disposición segura, control y prevención de
la polución; registro, evaluación y autorización; así como directrices
para el manejo de residuos (Franco y cols., 2007).

95
Impactos de la nanotecnología en el medIo ambIente y la salud humana
Toxicidad de los nanomateriales
Debido al potencial efecto adverso de los nanomateriales y a su dis-
tribución inevitable, dada su incorporación a una gran diversidad de
procesos industriales, existe desde ahora una demanda para crear
los centros o institutos que los evalúen, no con el afán de limitar su
uso, sino para que sean utilizados de forma segura (Bystrzejewska-
Piotrowska y cols., 2009), bajo disposiciones legales y normas apro-
piadas.
En una editorial de 2010 de Toxicology, con datos obtenidos en
el foro denominado “Potential hazard of nanoparticles: From proper-
ties to biological and environmental effects”, organizado por EURo-
ToX’2008, se menciona la importancia de estudiar tanto las propie-
dades de las nanopartículas, como sus efectos en el medio ambiente
y los biológicos, haciendo énfasis especial en el conocimiento de sus
efectos durante su ciclo de vida completo (Kahru y Savolainen, 2010).
Para citar un ejemplo, cabe mencionarse que en un estudio reciente
con ratones se aportan pruebas sobre el efecto de las nanomateria-
les, in vivo e in vitro, en el cual se muestran efectos adversos en la
espermatogénesis, movilidad de los espermatozoides y cambios en la
expresión genética (Ema y cols., 2010).
Nanopartículas metálicas y de óxidos
En uno de los primeros trabajos sobre el efecto tóxico de nanoma-
teriales, en los cuales se tomó como antecedente la toxicidad de la
sílica para los pulmones, se utilizaron nanopartículas de sílica (15 y
46 nm) para evaluar su incidencia sobre células de cáncer pulmonar
y se encontró citotoxicidad sobre las mismas, correlacionada con un
incremento en el stress oxidativo generado por los dos tamaños de
nanopartículas (Lin y cols., 2006).
Martínez-Méndez y su colaboradores (2006) encontraron que las
nanopartículas de óxidos de titanio, vanadio y niobio soportados so-
bre sílica ejercían un efecto catalítico sobre una serie de compuestos
orgánicos, lo cual demuestra el resultado positivo del uso de estos
materiales para la descomposición de compuestos orgánicos con di-
ferentes grados de toxicidad. En relación al tratamiento de distintos

Orrantia, Piñón, Concha, Sánchez, Montes, Arzate, Rodríguez, Duarte, Luna
96
tipos de cáncer —melanoma B16F10, carcinoma de pulmón de Lewis,
cáncer de próstata y fibroblatos 3T3— la utilización de nanopartícu-
las de dióxido de titanio fotocatalizado ha comprobado ser un agente
efectivo; sin embargo, la viabilidad celular depende de las dosis del
compuesto, su área superficial y, más importante aún, los grupos po-
lares superficiales y la dosis de luz UV, componentes fundamentales
por su carácter mutagénico (Thevenot y cols., 2008).
Desde hace muchos años se conoce el efecto inhibitorio de la
plata sobre microorganismos patógenos, estudios relativamen-
te recientes muestran el mismo efecto sobre bacterias autotróficas
nitrificantes (Choi y cols., 2008). En 2008, Ahamed y colaboradores
demostraron que nanopartículas de plata inducían daño en el DNA
de células de mamíferos, así como en proteínas de reparación como
Rad51 y muerte celular, al observar la expresion de annexinaV. Miao
y colaboradores (2009) señalaron que la oxidación de nanopartículas
de plata metálica al generar Ag+ ejerce un efecto tóxico sobre el alga
Thalassiosira weissflogii, la cual utiliza como mecanismo de desintoxi-
cación una sobreproducción de la síntesis de sustancias exopoliméri-
cas para quelar al catión.
Auffan y colaboradores (2009) han encontrado en una revisión
que las nanopartículas metálicas químicamente estables no tienen
toxicidad celular significativa, no así aquéllas que tienden a ser oxi-
dadas, reducidas o disueltas, las cuales pueden mostrar efectos cito-
tóxicos, incluyendo genotóxicos para diferentes organismos celulares.
Bregoli y sus colaboradores (2009) han demostrado el efecto tóxico de
nanopartículas de trióxido de antimonio sobre células humanas he-
matopoyéticas normales, no así en comparación con líneas celulares
inmortales de origen hematopoyético, lo que vuelve preocupante su
uso como modelo para pruebas toxicológicas de nanomateriales.
En un estudio reciente sobre neurotoxicidad en una línea celular
neuronal, Wang y colaboradores (2009) demostraron que las nano-
partículas de manganeso, plata y cobre inducen cambios en genes
específicos involucrados en mecanismos asociados a la neurodege-
neración. Estudios recientes revelan también que las nanopartículas
de plata inducen una sobreexpresión de superóxido dismutasa en cé-
lulas de hepatoma humano (Kim y cols., 2009), lo que parece confir-

97
Impactos de la nanotecnología en el medIo ambIente y la salud humana
mar lo que otros autores han demostrado: un stress oxidativo celular
incrementado. Ahamed y colaboradores (2010) encontraron que las
nanopartícuals de plata generan stress oxidativo y apoptosis —com-
probado por otros autores— y además inducen la producción de la
proteína 70 «heat shock» en Drosophila melanogaster, incluyendo pro-
teínas como p53 y p38, involucradas en reparación de DNA y caspasas
3 y 9, que actúan como marcadores de apoptosis.
otro efecto de nanopartículas de óxido de aluminio con tamaños
de 30 y 40 nm fue evaluado en médula de rata, en la cual se observa-
ron aberraciones cromosomales y una acumulación inusual en dife-
rentes tejidos, orina y heces fecales (Balasubramanyam y cols., 2009).
Un incremento en la producción de mRNA-metalotioneína, aunado a
una desestiblización lisozomal, se apreció también en embriones de
ostión expuestos a nanopartículas de plata por Ringwood y colabora-
dores (2009).
Trabajos en otros sistemas biológicos como el gusano Eisenia fe-
tida, un comensal de distintos suelos, para los cuales se utilizaron
nanopartículas de óxido de titanio y óxido de zinc, arrojaron una in-
ducción en la producción de enzimas antioxidantes, combinada con
daño en el DNA (ensayo cometa), así como una disminución en la
actividad de la celulasa (Hu y cols., 2010). Algunos estudios revelan
también que ciertos tipos de óxidos despliegan una respuesta immu-
ne, especialmente inflamatoria, corroborada por un incremento en la
expresión de citocinas (Palomäki y cols., 2010).
Pan y sus colaboradores (2010) realizaron estudios, utilizando el
ensayo de Ames, para evaluar la mutagenicidad de nanopartículas de
óxidos metálicos; encontraron que en general ésta fue negativa para
óxidos de aluminio, cobalto, titanio y zinc para cepas de E. coli, no así
para el óxido cuproso, que mostró un efecto mutagénico para S. typhi-
murium y efecto negativo en E. coli para formar colonias.
Por su parte, Roh y colaboradores (2010) evaluaron el efecto eco-
toxicológico de los óxidos de cerio y titanio en Caenorhabditis elegans,
utilizando varios ensayos que incluyeron expresión genética, creci-
miento, fertilidad y sobrevivencia, y hallaron que las nanopartículas
de estos metales pueden causar ecotoxicidad en el modelo estudiado.
Wei y colaboradores (2010) han probado el impacto de nanopartículas

Orrantia, Piñón, Concha, Sánchez, Montes, Arzate, Rodríguez, Duarte, Luna
98
de silica en un ecosistema acuático, evaluado a través del alga verde
Scenedesmus obliqus, con datos que demuestran efectos diversos sobre
la producción de clorofila y los carotenoides, lo cual indica que puede
haber efectos adversos parciales en algunos sistemas, con implicacio-
nes eventuales sobre los ecosistemas involucrados.
En un trabajo comparativo sobre el efecto citotóxico y genotóxi-
co de nanopartículas de óxidos de titanio y aluminio, se demostró
el efecto de las mismas en células CHo-K1, donde el hallazgo más
importante fue la ausencia de la metafase (Di Virgilio y cols., 2010).
Cabe mencionarse que aún existe controversia al respecto, pues se
ha n encontrado en otros reportes resultados no concluyentes sobre
efectos tóxicos en líneas celulares eucarióticas similares. Conocido es
también el efecto citotóxico y genotóxico sobre diversos microorga-
nismos de la plata y el óxido de titanio, donde el área superficial juega
un papel muy importante (Martínez-Gutiérrez y cols., 2010).
Nanotubos de carbono (figura 4)
Desde 2006, Tian y sus colaboradores han realizado estudios tendien-
tes a evaluar los nanotubos de carbono bajo diferentes formas: multi-
pared, pared sencilla, activados, negros y como grafito, encontrando
que la toxicidad está relacionada de forma fuerte con el área super-
ficial, donde uno de los principales indicadores son la apoptosis y la
necrosis en fibroblastos humanos.
Witzmann y Monteiro-Riviere (2006) hallaron que nanotubos de
carbono multipared alteran la expresión de las proteínas en querati-
nocitos humanos, esencialmente las relacionadas con metabolismo,
señalamiento y las dedicadas al tráfico molecular. Del mismo modo,
se ha demostrado que los nanotubos de carbono inducen apoptosis
en linfocitos T (Bottini y cols., 2006).

99
Impactos de la nanotecnología en el medIo ambIente y la salud humana
Figura 4. Nanotubos, tamaños y geometrías.
Como lo mencionan algunos autores (yang y cols., 2008), la utiliza-
ción de nanotubos para depositar medicamentos para el tratamiento
de células cancerosas requiere especial atención. Un estudio llevado
a cabo con las técnicas RAMAN y TEM exhibe stress oxidativo cuando
nanotubos de carbono se acumulan en hígado, pulmón y bazo, debido
al incremento en los niveles de malondialdehído y disminución de los
de glutación.
Una comparación de la toxicidad entre nanotubos de carbono y
nanopartículas de óxido de aluminio y óxido de titanio demostró ma-
yores niveles de toxicidad y acumulación de los nanotubos, al mar-
gen de la capacidad de los tres nanomateriales para incorporarse con
facilidad al citoplasma celular (Simon-Deckers y cols., 2008). Algu-
nos estudios arrojan, aunque no de manera concluyente, un efecto
citotóxico de los nanotubos en células fagocíticas al reaccionar con
proteínas membranales, irrumpiendo su mecanismo de acción al ge-
nerarse un efecto lítico (Hirano y cols., 2008).
A despecho de su toxicidad, los nanotubos de carbono parecen
ser el vehículo de elección para transportar medicamentos a célu-
las enfermas, gracias a sus atributos, entre los que se incluyen su
estructura, inserción de grupos funcionales, topología superficial y
desarrollo de manufacturas para su fabricación, entre otras (Foldvari
y Bagonluri, 2008). Células epiteliales bronquiales humanas fueron
evaluadas en su respuesta a nanotubos de carbono y nanofibras de
carbono y se encontró daño en el DNA e inducción de la formación

Orrantia, Piñón, Concha, Sánchez, Montes, Arzate, Rodríguez, Duarte, Luna
100
de micronúcleos (Lindberg y cols., 2009). Efectos tóxicos asociados a
inflamación pulmonar relacionados con nanotubos de carbono mul-
tipared se han descubierto, la respuesta inflamatoria está vinculada
con el ensamblaje de la estructura de los nanotubos, más que con las
impurezas que contienen, i. e. cobalto (Ellinger-Ziegelbauer y Paulu-
hn, 2009). Líneas celulares de plantas como Arabidopsis han sido uti-
lizadas como modelo para probar la toxicidad de los nanomateriales,
en 2009 Lin y colaboradores encontraron que nanotubos de carbono
multipared ejercen un efecto aglomerativo sobre las células de esta
planta, mismo que se incrementa conforme aumenta el área superfi-
cial de los mismos.
En un estudio que intenta elucidar en parte la controversia so-
bre la toxicidad de los nanotubos de carbono purificados sobre líneas
celulares humanas, se halló que estos ejercen un efecto tóxico sobre
células de neuroblastoma, lo cual los vuelve un vehículo sumamente
interesante para depositar drogas anticancerígenas en una gran va-
riedad de tumores malignos (Vittorio y cols., 2009). En 2009 Murray y
sus colaboradores demostraron que las impurezas en la fabricación
de los nanotubos de carbono, donde el fierro es parte del catalizador,
desencadenan una respuesta inflamatoria y stress oxidativo debido a
los radicales libres, generando toxicidad en la piel. En 2010 Alazzam
y colaboradores han publicado los efectos de nanotubos de carbono
de pared sencilla en células epiteliales bronquiales humanas, estu-
diando su efecto sobre la desregulación de genes y encontraron que
muchos de ellos están asociados en la codificación de la transducción
y la transcripción, así como de la apoptosis.
Pese a que los nanotubos han emergido como una opción para el
tratamiento de cáncer, además de su uso en bioingeniería y terapia
génica, los datos contradictorios sobre sus efectos tóxicos no los ha-
cen todavía un material de plena confianza para tales aplicaciones
(Firme III y Bandaru, 2010). Como puede apreciarse, se ha generado
una gran controversia sobre la toxicidad de los nanomateriales, cau-
sada en realidad por la carencia actual de estándares y normas para
evaluarlos, por ello debería ser posible realizar esfuerzos en este sen-
tido, a fin de tener métodos bien establecidos que permitan llegar a
concensos científicos y técnicos.

101
Impactos de la nanotecnología en el medIo ambIente y la salud humana
Bibliografía
Ahamed, M., M. Karns, M. Goodson, J. Rowe, S. M. Hussain, J. J. Schlager & y. Hong
(2008), “DNA damage response to different surface chemistry of silver na-
noparticles in mammalian cells”, Toxicology and Applied Pharmacology, 233:
404-410.
Ahamed, M., R. Posgai, T. J. Gorey, M. Nielsen, S. M. Hussain & J. J. Rowe (2010), “Silver
nanoparticles induced heat shock protein 70, oxidative stress and apoptosis
in Drosophila melanogaster”, Toxicology and Applied Pharmacology, 242: 263-
269.
Alazzam, A., E. Mfoumou, I. Stiharu, A. Kassab, A. Darnel, A. yasmeen, N. Sivaku-
mar, R. Bhat & A-E. A. Moustafa (2010), “Identification of deregulated genes by
single-walled nanotubes in human normal bronchial epithelial cells”, Nano-
medicine: NBM, in press.
Albini, A., V. Mussi, A. Parodi, A. Ventura, E. Principi, S. Tegami, M. Rocchia, E. Fran-
cheschi, I. Sogno, R. Cammarota, G. Finzi, F. Sessa, D. Mc. Noonan & U. Valbusa
(2010), “Interactions of single-wall carbon nanotubes with endothelial cells”,
Nanomedicine: NBM, 6: 277-288.
Auffan, M., J. Rose, M. Wiesner & J-y. Bottero (2009), “Chemical stability of metallic
nanoparticles: A parameter controlling their potential cellular toxicity in vi-
tro”, Environmental Pollution, 157: 1127-1133.
Baalousha, M. & J. R. Lead (2009), Overview of nanoscience in the environment. In: Envi-
ronmental and Human Health Impacts of Nanotechnology, West Sussex. U. K., John
Wiley & Sons, pp. 1-29.
Balasubramanyam, A., N. Sailaja, M. Mahboob, M. F. Rahman, S. Misra, S. M. Hus-
sain & P. Grover (2009), “Evaluation of genotoxic effects of oral exposure to
aluminum oxide nanomaterials in rat bone marrow”, Mutation Research, 676:
41-47.
Bottini, M., S. Bruckner, K. Nika, N. Bottini, S. Belluci, A. Magrini, A. Bergamaschi
& T. Mustelin (2006), “Multi-walled carbon nanotubes induce T lymphocyte
apoptosis, Toxicology Letters, 160: 121-126.
Bregoli, L., F. Chiarini, A. Gambarelli, G. Sighinolfi, A. M. Gatti, P. Santi, A. M. Marte-
lli & L. Cocco (2009), “Toxicity of antimony trioxide nanoparticles on human
hematopoietic progenitor cells and comparison to cell lines”, Toxicology, 262:
121-129.
Bystrzejewska-Piotrowska, G., J. Golimowski & P. L. Urban (2009), “Nanoparticles:

Orrantia, Piñón, Concha, Sánchez, Montes, Arzate, Rodríguez, Duarte, Luna
102
Their potential toxicity, waste and environmental management”, Waste Ma-
nagement, 29: 2587-2595.
Cho, W-S., M. Cho, S. R. Kim, M. Choi, J. y. Lee, B. S. Han, S. N. Park, M. K. yu, S. Jon
& J. Jeong (2009), “Pulmonary toxicity and kinetic study of Cy5.5-conjugated
superparamagnetic iron oxide nanoparticles by optical imaging”, Toxicology
and Applied Pharmacology, 239: 106-115.
Choi, o., K. K. Deng, N-J.Kim, L. Ross Jr., R. y. Surampalli & Z. Hu (2008), “The inhibi-
tory effects of silver nnaoparticles, silver ions, and silver chloride colloids on
microbial growth”, Water Research, 42: 3066-3074.
Cuenca, A. G., H. Jinag, S. N. Hochwald et al. (2006), “Emerging implications of na-
notechnology on cancer diagnostics and therapeutics”, Cancer, 107: 459-466.
Cui, Z., & R. J. Mumper (2003), “Microparticles and nanoparticles as delivery sys-
tems for DNA vaccines”, Crit. Rev. Ther. Drug Carrier Syst., 20: 103-137.
Di Virigilio, A. L., M. Reigosa, P. M. Arnal, & M. Fernández Lorenzo de Mele (2010),
“Comparative study of the cytotoxic and genotoxic effects of titanium dioxi-
de and aluminium oxide nanoparticles in Chinese hamster ovary (CHo-K1)
cells”, Journal of Hazardous Materials, 177: 711-718.
Ellinger-Ziegelbauer, H. & J. Pauluhn (2009), “Pulmonary toxicity of multi-walled
carbon nanotubes (Baytubes®) relative to α-quartz following 6 h inhalation
exposure of rats and a 3 months post-exposure period”, Toxicology, 266: 16-29.
Ema, M., N. Kobayashi, M. Naya, S. Hanai & J. Nakanishi (2010) “Reproductive and
developmental toxicity studies of manufactured nanomaterials”, Reproducti-
ve Toxicology, accepted manuscript.
Firme III, C. P., & Bandaru P. R. (2010), Toxicity issues in the application of carbon
nanotubes to biological systems. Nanomedicine: NBM. 6:245-256.
Foldvari, M., & M. Bagonluri (2008), “Carbon nanotubes as functional excipients for
nanomedicines: II. Drug delivery and biocompatibility issues”, Nanomedicine:
NBM, 4: 183-200.
Franco, A., S. F.Hansen, S. I. olsen, & L. Butti (2007), “Limits and prospects of the
“incremental approach” and the European legislation on the management of
risks related to nanomaterials”, Regulatory Toxicology and Pharmacology, 48:
171-183.
Freitas, R. A. (1998), “Exploratory design in medical nanotechnology: a mechanical
artificial red cell”, Artif. Cells Blood Substit. Immobil. Biotechnol., 26: 411:430.
Glenn, J. C. (2006), “Nanotechnology: Future military environmental health consi-
derations”, Technol. Forecast. Soc. Change., 73: 128-137.
Hirano, S., S. Kanno & A. Furuyama (2008), “Multi-walled carbon nanotubes injure

103
Impactos de la nanotecnología en el medIo ambIente y la salud humana
the plasma membrane of macrophages”, Toxicology and Applied Pharmaco-
logy, 232: 244-251.
Hu, C. W., M. Li, y. B. Cui, D. S. Li, J. Chen & L. y. yang (2010), “Toxicological effects of
Tio2 y Zno nanoparticles in soil on earthworm Eisenia fetida”, Soil Biology &
Biochemistry, 42: 586-591.
Ju-Nam, y., & J. R. Lead (2008), “Manufactured nanoparticles: An overview of their
chemistry, interactions and potential environmental implications”, Science of
the Total Environment, 400: 396-414.
Jung, H., D. B. Kittelson & M. R. Zachariah (2005), “The influence of a cerium additi-
ve on ultrafine diesel particle emissions and kinetics of oxidation”, Combus-
tion and Flame, 142: 276-288.
Kamat, P. V., R. Huehn & R. Nicolaescu (2002), “A ‘sense and shoot’ approach for
photocatalytic degradation of organic contaminants in water”, J. Physical
Chemistry B, 106: 788-794.
Kanel, S. R., B. Manning, L. Charlet & H. Choi (2005), “Removal of arsenic (III) from
groundwater by nanoscale zero-valent iron”, Environ. Sci. Tech., 39: 1291-1298.
Kahru, A., & K. Savolainen (2010), “Potential hazard of nanoparticles: From proper-
ties to biological and environmental effects”, Toxicology, 269: 89-91.
Kim, S., J. E. Choi, J. Choi, K-H. Chung, K. Park, J. yi & D-y Ryu (2009), “oxidative
stress-dependent toxicity of silver nanoparticles in human hepatoma cells”,
Toxicology in Vitro, 23: 1076-1084.
Köhler, A. R., C. Som, A. Helland & F. Gottschalk (2008), “Studying the potential re-
lease of carbon nanotubes throughout the application life cycle”, Journal of
Cleaner Production, 16: 927-937.
Kokura, S., o. Handa, T. Takagi, T. Ishikawa, y. Naito & T. yoshikawa (2010), “Silver
nanoparticles as a safe preservative for use in cosmetics”, Nanomedicine:
NBM, in press.
Lankoff, A., A. Banasik, A. Duma, E. ochniak, H. Lisowska, T. Kuszewski, S. Gózdz &
A. Wojcik (2006), “A comet assay study reveals that aluminium induces DNA
damage and inhibits the repair of radiation-induced lessions in human peri-
pheral blood lymphocytes”, Toxicology Letters, 161: 27-36.
Lee, J.J., P. o’Callaghan & D. Allen (1995), “Critical review of life cycle analysis and
assessment techniques and their application to commercial activities”, Re-
sources, Conservation and Recycling, 13: 37-56.
Lee, M.H., K. Cho, P. Shah & P. Biswas (2005), “Nanostructured sorbents for captu-
re of cadmium species in combustion environments”, Environ. Sci. Tech., 39:
8481-8489.

Orrantia, Piñón, Concha, Sánchez, Montes, Arzate, Rodríguez, Duarte, Luna
104
Lin, W., y-w. Huang, X-D Zhou & y. Ma (2006), “In vitro toxicity of silica nanoparti-
cles in human lung cancer cells”, Toxicology and Applied Pharmacology, 217:
252-259.
Lin., Ch., B. Fugetsu, y. Su & F. Watari (2009), “Studies on toxicity of multi-walled
carbon nanotubes on Arabidopsis T87 suspension cells”, Journal of Hazardous
Materials, 170: 578-583.
Lindberg, H. K., G. C.-M. Falck, S. Suhonen, M. Vippola, E. Vanhala, J. Catalán, K.
Savolainen & H. Norppa (2009), “Genotoxicity of nanomaterials: DNA damage
and micronuclei induced by carbon nanotubes and graphite nanofibers in
human bronchial epithelial cells in vitro”, Toxicology Letters, 186: 166-173.
Linkov, I., F. K. Satterstrom & L. M. Corey (2008), “Nanotoxicology and nanomedici-
ne: making hard decisions”, 4: 161-171.
Luongo, L. A. & X. Zhang (2010), “Toxicity of carbon nanotubes to the activated
sludges process”, Journal of Hazardous Materials, 178: 356-362.
Martínez-Gutiérrez, F., P. L. olive, A. Banuelos, E. orrantia, N. Nino, E. Morales
Sánchez, F. Ruiz, H. Bach & y. Av-Gay (2010) “Synthesis, characterization, and
evaluation of antimicrobial and cytotoxic effect of silver and titanium nano-
particles”, Nanomedicine: NBM, in press.
Martínez-Méndez, S., y. Henríquez, o. Domínguez, L. D’ornelas & H. Krentzien
(2006), “Catalytic properties of silica supported titanium, vanadium and nio-
bium oxides nanoparticles towards the oxidation of saturated and unsatura-
ted hydrocarbons”, Journal of Molecular Catalysis A: Chemical, 252: 226-234.
Mattigod, S. V., G. E. Fryxell, R. Skaggs & K. E. Parker (2006), “Functionalized nanopo-
rous ceramic sorbents for removal of mercury and other contaminants. Te-
chnical Proceedings of the 2006 NSTI Nanotechnology Conference and Trade
Show”, Nano Science and Technology Institute, 1: 355-357.
Miao, A-J., K. A. Schwehr, Ch. Xu, S-J. Zhang, Z. Luo, A. Quigg & P. H. Santschi (2009),
“The algal toxicity of silver engineered nanoparticles and detoxification by
exopolimeric substances”, Environmental Pollution, 157: 3034-3041.
Murray, A. R., E. Kisin, S. S. Leonard, S. H. young, C. Kommineni, V. E. Kagan, V. Cas-
tranova & A. A. Shvedova (2009), “oxidative stress and inflammatory response
in dermal toxicity of single-walled carbon nanotubes”, Toxicology, 257: 161-
171.
Nanoposts.com (2010), “The Global Market for Nanotubes to 2015: A Realistic As-
sessment – 2nd Edition”.
Nozik, A. J. (2002), “Quantum dot solar cells. Phys E: Low-dimensio”, Sys. Nanos-
truct., 14: 115-120.

105
Impactos de la nanotecnología en el medIo ambIente y la salud humana
Nyland, J. F., J. J. K. Bai, H. E. Katz & E. K. Silbergeld (2009), “In vitro interactions be-
tween splenocytes and dansylamide dye-embedded nanoparticles detected
by flow cytometry”, Nanomedicine: NBM, 5: 298-304.
Palomäki, J., P. Karisola, L. Pylkkänen, K. Savolainen & H. Alenius (2010), “Enginne-
red nanomaterials cause cytotoxicity and activation on mouse antigen pre-
senting cells”, Toxicology, 267: 125-131.
Pan, X., J. E. Redding, P. A. Wiley, L. Wen, J. S. McConnell & B. Zhsng (2010), “Mutage-
nicity evaluation of metal oxide nanoparticles by the bacterial reverse muta-
tion assay”, Chemosphere, 79: 113-116.
Patra, H. K., S. Banerjee, U. Chaudhuri, P. Lahiri & A. Kr. Dasgupta (2007), “Cell selec-
tive response to gold nanoparticles”, Nanomedicine: NBM, 3: 111-119.
PEN (2005) “The project on emerging nanotechnologies”, www.nanotechproject.org
Pitoniak, E., C. y. Wu, D. W. Mazyck et al. (2005), “Adsorption enhancement mecha-
nism of silica-titania nanocomposites for elemental mercury vapor removal”,
Environ. Sci. Tech., 39: 1269-1274.
Research and Markets (2010), The World Market for Metal Oxide Nanopowders, U. K.,
Future Market, Inc.
Rocco, M. C. (2003), “Nanotechnology: convergence with modern biology and medi-
cine”, Curr. opin. Biotechnol., 14: 337-346.
Rocco, M. C. & W. S. Brainbridge (2003), Converging technologies for improving human
performance nanotechnology, biotechnology, information technology and cognitive
sciences, New york, Kluwer Academic Publishers.
Roh., Ji-yeon, y-K. Park, K. Park & J. Choi (2010), “Ecotoxicological investigation
of Ceo2 and Tio2 nanoparticles on the soil nematode Caenorhabditis elegans
using gene expression, growth, fertility, and survival as endpoints”, Environ-
mental Toxicology and Pharmacology, 29: 167-172.
Ringwood, A. H., M. McCarthy, T. C. Bates & D. L. Carroll (2009), “The effects of silver
nanoparticles on oyster embryos”, Marine Environmental Research, in press.
Savolainen, K., H. Alenius, H. Norppa, L. Pylkkänen, T. Tuomi & G. Kasper (2010),
“Risk assessment of engineered nanomaterials and nanotechnologies. A re-
view”, Toxicology, 269: 92-104.
Sekhon, B. S. & S. R. Kamboj (2010), “Inorganic nanomedicine, Part 1 & 2”, Nanome-
dicine: NBM, in press.
Semete, B., L. Booysen, y. Lemmer, L. Kalombo, L. Katata, J. Verschoor & H. S. Swai
(2010), “In vivo evaluation of the biodistribution and safety of PLGA nanopar-
ticles as drug delivery systems”, Nanomedicine: NBM, in press.
Shlyakhtenko, L. S., B. yuan, S. Emadi, y. L. Lyubchenko & M. R. Sierks (2007), “Single-

Orrantia, Piñón, Concha, Sánchez, Montes, Arzate, Rodríguez, Duarte, Luna
106
molecule selection and recovery of structure-specific antibodies using atomic
force microscopy”, Nanomedicine: NBM, 3: 192-197.
Simon-Deckers, A., B. Gouget, M. Mayne-L’Hermite, N. Herlin-Boime, C. Reynaud
& M. Carrière (2008), “In vitro investigation of oxide nanoparticle and carbon
nanotube toxicity and intracellular accumulation in A459 human pneumo-
cytes”, Toxicology, 253: 137-146.
Som, C., M. Berges, Q. Chaudhry, M. Dusinska, T. F. Fernandes, S. I. olsen & B.
Nowack (2010), “The importance of life cycle concepts for the development of
safe nanoproducts”, Toxicology, 269: 160-169.
Thevenot, P., J. Cho, D. Wavhal, R. B. Timmons & L. Tang (2008), “Surface chemistry
influences cancer killing effect of Tio2 nanoparticles”, Nanomedicine: NBM,
4: 226-236.
Tian, F., D. Cui, H. Schwarz, G. G. Estrada & H. Kobayashi (2006), “Cytotoxicity of
single-wall carbon nanotubes on human fibroblasts”, Toxicology in Vitro, 20:
1202-1212.
Vaseashta, A. & D. Dimova-Malinovska (2005), “Nanostructured and nanoscale de-
vices, sensors and detectors”, Sci. Technol. Adv. Mat., 6: 312-318.
Vittorio, o., V. Raffa & A. Cuschieri (2009), “Influence of purity and surface oxida-
tion on cytotoxicity of multiwalled carbon nanotubes with neuroblastoma
cells”, Nanomedicine: NBM. 5: 424-431.
Wang, J., M. F. Rahman, H. M. Duhart, G. D. Newport, T. A. Patterson, R. C. Murdock,
S. M. Hussain, J. J. Schlager & S. F. Ali (2009), “Expression changes of dopami-
nergic system-related genes in PC12 cells induced by manganese, silver, or
copper nanoparticles”, NeuroToxicology, 30: 926-933.
Wei, Ch., y. Zhang, J. Guo, B. Han, X. yang & J. yuan (2010), “Effects of silica nanopar-
ticles on growth and photosynthetic pigment contents of Scenedesmus obliqus”,
Journal of Environmental Sciences, 22: 155-160.
yang, F., R. Murugan, S. Ramakrishna et al. (2004), “Fabrication of nano-structu-
red porous PLLA scaffold intended for nerve tissue engineering”, Biomat, 25:
1891-1900, yang y cols.
yang, S-T., X. Wang, G. Jia, T. Wang, H. Nie, C. Ge, H. Wang & y. Liu (2008), “Long-term
accumulation and low toxicity of single-walled carbon anotubes in intrave-
nously exposed mice”, Toxicology Letters, 181: 182-189.
yang, Z., y. Zhang, y. yang, L. Sun, D. Han, H. Li & Ch. Wang (2010), “Pharmacological
and toxicological target organelles and safe use of single-walled carbon na-
notubes as drug carriers in treating Alzheimer disease”, Nanomedicine: NBM.
6: 427-441.

107
Impactos de la nanotecnología en el medIo ambIente y la salud humana
yih, T. C., & M. Al-Fandi (2006), “Engineered nanoparticles as precise drug delivery
systems”, J. Cell Biochem., 97: 1184-1190.
Witzmann, F. A. & N. A. Monteiro-Riviere (2006), “Multi-walled carbon nanotube
exposure alters protein expression in human keratinocytes”, Nanomedicine:
NBM., 2: 158-168.
Zang, W. S. (2003), “Nanoscale iron particles for environmental remediation: an
overview”, J. Nanopart, Res. 5: 323-332.


Acerca de los autores
Alejandro Uribe Salas. Ing. Químico (1980) y M. en C. en Metalurgia y Ma-
teriales (1986) de la Universidad Michoacana de San Nicolás de Hidalgo.
Doctor en Ciencias (1991) del Departamento de Ingeniería Minera y Meta-
lúrgica de la Universidad McGill, Montreal, Canadá. Investigador CINVES-
TAV desde 1992. Sus áreas de interés se ubican dentro del procesamiento
de minerales, la extracción de metales mediante métodos hidrometalúr-
gicos y el tratamiento de efluentes acuosos. Ha dirigido y codirigido 10
doctores, 32 maestros en ciencias y 4 tesistas de licenciatura. Su produc-
ción escrita incluye tres capítulos de libro, alrededor de 65 artículos en
revistas indexadas, 120 artículos en memorias de congresos nacionales e
internacionales, 15 artículos en revistas nacionales y una patente inter-
nacional (EUA). Es miembro del Sistema Nacional de Investigadores (nivel
II) y ha recibido algunos reconocimientos nacionales e internacionales.
Ha desarrollado seis proyectos de investigación básica y seis proyectos de
desarrollo tecnológico con empresas del Grupo Peñoles.
Roberto Pérez Garibay. Realizó sus estudios de ingeniería química y
maestría en metalurgia en la Universidad Michoacana de San Nicolás de
Hidalgo. En 1996 terminó un doctorado en Ciencias en el Departamento
de Minas de la Universidad Laval, Québec, Canadá. Actualmente es in-
vestigador del Cinvestav-IPN (Unidad Saltillo) y sus áreas de interés se
centran en el procesamiento de minerales, la hidrometalurgia, la instru-
mentación y el control automático de procesos. Ha dirigido y codirigido
24 tesis de posgrado (tres de doctorado y 21 de maestría) y es coautor de
35 artículos publicados en revistas indexadas de prestigio internacional y
80 ponencias a través de las memorias de congresos nacionales e interna-
cionales. Es miembro del Sistema Nacional de Investigadores (nivel II) y
ha desarrollado varios proyectos de investigación básica con el CoNACyT
y de desarrollo tecnológico con empresas nacionales.
Sergio Gabriel Flores Gallardo. Ingeniero Químico (1997) y Doctor en
Polímeros (2002) del Centro de Investigación en Química Aplicada. A la

fecha, Investigador Titular B del Centro de Investigación en Materiales
Avanzados, S.C. en el área de polímeros. Sus líneas de Investigación se
orientan hacia el procesamiento de compuestos poliméricos, reología
de polímeros y desarrollo de sensores químicos. Tiene experiencia de 15
años en Investigación Básica y Aplicada en estudios de propiedades vis-
coelásticas de mezclas de polímeros con fibras naturales y/o reciclado de
plásticos, así como en el desarrollo de formulaciones plásticas empleadas
en procesos de transformación de plástico (moldeo por Inyección, com-
presión, extrusión y termoformado). Ha dirigido y codirigido 5 Doctores,
6 Maestros en Ciencia, 6 tesistas de licenciatura. Es autor de 20 artículos
científicos en revistas internacionales con arbitraje, 105 citas, 5 capítulos
de libro, 45 artículos en memorias de congresos, 14 Patentes registradas
en México (2 con título otorgado). Es miembro del Sistema Nacional de
Investigadores, Nivel I y ha recibido algunos reconocimientos nacionales.
Ha dirigido alrededor de 12 proyectos de investigación financiados por
instancias gubernamentales o por la iniciativa privada.
Clara Hilda Ríos Reyes. Profesor-Investigador Posdoctorante en la Uni-
versidad Autónoma del Estado de Hidalgo. Realizó estudios de Licenciatu-
ra en Química en la Universidad de Guadalajara y obtuvo grado de Maes-
tría y Doctorado en Ciencias e Ingeniería de Materiales en la Universidad
Autónoma Metropolitana-Azcapotzalco. Actualmente es miembro del
Sistema Nacional de Investigadores nivel 1. Sus líneas de investigación:
La síntesis de cúmulos nanométricos bimetálicos a base de Co y Fe para
su uso en el desarrollo de materiales con nuevas propiedades, la deter-
minación de sus propiedades por medio de técnicas químico-cuántico
computacionales, su modelación teórica mediante el desarrollo de mode-
los matemáticos de nucleación y crecimiento 3D, su caracterización por
diferentes técnicas de microscopía: SEM, AFM, MFM, entre otras; el estu-
dio del fenómeno upd de diversos metales sobre sustratos de diferente
naturaleza, entre otras.
Luis Humberto Mendoza Huizar. Profesor-Investigador titular C en la
Universidad Autónoma del Estado de Hidalgo. Realizó estudios de Licen-
ciatura en Ingeniería Química en la Universidad de Guanajuato y obtuvo
el grado de Doctor en Química por parte de la misma Universidad con la

distinción Summa Cum Laude. Actualmente es miembro del Sistema Na-
cional de Investigadores nivel 2 y cuenta con perfil PRoMEP. Sus líneas de
investigación: Los estudios teóricos químico cuánticos y experimentales
mediante técnicas electroquímicas de los fenómenos que se observan en
la interfase electrodo-solución; la electrosíntesis, crecimiento y carac-
terización de depósitos metálicos, a nivel fundamental, sobre diversos
sustratos; nanosíntesis de cúmulos y monocapas por técnicas electro-
químicas, así como la determinación de sus propiedades electrónicas y
estructurales mediante el empleo de la química-cuántica computacional
y las técnicas de microscopía AFM y STM; estudio de las propiedades mo-
leculares de cristales líquidos; y más recientemente la investigación de
mecanismos de degradación de herbicidas mediante el uso de la química
cuántica computacional.
Erasmo orrantia Borunda. obtuvo su grado de doctorado en Biotecno-
logía en la Facultad de Ciencias Biológicas de la Universidad Autónoma
de Nuevo León en 1997, donde recibió la Summa Cum Laude y el Premio a
la Mejor Tesis Doctoral en el área de Ciencias de la Tierra y Agropecua-
rias, en ese mismo año. Actualmente es director académico del Centro de
Investigación en Materiales Avanzados, también es investigador titular C
en dicha institución. Ha publicado más de 40 artículos en revistas inter-
nacionales, seis patentes, varios capítulos en libros, ha dirigido alrededor
de 15 proyectos de investigación financiados por instancias gubernamen-
tales o por la iniciativa privada. Ha dirigido alrededor de 28 tesis de docto-
rado y maestría. Sus temas de investigación incluyen la nanotoxicología
y la biohidrometalurgia.


Contenido
Héctor Hugo Lerma Triana, Alejandro
Uribe Salas, Roberto Pérez Garibay
Evaluación de surfactantes usados en la flotación de sulfuros
en términos del tamaño promedio de burbuja 9
Luz Cecilia Pérez Velásquez, Sergio Gabriel Flores Gallardo
Patricia de Lira Gómez, Tomás Lozano Ramírez
Estudio de nanocompuestos montmorillonita/PLA 29
Clara Hilda Ríos Reyes, Luis Humberto Mendoza Huizar,
Víctor Esteban Reyes Cruz, María Aurora Veloz Rodríguez
Estudio voltamperométrico y efecto del pH en los depósitos
de Fe sobre carbón vítreo 57
Nancy Ramos Lora, Luis Humberto Mendoza Huizar, Claudia
Hilda Ríos Reyes, Eduardo García Sánchez, Patricia de Lira Gómez
Estudio electrocinético del proceso
de electrodepositación de cobalto sobre carbón vítreo 71
Erasmo orrantia Borunda, Hilda Amelia Piñón Castillo,
Sandra Ixmucamé Concha Guerrero, Blanca Sánchez
Ramírez, Silvia Lorena Montes Fonseca, Carlos Arzate
Quintana, Vicente Rodríguez González, José Alberto
Duarte Möller y María Antonia Luna Velasco
Impactos de la nanotecnología en el medio ambiente
y la salud humana
85
Acerca de los autores 109

MINERALES, MATERIALES
y MEDIo AMBIENTE
de
Patricia de Lira Gómez
Uriel Ramírez-García Correa
Eduardo García Sánchez
(Coordinadores)
se terminó de imprimir en el mes de septiembre de 2014,
en los talleres gráficos de Signo Imagen.
Teléfono (449) 922 78 06.
Correo: [email protected]
1000 ejemplares