Extraccion Por Solventes .Ppthh
-
Upload
alejandro-salas-gonzales -
Category
Documents
-
view
147 -
download
9
Transcript of Extraccion Por Solventes .Ppthh
PLS MINERAL
E-1E-2
S-2 S-1LTK OC
PLS RIPIOS
REFINO
PILAS MINERAL PILAS RIPIOS
TK REC
ER
SXEW
LIXIVIACION MINERAL LIXIVIACION RIPIOS
AGLOMERADO MINERAL AGLOMERADO RIPIOS
MINERAL DESDE LONGACHO
MINA RIPIOS
CHANCADO
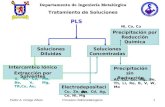
DIAGRAMA
INTRODUCCIÓN
• La extracción por solvente es un método de purificación de soluciones. Este método consiste en poner en contacto una solución rica de lixiviación con un reactivo orgánico el cual tiene la propiedad de extraer selectivamente los iones metálicos de interés. En una etapa posterior esta resina es descargada, es decir, esta resina devuelve los iones capturados y los entrega a una solución limpia.
• La extracción por solvente consiste al menos en dos etapas, la primera etapa, de carga, se conoce como extracción y la segunda etapa, de descarga, es llamada de reextracción o stripping.
OBJETIVOS DEL PROCESO DE EXTRACCIÓN POR SOLVENTES
• La separación y purificación de uno o más metales de interés de las soluciones que los contienen, las que suelen tener impurezas. La separación consiste en extraer el o los metales deseados desde soluciones o a la inversa, extraer las impurezas de la solución, dejando el o los metales deseados en ella.
• Concentración de los metales disueltos para disminuir los volúmenes a procesar y así reducir los costos del proceso siguiente (EW para el caso del cobre).Transferencia de los metales disueltos desde una solución acuosa compleja a otra solución acuosa diferente, que simplifique el proceso siguiente.
:
ETAPAS Y MECANISMOS
• La extracción por solventes consiste en un proceso de purificación y concentración de soluciones basada en la separación del elemento de interés - como el cobre - desde las soluciones de lixiviación. Para ello se utiliza un medio extractante líquido de alta selectividad al elemento a separar, pero inmiscible en dicha solución.
• En el proceso global de la extracción por solventes se distinguen tres momentos fundamentales, que consisten en:
ETAPAS Y MECANISMOS
• El líquido extractante se agrega a la solución primaria y se conecta con el ion metálico, que queda formando parte del extractante.
• Enseguida, este complejo extractante - ion metálico - es separado de la solución y llevado a una solución secundaria en el ion metálico.
• En esta solución secundaria se produce la re-extracción o descarga, es decir, el elemento de interés es nuevamente devuelto a una solución acuosa, pero exenta de impurezas, óptima para el proceso siguiente de electroobtención.
ETAPA DE EXTRACCIÓN O CARGA DEL REACTIVO
• La solución impura proveniente de la lixiviación en fase acuosa, rica en iones de cobre y con una acidez baja (pH entre 1,4 y 1,9), se introduce en mezcladores especiales donde se contacta con la fase orgánica de muy bajo contenido de cobre, llamado “orgánico descargado”.
• Como ambas fases son inmiscibles, para realizar la extracción y mezcla, es necesario aplicar una acción mecánica de elementos externos que proporcionan la energía necesaria para este propósito. Al mezclarse ambas fases ocurre una transferencia de la especie metálica disuelta en la fase acuosa, la que se desplaza químicamente con el reactivo extractante en la fase orgánica hasta alcanzar el respectivo equilibrio químico. Así, se genera una fase orgánica cargada con la especie metálica de interés y una solución acuosa descargada o refino.
ESQUEMA GENERAL PROCESO LIX-SX-EW
PLS
REFINO
Electrolito Rico
Electrolito Pobre
LIXIVIACION
ELECTROOBTECION
Ecuación de extracción
• Me2+ + 2RH ===== MeR2 + 2H+
R
HO
A
NOH
R=C9H19 ó C12H25
A=H, aldoxima C6H5, cetoxima
PROCEDIMIENTO BÁSICO• Los sistemas de extracción por solventes tienen tres componentes básicos, que
son un soluto a extraer, un solvente acuoso y un extractante orgánico. El proceso de extracción por solventes se basa en la reacción reversible de intercambio iónico que tiene lugar entre dos fases inmiscibles, la fase orgánica que corresponde al reactivo extractante disuelto en un diluyente orgánico, y la fase acuosa que corresponde a la solución. Se pone en contacto la solución de lixiviación o fase acuosa con el reactivo orgánico o fase orgánica, y se mezcla fuertemente por agitación.
• El reactivo orgánico contiene una molécula extractante, el que tiene una alta afinidad por el ion metálico que se quiere recuperar. Este ion de interés es transferido desde la fase acuosa o solución de lixiviación a la orgánica, a través de la interfase de los dos líquidos no inmiscibles. La mezcla resultante por la agitación se deja decantar para que se separe en dos capas o fases. La fase superior corresponde a la capa orgánica, que se mantiene allí debido a su menor peso específico. En esta fase orgánica, que se conoce como fase cargada o fase extracto, se encuentra retenido el ion metálico de interés formando un complejo orgánico-metálico.
• La capa acuosa inferior, denominada fase acuosa o de refino, es una solución estéril respecto de iones metálicos y tiene un peso específico mayor al de la fase orgánica.
T
R
E-2 S-2
S-1 L
EP
OC
ERREF
OCLOD
E-1
PLS
TK OC
DIAGRAMA DE FLUJOS PLANTA SX-EW
EXTRACCION REEXTRACCION ELECTROOBTENCION
• Al mezclarse las fases acuosa y orgánica, el equilibrio se irá dando paulatinamente, debido a que la transferencia de masa dentro de un reactor depende de los siguientes factores:
• Tiempo de residencia.• Área de interfases acuosa/orgánica.• Potencial químico en la interfase.• El equilibrio de la reacción es el factor más importante
en el proceso de intercambio y esto depende del tamaño de los equipos utilizados, la energía consumida en la agitación y otros factores que afecten en la totalidad de los costos del proceso.
• En 1963 se fabricó la primera resina capaz de extraer cobre comercialmente.
• En Chile la primera aplicación de esta tecnología se hizo en el año 1980, en la Sociedad Minera Pudahuel.
• CODELCO incorporó este proceso en el año 1985 en el mineral el Teniente.
REACTIVOS EXTRACTANTES USADOS COMERCIALMENTE
• En la siguiente tabla se presenta un listado en que se muestra el nombre y la respectiva descripción química de algunos reactivos extractantes, usados en diversas aplicaciones industriales para recuperación de metales por SX.
• Nombre comercial y descripción química de algunos extractantes de SX usados en la industria para recuperación de metales.
SOLUCIÓN ACUOSA
• La solución acuosa normalmente es rica en lixiviación y corresponde a la fase portadora del metal o de los metales que interesa procesar por extracción; se denomina PLS (pregnant liquor solution). Luego de ser procesada por extracción SX, cambia de denominación a solución pobre o refinado, RF de refinante y suele ser enviada de regreso a la lixiviación.
PROCESO DE RECUPERACION HIDROMETALURGICA
PLS MINERAL
E-1 E-2 S-2
S-1LTK
OC
PLS RIPIOS
REFINO
PILAS MINERALPILAS RIPIOS
TK REC
ER
EXTRACCION POR SOLVENTES (SX)
ELECTROOBTENCION (EW)
LIXIVIACION
(LIIX)
SOLUCIÓN ACUOSA
• Existen cuatro características o propiedades del PLS, las que pueden ser controladas o modificadas de manera de lograr una más eficiente separación o purificación del metal mediante SX:
• Acidez libre• Potencial de óxido-reducción expresado por el nivel de
Eh.Concentración de aniones que forman complejos como cloruro, sulfato y cianuro.
• Temperatura, la que influye directamente en el equilibrio de la extracción, las cinéticas de transferencia del metal, la solubilidad de las especies extraídas, la separación de fases y en las pérdidas por atropamiento y arrastre.
Esta recuperación la podemos hacer mediante diferentes operaciones como son:- Precipitación por reducción.- Precipitación por formación de compuestos insolubles en otra fase acuosa.- Re extracción del metal por paso a otra fase acuosa, de donde se puede recuperar.
Las dos primeras mencionadas no suelen utilizarse, realizándose generalmente la re extracción por la última de las operaciones mencionadas.
MECANISMOS DE REEXTRACCION
La extracción aprovecha en muchas veces para cambiar de medio acuoso hacia otro medio que resulta mas favorable como por ejemplo para un constituyente lixiviado en medio acido sulfúrico para el uranio resulta muy practica para su alta disponibilidad y bajos costos de acido sulfúrico en los tanques de minerales de baja ley. Posteriormente se le prefiere operar en medio de nitrato para que la operación de descarga se realice en este medio.
Reactivo Concentración (H2SO4)gpl
Extracción Stripping
Empleo
LIX 63 1 160 Extracción de Cu de soluciones amoniacales (Ni, Co).
LIX 64 3 160-200 Extracción de cobre de soluciones levemente ácidas
LIX 64 N 4 - 10 140-160 Ídem anterior; pero selectivo para Cu++ sobre ión férrico.
LIX 70 30-40 200-400 En soluciones altamente ácidas o con alta conc. de cobre y selectivo sobre Fe+3
LIX 71 (73) 10-15 220-230 Soluciones aciduladas de cobre y selectivo sobre Fe+3
SME-529 4-10 150-160 Similar LIX 64 N
ACORGA
P-5100
3-10 170-175 En soluciones diluidas y/o concentrasos en cobre y selectivo sobre Fe+3
KELEX 100 >13 160-225 Extracción de cobre de soluciones ácidas y selectivo sobre Fe+3
LIX 34 4-10 140-170 Para soluciones pobres en cobre, de alto hierro. Alta selectividad.
TABLA 3. CONDICIONES DE ACIDEZ EN EXTRACTANTES PARA COBRE Y EMPLEO GENERAL
PARA SOLUCIONES POBRES EN COBRE, DE ALTO HIERRO. ALTA SELECTIVIDAD. LAS PROPIEDADES QUE DEBE CUMPLIR UN EXTRACTANTE IDEAL, SON LAS SIGUIENTES
a)Extraer el máximo del elemento de interés y minimizar la cantidad de extractante a usar.
b)Elevada Capacidad de Saturación, la capacidad de saturación es la máxima concentración de especies valiosas que puede retener.
c)Propiedades físicas adecuadas para la transferencia de masa y separación de fases, tales como: densidad, viscosidad, etc.
d)Selectividad, esta es una importante características del extractante, debido a que una baja selectividad produce una menor purificación y además sitios activos del extractante estarán ocupados por otros elementos no deseados, luego la capacidad de carga disminuirá
e) Fácil re extracción, para que un extractante sea adecuado metalúrgicamente,
f) Seguridad (bajo punto de inflamación, baja toxicidad, etc.,)g) Disponibilidad y costo, además de medios baratos de regeneración.
El esquema general mostrado en figura 3.1 está constituido por 3 circuitos cerrados de soluciones:
1.- Lixiviación-Extracción
2.- Extracción-Stripping
3.- Stripping-Electroobtención.
1. El primer circuito corresponde a las soluciones provenientes de lixiviación que alimentan a las etapas de extracción, descargándose en cobre y constituyendo la solución refino, la cual retorna al proceso de lixiviación
2. El segundo circuito corresponde al circuito del orgánico, el cual se carga en cobre en las etapas de extracción al contactarse con las soluciones de lixiviación y se descarga en las etapas de stripping, al contactarse con el spent, retornando a las etapas de extracción.
3. El tercer circuito corresponde al circuito del electrolito, el cual se carga en cobre en las etapas del stripping, constituyendo el avance, se descarga en la etapa de electro obtención y retorna descargado (spent) a las etapas de stripping. De electro obtención se obtiene cátodos de buenas características físicas y químicas.
RECUPERACION DE COBRE POR SX EN MEDIO ACIDO
FASE ORGANICAEXTRACTANTES
En la reacciónEl subíndice “o” define a la fase orgánica y “A” a la fase acuosa. El reactivo orgánico, propiamente tal, se representa por HR y CuR2 el complejo formado producto del intercambio, en la fase orgánica. Extractante (también llamado reactivo), es un compuesto que contiene un grupo funcional que es capaz de reaccionar químicamente con una especie particular de la fase acuosa.
LOS PRIMEROS ESTUDIOS PARA LA EXTRACCIÓN DE COBRE EMPLEARON EXTRACTANTES ÁCIDO (O CATIÓNICOS) SIENDO SU PRINCIPAL INCONVENIENTE LA FALTA DE SELECTIVIDAD, YA QUE EXTRAEN SIMULTÁNEAMENTE EL COBRE Y OTROS ELEMENTOS, SIENDO ADEMÁS IMPOSIBLE APLICARLOS A LAS SOLUCIONES DE LIXIVIACIÓN DE MINERALES DE COBRE QUE TIENEN UN PH MÁS ÁCIDO QUE EL REQUERIDO PARA LA EXTRACCIÓN.
Para el tratamiento de las soluciones de lixiviación de minerales de cobre se emplean reactivos altamente selectivos para el Cu2+, como los reactivos de la conocida serie LIX (LIX 63; LIX 64; LIX-64-N, LIX 70, etc.), los productos ACORGA (P-5100; P-5300) y otros, cuyo poder de extracción para el Cu2+ relativo a otros iones es muy fuerte.
Reactivo Concentración (H2SO4)gpl
Extracción Stripping
Empleo
LIX 63 1 160 Extracción de Cu de soluciones amoniacales (Ni, Co).
LIX 64 3 160-200 Extracción de cobre de soluciones levemente ácidas
LIX 64 N 4 - 10 140-160 Idem anterior; pero selectivo para Cu++ sobre ión férrico.
LIX 70 30-40 200-400 En soluciones altamente ácidas o con alta conc. de cobre y selectivo sobre Fe+3
LIX 71 (73) 10-15 220-230 Soluciones aciduladas de cobre y selectivo sobre Fe+3
SME-529 4-10 150-160 Similar LIX 64 N
ACORGA
P-5100
3-10 170-175 En soluciones diluidas y/o concentrasos en cobre y selectivo sobre Fe+3
KELEX 100 >13 160-225 Extracción de cobre de soluciones ácidas y selectivo sobre Fe+3
LIX 34 4-10 140-170 Para soluciones pobres en cobre, de alto hierro. Alta selectividad.
TABLA 3. CONDICIONES DE ACIDEZ EN EXTRACTANTES PARA COBRE Y EMPLEO GENERAL
DILUYENTESEl diluyente suele ser un hidrocarburo u otra substancia inmiscible con el agua y sus propiedades son:
A.Ser capaz de disolver el extractante y de mantenerlo en solución.B.Tener baja viscosidad y densidad.C.Tener estabilidad química.D.Presentar baja solubilidad en la fase acuosa.E.Poseer un alto punto de inflamación, baja toxicidad y baja tasa de evaporación.
1. El diluyente y modificador al influir sobre estos fenómenos pueden condicionar los tiempos de retención para el proceso de extracción o stripping
1. Generalmente el kerosene ha sido el diluyente utilizado, pues se puede adquirir con facilidad y presenta en general buenas características
1. A veces el diluyente, por sí solo, no es suficiente para evitar ciertos problemas en la separación de fases, y entonces se añade un tercer componente para evitar la formación de una tercera fase el modificador.
1. Se suelen utilizar alcoholes de cadena larga, de 8 a 10 carbonatos, y también el fosfato de tributilo (TBP).
Tabla 4. Diluyentes comerciales empleados en la extracción de metales.
Contenido
en
aromáticos
Densidad a Punto de ebullición
Punto de inflamación
Composición
aproximada
Contenido alto
Solvesso 100
Solvesso 150
HAN
Chevron 3
Chevron 25
Chevron40L
Chevron 44L
Contenido medio
Escard 100
Napoleum 470
Contenido bajo
Isopar L
Isopar E
Isopar M
Norpar 12
Shell 140
Shell MSB 210
dx 3641
Escard 200
0.876
0.985
0.933
0.888
0.875
0.886
0.893
0.790
0.811
0.767
0.723
0.782
0.751
0.785
-0.783
0.793
0.796
157
188
180
182
158
182
186
191
210
189
116
207
196
185
-
183
195
44
66
40
63
46
60
68
76
79
62
7
78
69
60
74
57
67
Contenidos en aromáticos %
99
97
89
98
99
78
70
Contenido en aromático %
20
12
Contenido en alifáticos %
93
99,9
80
98
45º
-
45º
52º