Presentacion PH
-
Upload
kevinpaez7 -
Category
Education
-
view
21.432 -
download
0
Transcript of Presentacion PH

PHPresentado a:
Jhon Dairo ramos
Presentado por:Kevin López Páez
Duvan Zambrano Diaz
I.E.F.A2012

Contenido tematico Concepto PH Definición Resumen contexto PH Medida del PH Medida del ph Escala de PH de alimentos Indicador de PH PH de algunas sustancias POH Acidez Acido fuerte Acido débil Base

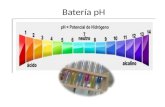
PH es una medida de la acidez o alcalinidad de una disolución. El pH
indica la concentración de iones hidronio [H3O+] presentes en determinadas sustancias. La sigla significa "potencial de hidrógeno. Este término fue acuñado por el químico danés Sørensen, quien lo definió como el logaritmo negativo en base 10 de la actividad de los iones hidrógeno. Esto es:
Desde entonces, el término "pH" se ha utilizado universalmente por lo práctico que resulta para evitar el manejo de cifras largas y complejas. En disoluciones diluidas, en lugar de utilizar la actividad del ion hidrógeno, se le puede aproximar empleando la concentración molar del ion hidrógeno.
Por ejemplo, una concentración de [H3O+] = 1 × 10–7 M (0,0000001) es simplemente un pH de 7 ya que: pH = –log[10–7] = 7
La escala de pH típicamente va de 0 a 14 en disolución acuosa, siendo ácidas las disoluciones con pH menores a 7 (el valor del exponente de la concentración es mayor, porque hay más iones en la disolución) , y alcalinas las que tienen pH mayores a 7. El pH = 7 indica la neutralidad de la disolución (cuando el disolvente es agua).

definición El pH se define como el logaritmo negativo de base 10 de la
actividad de los iones hidrógeno: Se considera que p es un operador logarítmico sobre la
concentración de una solución: p = –log[...] , también se define el pOH, que mide la concentración de iones OH−.
Puesto que el agua está disociada en una pequeña extensión en iones OH– y H3O+, tenemos que:
K(constante)w(water; agua) = [H3O+]·[OH–]=10–14 en donde [H3O+] es la concentración de iones hidronio, [OH−] la de iones hidroxilo, y Kw es una constante conocida como producto iónico del agua, que vale 10−14. Por lo tanto,
log Kw = log [H3O+] + log [OH–] –14 = log [H3O+] + log [OH–] 14 = –log [H3O+] – log [OH–] pH + pOH = 14 Por lo que se puede relacionar directamente el valor del pH con el del pOH.
En disoluciones no acuosas, o fuera de condiciones normales de presión y temperatura, un pH de 7 puede no ser el neutro. El pH al cual la disolución es neutra estará relacionado con la constante de disociación del disolvente en el que se trabaje.

Resumen El término de valor de pH procede del latín. Quiere decir pondus
hydrogenii peso de hidrógeno. Otra posible explicación del significado es potentia hydrogenii = efectividad del hidrógeno.
El valor de pH tiene un papel importante en la industria, la medicina, en el sector de la alimentación y en la agricultura. Se mide sobre todo en soluciones acuosas, extractos, pero también en productos con consistencia sólida (p.e. frutas) o también en el cuerpo humano (p.e. valor de pH de la piel). Tam- bién es importante que para hacer posible una medición correcta debe darse una humedad suficiente del objeto medido. El valor de pH se determina por medio de indicadores o con aparatos de medición digitales.Los indicadores son sustancias colorantes que cambian su color en un rango de pH determinado. El uso de tiras de prueba o de papeles indicadores han constituido las variantes de menor precisión al respecto. Con los aparatos de medición digitales se obtiene una determinación rápida y correcta.
Según la definición química, el valor de pH es el logaritmo negativo en décadas del valor numérico de la actividad molar de los iones de hidrógeno aH+. pH = - lgaH+
Las soluciones con un pH inferior a 7 reaccionan de manera ácida, con un valor de pH de 7 son neu- tras. En soluciones con un pH superior a 7 reaccionan de manera básica.

Medida del PH El valor del pH se puede medir de forma precisa
mediante un potenciómetro, también conocido como pH-metro, un instrumento que mide la diferencia de potencial entre dos electrodos: un electrodo de referencia (generalmente de plata/cloruro de plata) y un electrodo de vidrio que es sensible al ion de hidrógeno.
También se puede medir de forma aproximada el pH de una disolución empleando indicadores, ácidos o bases débiles que presentan diferente color según el pH. Generalmente se emplea papel indicador, que se trata de papel impregnado de una mezcla de indicadores cualitativos para la determinación del pH. El papel de litmus o papel tornasol es el indicador mejor conocido. Otros indicadores usuales son la fenolftaleína y el naranja de metilo.

Medida del PH A pesar de que muchos potenciómetros tienen escalas con valores
que van desde 1 hasta 14, los valores de pH también pueden ser aún menores que 1 o aún mayores que 14. Por ejemplo el ácido de batería de automóviles tiene valores cercanos de pH menores que uno, mientras que el hidróxido de sodio 1 M varía de 13,5 a 14.
Un pH igual a 7 es neutro, menor que 7 es ácido y mayor que 7 es básico a 25 °C. A distintas temperaturas, el valor de pH neutro puede variar debido a la constante de equilibrio del agua (Kw).
La determinación del pH es uno de los procedimientos analíticos más importantes y más usados en ciencias tales como química, bioquímica y la química de suelos. El pH determina muchas características notables de la estructura y actividad de las biomacromoléculas y, por tanto, del comportamiento de células y organismos.
En 1909, el químico danés Sorensen definió el potencial hidrógeno (pH) como el logaritmo negativo de la concentración molar (más exactamente de la actividad molar) de los iones hidrógeno.

Escala de PH

Indicador de PH es una sustancia que permite medir el pH de un medio. Habitualmente,
se utilizan como indicador de las sustancias químicas que cambian su color al cambiar el pH de la disolución. El cambio de color se debe a un cambio estructural inducido por la protonación o desprotonación de la especie. Los indicadores Ácido-base tienen un intervalo de viraje de unas dos unidades de pH, en la que cambian la disolución en la que se encuentran de un color a otro, o de una disolución incolora, a una coloreada.
Los más conocidos son el naranja de metilo, que vira en el intervalo de pH 3,1 - 4,4, de color rojo a naranja, y la fenolftaleína, que vira desde un pH 8 hasta un pH 10, transformando disoluciones incoloras en disoluciones con colores rosados / violetas. Además se pueden usar indicadores caseros como la disolución resultante de hervir con agua col lombarda (repollo colorado), pétalos de rosa roja, raíces de cúrcuma a partir de las cuales se obtiene curcumina, y otros(entre los cuales podemos destacar a la col morada y la piel de ciruela, que son usadas por algunas culturas indígenas).
Los indicadores de pH tienen una constante de protonación, , que informa sobre el desplazamiento de la reacción de protonación de la forma básica del indicador.
Se dice que el cambio de color de un indicador es apreciable cuando la concentración de la forma ácida o de la forma básica es superior o igual a 10 veces la concentración de la forma básica o la forma ácida respectivamente.

PH de algunas sustancias El pH de la leche es de 6,5 , el pH de la sangre es aproximadamente entre
7,35 y 7,45. El pH de detergentes es de 10,5. El pH del zumo de limón es de 2.
Para obtener un indicador orgánico se puede utilizar col morada siguiendo estos pasos:
Cortar la col en tiras. En un mortero colocar la col morada y molerla. Colocar alcohol en la disolución. Filtrar la sustancia con un filtro de papel. Colocar sustancias en varios recipientes como: bicarbonato de sodio, limón,
pomelo, vinagre, agua o limpiador de horno. Agregar en cada recipiente el indicador. Si los resultados son los siguientes se extrajo el indicador con éxito: Vinagre: color rosado (sustancia ácida) Bicarbonato de sodio: color verde (sustancia alcalina) Pomelo: color fucsia (sustancia ácida) Alcohol: color verde azulado (sustancia alcalina) Limpiador de horno: color amarillento (sustancia alcalina) Limón: color fucsia (sustancia ácida) . Agua: color violeta (sustancia neutra)

POH el logaritmo negativo en base 10 de la actividad de los aniones hidróxilo , o también
en términos de concentración de éstos, expresado como pOH = − log10.[OH − ]En soluciones acuosas, los iones OH- provienen de la disociación del agua:
H2O ↔ H+ + OH- o también, 2H2O ↔ H3O+ + OH-
Por ejemplo, si en una disolución se tiene una concentración [OH-] = 1×10-7 M (0,0000001 M), ésta tiene un pOH de 7 ya que : pOH = -log10[10-7] = 7
Dado que tiene la misma definición que pH, pero aplicado a la concentración de aniones hidroxilo, cumple las mismas propiedades que éste; típicamente tiene un valor entre 0 y 14 en disolución acuosa, pero en este caso son ácidas las disoluciones con pOH mayores a 7, y básicas las que tienen pOH menores a 7, puesto que en términos de concentración de reactivos, si el pH tiene un valor pequeño, significa que tiene una alta concentración de iones hidronio con respecto a la disolución neutra, y en esa misma proporción, pero al contrario, se produce por desequilibrio químico que tenga poca concentración de aniones hidroxilo, luego un pOH con un valor alto.
Así, considerando que el agua pura (disolución neutra) tiene un pH = pOH = 7 se cumple que:
pH + pOH = 14 ecuación que se mantiene constante ante las variaciones del pH (pOH).
DIFERENCIA ENTRE PH Y POH El pH mide las concentraciones de los iones hidronio, mientras que el pOH
mide las concentraciones de los aniones hidroxilo o iones hidróxido.

Acidez La acidez de una sustancia es el grado en el que es ácida. El
concepto complementario es la basicidad. La escala más común para cuantificar la acidez o la basicidad es el
pH, que sólo es aplicable para disolución acuosa. Sin embargo, fuera de disoluciones acuosas también es posible determinar y cuantificar la acidez de diferentes sustancias. Se puede comparar, por ejemplo, la acidez de los gases dióxido de carbono (CO2, ácido), trióxido de azufre (SO3, ácido más fuerte) y dinitrógeno (N2, neutro).
Asimismo, en amoníaco líquido el sodio metálico será más básico que el magnesio o el aluminio.
En alimentos el grado de acidez indica el contenido en ácidos libres. Se determina mediante una valoración (volumetría) con un reactivo básico. El resultado se expresa como el % del ácido predominante en el material. Ej: En aceites es el % en ácido oléico, en zumo de frutas es el % en ácido cítrico, en leche es el % en ácido láctico.

Acido fuerte Un ácido fuerte es un ácido que se disocia por completo en solución
acuosa para ganar electrones (donar protones), de acuerdo con la ecuación:
HA (aq) → H+ (aq) + A- (ac) Para el ácido sulfúrico, que es un ácido diprótico, la denominación de "ácido fuerte" se refiere sólo a la disociación del primer protón
H2SO4(aq) → H+(aq) + HSO4-(aq) Más precisamente, el ácido debe ser más
fuerte en solución acuosa que el ion hidronio, así ácidos fuertes son ácidos con una pKa < -1,74. Esto generalmente significa que en solución acuosa en condiciones normales de presión y temperatura, la concentración de iones hidronio es igual a la concentración de ácido fuerte introducido en la solución. Aunque por lo general se asume que los ácidos fuertes son los mas corrosivos, esto no es siempre cierto . El superácidocarborano H (CHB11Cl11), que es un millón de veces más fuerte que ácido sulfúrico es totalmente no corrosivo, mientras que el ácido débil ácido fluorhídrico (HF) es extremadamente corrosivo y puede disolver, entre otras cosas, el vidrio y todos los metales excepto el iridio.
En todas las otras reacciones ácido-agua, la disociación no es completa, por lo que estará representada como un equilibrio, no como una reacción completa

Acido debil es un ácido que no se disocia completamente.
La diferencia que separa las constantes de disociación ácida en los ácidos fuertes de la de todos los otros ácidos es tan pequeña que se trata de una demarcación razonable.
Debido a la disociación completa de los ácidos fuertes en solución acuosa, la concentración de iones de hidrógeno en el agua es igual a la re-duplicación de la del ácido introducido en la solución:
[HA] = [H+] = [A-]; pH = -log[H+].

Base es cualquier sustancia que en disolución acuosa aporta iones
OH− al medio. Un ejemplo claro es el hidróxido potásico, de fórmula KOH:
KOH → OH− + K+ (en disolución acuosa) Los conceptos de base y ácido son contrapuestos. Para medir la basicidad (o alcalinidad) de un medio acuoso se utiliza el concepto de pOH, que se complementa con el de pH, de forma tal que pH + pOH = pKw, (Kw en CNPT es igual a 10−14). Por este motivo, está generalizado el uso de pH tanto para ácidos como para bases. La teoría de Brønsted y Lowry de ácidos y bases, formulada en 1923, dice que una base es aquella sustancia capaz de aceptar un protón (H+). Esta definición engloba la anterior: en el ejemplo anterior, el KOH al disociarse en disolución da iones OH−, que son los que actúan como base al poder aceptar un protón. Esta teoría también se puede aplicar en disolventes no acuosos.