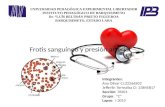
Frotis
-
Upload
fryda-naranjo-o -
Category
Documents
-
view
26 -
download
0
Transcript of Frotis

FrotisUn frotis de sangre es un mecanismo científico que consiste en el extendido de una gota de sangre en la
superficie de un portaobjetos o de un cubreobjetos, con el fin de analizarla posteriormente.
Es más adecuado emplear sangre que aún no ha estado en contacto con el anticoagulante, pues este
podría alterar los resultados (algunos anticoagulantes tienden a deformar las células de la sangre).
Su arquitectura de las células al formarse en la médula ósea.
1. Las alteraciones singulares en la forma de las células, que son una identificación especifica de
algunas enfermedades.
2. Algún indicador de los efectos nocivos de la quimioterapia y de la radioterapia.
3. La diferenciación y recuento de los elementos celulares de la sangre.
La fidelidad de la información obtenida de ellos, depende en gran parte de la calidad de las extensiones.
Estas no deben ser demasiado gruesas porque las células se amontonarían y no podrían ser
reconocidas, ni diferenciarse, ni demasiado delgadas porque las células se deformarían, distorsionarían
y destruirían. Por eso los frotis de sangre deben ser bien nivelados y para obtener buenos resultados es
necesario que:
1. Tanto portaobjetos como cubreobjetos deben estar bien limpios y desengrasados
(prefentemente nuevos).
2. La gota de sangre usada para la preparación de el frotis no debe ser muy grande ni pequeña,
de preferencia de el tamaño de la cabeza de un alfiler (entre 2 y 3 mm), obtenida por punción
capilar.
3. La sangre no haya estado en contacto con anticoagulante, pues podría deformarse la
morfología celular si pasase esto.
4. La lectura de las extensiones se hará en las zonas donde los eritrocitos "casi se tocan".
Extensión en el portaobjetos[editar]
Para llevar a cabo las extensiones en portaobjeto se coloca una gota de sangre de 3 a 4 mm de
diámetro, a unos 2 o 3 cm de uno de los extremos de el portaobjetos este se coloca en una superficie
plana y lisa. Con el borde de otro portaobjeto, con el que se toca la gota de sangre, la cual se desliza
por capilaridad a todo lo largo de el canto de dicho portaobjeto y con un movimiento rápido y uniforme,
en un angulo de 45 grados se desliza el portaobjetos dejando una capa de sangre en la superficie de el
otro. El espesor del extendido debe ser delgado.
Frotis

Un frotis de sangre es un mecanismo científico que consiste en el extendido de una gota de sangre en la
superficie de un portaobjetos o de un cubreobjetos, con el fin de analizarla posteriormente.
Es más adecuado emplear sangre que aún no ha estado en contacto con el anticoagulante, pues este
podría alterar los resultados (algunos anticoagulantes tienden a deformar las células de la sangre).
Su arquitectura de las células al formarse en la médula ósea.
1. Las alteraciones singulares en la forma de las células, que son una identificación especifica de
algunas enfermedades.
2. Algún indicador de los efectos nocivos de la quimioterapia y de la radioterapia.
3. La diferenciación y recuento de los elementos celulares de la sangre.
La fidelidad de la información obtenida de ellos, depende en gran parte de la calidad de las extensiones.
Estas no deben ser demasiado gruesas porque las células se amontonarían y no podrían ser
reconocidas, ni diferenciarse, ni demasiado delgadas porque las células se deformarían, distorsionarían
y destruirían. Por eso los frotis de sangre deben ser bien nivelados y para obtener buenos resultados es
necesario que:
1. Tanto portaobjetos como cubreobjetos deben estar bien limpios y desengrasados
(prefentemente nuevos).
2. La gota de sangre usada para la preparación de el frotis no debe ser muy grande ni pequeña,
de preferencia de el tamaño de la cabeza de un alfiler (entre 2 y 3 mm), obtenida por punción
capilar.
3. La sangre no haya estado en contacto con anticoagulante, pues podría deformarse la
morfología celular si pasase esto.
4. La lectura de las extensiones se hará en las zonas donde los eritrocitos "casi se tocan".
Extensión en el portaobjetos[editar]
Para llevar a cabo las extensiones en portaobjeto se coloca una gota de sangre de 3 a 4 mm de
diámetro, a unos 2 o 3 cm de uno de los extremos de el portaobjetos este se coloca en una superficie
plana y lisa. Con el borde de otro portaobjeto, con el que se toca la gota de sangre, la cual se desliza
por capilaridad a todo lo largo de el canto de dicho portaobjeto y con un movimiento rápido y uniforme,
en un angulo de 45 grados se desliza el portaobjetos dejando una capa de sangre en la superficie de el
otro. El espesor del extendido debe ser delgado.
Neutrófilo(Redirigido desde «Neutrófilos»)

Neutrófilo
Imagen tomada con un microscopio óptico en la que se observa
un neutrófilo rodeado deglóbulos rojos en un frotis
sanguíneo. Tinción de May Grünwald-Giemsa.
Representación 3D de un neutrófilo.
Latín Granulocytus neutrophilus; Neutrophilus;
Granulocytus neutrophilus segmentonuclearis
TH H2.00.04.1.02012
Sistema Inmune
Sinónimos
Polimorfonuclear

Enlaces externos
MeSH neutrophil
Los neutrófilos, también denominados polimorfonucleares (PMN), son glóbulos blancos de
tipo granulocito. Miden de 9 a 12 μm y es el tipo de leucocito más abundante de la sangre en el ser
humano, representando en torno al 60-70% de los mismos. Su periodo de vida media es corto,
durando horas o algunos días. Su función principal es la fagocitosis de bacterias y hongos.1
Se llaman neutrófilos porque no se tiñen con colorantes ácidos ni básicos, por lo que su citoplasma
se observa rosa suave. Se caracterizan por presentar unnúcleo con cromatina compacta
segmentada multilobulado -de 2 a 5 lóbulos conectados por delgados puentes-.1 En neutrófilos
inmaduros el núcleo se presenta sin segmentar, como una banda fuertemente teñida.
Su citoplasma contiene abundantes gránulos finos color púrpura, (con el colorante Giemsa) que
contienen abundantes enzimas líticas, así como una sustancia antibacteriana llamada fagocitina,
todo esto necesario para la lucha contra los gérmenes extraños.
Es una célula muy móvil y su consistencia gelatinosa le facilita atravesar las paredes de los vasos
sanguíneos para migrar hacia los tejidos, ayudando en la destrucción de bacterias y hongos y
respondiendo a estímulos inflamatorios. A este fenómeno se le conoce como diapédesis.
Los neutrófilos normalmente se encuentran en el torrente sanguíneo. Empero, durante el inicio
agudo de la inflamación, particularmente como resultado de infección bacteriana, son unos de los
primeros migrantes hacia el sitio de inflamación (primero a través de las arterias, después a través
del tejido intersticial), dirigidos por señales químicas como interleucina-8 (IL-8), interferón-gamma
(IFN-γ), en un proceso llamado quimiotaxis. Son las células predominantes en elpus.
La liberación de los neutrófilos desde los vasos sanguíneos está condicionada por la liberación
de histamina (liberada por mastocitos) y TNF-α (liberada por macrófagos). La TNF-α y la histamina
actúan sobre las células del endotelio del vaso, haciendo que se active mediante la expresión
de selectina-E. Los neutrófilos activados mediante IL-8 pueden unirse a la selectina-E mediante su
ligando glucídico. De esa manera son capaces de estar presentes en tejidos en apenas 5 horas
después de empezar la infección. Debido a sus funciones fagocíticas, los neutrófilos también se
conocen como micrófagos, para diferenciarlos de las células fagocíticas más grandes,
los macrófagos.
Índice
[ocultar]
1 Diapédesis
o 1.1 Adhesión al endotelio
o 1.2 Migración a través del endotelio
o 1.3 Quimiotaxis de los leucocitos
2 Reconocimiento de los microbios y los tejidos muertos

o 2.1 Receptores para componentes microbianos
o 2.2 Receptores acoplados a proteínas G
o 2.3 Receptores para opsoninas
o 2.4 Receptores para citoquinas
3 Eliminación del agente dañino: fagocitosis
o 3.1 Reconocimiento y unión
o 3.2 Incorporación en la vacuola fagocítica
o 3.3 Destrucción del material ingerido
4 Galería
5 Referencias
6 Bibliografía recomendada
7 Enlaces externos
Diapédesis[editar]
Los neutrófilos interaccionan con agentes quimiotácticos para migrar a sitios invadidos por
microorganismos, en un proceso denominado diapédesis o extravasación. Este proceso consta
de tres etapas:
1. En la luz del vaso sanguíneo: marginación, rotación y adhesión al endotelio (ver
también Inflamación aguda para más detalles de los pasos iniciales).
2. Migración a través de la pared del vaso sanguíneo.
3. Migración en el tejido hacia un estímulo quimiotáctico.
Adhesión al endotelio[editar]
Cuando se inicia el proceso de inflamación, se produce una vasodilatación iniciada por mediadores
químicos, que provoca la salida de líquido de la sangre hacia los tejidos, generando un edema.
Como consecuencia, la viscosidad de la sangre aumenta, debido al aumento de concentración de
los glóbulos rojos, lo que a su vez provoca un descenso en el flujo sanguíneo (estasis). En estas
condiciones hemodinámicas, los leucocitos se redistribuyen en posición periférica, un fenómeno
denominado marginación. A continuación, los leucocitos ruedan sobre la superficie del endotelio,
estableciendo contactos transitorios con las células endoteliales, soltándose y volviéndose a unir.
Finalmente, los leucocitos se adhieren firmemente al endotelio, antes de iniciar la migración.
Simultáneamente al efecto vasodilatador, los mediadores de la inflamación (TNF e IL-1) activan las
células endoteliales, que expresan proteínas de adhesión para los leucocitos. La fase
de rotación está mediada por la familia de proteínas de membrana denominadas selectinas, que
pueden ser de tres tipos:
selectina-L, que se expresa en los leucocitos
selectina-E, en las células endoteliales
selectina-P, en las plaquetas y en las células endoteliales

Los ligandos para selectinas son oligosacáridos sialilados unidos a cadenas de glicoproteínas. La
interacción entre los receptores de selectina de los neutrófilos y las selectinas de las células
endoteliales da lugar a que los neutrófilos rueden con lentitud a lo largo del recubrimiento endotelial
de los vasos.
Por otro lado, las quimiocinas de la inflamación provocan un cambio de estado de las integrinas de
la membrana de los PMN, que pasan de una conformación de baja afinidad a una conformación de
alta afinidad, mientras que la interleucina 1 (IL-1) y el factor de necrosis tumoral (TNF) inducen a
las células endoteliales para que expresen moléculas de adherencia intercelular tipo 1 (ICAM-1) y
VCAM-1 (vascular cell adhesion molecule-1), a las cuales se unen con avidez las moléculas de
integrina de alta afinidad de los neutrófilos, provocando la adhesión firme de los PMN al endotelio.
Migración a través del endotelio[editar]
Es el fenómeno denominado diapédesis o extravasación, y ocurre fundamentalmente en las
vénulas poscapilares. Las quimioquinas liberadas por los macrófagos y los mastocitos tisulares en
respuesta a la presencia de microorganismos, cuerpos extraños o daño tisular, actúan sobre los
PMN adheridos al endotelio, estimulando su migración a través de los espacios interendoteliales
hacia el sitio dañado o infectado. Algunas moléculas presentes en las uniones entre las células
endoteliales facilitan la migración de los neutrófilos, como CD31 o PECAM-1, proteínas de la
familia de las inmunoglobulinas. Después de atravesar el endotelio, los PMN deben romper
la lámina basal, probablemente segregando colagenasas, y entrar en el tejido extravascular. Para
ello, los leucocitos se adhieren a la matriz extracelular mediante la unión de sus integrinas
y CD44 a las proteínas de la matriz.
Quimiotaxis de los leucocitos[editar]
Una vez en el compartimiento de tejido conectivo, los leucocitos migran hacia la zona dañada por
un proceso denominado quimiotaxis, que se define como la locomoción dirigida a lo largo de un
gradiente químico. Las sustancias que generan dicho gradiente pueden ser exógenas (por ejemplo,
toxinas bacterianas) o endógenas, entre las que se encuentran diferentes mediadores químicos:
citoquinas , sobre todo las de la familia de las quimioquinas (como IL-8);
componentes del sistema del complemento, sobre todo C5a;
metabolitos del ácido araquidónico, sobre todo el leucotrieno B4 (LTB4).
Todos estos agentes se unen a receptores transmembrana acoplados a proteína G en la superficie
de los leucocitos. Esto desencadena una vía de señalización que resulta en la activación de
segundos mensajeros que aumentan el calcio citosólico y activan GTPasas y kinasas. Como
consecuencia, se induce la polimerización de la actina, que genera un aumento de actina
polimerizada en el extremo celular próximo a la región dañada, y localización de los filamentos
de miosina en la parte posterior celular. El leucocito se mueve extendiendo filopodios que tiran de
la parte posterior celular en dirección de la extensión, como un coche con tracción delantera. El
resultado final es que el leucocito se mueve hacia la zona objetivo.
Reconocimiento de los microbios y los tejidos muertos[editar]
Una vez que se encuentran en la zona objetivo, los neutrófilos deben reconocer de forma
específica el agente ofensivo, antes de proceder a eliminarlo. Tanto los neutrófilos como

los macrófagos (las células con capacidad fagocítica) presentan receptores de membrana que les
permite reconocer el agente externo y activar los procesos de fagocitosis. Los tipos de receptores
más importantes son:
Receptores para componentes microbianos[editar]
Los receptores de tipo Toll (TLR, por sus siglas en inglés) reconocen componentes de diferentes
tipos de microbios: lipopolisacáridos bacterianos, proteoglicanos bacterianos, nucleótidos CpG no
metilados (frecuentes en bacterias) o ARN de doble hebra (producido por algunos virus). Los TLR
están presentes en la superficie celular, pero también en los endosomas, de manera que pueden
detectar microbios extracelulares y fagocitados. Estos receptores activan kinasas que estimulan la
producción de sustancias microbicidas.
Receptores acoplados a proteínas G[editar]
Algunos de estos receptores reconocen péptidos que contengan fragmentos de N-
formilmetionina (que inician todas las proteínas bacterianas, pero sólo están presentes en las
proteínas mitocondriales de mamíferos). Otros receptores reconocen quimioquinas, fragmentos
del sistema del complemento, como C5a, y mediadores lipídicos,
como PAF, prostaglandinas o leucotrienos, todos los cuales se producen en el contexto de daño
celular. Unión del ligando a estos receptores induce la migración y la produción de sustancias
microbicidas.
Receptores para opsoninas[editar]
Los leucocitos expresan receptores para opsoninas, proteínas de defensa que recubren los
microbios mediante el proceso de opsonización. Estas sustancias incluyen anticuerpos, proteínas
del sistema del complemento y lectinas. Una de las formas más eficaces de mejorar la fagocitosis
de una partícula es recubrirla con anticuerpos tipo IgG específicas para esa partícula. Los IgG son
reconocidos por los receptores de alta afinidad para Fcγ de los fagocitos, denominados FcγR.
Asimismo, C3b (del sistema del complemento) es también una potente opsonina, y los fagocitos
expresan un receptor, CR1, capaz de detectarlo. La unión de las opsoninas a sus receptores en los
fagocitos promueven la fagocitosis y activan los leucocitos.
Receptores para citoquinas[editar]
Los leucocitos tienen receptores para citoquinas que son producidas en presencia de microbios. La
más importante de éstas citoquinas es el interferón-γ (IFN-γ), segregado por las células
NK activadas por microbios y por linfocitos T activados por antígenos durante la respuesta inmune
adaptativa. El IFN-γ es el principal agente activador de los macrófagos.
Eliminación del agente dañino: fagocitosis[editar]
La unión de los ligandos a los receptores de los leucocitos induce su activación, debido a la
iniciación de vías de señalización que producen un aumento de los niveles de calcio citosólicos y la
activación de enzimas como PKC y fosfolipasa A2. La respuesta funcional más importante es
la fagocitosis y la destrucción intracelular del agente dañino.
La fagocitosis se desarrolla en tres etapas secuenciales:

Reconocimiento y unión[editar]
Mediado por los receptores de manosa y receptores a diferentes opsoninas presentes en el agente
dañino. El receptor de manosa es una lectina que se une a los residuos de manosa y fucosa de las
glicoproteínas y los glicolípidos. Estos residuos son típicos de las paredes bacterianas, mientras
que las glicoproteínas y glicolípidos de mamíferos contienen residuos terminales de ácido siálico.
Por tanto, los receptores de manosa se unen de forma específica a moléculas bacterianas.
Incorporación en la vacuola fagocítica[editar]
Una vez que la partícula está unida a los receptores, se forman extensiones del citoplasma
(pseudópodo) que la rodean, la membrana plasmática se fusiona y se forma una vesícula
(el fagosoma) que contiene la partícula. El fagosoma se fusiona entonces con un lisosoma, que
descarga su contenido en el fagolisosoma. Durante este proceso el fagocito puede también liberar
el contenido de los lisosomas al espacio extracelular, sobre todo si la partícula que se pretende
fagocitar es demasiado grande para ser incorporada en una vesícula.
La fagocitosis (que es un proceso muy complejo) depende de la polimerización de actina, por lo
que las mismas señales que activan la quimiotaxis activan también la fagocitosis.
Destrucción del material ingerido[editar]
Los neutrófilos contienen tres tipos de gránulos:
los gránulos específicos (o secundarios), más grandes, que
contienen lisozima, colagenasa, gelatinasa, lactoferrina, activador
del plasminógeno, histaminasa y fosfatasa alcalina;
los gránulos azurófilos (o primarios) contienen mieloperoxidasa, factores bactericidas
(lisozima, defensinas), hidrolasas ácidas y una variedad de proteasas neutras
(elastasa, catepsina G y otras).
unos recién descubiertos gránulos terciarios que contienen gelatinasa y catepsinas, así como,
glucoproteínas insertadas en el plasmalema.2
Los dos primeros tipos mencionados pueden fusionarse con las vacuolas fagocíticas que contienen
el material ingerido, vertiendo su contenido para digerirlo.
Las bacterias no sólo se destruyen por la acción de enzimas sino también y sobre todo por la
formación de especies reactivas del oxígeno (ROS) y especies reactivas del nitrógeno (NOS)
dentro de los fagosomas de los neutrófilos. Algunos de estos compuestos son:
aniones superóxidos (02~), que se forman por acción de la oxidasa de NADPH (también
llamada fagocito oxidasa) sobre el O2 en una reacción oxidativa muy rápida que se
denomina estallido respiratorio;
el peróxido de hidrógeno (H2O2), formado por la acción de la superóxido dismutasa sobre el
anión superóxido;
hipoclorito (OCl*, el ingrediente activo de la lejía), formado por la acción de
la mieloperoxidasa (MPO) sobre el peróxido de hidrógeno en presencia de iones cloruro; el
sistema H2O2-MPO-Cloruro es el microbicida más eficaz de los neutrófilos;
la sintasa de óxido nítrico genera NO a partir de arginina; el NO también tiene efectos
microbicidas;

el NO puede reaccionar con el anión superóxido para generar el radical peroxinitrito (ONOO*),
altamente reactivo.
Todos estos radicales libres del oxígeno y del nitrógeno atacan y dañan los lípidos, proteínas y
ácidos nucleicos de los microbios, así como del huésped.
En ocasiones se libera el contenido de los gránulos azurófilos a la matriz extracelular y causa daño
tisular, pero por lo general la catalasa y la glutatión peroxidasa degradan el peróxido de hidrógeno.
Sin embargo, los leucocitos pueden causar daños importantes en las células normales y los tejidos
en algunas circunstancias:
en infecciones difíciles de erradicar, como la tuberculosis y ciertas enfermedades virales, la
respuesta prolongada del huésped contribuye más a la patología que el microbio en sí mismo,
ya que los tejidos adyacentes a la infección sufren daños colaterales de larga duración;
cuando la respuesta inflamatoria se dirige de forma inapropiada hacia los tejidos del huésped,
como en ciertas enfermedades autoinmunes;
cuando el huésped reacciona de forma exagerada a sustancias ambientales normalmente
inocuas, en enfermedades alérgicas como el asma.
En estos casos, los leucocitos dañan los tejidos sanos con los mismos mecanismos que atacan los
microbios, ya que una vez que son activados, no distinguen entre huésped y patógeno. Las
enzimas y las especies reactivas de oxígeno y nitrógeno liberadas al espacio intracelular pueden
dañar los tejidos sanos y el endotelio, amplificando la acción del patógeno. De hecho, en estos
casos los leucocitos en sí mismos constituyen la amenaza mayor, y subyacen como la causa
principal de las alteraciones presentes en muchas enfermedades humanas:
agudas: asma, rechazo agudo a un trasplante, síndrome respiratorio agudo
severo, glomerulonefritis, choque séptico o absceso pulmonar;
crónicas: artritis, asma, aterosclerosis, rechazo crónico a un trasplante, fibrosis
pulmonar, obesidad.
Los neutrófilos tienen una vida media corta y mueren por apoptosis unas pocas horas después de
dejar la sangre, una vez que han llevado a cabo su función de destruir microorganismos. Ello tiene
como efecto la formación de pus, en el que se produce la acumulación de leucocitos (sobre todo
neutrófilos) y bacterias muertos y líquido extracelular.
Los neutrófilos también están siendo objeto de debate en las terapias contra el cáncer. Si bien
ciertos estudios sugieren su posible participación en la angiogénesis y la metástasis, otros los
consideran elementos indispensables en la batalla contra los tumores sólidos, como en la
controvertida teoría desarrollada por el equipo multidisciplinar que dirige el físico e
investigador Antonio Brú.
Galería[editar]
Basófilo(Redirigido desde «Basófilos»)

Basófilo
Imagen tomada con un microscopio óptico, en la que se observa
un basófilo teñido conhematoxilina-eosina.
Representación 3D de un basófilo.
Latín Granulocytus basophilus; Basophilus
TH H2.00.04.1.02022
Sistema Inmune
Enlaces externos
MeSH basophil

Los basófilos conforman el tipo de leucocito menos abundante en sangre. Tiene núcleo irregular, difícil
de ver por la granulación basófila que lo cubre casi siempre. Tamaño semejante al de los segmentados.
Se denomina basófilo a cualquier célula que se tiñe fácilmente con
colorantes básicos (hematoxilinaprincipalmente). Sin embargo, cuando se emplea este término sin
ninguna aclaración adicional, suele referirse a uno de los tipos de leucocitos (glóbulos blancos de
la sangre) de la familia de los granulocitos.
Los basófilos son los responsables del inicio de la respuesta alérgica, según tres estudios que se
publican en la edición digital de la revista "Nature Immunology"
En las micrografías electrónicas se ven con claridad un pequeño aparato de Golgi,
algunas mitocondrias, un extenso RER y pequeñas inclusiones de glucógeno.
Los gránulos de los basófilos son gruesos pero escasos. Son células de unos 10 μm de diámetro y su
núcleo tiene una forma que recuerda a una S, su núcleo es globulado y se divide de 1 a 3 células. Se
originan en el mismo lugar que el resto de los granulocitos (médula ósea), y son los menos
numerosos, ya que constituyen sólo el 0,5% del total.1 Son muy parecidos a los mastocitos o células
cebadas, pero no son el mismo tipo celular, ni se diferencian a ellos.
Tienen una activa participación en la respuesta inmunitaria, a través de la liberación
de histamina, serotonina en bajas concentraciones, y otras sustancias químicas.
Tiene gránulos de dos clases:
Gránulos azurófilos: Contienen lisosomas, que a su vez estos contienen hidrolasas ácidas.
Gránulos específicos o secundarios: contienen histamina (vasodilatador), heparán
sulfato (vasodilatador), heparina (anticoagulante) y leucotrienos (hacen contraer el músculo liso de
las vías aéreas).
Los basófilos además de poseer gránulos en su interior, poseen receptores de IgE (inmunoglobulina E),
aquella inmunoglobulina relacionada con las alergias. Es por eso que el basófilo participa en
la respuesta inflamatoria.
Índice
[ocultar]
1 Galería
2 Véase también
3 Referencias
4 Enlaces externos

Galería[editar]
Linaje de células sanguíneas.
Tinción alternativa de un basófilo.
Eosinófilo(Redirigido desde «Eosinófilos»)
Eosinófilo
Imagen tomada con un microscopio óptico en la que se observa
un eosinófilo rodeado deglóbulos rojos en un frotis sanguíneo.

Representación 3D de un eosinófilo.
Latín Granulocytus acidophilus; Eosinophilus
TH H2.00.04.1.02017
Sistema Inmune
Enlaces externos
MeSH eosinophil
Un eosinófilo es un leucocito de tipo granulocito pequeño derivado de la médula ósea, que tiene
una vida media en la circulación sanguínea de 3 a 4 días antes de migrar a los tejidos en donde
permanecen durante varios días. Su desarrollo en la médula ósea es estimulado por
diversas interleucinas, como la IL-5, la IL-3y el factor estimulante de colonias granulocito-
macrófago. Es característico su núcleo bilobulado, al igual que sus distintivos
gránulos citoplásmicos. Estasproteínas granulares son responsables de muchas
funciones proinflamatorias, principalmente en la patogénesis de las enfermedades alérgicas,
como célulaefectora de hipersensibilidad inmediata, así como en la muerte de parásitos. Una de
las enzimas más importantes que contienen sus gránulos es lahistaminasa, que se encarga
de hidrolizar la histamina, regulando así la respuesta alérgica.
Índice
[ocultar]
1 Descripción
o 1.1 Estructura
2 Función

3 Imágenes adicionales
4 Véase también
5 Enlaces externos
Descripción[editar]
Estas células fueron descritas inicialmente por Paul Ehrlich en 1879, y les dio el nombre de
eosinófilos al observar que se teñían intensamente con ciertoscolorantes ácidos como la eosina.
Estructura[editar]
Son leucocitos polimorfonucleares.
A nivel ultraestructural poseen un núcleo bilóbulado, ambos lóbulos están unidos por estructuras
llamadas puentes intercromatinícos y abundantes gránulos específicos y azurófilos, que se tiñen de
rojo en los frotis de sangre periférica y cortes del tejido. Además, la heterocromatina compacta está
situada junto a la envoltura nuclear, mientras que la cromatina se halla en el centro del núcleo.
Son generados por mitosis de las células precursoras en la médula ósea donde permanecen unos
cuatro días. Pasan luego a la circulación general desde donde migran a los tejidos
(epitelio y mucosas). La maduración de los eosinófilos está regida por diversos mediadores como
IL-3, IL-5 y GM-CSF. Normalmente, los eosinófilos suponen menos del 4% de los leucocitos
circulantes, pues son células más tisulares que circulantes. Son atraídos hacia los tejidos diana por
diversas quimiocinas liberadas por las células inflamatorias y epiteliales. Su cantidad aproximada
en la sangre es de 150 células/microlitro, y constituyen entre el 2% y el 4% de los leucocitos.
Los eosinófilos poseen movimiento ameboide y tienen débil actividad fagocítica. Su tamaño es
semejante al del neutrófilo (10-12 μm). Constan de un núcleo bilobulado y su citoplasma está casi
completamente ocupado por unos 20 gránulos acidófilos, pues se tiñen de color naranja o marrón
anaranjado con las coloraciones panópticas. Los gránulos están formados por un núcleo
electrodenso rodeado por una matriz electrotransparente, y contienen cuatro clases principales de
proteínas: proteína básica mayor (MBP), proteína catiónica del eosinófilo (ECP), peroxidasa del
eosinófilo (EPO) y neurotoxina derivada del eosinófilo (EDN). Los eosinófilos son capaces de
sintetizar de nuevo otros productos, como mediadores lipídicos (PAF, LTC4), citocinas (IL-3, IL-
5, GM-CSF), quimiocinas (eotaxina) y óxido nítrico (NO).
Función[editar]
Los eosinófilos interaccionan con otras células por la expresión de múltiples receptores en su
superficie. Además, son células fagocitarias que demuestran especial afinidad por los
complejos antígeno-anticuerpo, por lo que la mayoría de los eosinófilos son atraídos
por quimiotaxis. También los eosinófilos pueden ser atraídos por sustancias liberadas de
los basófilos, como la histamina.
Los eosinófilos pueden regular la respuesta alérgica y las reacciones de hipersensibilidad mediante
la neutralización de la histamina por la histaminasa, y a su vez producir un factor inhibidor derivado
de los eosinófilos para inhibir la desgranulación de las células cebadas o de los basófilos, que
contienen sustancias vasoactivas.

Los eosinófilos juegan un papel de defensa del huésped frente a microorganismos no fagocitables,
poseen una función citotóxica (por sus proteínas granulares), inmunoreguladora (por las citocinas
que libera) y son capaces de participar en la reparación y remodelación tisular (liberando TGF-β).
Los mecanismos de acción de los eosinófilos mejor estudiados tienen que ver con la alergia y en la
defensa contra parásitos. Sus receptores para IgE explican su fijación a los parásitos recubiertos
previamente por esta inmunoglobulina, capacitándoles para destruir sus larvas, como acontece en
la esquistosomiasis o bilharziasis.
Imágenes adicionales[editar]
Linaje de las células sanguíneas.
Representación 3D de varios tipos de glóbulos blancos.
Imagen tomada con unmicroscopio óptico en la que se observa uneosinófilo rodeado deglóbulos
rojos. Tinción de Giemsa.
Esquema de un eosinófilocon sus diferentes partes:membrana, gránulos de secreción, núcleo, ycitoplasma.

Imagen tomada con unmicroscopio óptico en la que se observa uneosinófilo rodeado deglóbulos rojos y
algunaplaqueta en un frotis sanguíneo.
Representación de uneosinófilo.
Representación de uneosinófilo.
Véase también[editar]
infocito
Linfocito

Representación 3D de un linfocito B.
Representación 3D de un linfocito T.
Latín Lymphocytus
TH H2.00.04.1.02002
Enlaces externos
MeSH lymphocyte

Linfocito (microscopio electrónico de barrido).
Linfocito mostrando su grannúcleo (microscopio óptico).
Un linfocito es una célula linfática (se fabrican por células linfoides presentes en la médula ósea y que
posteriormente migran a órganos linfoides como el timo, ganglios linfáticos y bazo, constituyen el 99%
de las células linfáticas), que es un tipo de leucocito (glóbulo blanco) comprendido dentro de
los agranulocitos. Son los leucocitos de menor tamaño (entre 7 y 15 μm), y representan
aproximadamente el 30% (del 24 a 32%) del total en la sangre periférica. Presentan un
grannúcleo esférico que se tiñe de violeta-azul y de escaso citoplasma (en el que frecuentemente se
observa como un anillo periférico de color azul). Poseen un borde delgado de citoplasma que contienen
algunas mitocondrias, ribosomas libres y un pequeño aparato de Golgi.
Los linfocitos son células circulantes del sistema inmunitario que reaccionan frente a materiales extraños
y son de alta jerarquía en el sistema inmunitario, principalmente encargadas de la inmunidad específica
o adquirida.
Estas células se localizan fundamentalmente en la linfa y los órganos linfoides y en la sangre. Tienen
receptores para antígenos específicos y, por tanto, pueden encargarse de la producción
de anticuerpos y de la destrucción de células anormales. Estas respuestas ocurren en el interior de los
órganos linfoides, los cuales, para tal propósito, deben suministrar un entorno que permita la interacción
eficiente entre linfocitos, macrófagos y antígeno extraño. La principal causa de su aumento es el estrés.
Índice

[ocultar]
1 Tipos
2 Tráfico de linfocitos
3 Transmigración
4 Véase también
5 Referencias
6 Enlaces externos
Tipos[editar]
Presentación de antígeno.
1. Proteína invasora/antígeno
2. Macrófago/Célula presentadora de antígeno
3. Complejo antígeno:MHC II] (presentación de antígeno), activación de linfocito Th
4. Linfocito Th (cooperador)
5. Proteína invasora unido a anticuerpos demembrana
6. Linfocito B 7. Procesamiento de antígeno (MHC tipo II)
8. Complejo antígeno:MHC II (presentación de antígeno)
9. Producción de anticuerpos específicos para el antígeno
10. Activación de linfocitos B con los Th activados.
Los linfocitos son células difíciles de catalogar según su morfología, por eso se recurre al uso de sus
"CD" o cúmulo de diferenciación (del inglés Cluster of differentiation), los cuales son un conjunto de
marcadores biológicos para la identificación celular.
Linfocitos B (bursodependientes, la 'B' proviene del latín Bursa fabricii 1 , el órgano en el cual se
desarrollan los linfocitos B en las aves): son los responsables de la respuesta humoral, es decir, de
la producción de anticuerpos, proteínas (inmunoglobulinas) que se adhieren a
un antígeno específico (al cual reconocen de manera unívoca). Son capaces de
reconocer lípidos, proteínas y glúcidos. Se diferencian en el hígado y bazo fetal, y en la médula
ósea del adulto.

Linfocitos T (timodependientes, ya que se diferencian en el timo): Detectan antígenos proteicos
asociados a moléculas del complejo mayor de histocompatibilidad (MHC 0 CMH)
Linfocitos T colaboradores (en inglés "helper") o linfocitos CD4+. Reconocen antígenos
presentados por el MHC-II. Se les denomina colaboradores porque están involucrados en la
activación y dirección de otras células inmunitarias.
Linfocitos T citotóxicos o linfocitos CD8+. Reconocen péptidos presentados por MHC-I y tienen
capacidad lítica.
Células asesinas naturales , Natural Killer (NK) o linfocito grande granular. No tienen marcadores
característicos. Participan en la inmunidad innata, con la capacidad de reconocer lo "propio" y
también tienen propiedades líticas.
Tráfico de linfocitos[editar]
El tráfico de linfocitos entre los tejidos, el torrente sanguíneo y los ganglios linfáticos, permite que las
células sensibles a los antígenos los busquen y sean reclutadas en sitios en los cuales se está
desarrollando una respuesta. A su vez hay una diseminación de las células de memoria que permite la
organización de una respuesta más amplia.
1. Después de las 24 primeras horas (en que el antígeno se localiza por primera vez en los
ganglios linfáticos o en el bazo) las células reactivas al antígeno sufren una depleción
(disminución) del conjunto de linfocitos circundantes.
2. Días más tarde (después de la proliferación del antígeno en el sitio de localización), en el
conducto torácico aparece un pico de células activadas.
3. En los linfáticos eferentes va haber una caída en la producción de células, fenómeno designado
como “cierre celular” o “atrapamiento de linfocitos” que se cree es el resultado de la liberación
de factores solubles desde las células T inducida por el antígeno, este evento a estar seguido
de una producción de blastos activados que alcanza un máximo a las 80 horas.
4. Los Linfocitos vírgenes ingresan al ganglio linfático a través de los linfáticos aferentes y por el
pasaje guiado a través del endotelio de pared alta de las vénulas poscapilares especializado.
5. Endotelios de este tipo posibilitan el tránsito de células vinculadas en la inmunidad de las
mucosas a las placas de Peyer; también involucran la migración de linfocitos en tejidos
normales e inflamados.
6. Los linfocitos se unen a endotelios planos no especializados y los atraviesan.
7. Los linfoblastos y las poblaciones de células de memoria muestran una migración limitada al
tejido hacia los tejidos extralinfoides, como la piel o el epitelio mucoso; mientras que los
linfocitos, neutrófilos y monolitos se dirigen y migran a sitios de inflamación en respuesta a
mediadores producidos en forma local.

8. Tráfico y recirculación de linfocitos a través del tejido linfoide encapsulado y los sitios de
inflamación: Los linfocitos transportados por sangre entran en los tejidos y ganglios linfáticos
atravesando el endotelio de paredes altas de las vénulas poscapilares (HEV) y salen a través
de los linfáticos de drenaje. Los linfáticos eferentes, que salen desde el último ganglio se unen
para formar el conducto torácico por el que retornan los linfocitos por vía sanguínea. En el
bazo, que carece de HEV, los linfocitos ingresan en el área linfoide (pulpa blanca) desde las
arteriolas y pasan hacia los sinusoides del área eritroide (pulpa roja) y salen por vía esplénica.
9. Tráfico y circulación de linfocitos dentro del sistema linfoide asociado a mucosas-no
encapsulado (MALT): Las células estimuladas por un antígeno se mueven desde las placas
de Peyer, se mueven para colonizar la lámina propia y otras mucosas, y forman un sistema
inmune de mucosas común.
10. Este tráfico organizado se lleva a cabo dirigiendo los linfocitos relevantes a diferentes partes del
sistema linfoide y a otros tejidos, mediante una serie de receptores guía que incluyen:
miembros de la superfamilia de las integrinas (LFA-1, VLA, etc.) y un miembro de la
suúperfamilia de las selectinas, que es la L-selectina.
Las integrinas pueden unirse a la matriz extracelular, a las proteínas plasmáticas y a otras moléculas de
la superficie celular, sus ligandos complementarios incluyen las adresinas vasculares de superficie,
presentes en el endotelio de los vasos sanguíneos.
Estos receptores guía actúan como puertas selectivas que permiten que las poblaciones particulares de
linfocitos tengan acceso al tejido apropiado.
Las quimiocinas como SLC (quimiocina del tejido linfoide secundario) presentadas por el endotelio
vascular, tienen un papel importante para la detección de linfocitos; los receptores de la integrinas están
involucrados en la regulación positiva funcional de las integrinas.
Transmigración[editar]
Paso N°1 - Adherencia y rotación: Para que el linfocito se adhiera a la célula endotelial, debe
superar las fuerzas de cizallamiento creadas por el flujo sanguíneo. Esto se logra por medio de una
fuerza de atracción entre los receptores guía (integrinas y L-selectina) y sus ligandos sobre la pared
del vaso que opera a través de microvellosidades sobre la superficie del linfocito. Después de este
proceso de adherencia; el linfocito rota a lo largo de la célula endotelial y las integrinas VLA-4 o
LPAM-1 sobre el linfocito, se unen a sus ligandos sobre el endotelio.
Paso N°2 - Activación de LFA-1 y aplanamiento: Este proceso conduce a la activación y el
reclutamiento de la integrina LFA-1 hacia la superficie no vellosa del linfocito. Esta integrina se une

con mucha fuerza a ICAM-1 e ICAM-2 sobre la célula endotelial, y el contacto íntimo hace que el
linfocito se aplane.
Paso N°3 - Diapédesis: El linfocito aplanado utiliza ahora la interacción LFA-1-ICAM y el miembro
de la superfamilia de inmunoglobulinas PECAM-1 (molécula de adhesión al endotelio plaquetario,
CD31, no solo presente en las plaquetas), para abrirse paso entre las células endoteliales y en el
tejido, en respuesta a una señal quimiotáctica.
Véase también[editar]
Célula dendrítica
Glóbulo blanco
Linfoadenopatía
Linfocito B
Linfocito grande granular
Linfocito Natural Killer
Linfocito T
Linfocito T CD4+
Linfocito T CD8+
Linfocito T regulador
Linfocitosis
Linfoma
Linfopoyesis
Sangre
Linfocito B
Linfocito B

Linfocito B infectado por el virus Epstein-Barr.
Representación 3D de un linfocito B.
Latín Lymphocytus B
TH H2.00.04.1.02005
H2.00.04.3.07002
Sistema Inmune
Enlaces externos
MeSH b-lymphocyte

Los linfocitos B son los leucocitos de los cuales depende la inmunidad mediada por anticuerpos con
actividad específica de fijación de antígenos. Las células B, que constituyen un 5 a 15% del total
de linfocitos, dan origen a las células plasmáticas que producen anticuerpos.
Los linfocitos son de dos tipos principales, atendiendo a su origen y función: células T, que se
diferencian inicialmente en el timo, y las células B, que se diferencian en el hígado y bazo fetal, y en
la médula ósea del adulto (la 'B' proviene del latín Bursa fabricii, el órgano en el cual se desarrollan los
linfocitos B en las aves). Durante su desarrollo, los linfocitos T y B adquieren receptores específicos
para antígenos, el de las células B se le conoce como receptor de linfocito B (BCR).
Índice
[ocultar]
1 Origen de linfocitos B
2 Activación de células B
o 2.1 Activación dependiente de células T
o 2.2 Activación T-independiente
3 Galería
4 Véase también
5 Referencias
6 Enlaces externos
Origen de linfocitos B[editar]
Son familiares de los linfocitos-T y de los Macrófagos. Los linfocitos B se originan de un Precursor
Relativo, el mismo que da origen a los linfocitos T y las células NK. Es probable que la presencia de un
receptor de membrana sobre los precursores linfoides comunes al que se le llama Notch1 induce la
diferenciación de células T mientras que la ausencia de dicho receptor induce el destino hacia la línea
de linfocitos B.1 Aquellas destinadas a originar células B completan su desarrollo en la médula ósea. Las
células inmaduras pasan por diversas etapas de desarrollo, bajo la influencia de interleucina 7:
Pro-B. Es el momento en que ocurre la acomodación de los grupos de genes (reordenamiento
genético) que producirán la cadena pesada de lainmunoglobulina μ. Si uno de los dos alelos falla en
el reordenamiento del gen, el alelo del cromosoma homólogo completará la pautada reorganización
y una célula productiva. No prosigue la maduración del linfocito si falla el reordenamiento del
receptor de membrana activando mecanismos de apoptosis.
- En el reordenamiento genético de la cadena pesada de la futura inmunoglobulina
de membrana, primero se fusionan los fragmentos D y J (llamados DH y JH: la H por la sigla en

inglés de pesado, Heavy) y en una segunda fase, se asocia el fragmento variable de la cadena
pesada, llamada VH.
Pre-B. La cadena pesada del Igμ es expresada en la membrana formando la llamada pre-BCR.
La expresión de la Igμ estimula la reorganización de las cadenas livianas κ y λ que
corresponden. De igual manera que con la cadena pesada, dos alelos harán el intento de
reproducir el gen y la formación de unacélula productiva. El reordenamiento de cadenas
pesadas adicionales es inhibida.
- La cadena liviana que debería unirse con la cadena pesada, como es característico de todas
las inmunoglobulinas, incluyendo el BCR es sustituida por dosproteínas temporales.2
Linfocito B inmaduro. La cadena liviana es expresada conjuntamente con la cadena
pesada como una IgM de membrana inhibiendo la reorganización de cadenas livianas
adicionales. Con su BCR de membrana, los linfocitos B inmaduros migran de la médula
ósea en dirección al bazo para ser sometidos a selección positiva y negativa y producir un
linfocito B maduro.
Activación de células B[editar]
La activación de linfocitos B es una combinación de su proliferación y diferenciación terminal
en células plasmáticas. El reconocimiento de linfocitos B no es el único elemento requerido
para la activación de células B. Aquellas que aún no han sido expuestas a antígeno, pueden
ser activadas de manera dependiente o independiente de las células T.
Activación dependiente de células T[editar]
Cuando una célula B ingiere un patógeno, adhiere parte de las proteínas del organismo a la
proteína del complejo mayor de histocompatibilidad tipo II. Este complejo es llevado a la
superficie de la membrana celular, donde puede llegar a ser reconocido por los linfocitos T, los
cuales son compatibles con estructuras similares sobre la membrana de los linfocitos B. Si las
estructuras sobre la célula B y T son compatibles, el linfocito T activará al linfocito B, el cual
producirá anticuerpos en contra de segmentos que el patógeno lleva sobre su superficie.
La mayoría de los antígenos son T-dependientes, es decir, requieren cooperadores para la
producción máxima de anticuerpos. Con un antígeno T-dependiente, la primera señal proviene
del entrecruzamiento del antígeno y el receptor de la célula B (BCR), y la segunda señal viene
de una co-estimulación que provee una célula T. Los antígenos T-dependientes contienen
proteínas sobre las MHC-II de las células B que son presentadas a células T llamadas TH2.
Cuando una célula B procesa y presenta el mismo antígeno a la célula TH, ésta

secreta citocinas que activan a la célula B. Estas citocinas producen la proliferación y
diferenciación en células plasmáticas. El cambio al isotipo IgG, IgA, e IgE y la generación de
células de memoria ocurren en respuesta a antígenos T-dependientes.
Activación T-independiente[editar]
Muchos antígenos son T-independientes, es decir, puede emitir ambas señales a la célula B.
Los ratones sin timo (ratones atímicos que no producen células T), pueden responder en contra
de antígenos, llamados T-independientes. Muchas de las bacterias tienen epítopos repetitivos
de carbohidratos que estimulan a las células B, por medio de los llamados receptores
reconocedores de patrones, para que respondan sintetizando IgM en ausencia de cooperación
de un linfocito T. Hay dos tipos de activación T-independientes:
Tipo 1, o activación policlonal T-independiente;
Tipo 2, en la que los macrófagos presentan antígenos a la célula B de tal modo que causa
el entrecruzamiento de BCR requerido.
Galería[editar]
Linaje de las células sanguíneas.
Representación 3D de varios tipos de glóbulos blancos.
Linfocito T
Linfocito T

Micrografía de un linfocito T humano del sistema inmune de un donador
sano.
Representación 3D de un linfocito T.
Latín Lymphocytus T
TH H2.00.04.1.02007
Sistema Inmune
Precursor Timocito
Sinónimos
Célula T

Enlaces externos
MeSH T-lymphocyte
Los linfocitos T o células-T pertenecen al grupo de leucocitos que son conocidos como linfocitos.
Estas células tienen núcleos de forma ovoide que ocupan la mayoría del espacio intracelular.
Los linfocitos T son los responsables de coordinar la respuesta inmune celular constituyendo el 70% del
total de los linfocitos que segregan proteínas ocitoquinas. También se ocupan de realizar
la cooperación para desarrollar todas las formas de respuestas inmunes, como la producción
de anticuerpos por loslinfocitos B.
Se diferencian de los linfocitos B y de las células NK (o célula Natural Killer, en español "asesina
natural") por poseer un receptor especial en la superficie de lamembrana, el receptor de linfocitos
T (también llamado TCR, por su denominación en inglés T cell receptor). Sin embargo, en
un frotis microscópico de sangreno es posible distinguir uno de otro a simple vista.
La denominación de estos linfocitos como "T" se debe a que su maduración tiene lugar en
el timo (órgano linfoide que constituye uno de los controles centrales del sistema inmunitario del
organismo). El número de leucocitos en sangre periférica en un humano promedio es de 4 a 11 x 109 por
litro, del cual, normalmente, un 20% son linfocitos.
Los linfocitos T de un individuo concreto presentan una propiedad denominada restricción CMH: sólo
pueden detectar un antígeno si éste viene presentado por una molécula del complejo mayor de
histocompatibilidad (CMH) del mismo individuo. Esto se debe a que cada linfocito T tiene una
especificidad dual: el receptor del linfocito T (TCR) reconoce algunos residuos del péptido y
simultáneamente algunos residuos de la molécula CMH que lo presenta. Esta propiedad es muy
importante en el trasplante de órganos, e implica que, durante su desarrollo, los linfocitos T deben
"aprender" a reconocer las moléculas CMH propias del individuo, un proceso complejo que tiene lugar
en el timo. Puesto que las moléculas CMH sólo pueden presentar péptidos, esto implica que los
linfocitos T, dado que sólo pueden reconocer un antígeno si viene asociado a una molécula CMH, sólo
pueden reaccionar ante antígenos de origen proteico (procedentes de microorganismos) y no a otro tipo
de compuestos químicos (ni lípidos, ni ácidos nucleicos, ni azúcares). Las moléculas CMH adquieren el
péptido que presentan en el exterior de la membrana celular durante su propia biosíntesis, en el interior
celular. Por tanto, los péptidos que presentan las moléculas CMH provienen demicroorganismos que
están en el interior celular, y ésta es la razón por la cual los linfocitos T sólo detectan microorganismos
asociados a células y desencadenan una respuesta inmune contra microorganismos intracelulares.1
Índice

[ocultar]
1 Tipos
2 Maduración y selección de las células T
o 2.1 Reorganización de los genes TCR
o 2.2 Selección positiva de los timocitos
o 2.3 Elección entre las líneas T CD4+ y CD8+
o 2.4 Selección negativa de los linfocitos
3 Activación de linfocitos T
o 3.1 Receptor de la IL-2
o 3.2 CD28 y B7
o 3.3 IL-12, IL-4
o 3.4 CD40 y CD40L
4 Véase también
5 Galería
6 Referencias
7 Enlaces externos
Tipos[editar]
Un linfocito rodeado de glóbulos rojos en un frotis de sangre.

Linfocito T siendo atacado por el virus del VIH.
Se han descrito varios subtipos de células T, cada uno de ellos con una función distintiva.1
Los linfocitos TCR1 se descubrieron recientemente. Suponen sólo el 15% de los T totales, pero no
son circulantes, sino que se localizan en ciertos epitelios (por ejemplo, los linfocitos intraepiteliales
del intestino). Parece que están especializados en reconocer ciertos patógenos (por ejemplo,
micobacterias), que tienden a entrar por las mucosas.2
TCR2:
Linfocitos T citotóxicos (CTL, por sus siglas en inglés) o linfocitos CD8+ encargados de
las funciones efectoras de la inmunidad celular, mediante la interacción con un complejo
"péptido-CMH-I"; los CTL reconocen las células infectadas por el patógeno para células
tumorales, y las destruyen segregando una serie de moléculas (perforina, granzimas, FasL)
que activan la apoptosis de la célula diana.
Linfocitos T cooperadores , Linfocitos T ayudantes o linfocitos CD4+ o helper T cells: se
encargan de iniciar la cascada de la respuesta inmune coordinada mediante la interacción con
un complejo "péptido-CMH-II". Cuando se activan, los linfocitos CD4+ se especializan,
diferenciándose a su vez en linfocitos efectores, que se distinguen por el tipo de citoquinas que
producen:
Th1 , que migran a los tejidos infectados y colaboran en la activación de
los macrófagos, ya que los Th1 segregan fundamentalmente interferón γ; los Th1 son
importantes en la defensa frente a los microorganismos intracelulares y la inflamación;
Th2 , que permanecen sobre todo en los tejidos linfoides y colaboran en la activación de
los linfocitos B; segregan principalmente IL-4 (que estimula la secreción de Ig-E, que a
su vez activa los mastocitos) e IL-5 (que activa los eosinófilos); los Th2 son
importantes en las reacciones alérgicas y en la defensa frente a parásitos;
Th17 , denominados así porque segregan IL-17, además de IL-22; son los principales
mediadores en algunas reacciones alérgicas, y parecen estar implicados en el
desarrollo de enfermedades como la esclerosis múltiple, la artritis reumatoide y
la enfermedad inflamatoria intestinal.
La diferenciación en Th1, Th2 o Th17 no es al azar, sino que depende de los estímulos que
reciba el linfocito T4 virgen cuando contacte un antígeno extraño.

Linfocitos T de memoria: son células que se generan después de la activación de los
linfocitos T, por exposición a un antígeno extraño (un patógeno). Tienen vida larga, son
funcionalmente inactivos, y pueden circular durante meses o años, preparados para
responder a nuevas exposiciones al mismo microorganismo. El objetivo de las vacunas es
precisamente generar linfocitos de memoria (T y B) mediante la exposición a un patógeno
atenuado, de manera que el organismo responda de manera rápida y eficaz frente al
patógeno activo.
Linfocitos T reguladores (células Treg), anteriormente conocidos como células T
supresoras. Su función principal es eliminar la inmunidad mediada por células al final de la
reacción inmune y eliminar células T auto-reactivas que escaparon al proceso de selección
negativa en el timo.
Células T gamma/delta. Son un pequeño grupo de células T que poseen un TCR
específico en su superficie. La mayor parte de los linfocitos tienen un TCR compuesto por
dos cadenas glucoproteicas denominadas α y β. Sin embargo, en las células γδ, el TCR
está formado por una cadena γ y una cadena δ. Este grupo de linfocitos es muy poco
frecuente (5% del total), pero son abundantes en la mucosadel intestino, formando parte
de una población de linfocitos denominada linfocitos intraepiteliales. Los antígenos que
activan estos linfocitos eran desconocidos, se ha descubierto una presentación de
glucoproteinas como antígenos, en vez de péptidos. Sin embargo, los linfocitos γδ no
presentan restricción CMH, y parece que reconocen proteínas completas en lugar de
péptidos, aunque algunos reconocen moléculas CMH-IB.
Maduración y selección de las células T[editar]
Activación de b-células dependiente de t-células, mostrando T-células (izquierda) B-células (derecha) y
varias moléculas de interacción

Como pasa con todas las células linfocíticas, las células T provienen de
una célula progenitora hematopoyética. Las células progenitoras de los linfocitos T migran
desde la médula ósea hacia el timo, donde tiene lugar todo el proceso de maduración,
generando células que expresan TCR y CD4 o CD8. Varias etapas definen esa diferenciación:1
Reorganización de los genes TCR[editar]
Pro-T. La célula pro-T es el primer precursor de la línea de linfocitos T. Estas células
proliferan por efecto de la interleuquina IL-7 producida por las células del timo. En
el núcleo de algunas de estas células, se reordenan los genes que codifican la cadena β
del TCR, por recombinación mediada por la V(D)J recombinasa. El TCR no se expresa
aún en la superficie del pro-T. Tampoco se expresan en la membrana
celular las moléculas accesorias CD4 ni CD8. Por esa razón las células pro-T se
denominan CD4-/CD8- o dobles negativas.
- El reordenamiento de la cadena β ocurre al activarse uno de los dos alelos que codifican la
cadena β. El otro alelo es inhibido durante el reordenamiento del alelo activado (esto se
denomina "exclusión alélica"). Si no se produce una cadena β completa en una célula pro-T,
esa célula muere.
Pre-T. Si la recombinación VDJ tiene lugar con éxito y se sintetiza una cadena β, ésta
se expresa en la superficie celular, unida a una proteína invariante denominada pre-
Tα, para formar el complejo pre-TCR. Por tanto, la célula pre-T es la misma célula pro-
T a partir del momento en que la cadena β del TCR se expresa en la superficie
celular. La expresión de la cadena β marca el estadio pre-T y al mismo tiempo
comienza el reordenamiento de la cadena α. En las pre-T, aún siguen sin expresarse
en la membrana celular las moléculas accesorias CD4 ni CD8, así que las células pre-
T son CD4-/CD8- o dobles negativas.
- La expresión en microdominios de la membrana celular de la cadena β unida a la proteína pre-
Tα se conoce como pre-TCR y estimula el reordenamiento de uno de los alelos que codifican la
cadena α. Si una célula no es capaz de sintetizar una cadena α y el TCR completo, esa célula
muere.
Timocito doble-positivo. Estas son las células supervivientes, que expresan
tanto la cadena α como β, es decir un TCR completo, CD3 y
tanto CD4 como CD8. Por ello se denominan dobles positivas. Ello da paso a los
mecanismos de selección positiva y negativa.

Selección positiva de los timocitos[editar]
En esta fase tiene lugar la puesta en marcha del mecanismo de restricción CMH: los
linfocitos T de un individuo concreto sólo pueden detectar un antígeno si éste viene
presentado por una molécula delcomplejo mayor de histocompatibilidad (CMH) del
mismo individuo. Los diferentes clones de timocitos dobles positivos expresan
diferentes tipos de TCR αβ. Si el TCR de una célula T reconoce una molécula CMH
en el timo (que por definición es una molécula CMH presentando un péptido propio del
individuo), esa célula T es seleccionada para sobrevivir: por eso se habla de selección
positiva. Para asegurarse de que el linfocito T durante su maduración será expuesto a
todo tipo de péptido propio, las células epiteliales medulares del timo expresan
numerosos genes, que codifican la mayor parte de las proteínas presentes en los
tejidos periféricos.
Las células que no son capaces de reconocer un complejo "péptido propio-CMH" en el
timo mueren por apoptosis. Estas células no serían útiles al individuo, porque serían
incapaces de ver los péptidos presentados por las moléculas de CMH en los tejidos
periféricos.
Elección entre las líneas T CD4+ y CD8+[editar]
Durante el proceso de selección positiva, las células T que reconocen complejos
péptido-CMH clase-I preservan la expresión de CD8, el coreceptor que se une a la
molécula CMH-I, y pierden la expresión de las moléculas de CD4. A la inversa, las
células que reconocen complejos péptido-CMH clase-II preservan la expresión de
CD4 y pierden la de CD8.
Así, lo que se obtiene al final del proceso de selección positiva son timocitos simples
positivos, que son o bien CD8+, restringidos para ver CMH-I, o bien CD4+,
restringidos para CMH-II.
Además, durante este proceso, las células T también devienen segregadas
funcionalmente: las células T CD8+ pueden convertirse en linfocitos T
citotóxicos cuando se activan, mientras que las células T CD4+ serán linfocitos T
cooperadores. Se desconoce cómo la selección de co-receptores está asociada a la
segregación funcional.
Selección negativa de los linfocitos[editar]
Los linfocitos dobles positivos inmaduros cuyos receptores reconocen fuertemente los
complejos "péptido:CMH" en el timo también sufren apoptosis. Este es el proceso de

selección negativa, que sirve para eliminar linfocitos que podrían reaccionar de forma
dañina contra proteínas propias que se expresan en el timo. Por ello, se dice que este
mecanismo permite el establecimiento de la tolerancia central, al asegurar que las
proteínas propias no serán atacadas por los linfocitos T.
Las células T que han pasado los procesos de selección positiva y negativa
son linfocitos maduros, que presentan las siguientes características:
son simples positivos CD4+ o CD8+;
están restringidos para las moléculas CMH propias (CD4+:CMH-II, CD8+:CMH-I);
son tolerantes para las proteínas propias;
son vírgenes (naïves): no han encontrado nunca un antígeno extraño.
Los linfocitos maduros salen del timo y se distribuyen por la periferia a través
del sistema circulatorio, donde pueden encontrar una célula que presente un complejo
"péptido extraño:CMH", capaz de activar el linfocito y desecadenar una respuesta
inmune.
Es interesante destacar que la capacidad de reconocer los antígenos extraños por
parte de los linfocitos T no está sometida a selección, sino que es el producto del
azar: las células T que reconocen los complejos "péptido propio:CMH propio" de
forma débil puede que reconozcan fuertemente antígenos extraños, procedentes de
microorganismos, en la periferia del organismo.
Activación de linfocitos T[editar]

La activación de linfocitos T tiene dos consecuencias generales:
En el ganglio linfático, la activación de los linfocitos T conduce a la activación de
células efectoras inmunes.
En los téjidos periféricos, la activación de linfocitos T conduce a la erradicación
del microorganismo del foco infeccioso
Una de las primeras respuestas detectables de los linfocitos T a la presentación y
reconocimiento antigénico por células presentadoras de antígeno(CPA) es la
secreción de citocinas, en especial la Interleucina-2 (IL-2), la cual actúa como factor
de crecimiento sobre el mismo linfocito T que lo secreta, por tener ésta receptores
para la IL-2. Bajo el efecto de la IL-2, la célula T sufre una proliferación numérica
exponencial, denominadaexpansión clonal, la cual es el fundamento de la memoria
inmunitaria. La expansión clonal es seguida por una diferenciación celular,

produciendo linfocitos CD4 -encargados de la activación de macrófagos, linfocitos B y
otras células- y linfocitos CD8 -las cuales eliminan ciertas «células diana» infectadas y
también activan macrófagos en los tejidos afectados.
Receptor de la IL-2[editar]
Artículo principal: Interleucina-2
La Interleucina-2 es producida por el cuerpo durante una respuesta inmune,3 4 cuando
un antígeno (sea una molécula o un microorganismo) es reconocido por receptores
antigénicos sobre CPA (usualmente una célula dendrítica). La presentación y unión de
un pequeño segmento del antígeno, por el HMC, a una célula T por intermedio de su
receptor (TCR) estimula la secreción de IL-2 y al mismo tiempo, la expresión de
receptores de IL-2 (IL-2R). La subsecuente interacción de IL-2 con IL-2R, estimula el
crecimiento, diferenciación y supervivencia de las seleccionadas —por el tipo de
antígeno— células citotóxicas, por medio de la activación
de genes específicos.5 6 7 Esto asegura que solo la célula T con el receptor específico
al péptido antigénico sea la activada.
Una vez que IL-2 se une a los dominios externos de su receptor, IL-2R, y los dominios
internos son activados, la señal de activación continúa hasta que el complejo IL-2/IL-
2R es internalizada y degradada. Sin embargo, cada célula tomará el irrevocable
cometido de replicar su ADN y pasar por lamitosis y citocinesis solamente cuando un
número crítico de IL-2R han sido expresados y activados.8
CD28 y B7[editar]
Artículo principal: CD28
La activación de las células T ocurre a través de la interacción, tanto del receptor de la
célula T (TCR) y de la molécula CD28 con el complejo mayor de histocompatibilidad
(MHC) y la familia de receptores B7 sobre la CPA, respectivamente. Se requieren
ambas interacciones para la producción de una respuesta inmune eficaz. En la
ausencia de la co-estimulación del CD28, las señalizaciones dirigidas por el TCR
reultará en anergia. Desde este punto de activación, las vías de señalización del
linfocito T, ocupan muchas proteínas.
IL-12, IL-4[editar]
Las moléculas Interleucina-12 e Interleucina-4 juegan un papel importante en la
diferenciación de linfocitos T. IL-12 está involucrada en la diferenciación de células
CD4+ en células TH1, lo cual es importante en la activación de macrófagos (por medio

del interferón gamma) y la destrucción de patógenos. A su vez, IL-4 participa en la
diferenciación de linfocitos T en subpoblaciones células TH2.
CD40 y CD40L[editar]
La molécula del CD40 es una proteína co-estimuladora presente en CPA (un linfocito
B, por ejemplo), el cual se une a su ligando, CD40L (CD154) sobre los linfocitos T,
activando a la célula, en especial CD4+. Esta interacción CD40:CD40L, a su vez
potencia la capacidad de moléculas co-estimuladoras sobre las CPA para actuar en la
diferenciación de células T.
MonocitoEste artículo o sección necesita referencias que aparezcan en
una publicación acreditada, como revistas especializadas,
monografías, prensa diaria o páginas de Internetfidedignas. Este aviso
fue puesto el 29 de abril de 2013.
Puedes añadirlas o avisar al autor principal del artículo en su página de
discusión pegando: {{subst:Aviso referencias|Monocito}}
~~~~
Monocito
Imagen tomada con un microscopio óptico en la que se observan
2 monocitos rodeados deglóbulos rojos y alguna plaqueta en
un frotis sanguíneo. Tinción de Giemsa.

Representación 3D de un monocito.
Latín Monocytus
TH H2.00.04.1.02010
Sistema Fagocítico mononuclear
Enlaces externos
MeSH monocyte
Los monocitos son un tipo de glóbulos blancos agranulocitos. Es el leucocito de mayor tamaño,
llegando a medir 18 μm, y representa del 4 al 8% de losleucocitos en la sangre.El sistema
fagocítico mononuclear (SFM) está constituido por los monocitos circulantes y los macrófagos
tisulares. Los promonocitos de la médula ósea, al madurar salen de ella, diferenciándose en
monocitos circulantes, que al cabo de unas 8 horas emigran a distintos tejidos, donde se convierten
en macrófagos.
Como características destacables, presenta un núcleo en general arriñonado, lobulado o
cerebriforme, que se tiñe irregularmente en forma de "rejilla" o reticular de color violeta-azulado.
Usualmente el núcleo guarda una proporción de 2:1 en área con respecto al citoplasma que lo
rodea, y muy frecuentemente presenta una depresión profunda. El citoplasma es abundante y de
color gris azulado pudiendo estar acompañado de vacuolas blanquecinas.
Los monocitos se generan en la médula ósea y después viajan por la sangre, para luego emigrar a
diferentes tejidos como hígado, bazo, pulmones, ganglios linfáticos, huesos, cavidades serosas,
etc. Después de alrededor de 24 horas de permanecer en el torrente sanguíneo, los monocitos lo
abandonan y atraviesan el endotelio de los capilares o las vénulas poscapilares hacia el tejido
conectivo, donde se diferencian rápidamente a macrófagos.

Su principal función es la de fagocitar, es decir, comerse a diferentes microorganismos o restos
celulares. Para fagocitar se tienen en cuenta diversos factores como la presencia de antígenos. No
obstante, el procedimiento es sencillo, y consiste en rodear con los pseudópodos la molécula,
acción que es inhibida en los casos en que el macrófago reconoce a la célula como integrante de
un tejido propio del organismo, por medio de las proteínas del CMH (complejo mayor de
histocompatibilidad) presentes sobre las membranas celulares.
Galería[editar]