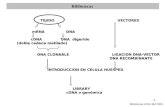
Detección de la secuencia...
Transcript of Detección de la secuencia...

1
Detección de la secuencia Alu mediante la técnica Reacción en Cadena de la Polimerasa (PCR )
N. Rodríguez

2
Objetivos • Entender la técnica: Reacción de Polimerasa
en Cadena (PCR por sus siglas en inglés) • Definir el concepto PCR y sus aplicaciones en
la investigación y los procesos biológicos • Extraer, amplificar y analizar muestras de
DNA de tejido bucal • Entender qué es Genética Poblacional y los
principios que cobijan la teoría Hardy-Weinberg

• Calcular las frecuencias alélicas y genotípicas de las muestras de cada sección
• Analizar e interpretar los resultados
Objetivos
3

4
Reacción de Polimerasa en Cadena
• ¿Qué es PCR?
• ¿Qué se necesita ?
• ¿Cómo trabaja?
• ¿Qué estamos amplificando?

5
¿Qué es PCR?
• ¡Replicación del DNA en un microtubo!
• Hacer muchas copias de una secuencia partiendo de un molde o templado
• Utiliza enzima resistente a altas temperaturas- Taq-Polymerasa

6
PCR
Melting 95 oC
Tem
pera
tura
100
0
50
Tiempo 5’ 3’
3’ 5’

7
PCR Melting
95 oC Te
mpe
ratu
ra
100
0
50
Tiempo 5’ 3’
3’ 5’
Calor

8
PCR
Melting 95 oC
Annealing Primers 58 oC
Extension 72 oC
Tem
pera
tura
100
0
50
Tiempo
3’ 5’
5’
5’
5’ 3’
Melting 95 oC

9
PCR Melting
95 oC Melting
95 oC Annealing Primers 58 oC
Extension 72 oC
Tem
pera
tura
100
0
50
Tiempo
30x
3’ 5’
5’ 3’
Calor
Calor
5’
5’
5’

10
PCR Melting
95 oC Melting
95 oC Annealing Primers 58 oC
Extension 72 oC
Tem
pera
tura
100
0
50
Tiempo
30x
3’ 5’
5’ 3’ 5’
5’
5’
5’
5’
5’

11
PCR Melting
95 oC Melting
95 oC Annealing Primers 58 oC
Extension 72 oC
Tem
pera
tura
100
0
50
Tiempo
30x
3’ 5’
5’ 3’ 5’
5’ 5’
5’
5’
5’
Calor
Calor

12
PCR Melting
95 oC Melting
95 oC Annealing Primers 58 oC
Extension 72 oC
Tem
pera
tura
100
0
50
Tiempo
30x
3’ 5’
5’ 3’ 5’
5’ 5’
5’
5’
5’
5’
5’
5’
5’

13
Fragmentos de largo definido
PCR Melting
95oC Melting
95 oC Annealing Primers 58 oC
Extension 72 oC
Tem
pera
tura
100
0
50
Tiempo
30x
3’ 5’
5’ 3’ 5’
5’ 5’
5’
5’
5’
5’
5’
5’
5’

DNA se replica
0 Número de Ciclos
Copias 1
3
8
2
4
1
2
4
16
5
32
6
64
14

Perkin Elmer GeneAmp 2400 Thermal Cycler PCR
15

16
Electroforesis de Productos de PCR
Heterocigótico Homocigótico para la presencia
de Alu
Homocigótico para la ausencia
de Alu

17
¿Qué se necesita para llevar a cabo PCR?
• Templado de interés • Iniciadores (primers) de secuencia específica que
flanqueen la secuencia del templado de interés è Forward (upstream) ç Reverse (downstream)
• Nucleótidos (dATP, dCTP, dGTP, dTTP)
• MgCl2 (cofactor enzima)
• Amortiguador • Taq Polimerasa

18
¿Cómo trabaja el PCR?
• Calor (95oC) para desnaturar las cadenas de DNA
• Enfriar (58oC) para pegar los “primers” al templado
• Calor (72oC) para activar la Taq-Polimerasa, encargada de extender los “primers”
• Repetir ciclos: 95°C - 1 minutos
58°C - 30 segundos 72°C - 30 segundos

19
Desnaturando el templado
Las altas temperatura permite la separación de las cadenas de DNA
3’
5’
5’
3’
95oC
5’
3’
3’
5’

20
Hibridización de los iniciadores (primers)
• Iniciadores hibridizan con el templado • Taq Polimerasa reconoce la doble cadena
3’
5’
5’
3’
58oC 3’
5’
5’
3’ 3’ 5’ 3’ 5’

21
Diseño de los iniciadores (primers)
• El contenido en G + C debe ser aproximadamente del 50%. La relación máxima de purinas/pirimidinas será 60%/40%.
• Evitar zonas con largas secuencias de una sóla base. • Tamaño: se recomienda de 18-30pb. • La temperatura de hibridización de los iniciadores debe
ser similar en ambos y será variable en función de la secuencia de los mismos. Generalmente oscila entre los 45 y 60°C.
Tm=4 (G +C) +2 (A+T)

22
Sales
KCl- Influye en la desnaturalización del DNA. Altas concentraciones de K+ favorece la desnaturalización de secuencias cortas de DNA. Bajas concentraciones de K+ ayudan en la desnaturalización de secuencias largas.
MgCl2- Aumenta la temperatura de hibridización del DNA.
• Altas concentraciones de Mg++ disminuyen la especificidad de la reacción.
• Bajas concentraciones de Mg++ aumentan la especificidad de la reacción.

23
Extensión
3’
5’
5’
3’
Repetir 30 veces: desnaturación, hibridización, y extensión
3’ 5’ 3’ 5’
72oC
3’
5’ 3’ 5’ 3’ 5’
5’
3’
Extensión Extensión
• Taq Polimerasa extiende los iniciadores • Se sintetiza de una cadena sencilla (produciendo un fragmento
doble por la complementaridad) en la dirección 5’ 3’

24
3’ 5’
5’ 5’
3’
5’ 3’
5’ 3’
3’ 5’ 3’ 5’
5’ 3’
3’
Ciclo 1
Ciclo 2
Ciclo 3 3’ 3’
3’ 3’ 5’
5’ 5’
5’
El producto amplificado se logra a partir del tercer ciclo

25
Secuencia de interés
• Cromosoma 8 • Intron en el gen TPA (tissue plasminogen activator) • Alu-TPA25
Exon 8 Exon 9 Exon 10 5’ 3’ Alu
Intron 8
Amplified Region

26
Alu-TPA25
• No está asociado a ningún desorden o enfermedad
• La familia de elementos Alu consiste de secuencias repetitivas (200-300 pb) que se repiten a lo largo del genoma. Estos elementos derivan su nombre por el lugar de reconocimiento que tiene la enzima Alu I.
Exon 8 Exon 9 Exon 10 5’ 3’ Alu
Intron 8
Amplified Region

27
Secuencias Alu
• Cada secuencia Alu está flanqueada por “direct repeats”
• Surgen como resultado de retrotransposiciones.
• Occurre ~300,000 veces en el genoma humano
Exon 8 Exon 9 Exon 10 5’ 3’ Alu
Intron 8
Amplified Region

28
Significado evolutivo Alu-TPA 25
• Secuencias altamente conservadas • Se insertó hace 1,000,000 años
• Dimorfismo (+/+, +/-, -/- ) • Utilizado en genética poblacional, pruebas
forenses y análisis de paternidad

29
Procedimiento Extracción del DNA genómico
v Chelex (resina de intercambio iónico) enlaza MgCl2
v 56oC libera el tejido conectivo e inactiva las DNasas
v 100oC Rompe la membrana celular y desnatura las proteínas

30
Extracción de ADN
Calor rompe la membrana
Membrana celular
Membrana nuclear
La resina Chelex enlaza los iones de Mg++
DNA genómico
Mg++
Mg++
Mg++
Mg++
Mg++
Mg++

31
• Asegurarse de no transferir la resina • Mezclar bien el DNA templado junto a los “primers”
y el “bead” • El “bead” contiene: Taq-Polimerasa, amortiguador,
dNTPs, MgCl2
Programa máquina PCR: 95ºC 5 minutos 95ºC 1 minuto 58ºC 30 segundos 72ºC 30 segundos 4ºC ∞
30 ciclos
Preparación de la reacción de PCR

32
Resultados….
• La inserción es dimórfica. Esto significa que puede estar presente en unos individuos y en otros no.
Productos: fragmento 400 bp fragmento 100 bp
Existen tres posibles genotipos: +/+, -/-, +/-
Exon 8 Exon 9 Exon 10 5’ 3’ Intron 8
Amplified Region Alu

33
Resultados Alu-PCR
+/+
-/-
+/-
400pb 100pb
Marcador 100pb

34
v Amplificar la región Alu de una muestra representativa de una población
v Calcular la frecuencia genotípica observada y la frecuencia alélica
Para estimar la frecuencia de Alu en la población

35
Equilibrio Hardy-Weinberg
p2 + 2pq + q2 = 1
+/+ = p2 +/- = 2pq -/- = q2
pp pq
qq pq
p
p
q
q
Alu y Genética Poblacional

36
Calcular la Frecuencia Genotípica Observada
Genotipo +/+ (p2) +/- (2pq) -/- (q2) Total (N)
# de individuos Frecuencia observada

37
Calcular la frecuencia alélica observada
• Frecuencia de p = número de alelos p (+) = total alelos
• Frecuencia de q = número de alelos q (-) = total alelos

38
Frecuencias genotípicas de una muestra al azar de una población
Genotipo # de cada genotipo
Frecuencia
+/+ 2422 0.2422
+/- 5528 0.5528
-/- 2050 0.2050
Total 10,000 1.0 § Calcular las frecuencias alélicas para toda la población. § ¿Serán las frecuencias alélicas y genotípicas de la clase
similares a las de la población? § ¿Qué prueba estadística debemos utilizar?

39
Equilibrio Hardy-Weinberg
• Determinar frecuencia genotípica esperada • p2, 2pq y q2 Ejemplo: • Si p = 0.45 , entonces q = 0.55 ya que p + q = 1
p2 + 2pq + q2 = 1 (0.45)2 + 2 (0.45)(0.55) + (0.55)2 = 1
0.20 + 0.50 + 0.30 = 1 • p2 = 0.20 • 2pq = 0.50 • q2 = 0.30
Representa las frecuencias genotípicas esperadas si la población está en
equilibrio genético.

40
Calcular el número de genotipos
• Calcular la frecuencia genotípica esperada para la clase presumiendo que la población está en equilibrio genético
• Calcular el # de genotipos esperados. • Qué prueba estadística podemos usar para
determinar si la población se encuentra en equilibrio?

41
( )∑
−=
EEO 2
2χPrueba χ2
Observados Esperados (O-E)2/E
+/+
+/- -/-
Observados Esperados (O-E)2/E
+/+
+/- -/-
Clase
Población