COLABORATIVO 2 ORGANICA.docx
-
Upload
alexanderortiz -
Category
Documents
-
view
252 -
download
0
Transcript of COLABORATIVO 2 ORGANICA.docx
QUIMICA INORGANICATALLER TRABAJO COLABORATIVO 2
Presentado por:
ALEXANDER ORTIZ ROJAS / 96343016 CEAD FLORENCIACRISTIAN ANDRES ARIAS / CEAD FLORENCIADIANA CHAVEZ CASIANO / 40614503 CEAD FLORENCIALUIS ALEJANDRO RODRIGUEZ / 1032463335ROBINSON OCHOA MARTINEZ / 1115792560 CEAD FLORENCIA
GRUPO No: 358005_94
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNADFLORENCIA CAQUETAAO 2015
TALLER
1. El nitrato de amonio es una sal formada por iones de nitrato y de amonio. Su frmula es NH4NO3. Se trata de un compuesto incoloro e higroscpico, altamente soluble en agua. Es explosivo y autodetonante en ausencia de agua o aplicacin de calor o fuego. Es usado como abono y ocasionalmente como explosivo. El nitrato de amonio se obtiene por neutralizacin de cido ntrico con hidrxido de amonio tras la evaporacin del agua:
NH4 OH (l) + HNO3 (l) NH4NO3 (s) + H2O (v)1. Calcular GR, HR y SR SustanciaHR (KJ/mol)SR (J/molK)GR, (KJ/mol)
HNO3 (l)-173,2155,6-79,91
H2O (v)-241,8188,7-228,6
NH4NO3 (s)-365,6151,1-184,0
NH4 OH (l)132.5113.479.31
GR=GR = GR = GR = HR=HR =HR =HR =SR=Sp-SrSR =SR =SR =
1. Asumir que HR y SR se mantienen constantes. Realizar una tabla de GR para varias temperaturas y graficar. Analizar los resultados obtenidos en relacin al incremento de la temperatura. Tabla de Datos No 1HR SR KGR
301,770,8278-19380,7
301,770,8288-20088,7
301,770,8298-20796,7
301,770,8308-21504,7
301,770,8318-22212,7
301,770,8328-22920,7
301,770,8338-23628,7
301,770,8348-24336,7
301,770,8358-25044,7
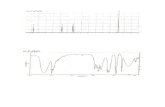
Grafica No 1
1. Ser una reaccin exotrmica y espontnea a temperatura ambiente?Para que una temperatura sea espontanea se considera que GR < 0; Para este caso a temperatura ambiente 25C (298.15K) ser una reaccin exotrmica y espontneaHR SR KGR
301,770,8298,15-20807,32
2. La inyeccin de caliza es el sistema ms avanzado para la eliminacin del SO2 del gas de chimenea. Se han realizado unos veinte programas de planta piloto. En uno de los procesos, se inyecta caliza en forma pulverizada al fogn, donde se descompone de acuerdo con la siguiente reaccin:
La cal resultante (CaO) reacciona a elevada temperatura con el SO2 y el exceso de O2 en el fogn, formndose sulfato de calcio:
El CaSO4, resultante, el CaO y el SO2, que no han reaccionado, as como las cenizas flotantes, son absorbidos en el agua de un purificador hmedo. En l, la reaccin entre el CaO y el SO2, sigue dando CaSO4. Esta ltima sustancia en esta slido y las cenizas voltiles, se recogen y eliminan. El problema principal de esta tcnica es la tendencia de las sales de calcio, como el CaSO4, a depositarse en las superficies de los purificadores y del equipo asociado. Los rasgos especialmente atractivos de este sistema incluyen los bajos costos de los absorbentes, as como el hecho que los productos finales en su mayor parte yeso puedan eliminarse con un reducido efecto adverso para el medio ambiente. a. Si una empresa que utiliza carbn lignito despus de realizar un estudio de emisiones, encuentra que no est cumpliendo con la normatividad ambiental, donde el lmite mximo permisible para xidos de azufre es de 500 mg/m3 y sus emisiones en la actualidad son de 3000 mg/m3. Deciden implementar un sistema utilizando carbonato de calcio CaCO3. Sin embargo para ello requieren de un ingeniero que estime la cantidad necesaria de este compuesto para cumplir con el objetivo de reducir la concentracin de SO2 de sus emisiones. Sumado a ello ser necesario estimar el excedente de aire que se debe suministrar al proceso de combustin, en relacin al oxgeno terico, todo ello con el propsito de conocer la capacidad a instalar del compresor.
b. Cul ser la cantidad de yeso o de sulfato de calcio que se formar en el proceso? Ser un producto con alguna rentabilidad, a nivel comercial? c. Si se alimenta al proceso de combustin una cantidad de 300 kg de CaCO3, y aproximadamente por cada kilogramo de carbn que se introduce, se producen 10 m3 de gas. Cul ser la concentracin de SO2 que estara neutralizando este compuesto?
Solucin
a) Para minimizar la emision de gas ) deben reaccionar:
Paso de mmol a mg
Excedente de airePor estequiometria la reaccion que es 2:1 se toma la mitad de las moles de y se multiplica por el peso molecular del
= 252000
=24000 mL aire Se requieren.b) Tomo los 39,06 mmol de y paso a mgCantidad de (Yeso) formado en el proceso
Nota: No presentaria mucha rentabilidad puesto que es muy poco lo que se obtine en el proceso
c) Los Kg los paso a g
Los g los paso a moles
Relacin 1:1 por la estequiometria de la reaccin
Concentracin del
3. Se debe evaluar la eficiencia en la aplicacin de dos tipos de fertilizantes como lo son el nitrato de potasio y el nitrato de amonio a un cultivo de papa, el cual tiene altos requerimientos de nitrgeno y donde el propsito ser incrementar su productividad. Sin embargo para ello, se tendr que establecer la capacidad de estos compuestos para solubilizarse en agua y as evitar los inconvenientes por la obstruccin en el sistema de riego. Entonces si la solubilidad del nitrato de potasio en agua a 25 C es de 316 g/L, cul ser la mxima concentracin de nitrato de amonio que se debe adicionar para que no haya lugar a la formacin de un precipitado?Solucin
El producto inico, es igual al producto de solubilidad
La mxima concentracin de que se debe adicionar para inhibir la formacin de precipitados es de 1.938mol/l; 154.627 g /l
4. La sntesis qumica de fertilizantes le facilit al hombre una gran independencia en la produccin de cultivos al no depender exclusivamente de las fuentes naturales. Pero el uso masivo de los fertilizantes ha trado como consecuencia la acidificacin de los suelos. El amonio tiene un gran potencial acidificante del suelo, por lo que todos los fertilizantes amoniacales podran acidificarlo, incluyendo el amoniaco (NH3). El cual inicialmente alcaliniza el medio. Determinar entonces la capacidad amortiguadora de un suelo con pH de 7.3, 300 ppm de ion nitrato y en el cual se da solamente el equilibrio nitrato de amonio nitrato, considere que caen 15 L de lluvia cida (pH=3) por cada m3 de suelo a la semana.
La capacidad amortiguadora permite cuantificar la efectividad de la accin reguladora de un buffer, para mantener el pH constante al agregar pequeas cantidades de cidos o bases fuertes. Se define como el volumen (en ml) de cido o base fuerte de una determinada concentracin que debe agregarse a una solucin buffer (amortiguadora, o tampn) para modificar el valor de su pH en una unidad.
Las soluciones amortiguadoras son soluciones que resisten a los cambios en el pH. Son importantes en los sistemas qumicos y biolgicos. La capacidad de amortiguamiento (B) est definida como la habilidad de la solucin de retener su pH cuando los iones de hidrxido (OH-) son cambiados. B vara segn un nmero de factores, incluyendo temperatura, la concentracin de la solucin, el pH de la solucin y la constante de disociacin del componente cido de la solucin amortiguadora: BKW= 10-14 Si pH= -log [H+] entonces 7,3= -log [H+], y [H+] = 10-7,3Ca=[H+]+[HA] entonces Ca = 10-7,3+ 10-7,3 = 1,002X10-7 Si entonces Sustituyendo:
B= 91901 LITROS
Tabla 2: energa libreEnerga libre de Gibbs KJ/molT K
-9168,16283,15 -9168,16
-9481,96293,15 -9481,96
-10109,56313,15 -10109,56
-10109,56323,15 -10423,36
-10423,36333,15 -10737,16
-10737,16343,15 -11050,96
-11050,96353,15 -11364,76
-11678,56363,15 -11678,56
CONCLUSION
El desarrollo de este trabajo nos permiti conocer nuestras fortalezas y debilidades; frente a los conocimientos requeridos hasta el momento en el desarrollo del curso de qumica inorgnica, destacando la importancia del trabajo colaborativo como herramienta eficaz y esencial en el aprendizaje a distancia; ya que sencillamente si uno no tiene claro un concepto otro compaero lo puede tener, entre todos se construye y se cumple con el objetivo final que es aprender.
REFERENCIAS BIBLIOGRAFICAS
1.JORGE HERNAN OBANDO CHACON. MODULO DQ UIMICA INORGANICA.UNIVERSIDAD NACIONAL ABIERTA Y ADISTANCIA 2011.
2.Obando, J. H. (2011).Qumica Inorgnica. Medelln. UNADhttp://datateca.unad.edu.co/contenidos/358005/Modulo_inorganica.pdf
3.Obando, J. H. (2011).Protocolo Qumica Inorgnica. Medelln. UNADhttp://datateca.unad.edu.co/contenidos/358005/Protocolo.pdf -Modulo Qumica General 2012.
4.Chang, R (2002). Qumica Sptima edicin Mxico: MC Graw Hillhttp://www.slideshare.net/yoel88/mcgraw-hillraymond-chang-quimica-general-7-edicion