ACTUALIZACIÓN EN NEUROBLASTOMA...en el cómputo total tras leucemias, tumores del sistema nervioso...
Transcript of ACTUALIZACIÓN EN NEUROBLASTOMA...en el cómputo total tras leucemias, tumores del sistema nervioso...

ACTUALIZACIÓN EN NEUROBLASTOMA
AVALADO POR PATROCINADO POR

Reservados todos los derechos. Ninguna parte de esta publiciación puede ser reproducida ni transmitida en ninguna forma o medio alguno, electrónico o mecánico, incluyendo las fotocopias o las grabaciones en cualquier sistema de recuperación del almacenaje de información, sin el permiso escrito de los titulares del copyright.
Edita: Canal Editorial S.L.
Título original: ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA
Autores: Dra. Mar Bermúdez Cortés et al.
® Copyright Contenidos: Los autores
ISBN: 978-84-17524-57-9

NEUROBLASTOMA enfocado a ENFERMERÍA
ÍNDICE
MÓDULO 01 INTRODUCCIÓN A LA PATOLOGÍA. MÉTODOS DIAGNÓSTICOS Y DE EVALUACIÓN DE RESPUESTA
1.1. EPIDEMIOLOGÍA Y PRESENTACIÓN CLÍNICAM. Bermúdez
1.2. DIAGNÓSTICO PATOLÓGICO/BIOLÓGICO S. Navarro
1.3. ESTADIFICACIÓNC. Sangüesa Nebot
1.4. GRUPOS PRONÓSTICOS DE RIESGO Y EVALUACIÓN DE LA RESPUESTAM. Bermúdez
MÓDULO 02 CUIDADOS DE ENFERMERÍA DURANTE EL TRATAMIENTO AL PACIENTE, FAMILIA Y ENTORNO
2.1. CUIDADOS Y ATENCIÓN DE ENFERMERÍA EN LA FASE DE INDUCCIÓN A. Miguel Pellón, I. M. Romero Pinilla y M. Cantos Muñoz
2.2. CUIDADOS Y ATENCIÓN DE ENFERMERÍA EN LA FASE DE CONSOLIDACIÓN A. Miguel Pellón, I. M. Romero Pinilla y M. Cantos Muñoz
2.3. CUIDADOS Y ATENCIÓN DE ENFERMERÍA EN LA FASE DE MANTENIMIENTO A. Miguel Pellón, I. M. Romero Pinilla y M. Cantos Muñoz
2.4. ATENCIÓN DOMICILIARIA AL NIÑO CON NEUROBLASTOMAA. Miguel Pellón, I. M. Romero Pinilla y M. Cantos Muñoz

NEUROBLASTOMA enfocado a ENFERMERÍA
MÓDULO 03 HUMANIZACIÓN DE LOS CUIDADOS EN EL PACIENTE INFANTIL CON NEUROBLASTOMA
3.1. INTRODUCCIÓN: QUÉ ES HUMANIZAR EL CUIDADO EN PEDIATRÍA ONCOLÓGICA Y CÓMO SE CONSIGUEM. Die Trill y F. Muñoz Torres
3.2. IMPACTO EMOCIONAL DEL NEUROBLASTOMA M. Die Trill y F. Muñoz Torres
3.3. EL PRIMER ENCUENTRO: CÓMO LLEVAR A CABO LA ACOGIDA M. Die Trill y F. Muñoz Torres
3.4. CÓMO HABLAR CON LOS NIÑOS Y ADOLESCENTES GRAVEMENTE ENFERMOSM. Die Trill y F. Muñoz Torres
3.5. EL TRABAJO PSICOTERAPÉUTICO CON EL NIÑO Y ADOLESCENTE CON NEUROBLASTOMAM. Die Trill y F. Muñoz Torres
3.6. CÓMO TRABAJAR CON LA FAMILIA DEL NIÑO Y ADOLESCENTE CON NEUROBLASTOMAM. Die Trill y F. Muñoz Torres
3.7. LOS PROFESIONALES SANITARIOS QUE TRABAJAN EN PEDIATRÍA ONCOLÓGICAM. Die Trill y F. Muñoz Torres

NEUROBLASTOMA enfocado a ENFERMERÍA
MÓDULO 04 CASOS CLÍNICOS
CASO 1. NIÑA DE 9 MESES CON MASA ABDOMINAL M. Bermúdez
CASO 2. NIÑA DE 5 AÑOS CON UNA HISTORIA RECIENTE DE DOLOR EN FOSA ILIACA DERECHAS. Navarro
CASO 3. NIÑA DE 4 AÑOS DE EDAD CON EPISODIOS DE RETENCIÓN DE ORINA EN LAS ÚLTIMAS SEMANASC. Sangüesa Nebot
CASO 4. NIÑO DE 3 AÑOS CON MASA ABDOMINALA. Miguel Pellón, I. M. Romero Pinilla y M. Cantos Muñoz
CASO 5. NIÑA DE 7 AÑOS CON NEUROBLASTOMA DE ALTO RIESGO CON METÁSTASIS ÓSEAS Y EN MÉDULA ÓSEAA. Miguel Pellón, I. M. Romero Pinilla y M. Cantos Muñoz
CASO 6. GESTIÓN DE LA NEGACIÓN AL FINAL DE LA VIDA Y SENTIMIEN-TOS DE IMPOTENCIA EN LOS PROFESIONALES SANITARIOSM. Die Trill y F. Muñoz Torres
CASO 7. CONFLICTOS FAMILIARES Y SU INTERFERENCIA EN LA ADMINIS-TRACIÓN DEL TRATAMIENTO MÉDICO ADECUADOM. Die Trill y F. Muñoz Torres

1INTRODUCCIÓN A LA PATOLOGÍA. MÉTODOS DIAGNÓSTICOS Y DE EVALUACIÓN DE RESPUESTA
ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA MÓDULO 01

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
QUÉ ES EL NEUROBLASTOMA. EPIDEMIOLOGÍA
El neuroblastoma (NB) es una patología poco frecuente con una incidencia que oscila entre 8 a 10 casos por millón de niños y año. Sin embargo, el NB constituye el tumor sólido extracraneal más frecuente de la infancia1. Representa el 7% de todos los cánceres pediátricos, siendo el cuarto en el cómputo total tras leucemias, tumores del sistema nervioso central y linfomas. Además es el cáncer más frecuente durante el primer año de vida y se considera responsable del 15% de la mor-talidad por cáncer en la infancia2.
La mediana de edad al diagnóstico es de 18 meses y el 90% de los casos se diagnostican antes de los 10 años. Es muy infrecuente en la adolescencia y en la edad adulta (aunque pueden darse casos).
En una minoría de casos (el 1-2% de los NB) puede existir presentación familiar3. Característi-camente se ha descrito una herencia autosómica dominante, con penetrancia incompleta. Puede aparecer en edades precoces, con enfermedad multifocal o bilateral en el 20% de los casos y, ade-más, muestran una amplia variabilidad clínica dentro de la misma familia, con aparición de NB de bajo y de alto grado en la misma línea familiar. Se han identificado distintos genes causantes de este NB hereditario, aunque en aproximadamente un 15% de los casos familiares no se conoce aún la causa:
• Mutaciones de pérdida de función en PHOX2B en línea germinal, identificadas por primera vez en neurocristopatías (como enfermedad de Hirschprung y síndrome de hipoventilación congénita donde existe mayor incidencia de NB). Se encuentran en un 10% de los NB familia-res.
• Mutaciones de ganancia de función en el gen ALK, presentes en un 75% de los casos de NB familiar4.
• Alteraciones inactivantes de KIF1Bß5,6 (gen supresor de tumores) en línea germinal, se han descrito en una familia afectada de tumores derivados de cresta neural (NB, ganglioneuroma y feocromocitomas) y no neurales (leiomiosarcomas y adenocarcinoma de pulmón).
El NB se ha descrito también asociado a otras alteraciones genéticas en línea germinal pre-disponentes al cáncer como mutaciones en la vía RAS: síndrome de Costello, síndrome de Noonan o Neurofibromatosis tipo 1, mutaciones en TP53 (síndrome de Li Fraumeni, particularmente R337H) y otras como BRCA1/2 y APC2,5,6.
Existe una mayor frecuencia de NB en pacientes afectados de síndrome de Beckwith-Wiede-man, síndrome de ROHHAD, síndrome de Weaver, síndrome de paraganglioma/feocromocitoma familiar y anemia de Fanconi2,6.
1.1. EPIDEMIOLOGÍA Y PRESENTACIÓN CLÍNICA
M. BERMÚDEZ

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
FORMA DE PRESENTACIÓN
El NB deriva de las células primitivas de la cresta neural del sistema nervioso simpático por lo que puede aparecer a lo largo de todo el eje paravertebral y en las glándulas suprarrenales. En general, la mayoría (46%) aparecen en la glándula suprarrenal, un 18% se origina en abdomen, fuera de la glándula suprarrenal, un 14% en el mediastino y en el tórax; el resto aparece en cuello, pelvis o en otras localizaciones. (Figura 1)
Figura 1. Presentación NB
El NB es una patología muy heterogénea en cuanto a comportamiento clínico y biológico.
Puede presentarse de forma locoregional ( estadios 1, 2 y 3 o L1, L2) o bien de forma metas-tásica. Aproximadamente, el 50% de los casos presentan metástasis al diagnóstico afectando por orden de frecuencia a ganglios linfáticos, medula ósea, hueso y, menos frecuentemente, a hígado y piel, e incluso a cerebro. Además existe una forma metastásica capaz de regresar y madurar de forma espontánea ( estadio 4s o Ms) en niños menores de 18 meses.
Por tanto, la presentación clínica puede también ser muy variada, desde un hallazgo inci-dental del tumor en un paciente asintomático, hasta un paciente afectado de síntomas generales y constitucionales secundarios a enfermedad metastásica. La localización del tumor primario y la presencia/ausencia de metástasis dictarán la forma de presentación inicial.
Cuando la localización es cervical o abdominal pueden presentarse como masa palpable asintomática. Una hemorragia intratumoral puede causar dolor abdominal severo y brusco por distensión de la cápsula tumoral. Cuando se presentan en localización torácica, puede existir difi-cultad respiratoria secundaria a compromiso por desplazamiento de la vía aérea o por ocupación pulmonar. Ocasionalmente, pueden producir síndrome de vena cava superior.
Los NB pueden afectar a las raíces nerviosas circundantes puesto que la mayoría se pre-sentan en zona paravertebral. Los tumores de origen cervical pueden causar síndrome de Horner (ptosis, miosis y anhidrosis) por afectación del ganglio estrellado, y los tumores pélvicos pueden producir disfunción vesical, estreñimiento o dolor radicular nervioso o debilidad de miembros in-

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
feriores por compresión de las raíces nerviosas. Así mismo, cualquier tumor paraespinal (cervical, torácico, abdominal o pélvico) puede invadir los agujeros de conjunción, extenderse al espacio epidural o intradural y causar síntomas secundarios a compresión de médula espinal. Un dolor de espalda que empeora con el decúbito debe hacernos sospechar esta complicación que se consi-dera una emergencia por el riesgo de producir paraplejia irreversible.
Las metástasis afectan generalmente a médula ósea, hueso y ganglios linfáticos. En lactan-tes, puede presentarse afectación hepática masiva con disfunción hepática, coagulopatía, com-presión de vena cava con edema en escroto y en miembros inferiores y dificultad respiratoria o disfunción renal secundaria a distensión abdominal.
Pueden presentarse metástasis en piel (también más frecuentes en lactantes) como nódu-los subcutáneos no dolorosos de color violáceo o azulado. La afectación de médula ósea (presente en el 80% de la enfermedad metastásica) puede causar anemia y trombocitopenia.
Las metástasis óseas suelen ser dolorosas, con impotencia funcional del miembro afecto. Un cuadro típico (y poco frecuente) es la afectación orbitaria, con proptosis y equimosis periocular (síndrome de Hutchinson o ojos de mapache).
Ocasionalmente (y generalmente, en formas metastásicas), pueden presentarse síntomas constitucionales como astenia, pérdida de peso, sudoración nocturna y fiebre. Algunos neuroblas-tomas pueden liberar catecolaminas con sintomatología derivada como flushing, taquicardia e hipertensión. También pueden presentar hipertensión mediada por renina secundaria a compre-sión de los vasos renales.
Muy rara vez pueden presentar síndromes paraneoplásicos como diarrea acuosa secundaria a liberación de péptido vasoactivo intestinal (VIP) o síndrome de opsoclono-mioclono.
La diarrea secundaria a la secreción de péptido vasoactivo intestinal solo se presenta en el 7-9% de los NB. Puede producir diarrea acuosa intratable con hipopotasemia, hiponatremia, acidosis y deshidratación. Cuando se presenta al diagnóstico (lo más frecuente), suele ocurrir en NB localizados de histología diferenciada y de buen pronóstico. Sin embargo, si aparece durante el tratamiento, generalmente aparece en tumores metastásicos pobremente diferenciados. No mejora con quimioterapia, pero desaparece rápidamente tras la resección tumoral7.
El síndrome de opsoclono-mioclono (OMS) se caracteriza por salvas de movimientos ocula-res erráticos en cualquier dirección (opsoclono), movimientos involuntarios musculares (mioclo-nias), ataxia e irritabilidad. Aunque puede presentarse de forma esporádica, en un 50-80% de los OMS puede detectarse un NB, pero sólo el 2-3% de los niños con NB padecerán OMS. Los síntomas neurológicos probablemente son secundarios a reactividad cruzada de anticuerpos antineurona-les antineuroblastoma con antígenos presentes en el sistema nervioso5. Característicamente se presenta en neuroblastomas localizados sin amplificación del gen N-myc, en lactantes o niños pe-queños (< 2 años) con buen pronóstico vital. Desafortunadamente puede producir graves secuelas con déficits motores, cognitivos y comportamentales a largo plazo.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
CONCLUSIONES
• El NB es una enfermedad rara (8 a 10 casos por millón de niño y año)
• El NB constituye la neoplasia sólida extracraneal más frecuente de la infancia. Representa el 7% de los cánceres infantiles y es el responsable del 15% de la mortalidad por cáncer en la infancia
• Aunque su origen es desconocido, existen formas hereditarias (asociadas a mutaciones en el gen ALK en la mayoría de los casos) y se puede asociar a síndromes predisponentes a cáncer
• El NB presenta una gran diversidad de presentaciones clínicas y comportamientos biológi-cos, dependiendo de su localización y de la presencia o no de metástasis. Se presenta de for-ma más frecuente en el abdomen (suprarrenal) y en un 50% de los casos presenta metástasis al diagnóstico
• Puede presentar involución espontánea incluso en las formas metastásicas en lactantes pe-queños
BIBLIOGRAFÍA
1. Maris J. Recent Advances in Neuroblastoma. N Engl J Med 2010; 362:2202-11.
2. Balaguer J, Castel V. Neuroblastoma. An Pediatr Contin 2008; 6(5)276-83.
3. Tolbert V, Coggins G and Maris J. Genetic susceptibility to neuroblastoma. Curr Opin Genet Dev 2017; 42:81-90.
4. Ritenour L, Randall M, Bosse K et al. Genetic susceptibility to neuroblastoma:current knowledge and future directions.
Cell and Tissue Research 2018; 372:287-307.
5. Tolbert, V.P., Matthay, K.K. Neuroblastoma: clinical and biological approach to risk stratification and treatment. Cell Tis-
sue Res [Online] 2018; 372:195. Avaliable from https://doi.org/10.1007/s00441-018-2821-2 [Accessed 5th February 2019].
6. Barr E, Applebaum M. Genetic predisposition to Neuroblastoma. Children 2018; 5:119.
7. Bourdeaut F, de Carli E, Timsit S et al. VIP Hypersecretion as primary or secondary syndrome in neuroblastoma: A retros-
pective study by the societe francaise des cancers de l´enfant (SFCE). Pediatr Blood Cancer 2009; 52:585-590.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
ASPECTOS CLÍNICOS
Desde el punto de vista clínico, hay dos factores importantes que marcan el pronóstico de la enfermedad tumoral que son la edad (más favorable en niños menores de 18 meses) y el estadiaje tumoral, bien utilizando el sistema clásico INSS (considera los estadios 1, 2, 3, 4, 4S) o bien la más reciente clasificación en grupos de riesgo de la INRG (Tabla 1), que reconoce los estadios localiza-dos L-1 y L-2 y los metastáticos M y MS1,2,3.
ASPECTOS ANATOMOPATÓLOGICOS
Dependiendo del estadiaje, la actitud terapéutica varía y así, se supone que los estadios loca-lizados, son susceptibles de tratamiento quirúrgico. Ello va a implicar que el patólogo pueda recibir diferentes tipos de muestra para su análisis morfológico, inmunohistoquímico y molecular.
En el caso de resecciones quirúrgicas completas, el espécimen a ser posible, debe recibirse en fresco, tomándose muestras para congelación utilizables en estudios de Biología Molecular así como archivando muestras en el biobanco pertinente.
El protocolo de tallado de la pieza quirúrgica incluye la descripción macroscópica del tumor con sus diámetros máximos así como el pesado de la pieza.
Es importante la posible detección de uno o varios nódulos, así como la presencia de necrosis y calcificación, especialmente en casos tratados con quimioterapia previa.
El estudio de los márgenes quirúrgicos se facilitará pintando la superficie de la pieza con tin-ta china. Posteriormente, se realizarán varias secciones de la pieza para su estudio histopatológico e inmunohistoquímico.
El procesado histológico es el convencional: fijación formólica e inclusión en parafina. En el caso de recibir las piezas en fresco, se recomienda realizar improntas citológicos para ulteriores estudios moleculares (FISH).
En aquellos casos irresecables o en estadios avanzados metastáticos, el material remitido puede ser un fragmento obtenido por procedimientos quirúrgicos, biopsias con aguja gruesa (de 3 a 5 muestras), o aspirados de médula ósea.
Para el estudio histopatológico se usa actualmente la clasificación INPC (International Neu-roblastoma Pathology Classification). Basada en una modificación del sistema Shimada, esta cla-sificación no solo posee valor diagnóstico, sino también impacto pronóstico4.
1.2. DIAGNÓSTICO PATOLÓGICO/BIOLÓGICO
S. NAVARRO

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Este sistema distingue las siguientes categorías principales:
• Neuroblastoma pobre en estroma Schwaniano, que a su vez presenta tres subtipos:
• Neuroblastoma indiferenciado: se considera así cuando la neoplasia está constitui-da por células neuroblásticas sin neuropilo aparente. Desde el punto de vista histo-lógico, forma parte de la familia de tumores de células redondas y debe realizarse diagnóstico diferencial con el tumor de Ewing/PNET, rabdomiosarcoma sólido al-veolar, tumor de Wilms con predominio blastematoso y con el linfoma linfoblástico. (Figura 1 a y b)
• Neuroblastoma pobremente diferenciado: es un tumor pobre en estroma con neu-roblasto y neuropilo evidente. La presencia de células en diferenciación debe ser inferior al 5% de la población tumoral. En este subtipo son características las pseu-dorosetas de Homer-Wright. (Figura 2)
• Neuroblastoma en diferenciación: en este caso observamos más del 5% de celulari-dad tumoral con rasgos de diferenciación. Para definir un neuroblasto en diferen-ciación, el citoplasma ha de ser amplio y eosinófilo (dos veces mayor tamaño que el núcleo). El núcleo es redondeado con nucleolo prominente. (Figura 3)
• Neuroblastoma rico en estroma. El subtipo histológico característico es el denominado Gan-glioneuroblastoma entremezclado, constituido por un estroma Schwaniano abundante en el que se entremezclan neuroblastos que a menudo presentan rasgos de diferenciación. (Figura 4)
• Neuroblastoma con estroma Schwaniano dominante. Esta categoría incluye el Ganglioneu-roma en maduración y el Ganglioneuroma maduro, consistentes en tumoración con un es-troma prominente y células ganglionares en maduración (pequeño tamaño) o bien células ganglionares maduras. (Figura 5)
• Ganglioneuroblastoma nodular. Es un tipo especial de neuroblastoma que representa a un tumor rico o dominante en estroma con presencia de uno o varios nódulos compuestos por neuroblastoma pobre en estroma. (Figura 6)
Cuando el tumor no puede ser clasificado en las categorías anteriormente mencionadas, bien por material escaso o artefactado, se puede utilizar el término Neuroblastoma NOS.
Figura 1 a. Neuroblastoma indiferenciado Figura 1 b. Neuroblastoma indiferenciado
NB84 HNK-1
Fuente: Shimada, H y cols: atlas INPC. Fuente: Shimada, H y cols: atlas INPC.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Figura 2. Neuroblastoma pobremente diferenciado Figura 3. Neuroblastoma en diferenciación
Figura 4. Ganglioneuroblastoma entremezclado Figura 5. Ganglioneuroma
Figura 6. Ganglioneuroblastoma nodular
Fuente: Shimada, H y cols: atlas INPC.
Fuente: Shimada, H y cols: atlas INPC.
Fuente: Shimada, H y cols: atlas INPC.
Fuente: Shimada, H y cols: atlas INPC.
Fuente: Shimada, H y cols: atlas INPC.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Otro de los factores imprescindibles que deben ser evaluados en esta clasificación es el de-nominado Índice Mitosis-cariorrexis (IMK), cuyo impacto histopronóstico es fundamental. (Figura 7). La evaluación consiste en el contaje de figuras mitóticas y/o de cariorrexis en un total de 5.000 células neuroblásticas. Se considera MKI alto si se evidencian más de 200 figuras/5.000 células. Si se aprecian entre 100 y 200 figuras hablaremos de MKI intermedio. (Figura 8) En el caso de ob-servar menos de 100 figuras, el MKI será considerado bajo. En la tabla 2 se muestra el algorítmo pronóstico de la clasificación INPC, teniendo en cuenta la edad del paciente, el IMK y la categoría tumoral distinguiendo así los casos con histopronóstico favorable y desfavorable. (Figura 9)
Desde el punto de vista inmunohistoquímico, el panel básico de marcadores para diagnósti-co incluye los siguientes marcadores: NB-84, Tirosin-hidroxilasa (TH), CD-56 (N-CAM), Synaptofisi-na, y Proteína S-100 (para identificar el componente Schwaniano).
En el caso de los neuroblastomas indiferenciados, el diagnóstico diferencial con los otros tumores de células redondas anteriormente mencionados, incluye la detección inmunohistoquí-mica de CD-99 (tumor de Ewing y linfoma linfoblástico), myogenina, Myo-D1 y desmina (rabdo-miosarcoma sólido alveolar) y WT-1, (Tumor de Wilms).
El modelo de informe anatomopatológico utilizado por el panel de patólogos de la SIOP para la revisión de los casos de neuroblastoma incluidos en los distintos protocolos europeos, aparte de las categorías y el MKI, incluye información de la presencia de calcificación, estado de los márgenes quirúrgicos, la invasión ganglionar así como el porcentaje de neuroblastos y células de Schwann para los futuros estudios biológicos.
Figura 7. IMK: Índice Mitosis Cariorrexis Figura 8. IMK: Índice Mitosis Cariorrexis
Tabla 2. Algoritmo pronóstico de la clasificación INPC
Bajo < 100/5.000 células ó < 2%
Intermedio 100-200/5.000 células ó < 2-4%
Alto > 200/5.000 células ó > 4%
Bajo IMK Intermedio IMK Alto IMKFuente: Shimada, H y cols: atlas INPC.
Fuente: Shimada, H y cols: atlas INPC.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
IMK Indiferenciado Pobremente diferenciado En diferenciación
Bajo D F F
Medio D F F
Alto D D D
Figura 9. INPC. Categorización, IMK, Edad
IMK Indiferenciado Pobremente diferenciado En diferenciación
Bajo D D F
Medio D D D
Alto D D D
IMK Indiferenciado Pobremente diferenciado En diferenciación
Bajo D D D
Medio D D D
Alto D D D
GNB EM (entremezclados) y GN (ganglioneuromas) - cualquier edad - F
IMK: Índice Mitosis Cariorrexis ; D: Desfavorable; F: Favorable
MARCADORES MOLECULARES DE IMPORTANCIA PRONÓSTICA/ TERAPÉUTICA
Adicionalmente a los factores clínicos (edad y estadiaje) y anatomopatológicos (INPC), se ha demostrado el impacto pronóstico y su influencia en las estrategias terapéuticas, de diversos marcadores moleculares.
La alteración genética de mayor relevancia es la amplificación del oncogén N-MYC localiza-do en el cromosoma 2 (2p24). (Figura 10) Esta alteración ocurre entre el 20 y el 25% de los neuro-blastomas primarios y está fuertemente asociada a casos desfavorables de comportamiento agre-sivo, estadios avanzados y alto riesgo de recaídas y progresión tumoral. La amplificación de N-MYC fue el primer marcador genético incluido obligatoriamente en los sistemas de estratificación de riesgo y así, los pacientes con esta alteración son considerados siempre de alto riesgo3. (Figura 11)
El estatus de N-MYC se determina mediante técnica de FISH.
Otra alteración genética importante asociada a mal pronóstico es la pérdida de 11q, presente en el 20-30% de pacientes, estando inversamente relacionada con la amplificación de N-MYC, in-dicando que estas anormalidades representan distintos subtipos genéticos de neuroblastoma en estadios avanzados5,6.
La determinación del contenido de ADN o ploidía tumoral, medida por citometría estática o citometría de flujo, también ha demostrado impacto pronóstico, especialmente en niños menores de 12-18 meses con enfermedad diseminada sin amplificación de N-MYC. Así, tumores con conte-nido diploide/tetraploide, presentan una inestabilidad genómica con múltiples reacomodamien-tos genéticos , resultando en un comportamiento desfavorable4. (Figura 12)

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Figura 10. Factores biológicos. Amplificación de N-MYC y Cromosoma 2p24
Figura 11. Factores biológicos. Amplificación de N-MYC
CITOGENÉTICA CLÁSICA
N-MYC
PCR
FISHSOUTHERNBLOT
M NB IMR32
N-MYC
LH
Amplificado dmins
Figura 12. Factores biológicos. Contenido DNA
HISTOGRAMA IOD HISTOGRAMA IOD

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Otros marcadores genéticos con impacto pronóstico incluye la deleción del brazo corto del cromosoma 1 (del 1p36), identificada en el 25-30% de los casos. Esta alteración, se correlaciona con la amplificación de NMYC y predice un alto riesgo de recaídas en pacientes con neuroblastoma localizado6.
La ganancia de 17q es otro de los marcadores asociados a alto riesgo y estadios avanzados, estando considerada como un factor independiente de pronóstico adverso7.
ALK, situado en el cromosoma 2 (2p23.2) está activado por mutaciones y/o amplificaciones en casos de neuroblastoma familiar y esporádico.
También se han descrito mutaciones del gen PHOX2B, asociadas a mal pronóstico. Actual-mente se están llevando a cabo estrategias terapéuticas utilizando antagonistas de estos genes como dianas terapéuticas8.
Utilizando técnicas pangenómicas de alto rendimiento, se ha demostrado el impacto pro-nóstico de las aberraciones segmentarias cromosómicas (del1p, 3p, 4p, 11q y ganancias de 1q, 2p, y 17), estando asociadas a alto riesgo de recaídas. (Figura 13)
Finalmente, la expresión de microARNs como el 25 miARN y los cambios epigenéticos como el fenotipo metilador, son considerados como factores de impacto pronóstico desfavorable9,10.
Figura 13. Factores biológicos. Ganancias/Pérdidas Cromosómicas
1p- / 11q- / 14q- / 17q+
Amplificación genómica
Ganancias cromosómicas
Pérdidas cromosómicas
Panel representativo 29 Nb primarios. Genes Cromosom Cancer 18:162-169, 1997.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
BIBLIOGRAFÍA
1. Cohn SL, Pearson AD, London WB, et al.: The International Neuroblastoma Risk Group (INRG) classification system: An
INRG task force report. J Clin Oncol 2009; 27:289-97.
2. Maris JM, Hogarty MD, Bagatell R, Cohn SL. Neuroblastoma. Lancet 2007; 369:2106-20.
3. Brodeur GM. Neuroblastoma: Biological insights into a clinical enigma. Nat Rev Cancer 2003; 3:203-16.
4. Shimada H, Ambros IM, Dehner LP, et al. The International neuroblastoma pathology classification (the Shimada sys-
tem). Cancer 1999; 86:364-72.
5. Navarro S, Piqueras M, Villamon E, et al. New prognostic markers in neuroblastoma. Expert Opin Med Diagn 2012; 5:555-
67.
6. Attiyeh EF, London WB, Mosse YP, et al. Chromosome 1p and11q deletions and outcome in neuroblastoma. N Engl J Med
2005; 353:2243-53.
7. Bown N, Cotterill S, Lastowska M, et al. Gain of chromosome arm 17q and adverse outcome in patients with neuroblasto-
ma: N Engl J Med 1999; 1954-61.
8. Bachetti T, Di Paolo D, Di Lascio S, et al. Phox2b-mediated regulation of alk expression:in Vitro identification of a functio-
nal relationship between two genes involved in neuroblastoma. PLoS One 2010; 5(10). Pii:e13108.
9. De Preter K, Mestdagh P, Vermeulen J, et al. Mirna expression profiling enables risk stratification in archived and fresh
neuroblastoma tumor samples. Clin Cancer Res 2011; 17:7684-92.
10. Alaminos M, Davalos V, Cheung NK, et al. Clustering of gene hypermethylation associated with clinical risk groups in
neuroblastoma. J Natl Cancer Inst 2004; 96:1208-19.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
1.3. ESTADIFICACIÓN
C. SANGÜESA NEBOT
La amplia variabilidad de comportamiento del neuroblastoma (regresión espontánea, ma-duración a ganglioneuroma o progresión tumoral) implica diferentes conductas terapéuticas: des-de la más inocua u observacional hasta las más agresivas (cirugía, quimioterapia, radioterapia, megaterapia, inmunoterapia). Con el fin de ajustar el tratamiento minimizando alguno e intensi-ficando otros, el grupo internacional de neuroblastoma (INRG) estadifica a los neuroblastomas en grupos de riesgo. El año 2004 fue un punto de inflexión; tras revisar más de 8800 pacientes vistos entre los años 1990 y 2002 y estudiando 35 variables, se fija en siete los factores asociados signifi-cativamente al pronóstico del neuroblastoma: edad, estadio, histología, grado de diferenciación, amplificación o no del oncogen n-MYC, alteración cromosómica segmentaria del 11q, ploidia. De la combinación de ellos resultan los diferentes grupos de riesgo (INRGSS)1. (Esquema 1)
Esquema 1. Grupos de Riesgo INRGSS (International Neuroblastoma Risk Group Sating Syastem)3
Estadio INRG Edad (meses) Histología Diferenciación n-MYC 11q Ploidía Grupo de riesgo
L1/L2• GN en maduración • GNB entremezclado
A Muy bajo
L1• Cualquiera, excepto GN en maduración y GNB entremezclado
NA B Muy bajo
A K Alto
L2
< 18• Cualquiera, excepto GN en maduración yGNB entremezclado
NA No D Bajo
Sí G Intermedio
≥ 18 • GNB Nodular• Neuroblastoma
• Diferenciado NA No E Bajo
Sí
H Intermedio • Pobremente diferenciado /indiferenciado
NA
A N Alto
M
< 18 NA > 2n F Bajo
< 12 NA 2n I Intermedio
12 a < 18 NA 2n J Intermedio
< 18 A O Alto
≥ 18 P Alto
Ms < 18NA
No C Muy bajo
Sí Q Alto
A R Alto

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Uno de los siete factores pronósticos es el estadio del tumor. El sistema de estadiaje INSS (International Neuroblastoma Staging System) creado el 1988 y revisado en 1993 (Tabla 1) se basada en hallazgos quirúrgicos y patológicos estando expuesto a variables como la habilidad del cirujano o a que neuroblastomas sujetos a observación quedasen fuera del mismo. En 2009 el grupo INRG propone un nuevo sistema de estadiaje antes de cualquier tratamiento separando los tumores en localizados (L1 y L2) y metastásicos (M y MS). (Tabla 2) Los localizados son clasificados en L1 o L2 de acuerdo a los factores de riesgo definidos por imagen (IDRFs) (Tabla 3) que marcan la dificultad de una cirugía completa en el momento del diagnóstico. Así, se pasa de una clasificación basada en hallazgos quirúrgicos y patológicos a una basada en los hallazgos de imagen, consiguiendo estadiar de forma más objetiva además de poder almacenar, revisar y evaluar las imágenes por un sistema centralizado de radiólogos expertos2,3.
Estadios Descripción
Estadio 1
Tumor localizado con resección macroscópica completa, con o sin enfermedad residual mi-croscópica: ganglios linfáticos ipsilaterales representativos, negativos para el tumor microscó-picamente (los nódulos adheridos al tumor primario y que fueron extirpados junto con éste, pueden ser positivos).
Estadio 2A
Tumor localizado con resección macroscópica incompleta; ganglios linfáticos ipsilaterales representativos, negativos para el tumor microscópicamente.
Estadio 2B
Tumor localizado con o sin resección macroscópica completa; ganglios linfáticos ipsilaterales no adherentes, positivos para el tumor. Los ganglios linfáticos contralaterales agrandados deben ser negativos microscópicamente.
Estadio 3
Tumor irresecable unilateral, infiltrante más allá de la línea media, con o sin afectación de los ganglios linfáticos regionales; o tumor unilateral localizado con compromiso de los ganglios linfáticos regionales contralaterales; o tumor en la línea media con extensión bilateral por infiltración (irresecable) o por afectación del ganglio linfático. La línea media está determina-da por la columna vertebral. Los tumores que se originan en un lado y cruzan la línea media deben infiltrarse sobre ésta, o hacia el aldo opuesto de la columna vertebral.
Estadio 4
Cualquier tumor primario con diseminación a los ganglios linfáticos distantes, huesos, médu-la ósea, hígado, piel u otros órganos (excepto los definidos para la etapa 4S).
Estadio 4S
Tumor primario localizado (como se define en etapa 1, 2A o 2B), con diseminación limitada a piel, hígado o médula ósea (circunscrito a lactantes menores de un año). La afectación medular debe ser mínima (o sea <10% de células nucleadas totales identificadas como malig-nas por biopsia de hueso o por aspirado de médula ósea). Una afectación más extensa de la médula ósea se consideraría como enfermedad en etapa IV. Los resultados de la gamagrafía con metayodobencilguanidina (MBIG) en caso de que se efectúe deben ser negativos para la enfermedad en la médula ósea.
Tabla 1. Clasificación INSS (International Neuroblastoma Staging System)
El estadiaje es un factor pronóstico en la combinación de grupos de riesgo del neuroblastoma.
El sistema actual de clasificación por INRG estadia los neutoblastomas en localizados (L1, L2) y metastásicos (M y Ms).

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
estadios Descripción
L1Localizados sin IDRF. Un compartimento.Tumor localizado que no afecta a estructuras vitales según definen la lista de factores de ries-go definidos por la imagen y confinado a un compartimento corporal.
L2Localizados, al menos un IDRF. Dos compartimentos contiguos.Tumor locoregional con la presencia de uno o más factores de riesgo definidos por la imagen.
MMetastásicos excepto MS.Enfermedad metastásica a distancia (excepto la definida como MS).
MS< 18 meses con metástasis: piel, hígado, ósea (<10%). Puede ser L1 o L2.Enfermedad metastásica en niños menores de 18 meses con metástasis limitadas a piel, híga-do y/o médula ósea.
Tabla 2. Estadiaje INRGSS
Extensión ipsilateral tumoral en dos compartimentos corporales
Cervicotorácico, Toracoabdominal, Abdominopélvico
Cervical
Tumor que engloba carótida y/o arteria vertebral y/o vena yugular interna
Tumor que se extiende a la base del cráneo
Tumor que comprime la tráquea
Unión cervicotorácica
Tumor que engloba las raíces del plexo braquial
Tumor que engloba los vasos subclavios y/o la arteria vertebral y/o la arteria carótida
Tumor que comprime la tráquea
Tórax
Tumor que engloba la aorta y/o sus ramas mayores
Tumor que comprime la tráquea y/o sus bronquios principales
Tumor mediastínico inferior que infiltra la unión costovertebral entre T9 y T12
Toracoabdominal
Tumor que engloba la aorta o la cava
Abdomen/Pelvis
Tumor que infiltra la porta o el ligamento hepatoduodenal
Tumor que engloba las ramas de la arteria mesentérica superior en la raíz mesentérica
Tumor que engloba el nacimiento del tronco celíaco y/o la arteria superior mesentérica
Tumor que invade uno o ambos pedículos renales
Tumor que engloba los vasos iliacos
Tumor pélvico que cruza el hueco ciático
Extensión intraespinal tumoral ( cualquier localización) si:
Invade más de un tercio del canal espinal en el plano axial y/o el espacio leptomeningeo perimedular no es visible y/o existe anormalidad de la señal de la médula espinal
Infiltración de los siguientes órganos o estructuras:
Pericardio, diafragma, riñón, hígado, bloque duodeno pancreático y mesenterio
Tabla 3. Factores de riesgo definidos por imagen en tumores neuroblásticos

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
ESTADIOS INRG
• Estadio L1. El tumor está localizado, no envuelve estructuras vitales de acuerdo a la lista IDRF. (Figura 1) Debe estar confinado en un único compartimento: cuello, tórax, abdomen o pelvis. Una extensión dentro del conducto espinal menor a 1/3 se considera L1.
• Estadio L2. Tumores localizados locoregionales con uno o más IDRFs. La afectación de dos compartimentos contiguos ipsilaterales se considera L2. (Figura 2) Si no son ipsilaterales o si son discontinuos se considera ya metastásico.
• Estadio M. Presencia de metástasis a distancia excepto las definidas para estadio MS. Los ganglios no regionales o cercanos al tumor se consideran metastásicos. La ascitis y el derra-me pleural aunque tengan células tumorales no son enfermedad metastásica a menos que estén lejos del compartimento primario del tumor (por ejemplo un neuroblastoma medias-tínico y ascitis). (Figura 3)
• Estadio MS. Niño menor de 18 meses (547 días) con metástasis confinadas a piel, hígado y/o médula ósea. La afectación de la médula ósea debe limitarse a menos del 10% de infiltración. La MIBG debe ser negativa en hueso y médula ósea. El tumor primario puede ser estadio L1 o L2. (Figura 4)
Figura 1. Neuroblastoma estadio L1
RM abdominal corte transversal (a) y coronal (b) en T2 muestra un neuroblastoma suprarrenal derecho (flechas blancas) bien delimitado sin criterios IDRF. Estadio L1.
Figura 2. Neuroblastoma estadio L2
RM corte coronal T1 con contraste muestra masa (entre flechas blancas) con extensión toracoabdominal. Extensión dos comparti-mentos contiguos. Criterio IDRF. Estadio L2.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
VALORACIÓN POR IMAGEN DE LOS IDRFS
• Términos del IDRF:
Separación: existe buen plano, generalmente grasa, entre el tumor y las estructuras vecinas. No hay IDRF.
Contacto: no hay plano entre el tumor y las estructuras vecinas. Si el contacto es con un vaso, tiene que ser menor al 50% de la circunferencia del mismo. Las venas pueden disminuir y es-tar colapsadas pero es visible la luz. No es criterio de IDRF salvo con los vasos renales donde cualquier contacto es ya criterio IDRF.
Englobados: las estructuras están rodeadas por tumor. En los vasos, más del 50% de su cir-cunferencia está en contacto con el tumor. Una vena sin luz también se considera engloba-da. Es criterio IDRF.
Compresión: hace referencia a la compresión de la tráquea por el tumor; el cambio de diá-metro de la luz de la misma es criterio IDRF.
Infiltración: extensión del tumor a órganos vecinos. Indica presencia de IDRF.
• Los IDRFs según la localización anatómica:
Neuroblastoma cervical: nace de la cadena simpática cervical detrás de la arteria carótida in-terna. Hay IDRFs si engloba los vasos cervicales, comprime la tráquea o se extiende a la base del cráneo. Raramente se hace intraespinal a este nivel.
Neuroblastoma cervicotorácico: nace del área del ganglio estrellado. Es un área de alta difi-cultad quirúrgica. IDRFs existen si el tumor engloba las raíces del plexo braquial, vasos sub-clavios y cervicales y comprime tráquea.
Neuroblastoma torácico: nace de la cadena simpática paraespinal mediastínica posterior. La invasión intraespinal es frecuente en esta localización, si es mayor a 1/3 del conducto espinal, si existe obliteración del LCR en el espacio leptomeníngeo o alteración en la médula, indica IDRFs presentes.
Figura 3. Neuroblastoma estadio M
RM abdominal corte transversal T2 en lactante de 27 días con presencia de masas en ambas supra-rrenales (flechas gruesas blancas) e importante hepatomegalia con múltiples lesiones focales por infiltración metastásica. Estadio Ms.
Figura 4. Neuroblastoma estadio Ms
RM corte coronal T2 mues-tra masa en suprarrenal izquierda (flecha gruesa negra) con múltiples lesiones hiperintensas en hígado(flechas blancas finas). Estadio M.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Neuroblastoma mediastínico inferior: infiltración de la unión costovertebral entre los niveles T9 a T12 indica IDRF por presencia de arteria espinal anterior (arteria de Adamkievicz). Tam-bién en este nivel se valora la relación del tumor con la aorta descendente, pedículos pulmo-nares, compresión de bronquios, e infiltración de pleura, pericardio y diafragma.
Neuroblastoma abdominal: tienen su origen en la glándula adrenal de la cadena simpática abdominal, órgano de Zuckerkandl. La estrecha relación del tumor con los vasos abdomina-les (tronco celíaco, mesentéricas, vasos renales, iliacos) lo hacen de alta complejidad quirúr-gica. Además las estructuras adyacentes al tumor deben valorarse: porta hepatis, diafragma, riñones, mesenterio.
Neuroblastoma pélvico: nace de los plexos simpáticos hipogástricos o de los ganglios simpá-ticos presacros. Se extienden hacia los agujeros foraminales lumbosacros y vasos iliacos. La extensión por debajo de L2 hacia los agujeros foraminales da lugar a afectación radicular en vez de compresión medular. Es importante su extensión por la escotadura ciática al conside-rarse IDRF.
ESTADIAJE
Una adecuada estadificación requiere valorar:
a. Tumor local y sus relaciones IDRF
b. Extensión
c. Estudio médula ósea
a) El tumor local y sus relaciones IDRF
El diagnóstico de tumor neuroblástico se sospecha en base a la edad y a la imagen. El uso racional de las diferentes técnicas de imagen es fundamental.
• En caso de neuroblastoma torácico o cervicotorácico, la radiografía simple de tó-rax descubre una masa de partes blandas en mediastino posterior sospechando malignidad cuando hay erosión o separación costal con o sin afectación vertebral y ensanchamiento de los agujeros de conjunción. La ecografía es fácil y accesible para confirmar la presencia y localización de una masa abdominal o pélvica, muy heterogénea y con pequeñas calcificaciones en el interior entre 30-90% de los casos. (Figura 5) El Doppler muestra la presencia de vascularización tumoral. Los neuroblas-tomas tienden a englobar y desplazar los vasos en vez de infiltrarlos4.
• Sin embargo las técnicas de imagen seccionales como Tomografía Computarizada (TC) y Resonancia Magnética (RM) son necesarias para la valoración de los IDRFs. Am-bas se usan de forma rutinaria dependiendo en general de la disponibilidad y de la preferencia del radiólogo por cada una de ellas. La RM es de elección siempre que sea posible por la ausencia de radiación, mayor caracterización tisular y resolución espacial, siendo especialmente útil en la evaluación del canal medular y de la médu-la ósea. (Figura 6) No obstante la necesidad de sedación de los niños menores a 7-8 años es su principal desventaja. Las características por imagen de los neuroblasto-mas, ganglioneuroblastomas y ganglioneuromas son similares. Ambas estudian el tumor y los ganglios locorregionales (no considerados metastásicos)4.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
• Para la valoración de respuesta tras el tratamiento QT es esencial realizar medidas sobre el tumor. Hasta hace poco la evaluación se realizaba con la reducción volumé-trica de los tumores. Considerando la poca uniformidad de los mismos se aplicaba la formula longitud x anchura x profundidad x 0,52. Esto ha sido sustituido por los criterios RECIST con una única medida. El diámetro máximo tumoral es el que marca la respuesta al tratamiento en las lesiones diana. Por tanto, es importante la visualiza-ción y medida del tumor en los tres ejes del espacio y referenciar la medida mayor5.
Particularidades de cada técnica:
• Tomografía computarizada (TC)
La posibilidad de equipos de TC multicorte con adquisiciones rápidas evitan artefactos de movimiento y reducen la necesidad de sedación además de permitir reconstrucciones multiplanares de vista sagital y coronal del tumor. No obstante requiere el uso de contras-te intravenoso yodado para demostrar la relación del neuroblastoma con los vasos y con las estructuras adyacentes.
La TC queda reservada para planificaciones prequirúrgicas, pudiendo obtenerse mode-los de impresión 3D a partir del mismo. (Figura 7) Además permite en los casos donde se requiera radioterapia posterior, tener una referencia para situar los campos de radiación adecuados.
En la TC, el neuroblastoma se presenta como masa de partes blandas demostrando calci-ficaciones hasta en el 90% de los casos, heterogénea tras el contraste por la presencia de hemorragia y necrosis4.
Figura 5. Estudio ecográfico de neuroblastoma
Ecografía abdominal corte transversal: gran masa (M) retroperitoneal heterogénea con múltiples focos ecogénicos por presencia de calcificaciones intratumorales. H: hígado.
Figura 6. RM neuroblastoma en reloj de arena
RM lumbar corte sagital (a) y transversal (b) en T1 con contraste con tumoración (cabeza de flechas blancas) que se introduce por agujero de conjunción, ocupando más de 1/3 del conducto medu-lar desplazando la médula (flecha blanca larga).
La RM es la técnica de elección en el estudio del neuroblastoma.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
• Resonancia magnética (RM)
Reconocida como la técnica de elección en la valoración local y regional de los neuro-blastomas. Como se ha dicho, su principal limitación es la necesidad de sedación de los niños. Obligada en la valoración intraespinal del tumor por la excelente visualización del conducto espinal, raíces y espacio subaracnoideo. El neuroblastoma se presenta como masa hipointensa en T1 e hiperintensa en T2 con heterogeneidad tras el contraste con ga-dolinio. Desde hace pocos años diferentes estudios intentan añadir a la parte morfológica de la RM una parte funcional a través de estudios de perfusión tumoral y de secuencias de difusión, donde la celularidad del tumor contribuye a los diferentes valores ADC (apparen-te diffusion coefficient) dentro del rango desde neuroblastoma, ganglioneuroblastoma y ganglioneuroma así como en el estudio de la respuesta terapéutica4,6.
b) Extensión
Aproximadamente el 70% de los niños con neuroblastoma presentan enfermedad metastá-sica en el momento del diagnóstico4.
La extensión de la enfermedad metastásica se evalúa mediante una exploración con meta-yodobencilguanidina (MlBG), que se aplica a todos los sitios de la enfermedad. La MIBG es un radiotrazador marcado con una molécula similar en estructura a la norepinefrina y es toma-da por transportador de la misma. La avidez por MIBG no está en relación a la diferenciación tumoral sino al sistema de transporte de la noradrenalina. Sin embargo, no está claro porqué algunos neuroblastomas presentan menos expresión a este gen transportador. Alrededor de 90% de los neuroblastomas son ávidos a la MIBG. (Figura 8) La exploración con MIBG tiene una sensibilidad y especificidad de 90 a 99 % y la avidez de MIBG se distribuye del mismo modo entre los sitios primarios y metastásicos. El hueso es el lugar más común de metástasis con lesiones corticales y medulares. Dado que no hay una avidez fisiológica ni en el hueso ni en la médula ósea por la MIBG, resulta un método seguro para detectar metástasis a dicho nivel. La MIBG como técnica funcional puede combinarse con otra modalidad de imagen morfológica como el Single-Photon Emission Computed Tomography (SPECT) y mejora la topo-grafía y localización de las lesiones7.
Figura 7. TC, estudio prequirúrgico con modelo 3D
a) Reconstrucción coronal de TC abdominal con contraste mostrando neuroblastoma (flechas blancas) que engloba vasos principales retroperitoneales. b) Modelo 3D realizado a partir del TC del neuroblastoma (flechas blancas) y su relación con estructuras vecinas.
La MIBG se debe realizar en todos los niños en estudio por neuroblastoma.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Una única lesión inequívoca MIBG positiva a distancia es suficiente para definirla como me-tástasis mientras que si existen dudas se debe completar con otra modalidad de imagen (radiología simple/RM) e incluso biopsia8,9.
La INRG recomienda el uso de métodos semicuantitativos para asegurar la extensión de la enfermedad, y la respuesta al tratamiento tras la quimioterapia. La SIOPEN (Society interna-tional oncology pediatric european neuroblastoma) ha creado un sistema de puntaje en el que se divide el cuerpo en 12 segmentos asignando grados de absorción de MIBG en cada segmento10. (Esquema 2)
Figura 8. Neuroblastoma MIBG positivo
a) RM corte transversal T2 con tumoración retroperitoneal (fechas blancas) correspondiente a neuroblastoma que en el estudio b) MIBG muestra avidez (flechas negras).
Esquema 2. Dibujo anatómico de las regio-nes determinadas para el SIOPEN score
1
7
2 2
8 8
9 10
11 12
3 4
5 6
En el 10% de los casos donde la MIBG es negativa o en caso de discrepancias con pruebas radiológicas, debe realizarse el 18-fluordesoxiglucosa (FDG) con tomografía con emisión de positrones (PET TC) donde se demuestra la avidez de estos tumores por la glucosa y la rela-ción de la misma con la diferenciación celular del tumor4,7.
El papel de la RM cuerpo entero para valorar la enfermedad metastásica y afectación de la médula ósea todavía no está definido debido a limitaciones como baja especificidad de la RM por los cambios de médula ósea con los tratamientos, por la conversión de médula roja a amarilla y la falta de scores de respuesta al tratamiento. La RM es necesaria en caso de sos-pecha de afectación metastásica del SNC y medular11.
En los casos con MIBG negativa se debe realizar 18 FDG PET.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Las metástasis pulmonares y pleurales son excepcionales en los neuroblastomas y la técnica adecuada es el TC pulmonar4.
La gammagrafía con Tecnecio 99 empleada antes de forma sistemática junto a la MIBG está en desuso por el empleo generalizado del PET/ TC.
c) Estudio médula ósea
La médula ósea se evalúa mediante aspiración bilateral de la cresta ilíaca y biopsias con ci-lindro de al menos 1cc. Se deben realizar un total de cuatro muestras (derecha e izquierda, delante y detrás) dos de aspirado y dos de biopsia.
El porcentaje de infiltración tumoral de la médula ósea se evalúa por la histología del trépano con inmunohistoquimia o por citología con inmunocitología dividido por el número de cé-lulas hematopoyéticas o mononucleares. Existe afectación de médula ósea cuando hay más del 5% de infiltración celular tumoral. Dado que la infiltración medular puede estar hetero-géneamente distribuida por el esqueleto y debido a que el impacto clínico de la misma no ha sido totalmente evaluado, la detección entre 0% a <=5% de infiltración en la médula ósea se presenta como una enfermedad mínima. La respuesta al tratamiento se evalúa de la misma manera siendo completa si no existe infilración y persistiendo como enfermedad mínima residual si permanece entre un 0%-5% de infiltración12.
Trabajos donde se compara la biopsia de médula ósea con el PET TC han demostrado que todos los casos donde había PET TC negativo también lo era la médula ósea, pero no al revés debido a la infiltración focal medular; por lo que el PET TC puede ser en el futuro un buen sustituto de la biopsia de médula ósea13.
• El estadio inicial del neuroblastoma es decisivo para su clasificación en grupos de riesgo en orden a elegir su mejor opción terapéutica.
• La ecografía es a menudo la primera modalidad de imagen para identificar un tumor neuro-blástico.
• La RM es la técnica de elección en el estudio del tumor local y evaluar los IDRFs.
• La extensión se realiza con MIBG y /o PET así como con el estudio de médula ósea.
CONCLUSIONES

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
BIBLIOGRAFÍA
1. Cohn SL, Pearson AD, London WB, Monclair T, Ambros PF, Brodeur GM, et al.INRG Task Force. The International Neuro-
blastoma Risk Group (INRG) classification system: An INRG Task Force report. J Clin Oncol. 2009; 27:289-97.
2. Monclair T, Brodeur GM, Ambros PF, Brisse HJ, Cecchetto G, Holmes K, et al. INRG Task Force. The International Neuro-
blastoma Risk Group (INRG) staging system: An INRG Task Force report. J Clin Oncol. 2009; 27:298-303.
3. Brisse H, McCarville MB, Granata, C,Krug KB, Wootton-Gorges SL, Kanegawa K. et al. Guidelines for Imaging and Staging
of Neuroblastic Tumors: Consensus Report from the International Neuroblastoma Risk Group Project. Radiology. 2011;
261:243-57.
4. Swift C, Eklund M, Kraveka J, Alazraki A. Updates in diagnosis, management and treatment of neuroblastoma. Radiogra-
phics. 2018; 38: 566-80.
5. Park J, Bagatell R, Cohn S, Pearson A, Villablanca J, Berthold F. Revisions to the international response criteria: a con-
sensus stament from the national cancer institute clinical trials planning meeting. Jounal of Clinical Oncology. 2017; 35:
2580-87.
6. Demir S, Altinkaya N, Kocer NE, Erbay A, Oguzkurt P. Variations in apparent diffusion coefficient values following chemo-
therapy in pediatric neuroblastoma. Diagn Interv Radiol. 2015;21: 184-8.
7. Pfluger T, Piccardo A. Neuroblastoma: MIBG Inaging and new tracers. Semin Nucl Med. 2017; 47: 143-157.
8. Matthay KK, Shulkin B, Ladenstein R, Michon J, Giammarile F, Lewington V, et al. Criteria for evaluation of disease extent
by (123) Imetaiodobenzylguanidine scans in neuroblastoma: A report for the International Neuroblastoma Risk Group
(INRG) Task Force. Br J Cancer. 2010;102:1319-26.
9. Mueller WP, Coppenrath E, Pfluger T. Nuclear medicine and multimodality imaging of pediatric neuroblastoma. Pediatr
Radiol. 2013; 43:418–27.
10. Ladenstein R, Lambert B, Potschger U, Castellani MR, Levington V, Bar-Sever A et al. Validation of the MIBG skeletal SIO-
PEN scoring method in two independent high risk neuroblastoma populations: SIPOEN and COG trials. Eur J Nucl Med
Mol Imaging. DOI 10.1007/s00259-017-3829-7.
11. Chavhan GB, Babyn PS. Whole-body MR imaging in children: principles,technique, current applications, and future di-
rections. RadioGraphics. 2011; 316: 1757–72.
12. Burchill S, Beiske K, Shimada H, Ambros P, Seeger R, Tygay G. et al. Recommendations for the standardization of bone
marrow disease assessment and reporting in children with neuroblastoma on behalf of the International Neuroblastoma
Response Criteria Bone Marrow Working Group. Cancer. 2017; 123: 1095-105. DOI: 10.1002/cncr.30380m.
13. Zapata C, Cuglievan B, Zapata CM, Olavarrieta R, Raskin S Desali K. et al. PET / CT versus bone marrow biopsy. Pediatr
Blodd Cancer. 2017. DOI /10.1002/pbc.26814.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
1.4. GRUPOS PRONÓSTICOS DE RIESGO Y EVALUACIÓN DE LA RESPUESTA
M. BERMÚDEZ
Como ya hemos señalado, una de las características más remarcables del NB es la impresio-nante diversidad de presentación clínica y comportamiento biológico, desde tumores metastá-sicos con resolución o maduración espontánea en lactantes, hasta enfermedad localizada o me-tastásica muy agresiva con supervivencias bajas a pesar de tratamiento enérgico. Por tanto, la estratificación en grupos de riesgo fundamentada en base a factores pronósticos es crucial para seleccionar el tratamiento apropiado1,2.
El sistema actual de clasificación internacional del NB, ya mencionado en grupos de riesgo, (INRG) fue desarrollado en 2008 por la INRG Task Force, constituida por expertos en NB de Austra-lia, China, Europa, Japón y Norte América que representaban a los mayores grupos cooperativos pediátricos. Su objetivo fue definir cohortes homogéneas de pacientes pretratamiento para facili-tar la comparación de los diferentes ensayos clínicos basados en grupos de riesgo conducidos en distintas regiones del mundo2-4.
El estadiaje del NB (INRGSS) se basa en los estudios de imagen al debut, la presencia o au-sencia de factores de riesgo quirúrgico al diagnóstico y la presencia de enfermedad metastásica al diagnóstico.
Los factores de riesgo quirúrgico (definidos por imagen) implican que la presentación tumo-ral o bien amenaza la vida del paciente o que la resección tumoral es más peligrosa y, por tanto, menos posible.
Como ya se ha comentado el estadio M indica la presencia de enfermedad diseminada al diagnóstico. El estadio MS se define como la presencia de enfermedad metastásica limitada a piel, hígado o médula ósea en un paciente con edad inferior a 18 meses (547 días), siempre que la infil-tración en médula ósea sea menor del 10% de las células nucleadas totales en citología o biopsia4.
CLASIFICACIÓN DEL NB EN GRUPOS DE RIESGO (INRG)
La clasificación del NB en INRG se estableció analizando 35 potenciales factores de riesgo y correlacionándolos con la supervivencia libre de evento a los 5 años (SLE 5a). Una vez analizados estos factores de riesgo se eligieron aquellos con mayor correlación pronóstica y que permitían el desarrollo de un algoritmo pretratamiento de grupos de riesgo. Identificaron, además del estadio, otros 7 factores pronósticos: edad, histología y grado de diferenciación, ploídia de ADN, estado de amplificación de n-MYC, y estado de cromosoma 11q, para definir 16 grupos pretratamiento, agru-pados en 4 grupos de riesgo: muy bajo (SLE 5a > 85%) bajo (SLE 5a >75 a ≤ 85%), intermedio (SLE 5a ≥ 50 a ≤ 75%) y alto riesgo (SLE 5a < 50%)2,5. (Tabla 1)

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
La edad se demostró como una variable continua para la estratificación del riesgo, puesto que el pronóstico empeora gradualmente conforme se incrementa la edad. Sin embargo, se consi-deró que era más práctico usar dos grupos de edad para estratificar a los pacientes y los resultados demostraron un punto de corte óptimo entre 15 a 19 meses. Se escogió un corte en 18 meses (547 días), aunque para los pacientes con estadio M diploides y sin amplificación de n-MYC se escogió un corte de edad más conservador en 12 meses (365 días).
EstadioINRG
Edad (meses)
Grado Histológico
Diferenciación n-MYC11q
aberraciónPloidía
Grupo de riesgo Pretratamiento
L1/L2• GN en maduración • GNB entremezclado
A Muy bajo
L1• Cualquiera, excepto • GN en maduración • GNB entremezclado
NAB Muy bajo
AmpK Alto
L2< 18
• Cualquiera, excepto • GN en maduración • GNB entremezclado
NA NoD Bajo
SíG Intermedio
≥ 18 • GNB Nodular• Neuroblastoma
• DiferenciadoNA No E Bajo
SíH Intermedio
• Pobremente diferenciado • Indiferenciado
NA
Amp N Alto
M< 18
NA HiperdiploidíaF Bajo
< 12 NA Diploide I Intermedio
12 a < 18 NA Diploide J Intermedio
< 18 Amp O Alto
≥ 18P Alto
Ms < 18 NA No C Muy bajo
Sí Q Alto
Amp R Alto
Tabla 1. Clasificación del NB en grupos de riesgo (INRG)

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Respuesta Tumor Primario Metástasis
Remisión completa No tumor No tumor; catecolaminas urinarias normales
Muy buena respuesta parcial Disminución al 90-99% No tumor, catecolaminas urinarias normales (se permiten cambios en Gammagrafia con Tc 99)
Respuesta parcial Disminución del tumor > 50% • Todos los sitios medibles disminuidos en > 50%.• Disminución de número metástasis óseas > 50%• No se permite más de una médula ósea positiva (biopsia o aspirado)
Respuesta mixta • No lesiones nuevas; > 50% de reducción de cualquier lesión medible ( primaria o metastásica) con < 50% de reducción en cualquier otra, < de 25% de aumento de cualquier lesión
No respuesta • No lesiones nuevas, < 50% de reducción pero < 25% de aumento de cualquier lesión
Enfermedad progresiva • Cualquier lesión nueva, aumento de cualquier lesión medible > 25%, presencia de médula ósea positiva si previamente negativa
Tabla 2. Criterios internacionales de respuesta para el NB
EVALUACIÓN DE RESPUESTA
Los grandes ensayos clínicos colaborativos han conseguido la mejora del pronóstico de aque-llos pacientes afectos de NB de alto riesgo y disminuir la intensidad del tratamiento para aquellos afectos de NB sin estas características. Para continuar avanzando en esta dirección se necesita un consenso sobre cómo definir la respuesta de la enfermedad a los distintos tratamientos tanto a nivel de tumor primario como de las metástasis fundamentalmente en hueso y médula ósea.
Los criterios internacionales de respuesta para el NB (INRC) se actualizaron en 19933. Estos criterios recomiendan que el volumen del tumor primario y de las metástasis (con medición en tres dimensiones de la masa de partes blandas), evaluado mediante Resonancia Magnética Nu-clear (RM) o Tomografía Axial Computerizada (TAC), sea usado para la definición de la respuesta. Para evaluar la respuesta metastásica se emplea la Gammagrafía con Metayodo Bencil Guanidina (123MIBG) o la Gammagrafía con Tc 99 en caso de negatividad de la primera así como aspirados y biopsias de ambas crestas iliacas (2 aspirados y dos biopsias de distintos sitios). (Tabla 2)
Esta evaluación presenta limitaciones fundamentalmente en la definición precisa de la res-puesta en médula ósea y hueso. Para solventar este problema, 52 investigadores internacionales de 13 países en representación de los grandes grupos cooperativos involucrados en el estudio del NB, han revisado estos criterios internacionales de respuesta mediante conferencias internaciona-les mensuales desde 2011 a 2015. Se han revisado datos clínicos de 17.938 pacientes diagnosticados de NB desde 1974 a 20156.
Para la evaluación de la respuesta se incluye la imagen anatómica de los tejidos blandos, la imagen de medicina nuclear usando 123MIBG o Tomografía con emisión de positrones con 18-fluor-desoxiglucosa (FDG-PET) y aspirados y biopsias de médula ósea para evaluar la infiltración de mé-dula ósea. En ocasiones pueden ser necesarias biopsias de tejido para verificar la presencia de NB viable. No se usarán las catecolaminas urinarias por falta de estandarización del procedimiento.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Definen lesiones objetivas como aquellas lesiones medibles (masas en tejidos blandos ≥ 10 mm de diámetro mayor o ganglios linfáticos ≥ 15 mm de eje corto), que presenten o captación en 123MIBG (o FDG-PET) o bien biopsia positiva para neuroblastoma o ganglioneuroblastoma. Las lesiones no objetivas, son aquellas que no cumpliendo criterio de lesión objetiva se consideran tumorales activas.
La afectación de tejidos blandos (primaria o metastásica) se evaluará mediante RM y/o TAC. Se sustituye la estimación del volumen tumoral mediante medición de las tres dimensiones, por criterios RECIST7,8 (medición de las lesiones mediante el diámetro más largo en tumor, o el eje más corto en ganglios linfáticos). La suma de diámetros se define como la suma de los ejes más cortos de los ganglios linfáticos con los diámetros más largos de las metástasis en tejidos blandos. Esta aproximación fue validada en un análisis retrospectivo en 229 pacientes afectos de NB de alto ries-go no encontrando diferencias significativas en pronóstico cuando se compararon la evaluación con RECIST con la medición volumétrica9.
Se evaluará la respuesta en el tumor primario y en las metastásis de partes blandas usando criterios RECIST y captación en 123MIBG (o captación FDG-PET en caso de no presentar captación en MIBG, aunque en éste último caso podría ser necesario confirmación histológica).
Para la evaluación de la afectación metastásica ósea se empleará captación en 123MIBG (o captación FDG-PET en caso de negatividad).
La evaluación de médula ósea se realizará mediante aspirados y biopsia de médula ósea bi-laterales (un total de cuatro muestras), demostrando afectación mediante morfología conjugada con inmunocitología (si disponible) o bien inmunohistoquímica. Debe evaluarse el porcentaje de infiltración de médula ósea o el contaje de número de células tumorales por células hematopo-yéticas o mononuceladas en aspirado para obtener porcentaje. (Se usará el mayor porcentaje de infiltración). La evaluaciónes de la respuesta tanto local como metastásica y la global se resumen en las Tablas 3 a, b, c y d.
Respuesta Imagen anatómica + 123MIBG (FDG-PET)
Remisión completa < de 10 mm tumor residual en sitio primario y resolución completa de captación de 123MIBG (o FDG-PET) en localización primaria
Respuesta parcial ≥ 30% de disminución en el diámetro mayor del sitio primario y estabilidad, mejoría o resolución de captación 123MIBG (o FDG-PET)
Enfermedad progresiva > 20% de aumento en el diámetro mayor (tomando como referencia la sumación de diámetros más pequeña en el estudio, incluyendo la inicial si ésta es la menor) y aumento absoluto mínimo de 5 mm en la mayor dimensión
Enfermedad estable Ni suficiente disminución para definición de respuesta parcial ni suficiente aumento para enfermedad progresiva en tumor primario
Tabla 3 a. Respuesta en tumor primario de tejidos blandos

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Tabla 3 b. Respuesta en tumor en metástasis de tejidos blandos y óseas
Respuesta Imagen anatómica + 123MIBG (FDG-PET)
Remisión completa Resolución de todos los sitios de enfermedad definidas como: • Lesiones no primarias menores de 10 mm (objetivas y no objetivas)• Ganglios linfáticos identificados como lesiones objetivas con disminu-ción de eje corto < de 10 mm • Resolución completa de captación de 123MIBG (o FDG-PET) en localizaciónes no primarias
Respuesta parcial ≥ 30% de disminución en la suma de los diámetros de las lesiones no primarias objetivas en comparación con las basales y todo lo siguiente: • Las lesiones no objetivas deben ser estables o menores de tamaño • No aparición de nueva lesiones ≥ 50% de reducción de escore óseo absoluto en 123MIBG (score óseo relativo MIBG ≥ 0.1 a ≤ 0.5 ) o ≥ 50% de reducción del número de lesiones óseas captantes en FDG-PET
Enfermedad progresiva > 20% de aumento en el diámetro mayor (tomando como referencia la sumación de diámetros más pequeña en el estudio, incluyendo la inicial si ésta es la menor) y aumento absoluto mínimo de 5 mm en la mayor dimensión
Enfermedad estable Ni suficiente disminución para definición de respuesta parcial ni suficien-te aumento para enfermedad progresiva en tumor primario
Respuesta Citología/Histología
Remisión completa No infiltración tumoral independientemente de la infiltración basal
Enfermedad progresiva Cualquiera de lo siguiente: • > 5% de infiltración tumoral en reevaluación sí previamente no infiltrada la médula ósea o • Infiltración tumoral que > el doble y > 20% de infiltración tumoral en reevaluación
Enfermedad mínima Cualquiera de lo siguiente: • Infiltración basal en médula ósea ≤ 5 % que permanece 0- ≤ 5% en reevaluación o • No infiltración basal de médula ósea e infiltración en médula ósea ≤ 5% en reevaluación o• Infiltración basal de médula ósea > 50% con infiltración de 0- ≤ 5% en reevaluación
Enfermedad estable Permanencia de infiltración de médula ósea > 5% en reevaluación pero que no cumple criterios de enfermedad progresiva o mínima
Tabla 3 c. Respuesta en metástasis en médula ósea

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Respuesta Citología/histología
Remisión completa Remisión completa en todos las evaluaciones
Respuesta parcial Respuesta parcial en al menos una evaluación y todos los demás compo-nentes son al menos remisión completa o enfermedad mínima (médula ósea), respuesta parcial (tejidos blandos o hueso) o no afectado al inicio, no enfermedad progresiva en ninguna evaluación
Respuesta menor Respuesta completa o parcial en al menos una evaluación y al menos otra evaluación con enfermedad estable; ninguna evaluación con enfermedad progresiva
Enfermedad estable Enfermedad estable en una evaluación, con no respuesta mejor que enfer-medad estable o no afecta al inicio en otras evaluaciones, ninguna evalua-ción con enfermedad progresiva
Enfermedad progresiva Cualquier evaluación con enfermedad progresiva
Tabla 3 d. Respuesta global
CONCLUSIONES
• El estadiaje se basa en la presencia o no de factores de riesgo quirúrgico definidos por el es-tudio de imagen inicial y la presencia o no de metástasis
• La clasificación en grupos de riesgo se basa en el estadiaje y en 7 factores pronósticos: edad, histología y grado de diferenciación, ploidía de ADN, estado de amplificación de n-MYC, y estado de cromosoma 11q
• Permite diferenciar grupos de riesgo en función de supervivencia libre de evento a los 5 años (Muy bajo riesgo, bajo riesgo, riesgo intermedio y alto riesgo)
• La evaluación de la respuesta, tanto a nivel del tumor primario como en metástasis (tejidos blandos, óseas y en médula ósea), a nivel internacional va a ser sometida a un profundo cam-bio de los estándares, implementándose en los próximos años

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
BIBLIOGRAFÍA
1. Morgenstern D, Bagatel R et al. The challenge of defining “ultra-high-risk” neuroblastoma. Pediatr Blood Cancer [Online]
2018; e27556. Avaliable from: https://doi.org/10.1002/pbc.27363 [Accessed 5th February 2019].
2. Cohn S, Pearson A, London W et al. The International Neuroblastoma Risk Group (INRG) Classification System: An INRG
Task Force Report. J Clin Oncol 2008; 27(2):289-297.
3. Brodeur GM, Pritchard J, Berthold F et al. Revisions of the international criteria for neuroblastoma diagnosis, staging and
response to treatment. J Clin Oncol 1993; 11:1466-1477.
4. Monclair T, Brodeur M Ambros P et al. The International Neuroblastoma Risk Group (INRG) Staging System: An INRG Task
Force Report. J Clin Oncol 2008; 27(2):298-303.
5. Tolbert, V.P., Matthay, K.K. Cell Tissue Res [Online] 2018: 372: 195. Avaliable from https://doi.org/10.1007/s00441-018-2821-2
[Accessed 5th February 2019].
6. OPark J, Bagatell R, Cohn S et al. Revisions to the International Neuroblastoma Response Criteria: A Consensus State-
ment From the National Cancer Institute Clinical Trials Planning Meeting. J Clin Oncol 2017; 35:2580-2587.
7. Therasse Pm Arbuck SGm Eisenhauer EA et al. New guidelines to evaluate the response to treatment in solid tumors:
European Organization for Research and Tratment of Cancer, National Cancer Institute of the United States, National
Cancer Institute of Canada. J Natl Cancer Inst 2000; 92:205-216.
8. Eisenhauer EAm Therasse P, Bogaerts J et al. New response evaluation criteria in solid tumours: Revised RECISTguideli-
ne (version 1.1) Eur J Cancer 2009; 45:228-247.
9. Bagatell R, McHugh K, Naranjo A et al. Assesment of primary site response in children with high risk neuroblastoma: An
international multicenter study. J Clin Oncol 2016; 34:740-746.

2CUIDADOS DE ENFERMERÍA DURANTE EL TRATAMIENTO AL PACIENTE, FAMILIA Y ENTORNO
ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA MÓDULO 02

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
ADMINISTRACIÓN DE QUIMIOTERAPIA: SEGURIDAD EN EL MANEJO DE FÁRMACOS CITOSTÁTICOS
Un citostático, se puede definir como aquella sustancia capaz de inhibir o impedir la evolu-ción de la neoplasia, restringiendo la maduración y proliferación de células malignas, actuando so-bre fases específicas del ciclo celular, y que por ello son activas frente a células que se encuentran en proceso de división.
Estos fármacos, pueden generar diferentes acciones tóxicas al administrarse al paciente y también al personal que lo manipula.
Por ello, los citostáticos deben llegar preparados desde el servicio de farmacia del hospital su manipulación requiere la utilización de un equipo de protección individual (EPI). Un EPI se define como cualquier equipo destinado a ser llevado o sujetado por el trabajador para que le proteja de uno o varios riesgos que puedan amenazar su seguridad o su salud, así como cualquier comple-mento o accesorio destinado a tal fin.
En la fase de inducción del tratamiento del paciente con neuroblastoma de alto riesgo, la quimioterapia se administra por vía intravenosa, por ello debemos seguir los siguientes pasos para una correcta administración:
1. Comprobar la coincidencia de la prescripción médica con la etiqueta del fármaco dispensado por el Servicio de Farmacia:
• Datos identificativos del paciente, como pueden ser nº de historia clínica, nombre y apellidos, ubicación del paciente...
• Fármaco a administrar
• Dosis del fármaco
• Tipo de suero en el que va preparado
• Volumen total
• Tiempo de administración
• Velocidad de administración
• Fecha de preparación
• Estabilidad o caducidad de la solución
2.1. CUIDADOS Y ATENCIÓN DE ENFERME-RÍA EN LA FASE DE INDUCCIÓN
A. MIGUEL PELLÓN, L. MARGARITA ROMERO PINILLA Y M. CANTOS MUÑOZ

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
2. Colocar el equipo de protección individual
• Bata de un solo uso, con abertura trasera, puños elásticos e impermeable
• Doble guante (interno por debajo del puño y externo de nitrilo por encima)
• Mascarilla FFP2 o FFP3 (las quirúrgicas no protegen frente a los aerosoles de los ci-tostáticos)
• Gafas con protección lateral
3. Preparar el equipo de administración
• Purgar los sistemas de suero con suero fisiológico o glucosado, en función de la pre-paración del fármaco
• Utilizar conectores de seguridad para evitar la punción directa entre el sistema y la bolsa de preparado
• Desinfectar de forma estéril las conexiones entre la bolsa y el sistema
4. Comprobar vía de administración
• Verificar que la vía es permeable y refluye
5. Administrar el citostático:
• Programar la bomba de infusión según los valores indicados en la etiqueta
• Entre un fármaco y otro lavar con 35-40 cc del suero principal a la misma velocidad en la que se administró el último. Siempre finalizar lavando todo el sistema de infu-sión con el suero principal
6. Eliminación de residuos:
• Colocación del equipo de protección individual completo
• Introducir todo el material y los guantes de nitrilo en el contenedor rígido para su trasporte
MANEJO Y CUIDADOS DEL PORTH-A-CATH
El Port-a-cath, (PAC) es la vía central más utilizada en pediatría para la administración de citostáticos. Además, facilita el acceso venoso para las numerosas extracciones a las que se ve so-metido el paciente con neuroblastoma.
Consta de un dispositivo situado a nivel subcutáneo y su implantación se hace mediante pro-cedimiento quirúrgico. Está formado por un borde de acero o poliéster plástico y una membrana interior de silicona. Esta parte va conectada a un catéter flexible, con una o dos vías, llegando el extremo distal a nivel de la unión de la vena cava superior con la aurícula derecha.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
Su punción, está considerada un procedimiento estéril, por lo que necesitaremos:
• Paño y guantes estériles
• Gasas estériles
• Mascarilla quirúrgica
• Antiséptico
• Agujas específicas para reservorios (actualmente modelo “Gripper”)
• Jeringuillas de mínimo 10 cc para evitar una presión elevada durante la manipulación
• Suero fisiológico
• Apósitos
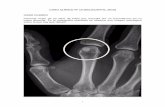
Figura 1. Inserción de Gripper
Una vez preparado el campo estéril, nos dirigimos a su punción. (Figura 1) Para ello, primero limpiaremos la zona con agua y jabón y desinfectaremos preferiblemente con clorhexidina, dejan-do que se seque. Seguidamente, palparemos hasta localizar e inmovilizaremos la membrana cen-tral con la mano no dominante y con la otra insertaremos el "gripper" (purgado previamente) de forma perpendicular hasta dar con el borde metálico. Una vez pinchado, retiramos el pinzamiento del sistema de la aguja y aspiramos con una jeringa de 10 cc comprobando el reflujo sanguíneo. Seguidamente, cambiamos la jeringa por una jeringa con suero y lavamos el sistema.
Finalizado este proceso, nos dirigimos a fijar correctamente con un apósito transparente que nos permita observar cualquier tipo de incidencia.
Se ha comprobado que el lavado del catéter con heparina tras su utilización, ayuda favora-blemente a la permeabilidad para próximos usos. La forma más extendida es la heparina sódica al 1% en viales de 1.000 UI/ml, preparando una dilución de 1 cc de heparina y 9 cc de suero fisiológico. El preparado se administra lentamente con una jeringa de 10 cc hasta completar el recorrido del

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
"gripper" (entre 3 y 4 cc) y se clampa al finalizar generando presión positiva en el sistema. Cabe se-ñalar que también existen preparados de heparina sódica en concentración de 20 UI/ml que pue-den utilizarse de igual forma para realizar el sellado sin necesidad de diluirse previamente siendo la cantidad indicada hasta 5 ml.
Si el Port a cath no se usa durante un largo plazo de tiempo, se debe mantener mediante sellados con heparina. Existen diferentes protocolos dependiendo del centro o la unidad. Una de las recomendaciones utilizadas sería renovar el sellado aproximadamente una vez al mes, de esta forma también se comprueba su funcionamiento.
CONTROL DE REACCIONES Y/O EFECTOS ADVERSOS EN EL TRATAMIENTO CON QUIMIOTERAPIA
La fase de inducción dura 3-4 meses. Se inicia con poliquimioterapia para eliminar las me-tástasis. Al finalizar la quimioterapia, si la respuesta de las metástasis ha sido adecuada (desapari-ción completa o disminución del 50% con persistencia de un máximo de tres lesiones) se procede a la extirpación quirúrgica completa del tumor primario. Los pacientes que no han presentado respuesta metastásica adecuada tras la inducción, pasan a recibir tratamiento de segunda línea (habitualmente, ensayos clínicos fase II) como casos refractarios.
La vía de tratamiento es intravenosa y la administración más usada en Europa es la combi-nación de cisplatino, carboplatino, ciclofosfamida, vincristina y etopósido. Este tratamiento recibe el nombre de COJEC. (Figura 2)
Figura 2. Esquema de quimioterapia de inducción en neuroblastoma de riesgo alto
Esquema COJEC rápido Ocho ciclosSecuencia: A B C B A B C BDuración teórica: 70 días
Esquema N7 modificado Cinco ciclosSecuencia: CAV CAV P/E CAV P/EDuración teórica: 87 días
Ciclo AVincristina 1,5 mg/m2
Carboplatino 750 mg/m2
Etopósido 350 mg/m2 en dos dosis
Ciclo CAVVincristina 0,066 mg/kg en 72 horasAdriamicina 75 mg/m2 en 72 horasCiclofosfomaida 140 mg/kg en dos dosis
Ciclo BVincristina 1,5 mg/m2
Cisplatino 80 mg/m2
Ciclo P/ECisplatino 200 mg/m2 en cuatro dosisEtopósido 600 mg/m2 en tres dosis
Ciclo CVincristina 1,5 mg/m2
Ciclofosfomaida 1.050 mg/m2 en dos dosisEtopósido 175 mg/m2
Dosis acumuladas
FármacoVincristinaCiclofosfomaidaEtopósidoCisplatinoCarboplatinoAdriamicina
COJEC12 mg/m2
4.200 mg/m2
1.400 mg/m2
320 mg/m2
1.500 mg/m2
-
N70,2 mg/kg (equivalente a 6 mg/ m2)420 mg/kg (equivalente a 12.600 mg/ m2)1.200 mg/m2
400 mg/m2
-225 mg/m2

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
La administración de dichos fármacos puede conllevar la aparición de efectos adversos de forma común. Dentro de estos, podemos encontrar reacciones alérgicas que aparecen de forma inmediata durante o justo al finalizar la infusión del fármaco. Reacciones alérgicas de alarma se-rían eritema, picazón; dificultad respiratoria; hinchazón de cara o labios; sensación de mareo; dolor de abdomen, la espalda o el pecho o malestar. En ese caso, se debería detener la infusión inmedia-tamente y se avisaría al médico responsable en ese momento para tomar las medidas necesarias.
Por otro lado, encontraríamos los efectos secundarios que aparecen fuera de la administra-ción del tratamiento pero que están relacionados con su toxicidad e interacción.
Farmacología Toxicidad Efectos adversos
Cisplatino
Metabolización espontánea, pero eli-minación renal proporcional al filtrado glomerular. Importante tener en cuen-ta la función renal pre-trasplante. Vida
media de 24 horas
Toxicidad renal, ototoxici-dad y neuropatía periférica
Alto potencial emético.
Muy nefrotóxico.Alopecia poco
frecuente
Carboplatino
Se elimina hasta el 80% en las primeras 24 horas vía renal Vida media de hasta 20 horas, pero en general tras 24 horas se ha excretado todo el fármaco libre
Toxicidad hepática, neuró-pata y ototoxicidad
Alto potencial emético.
Muy nefrotóxico.Alopecia poco
frecuente
Etopósido
Se metaboliza por el hígado y se elimina hasta 1/3 en la orina sin sufrir metabolización y su dosis debe de ser modificada en caso de insuficiencia
renal. Vida media de 4-8 horas
Toxicidad en mucositis
Neuropatía periférica.Alopecia
Mielosupresión.Afectación mús-culo-esquelética
CiclofosfamidaSe elimina por la orina.
Vida media de 3-9 horas
Toxicidad cardiaca, sobre-todo en dosis >150 mg/kg
entre 24 horas y 2 semanas de su administración.
Cistitis hemorrágica y toxici-dad pulmonar, renal y SOS.
La ciclofosfamida reduce los niveles de ciclosporina y de tacrolimus hasta dos sema-nas, por lo que necesita un seguimiento muy cercano.Puede requerir modifica-
ción de dosis en insuficien-cia renal/hepática
Atraviesa la ba-rrera hematoen-cefálica: depre-sión medular.
Nauseas, vómitos.
Pueden aparecer segundas neoplasias
Adriamicina
La vida media terminal es de 30 a 50 horas. El fármaco inalterado y sus me-tabolitos se excretan principalmente en la bilis (50%) y las heces, con una
pequeña cantidad (<10%) se excreta en la orina
Toxicidad cardíaca
Fiebre, reaccio-nes cutáneas,
neumonítis aguda.
Mielosupresión
Vincristina
El 66% de la dosis es eliminada por vía biliar en las 72 horas siguientes a su
administración. La semi-vida final de eliminación oscila entre 23 y 85 horas. Esta larga semi-vida de eliminación es la responsable de que las dosis repeti-das de vincristina induzcan toxicidad
por acumulación del fármaco
Toxicidad neurológica
Neuropatía periféricaAlopecia
MielosupresiónAfectación mús-culo-esquelética

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
Es importante un buen control de la sintomatología para evitar complicaciones asociadas. Para ello, es necesario un buen seguimiento del paciente por el personal médico y de enfermería. Un ejemplo sería el control de diuresis del paciente. Con éste, no solo valoramos el balance hídrico, sino que es importante realizar tiras reactivas en orina para ver de una forma rápida e instantánea la posible presencia de alteraciones generadas por el tratamiento, entre ellas, la hematuria.
EDUCACIÓN SANITARIA EN LOS HÁBITOS Y EL ENTORNO DEL PACIENTE CON NEUROBLASTOMA DE ALTO RIESGO
El objetivo de la educación sanitaria es favorecer el bienestar y el afrontamiento de los pa-dres y niños con neuroblastoma con el fin de mejorar su calidad de vida.
Es importante hacer partícipes tanto al niño como a sus cuidadores de la situación y de todo el proceso.
Una buena educación en enfermería favorece la adherencia al tratamiento y el control de la sintomatología asociada. Son muchas las dudas que un familiar o el mismo niño se plantean ante la situación.
Explicar las medidas con las que se cuentan para contrarrestar los efectos derivados de los ciclos de quimioterapia ayuda a reducir la inquietud en esta etapa.
Al iniciar la fase de inducción el personal médico informa a los padres del esquema de tra-tamiento a seguir, marcando unos plazos o fechas. Es importante hacer comprender que ese ca-lendario es orientativo pues es habitual que los ciclos puedan retrasarse por no cumplir criterios para poder comenzar la administración de la quimioterapia, situación que eleva la preocupación de los padres. Deben conocer en qué consiste la neutropenia y familiarizarles con medicaciones que van a ser habituales como el uso de los Factores Estimulantes de Colonias de Granulocitos (G-CSF) o filgrastim, cuyo objetivo entre ciclos es la recuperación de dicha neutropenia. Se puede administrar tanto vía intravenosa como subcutánea, siendo esta última de elección a la hora de la administración en casa por parte de los cuidadores del niño. El momento propicio para aprender es durante la estancia hospitalaria. Es ahí cuando enfermería debe formar a los padres, siendo beneficioso tanto para ellos como para el niño, pues comenzar el manejo junto con el personal de enfermería les hace ganar confianza y seguridad al tener un referente para poder solventar sus miedos y dudas.
Uno de los efectos secundarios de la quimioterapia más extendidamente conocidos son los vómitos. Fármacos como el cisplatino, carboplatino o la ciclofosfamida son altamente eméticos. Para su control se prescriben antieméticos como los antagonistas de los receptores de serotonina 5-HT3, o corticoides como la dexametasona.
Otro de los aspectos durante la inducción que puede ser motivo de intranquilidad para los padres es la falta de apetito de los niños o en ocasiones la disminución de peso, por procesos como por ejemplo la mucositis, ocasionada por la administración de quimioterapia y la neutropenia, que se abordará más ampliamente al tratar el trasplante de progenitores hematopoyéticos. En casos graves el niño podría precisar de soporte nutricional con nutrición parenteral o nutrición enteral. Un seguimiento por parte del servicio de nutrición y el aporte de suplementos orales tipo batidos hipercalóricos son de gran utilidad.
Señalar también la importancia para el personal de enfermería en el manejo de la adminis-tración de hemoderivados pues debido a la pancitopenia que experimentarán los pacientes va a ser frecuente la necesidad de transfusiones, sobre todo de hematíes y plaquetas. La cantidad a

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
administrar será indicada por el oncólogo y el tiempo de infusión será de 20 a 40 minutos en el caso de las plaquetas y pudiendo variar en el caso de los hematíes dependiendo del paciente o situación, siendo habitual en el paciente pediátrico la transfusión en mínimo 2 horas. Por ello uno de los primeros pasos a seguir es revisar la prescripción médica para confirmar cantidad, tiempo de infusión o necesidad de premedicación. Comprobar el grupo sanguíneo del niño y su compati-bilidad con la donación, (Tabla 1) y la identificación antes de comenzar la transfusión del paciente con nombre, apellidos y fecha de nacimiento. Las principales reacciones agudas transfusionales que pueden surgir son la reacción hemolítica agua por incompatibilidad del grupo AB0, cursando con taquicardia, disnea, dolor torácico o lumbar, fiebre y escalofríos, hematuria, sangrado, incluso shock. Otras de las complicaciones serían la fiebre no hemolítica, acompañada también por tirito-nas, reacción alérgica manifestada por habones, eritema o prurito, reacción anafiláctica, o sobre-carga circulatoria por administración de gran cantidad de volumen o infusión demasiado rápida.
Tabla 1. Compatibilidades grupos sanguíneos
GRUPO SANGUÍNEO PUEDE RECIBIR DONACIÓN DE...
A+ A+, A-, 0+, 0-
A- A-, 0-
B+ B+, B-, 0+, 0-
B- B-, 0-
AB+ DE TODOS LOS GRUPOS
AB- A-, B-, AB-, 0-
0+ 0+, 0-
0- 0-
Los cuidadores de un paciente con neuroblastoma experimentan mucho miedo, por lo que una buena educación sanitaria reduce la ansiedad y genera seguridad ante la situación.
CUIDADOS ENFERMEROS EN LA FASE QUIRÚRGICA
El papel de la cirugía en el neuroblastoma tiene dos objetivos, diagnóstico y terapéutico. Con respecto a este último, el objetivo principal es la resección completa del tumor primario, siendo relativamente sencilla en los casos localizados, pero en ocasiones es difícil realizarla sin dejar re-siduo tumoral ya que el tumor puede rodear los grandes vasos o estructuras próximas. A veces es necesaria la resección parcial del tumor, o incluso la disección a través del tumor, para lograr visualizar las estructuras nobles que engloba, y así no dañarlas, consiguiendo resecciones lo más completas posibles.
Muchos de los pacientes con neuroblastoma precisarán la eliminación de un tumor sólido mediante la cirugía. Esta se practica después de haber realizado una quimioterapia previa, con el objeto de que el tumor se reduzca para facilitar algo más su extirpación y por otra parte limitar al máximo una posible diseminación yatrógena durante la operación. En algunos casos, sin embar-go, la cirugía puede estar más indicada en el momento del diagnóstico o en fases más avanzadas de tratamiento.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
Los cuidados de enfermería, serían muy parecidos a los de cualquier paciente pediátrico en situación de una intervención quirúrgica.
El día de la intervención deberemos de tener en cuenta:
• Higiene completa
• Comprobar que tiene una analítica preoperatoria y pruebas cruzadas con sangre en reserva
• El paciente está en ayunas
• Comprobaremos que su vía venosa (periférica o central) está en buen estado
• Consentimiento informado firmado por los tutores legales
• Rasurado de la zona quirúrgica: si la zona a intervenir tiene poco vello, no lo rasuraremos
• Medición de constantes vitales
• Retirada de joyas, prótesis dentales, etc.
• Cuando el celador acuda a buscar al paciente para llevarlo al quirófano, éste debe ir acom-pañado de un familiar y con su historia clínica completa
Cuando el paciente vuelve a la unidad de hospitalización, lo primero que haremos es hacerle una valoración en la que:
• Vigilaremos el nivel de consciencia
• Tomaremos las constante vitales
• Observaremos que el apósito o vendaje venga limpio de quirófano
• Comprobaremos el buen funcionamiento de vía venosa
• Comprobaremos la analgesia pautada y la comenzaremos a administrar cuando fuera necesario
• Miraremos la hora para iniciar la tolerancia de la dieta. Comenzaremos administrando sólo líquidos y si los tolerase, en la siguiente comida ya podremos administrar alimentos blandos. Si no viniese indicada, esperaremos unas 4 horas para iniciarla

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
2.2. CUIDADOS Y ATENCIÓN DE ENFERMERÍA EN LA FASE DE CONSOLIDACIÓN
ATENCIÓN DE ENFERMERÍA EN LAS DIFERENTES FASES DEL TRASPLANTE AUTÓLOGO DE PROGENITORES HEMATOPOYÉTICOS
Lo primero antes de entrar en materia en este apartado es definir a qué llamamos trasplan-te autólogo. Este procedimiento consiste en la infusión de células progenitoras hematopoyéticas (células madre hematopoyéticas) que previamente han sido extraídas del propio paciente. La fi-nalidad es reemplazar sus propias células madre dañadas por enfermedad, radiación o dosis altas de quimioterapia. Al requerir dosis elevadas de éstas, la médula ósea del paciente se ve afectada y necesita del trasplante para restaurar su capacidad hematopoyética. En los casos de neuroblasto-ma, y en concreto en los neuroblastomas de alto riesgo, el tratamiento de quimioterapia en la fase de inducción no es suficiente, pudiendo persistir células cancerígenas y contribuyendo a un peor pronóstico.
A modo resumen, las fases son:
A. MIGUEL PELLÓN, L. M. ROMERO PINILLA Y M. CANTOS MUÑOZ
1. Obtención de progenitores hematopoyéticos para el trasplante autólogo
En la actualidad la mayoría de trasplantes autólogos se realizan a partir de células progenito-ras hematopoyéticas de sangre periférica. Se obtienen cuando el paciente se encuentra en remisión, es decir, ha respondido al tratamiento.
Para su extracción se usa la aféresis o leucocitaféresis. Días previos a este procedimiento se administran fármacos para estimular la salida de células madre al torrente sanguíneo, cono-cidos como agentes movilizadores, como G-CSF (Factor Estimulante de Colonias de Granu-
La llamada “recolecta” o extracción de progenitores hematopoyéticos del paciente. Almacenaje y crio-
conservación para su futura administración
Acondicionamiento y terapia mielosupresora
Infusión de las células progenitoras hematopoyéticas al paciente
Fase de recuperación hematopoyética e inmunológica
En el trasplante autólogo el paciente es su propio donante

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
locitos), solo o en combinación con quimioterapia, pudiéndose utilizar el mismo esquema de base. Se administra por vía subcutánea de 4 a 5 días antes y sus efectos más frecuentes son dolor óseo, fatiga, cefalea y febrícula.
La aféresis se realiza mediante un catéter venoso central tipo Hickman o una vía femoral (en el siguiente punto se profundizará en los tipos de catéteres más utilizados durante el tras-plante autólogo y su manejo). La sangre pasa por una máquina que hace una selección de las células que se quieren obtener, separando los progenitores hematopoyéticos y regresan-do al paciente la sangre restante. Las células se criopreservan entonces hasta el momento de su infusión. Esta técnica incluye la adición de un crioprotector, siendo el más utilizado el DMSO (dimetil-sulfóxido). Después se pasaría a la congelación a velocidad controlada y al almacenamiento a temperaturas inferiores a -80ºC (utilización antes de 6 meses) o a menos de -150ºC (más de 6 meses).
2. Fase de acondicionamiento
La infusión de células progenitoras hematopoyéticas se realiza después de un régimen prepa-ratorio o de "acondicionamiento" o terapia mielosupresora. La quimioterapia mielosupresora y el trasplante de células madre van encaminados a erradicar la enfermedad residual mínima, objetivo importantísimo en el neuroblastoma de alto riesgo por su tendencia a recidivas.
El primer paso en esta fase es la acogida del paciente y familia. Podemos encontrar que el niño y su entorno hayan conocido al personal durante la fase de diagnóstico y la fase de inducción, pero en ciertos casos los pacientes pueden llegar a la unidad para realizar el trasplante derivados de otros hospitales en los cuales han realizado toda la fase previa. Este proceso del trasplante es un procedimiento largo, con un ingreso prolongado y que requiere aislamiento. De ahí la importancia del apoyo que supone el personal de enfermería en esta acogida y el valor que debemos dar a esa parte emocional tanto del niño como de su familia.
• Tipo de aislamiento durante el trasplante autólogo
La inmunosupresión provocada por el régimen de acondicionamiento es causa de morbimortalidad en pacientes sometidos a trasplante en cualquiera de sus fases. A partir de esta etapa el paciente tendrá tratamiento profiláctico antimicrobiano hasta su completa inmunoreconstitución.
Comenzamos haciendo referencia al uso de los filtros HEPA como parte del ambiente protector en el trasplante. Su principal función es la prevención de infecciones fúngicas trasportadas por el aire. A pesar de su indicación para los trasplantes alogénicos (do-nante emparentado o no emparentado), se observa que también es utilizado en tras-plantes autólogos. En contraposición podemos encontrar centros que no lo incluyen, ni siquiera para trasplantes alogénicos. Será necesario por tanto evaluar las caracterís-ticas del paciente y condiciones y funcionamiento de cada unidad a la hora de tomar decisiones sobre su uso.
Otras de las medidas constituyentes del ambiente protector son las habitaciones indi-viduales con presión de aire positiva para evitar el paso de agentes patógenos transmi-tidos por aire desde áreas más contaminadas. La puerta de la habitación debe perma-necer cerrada.
La utilización de medidas de barrera tiene gran importancia: higiene de manos y uso de equipos individuales (mascarilla tipo quirúrgica, guantes, bata y calzas antes de en-trar a la habitación). El lavado de manos ha demostrado disminuir la incidencia de in-fecciones (Figura 3). Los guantes no sustituyen la higiene de manos.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
Figura 3. Correcta higiene y desinfección de manos
El hecho de que parte de las infecciones en el paciente sometido a trasplante surjan por agentes originarios de la propia microflora endógena, que debido a la neutropenia rompen las barreras físicas de protección de piel y mucosas, nos lleva a recomendar una serie de pautas a seguir en cuanto a la higiene y la dieta. En la dieta con baja carga bacteriana se deben consumir alimentos cocinados, cocidos o hervidos, evitando ver-duras crudas y tomando frutas que puedan ser peladas y productos lácteos pasteuri-zados. En caso de diarrea, dieta exenta de lactosa, sin residuos y sin gluten (en caso de malabsorción). Se debe seguir una adecuada higiene en la manipulación, un correcto almacenamiento y una correcta conservación, consumiendo productos envasados en atmósfera protectora. La higiene del niño incluye ducha diaria e hidratación, mantener la higiene bucal de dientes, lengua y encías, e importante higiene de manos, especial-mente antes y después de las comidas y de la utilización del W.C. Los juguetes de los niños deben ser limpiados y desinfectados.
Enseñar a la familia el manejo e importancia de estas medidas es fundamental para llevar a cabo un aislamiento inverso o protector efectivo. Habrá restricción en las visi-tas, quedando limitado el acompañamiento del paciente a un solo acompañante. No se desplazará al paciente salvo necesidades esenciales, en cuyo caso precisará de la colocación de mascarilla durante el traslado.
• Mucositis
La mucositis se define como la lesión inflamatoria de la mucosa a nivel bucal y también de todo el tracto gastro-intestinal. Depende en gran medida del tipo de acondiciona-miento empleado y los agentes quimio-radioterápicos utilizados. Suele aparecer a los 3 ó 5 días del acondicionamiento y su pico máximo es a partir de los 7 días, con una

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
duración media de 10 a 15 días. Es una complicación dolorosa para el paciente, requi-riendo en muchos casos opiáceos para el control del dolor y provocando la inadecuada ingesta de alimentos. Cuando se llega a este grado de mucositis que impide la correcta nutrición del niño, se recurre al soporte nutricional con suplementos nutricionales ora-les, nutrición parenteral o nutrición enteral (Figura 4).
Figura 4. Pilares fundamentales en el manejo de la mucositis
PREVENCIÓNTRATAMIENTO
DEL DOLORSOPORTE
NUTRICIONAL
Signos y síntomas
• Ulceraciones en cavidad bucal, pudiendo visualizarse placas blanquecinas
• Eritema y edema de la mucosa oral, lengua y/encías
• Sequedad, sensación de quemazón y alteraciones del gusto
• Dolor con imposibilidad para la deglución, dificultad para abrir la boca y para hablar
• Diarrea con deposiciones líquidas dolorosas
• Dolor abdominal con aumento del perímetro
Las escalas para calcular el grado de mucositis se basan en la evaluación de la cavi-dad oral, la capacidad de tragar y el grado de dolor del paciente (Figura 5).
Figura 5. Clasificación de la mucositis según la OMS
CALCIFICACIÓN DE LA MUCOSITIS SEGÚN LA OMS
GRADO SÍNTOMAS
01234
NingunoEritemaEritema, úlceras, puede comer sólidosEritema, edema o úlceras. Solo admite líquidosRequiere soporte enteral o parenteral

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
Medidas a llevar a cabo
• Correcta higiene bucal con cepillado diario de los dientes, lengua y encías con un ce-pillo de cerdas blandas o sustituirlo por gasas empapadas en antiséptico sobre todo en caso de sangrado o plaquetopenia, después de las comidas y antes de acostarse.
• Enjuagues bucales como por ejemplo solución salina fisiológica al 0,9% o bicarbo-nato sódico y/o agua, sin claras evidencias en cuanto a superioridad entre ellas a la hora de prevenir la mucositis, o solución acuosa de clorherixidina 0,2%, no existien-do tampoco resultados mejores en cuanto a prevención con respecto a los anterio-res. Evitar las soluciones alcohólicas.
• Preparados de soluciones para mucositis cuando existe mucositis activa en cuya composición encontramos antibióticos, corticosteroides, anestésicos tópicos como soluciones de lidocaína viscosa al 2%, etc.
• Sobre la crioterapia o uso de hielo en la cavidad bucal mientras se administra la qui-mioterapia, se ha comprobado su utilidad en mucositis por melfalán.
• Evitar alimentos ácidos, amargos, secos, picantes o comidas calientes, procurando una dieta blanda e incrementando el aporte de líquidos, preferentemente fríos.
• Inspeccionar diariamente la cavidad bucal, control de la ingesta y estado nutricional del niño; peso diario.
• Valoración del dolor: prestando atención a síntomas de esofagitis, náuseas y vómi-tos, distensión abdominal, frecuencia y características de las deposiciones (Figura 6).
La mucositis se resuelve con la recuperación hematopoyética del paciente.
Figura 6. Ejemplo de escala visual para paciente pediátrico
• Quimioterapia utilizada en la etapa de acondicionamiento
En puntos anteriores se ha hablado sobre el manejo y seguridad a la hora de la ad-ministración de fármacos citostáticos. En este apartado simplemente señalar que la quimioterapia usada como acondicionamiento para el trasplante autólogo en el neuro-blastoma puede ser busulfán/ melfalán o también carboplatino, etopósido y melfalán.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
3. Infusión de células progenitoras hematopoyéticas
El día de la infusión se conoce como día “0”. Comienza con el transporte de las células criopre-servadas hasta el lugar de la infusión pudiendo ser necesario un contenedor de transporte llenado con nitrógeno líquido. Se procede entonces a la fase de descongelación. La bolsa criopreservada es descongelada en un baño con solución salina estéril a 37ºC en cámara de flujo laminar y en un tiempo aproximado de 5 minutos. La infusión debe completarse tan pronto como sea posible tras la descongelación, de hecho el tiempo máximo de la infusión ha de ser de 15 minutos. Si tenemos varias bolsas criopreservadas lo recomendado es des-congelar cada bolsa antes de infundirla para minimizar el tiempo entre la descongelación y la administración.
La preparación de la unidad es fundamental, debiendo revisarse el buen funcionamiento de la red de oxígeno y de aspiración, preparar un equipo de oxigenoterapia, comprobar el mo-nitor y que el carro de parada esté debidamente equipado.
Se deberá tener preparada medicación de emergencia por posible reacción hemolítica agu-da, reacción al DMSO, reacción alérgica o anafiláctica. Incluye antihistamínicos, corticoides, atropina y adrenalina, aerosoles y diuréticos. También es necesaria la administración de pre-medicación normalmente con antipiréticos, antihistamínicos y corticoides.
La infusión se realiza exclusivamente por una luz, la luz de mayor calibre, a través de un infu-sor sin filtro y directo al catéter venoso central. Durante ese tiempo la enfermería vigila a pie de cama al paciente, monitorizando sus constantes vitales y la aparición de efectos adversos. La medición de la Presión Venosa Central (PVC) se hace necesaria también para detectar la sobrecarga de volumen. Se mantendrá la monitorización del niño mínimo durante la hora posterior a la infusión.
El volumen en cada bolsa varía de 120 a 180 ml. En pacientes malos movilizadores pueden obtenerse varias bolsas pero cada una con poca celularidad. Por ello la infusión también se puede realizar en días consecutivos para que la cantidad de crioprotector (DMSO) no supere la máxima recomendada que pueden recibir los pacientes por día (1 ml/kg/día).
Signos de posibles reacciones adversas inmediatas durante la infusión
• Reacción hemolítica aguda: escalofríos, fiebre, disnea, dolor torácico, eritema, san-grado anormal, shock, CID (Coagulación Intravascular Diseminada)
• Reacción alérgica: sibilancias, prurito, urticaria, angioedema. Reacción anafiláctica, siendo más infrecuente: hipotensión, disnea severa, broncoespasmo, edema larín-geo, dolor abdominal, sudoración
• Fiebre: en las primeras dos horas de infusión
• Toxicidad por DMSO: tos, enrojecimiento, dolor torácico, náuseas, vómitos, bradi/ta-quicardia, hipertensión arterial
• Otros: cefalea, hipotermia, sobrecarga hídrica

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
4. Postrasplante inmediato y reconstitución de la hematopoyesis
• Enfermedad veno-oclusiva hepática (EVO) o Síndrome de Oclusión Sinusoidal (SOS)
Consecuencia de la toxicidad hepática producida sobre todo por la terapia empleada en la fase de acondicionamiento, este síndrome se caracteriza por aumento de peso (no justificable por un aporte excesivo de líquidos), edemas y hepatomegalia, pudiendo aparecer ascitis. La ictericia cutánea y de mucosas es frecuente en adultos pero no es tan habitual que se manifieste en niños. Se da un aumento de las transaminasas y es-caso rendimiento de las transfusiones de plaquetas por un consumo excesivo.
Para su tratamiento, además de restricción hídrica y diuréticos, el fármaco empleado es el Defibrotide mediante perfusión intravenosa durante dos horas y siempre diluido antes de usarse. El tiempo de tratamiento suele ser de 15 días según respuesta.
• Síndrome del implante
Más habitual en el trasplante autólogo, este síndrome se caracteriza por liberación de citoquinas por los tejidos lesionados en el acondicionamiento y la recuperación de neu-trófilos. La clínica incluye fiebre no infecciosa, exantema cutáneo, infiltrados pulmona-res, hipoxemia; pueden darse diarreas sin otras causas asociadas, disfunción renal, dis-función hepática, encefalopatía transitoria. El uso de factores de crecimiento (G-CSF) se asocia a un riesgo más elevado de esta complicación. Por ello, el tratamiento va desde su suspensión a la administración de metilprednisolona con buena respuesta y siendo importante el tratamiento de manera precoz.
• Cistitis hemorrágica
Es la presencia de hematuria tanto macroscópica como microscópica que puede apa-recer en algún momento del trasplante desde que se inicia el acondicionamiento. Pue-de ser debida a la toxicidad de la quimioterapia sobre el urotelio o a causas víricas, como infección del tracto urinario por el poliomavirus humano bk/jc, adenovirus o CMV. Para su prevención, sobre todo en la cistitis por toxicidad de los tratamientos, es impor-tante la hiperhidratación del paciente, realizándose balances hídricos por turno. Espe-cial mención requiere si se usara la ciclofosfamida, pues además de la hiperhidratación debe asociarse mesna, cuya duración suele prolongarse hasta 24h después de la última ciclofosfamida.
• Recuperación hematopoyética y reconstitución inmune
Su duración es de varios meses en los receptores de un trasplante autólogo, a partir de 6 meses. Las cifras de neutrófilos se recuperan en 2-4 semanas, pudiendo funcional-mente tardar hasta 4 meses. El tiempo para la recuperación de plaquetas sin requerir transfusiones es similar. En cuanto a los linfocitos T, el recuento de CD3+ se normaliza entre las 6 y 8 semanas, mientras que CD8+ y CD4+ se recuperan a los 4 meses los pri-meros y a partir de los 6 meses los segundos. Los linfocitos B CD19 + aumentan pasados los 3-6 meses.
Para concluir este punto tan importante en el tratamiento del neuroblastoma de alto riesgo que es el trasplante de células progenitoras hematopoyéticas, recordar que los cuidados de enfermería destinados a estos pacientes deben basarse en conocimientos sólidos que fundamenten cada una de las acciones llevadas a cabo. La función de en-fermería dirigida a la prevención, detección temprana y tratamiento precoz es vital para un correcto trasplante de médula ósea.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
MANEJO DE DIFERENTES VÍAS CENTRALES
Ya en la fase de inducción el niño ha precisado la canalización de un catéter venoso central para poder llevar a cabo los diferentes ciclos de quimioterapia, además de ser de gran utilidad para los frecuentes controles analíticos y transfusiones. El acceso venoso más empleado en niños es el Port-a-cath, ya mencionado. Durante el trasplante de progenitores hematopoyéticos el número de fármacos empleados aumenta (antibióticos, antifúngicos, perfusiones de opiáceos, NPT, sopor-te transfusional, etc.), siendo necesaria la implantación de otro catéter venoso central.
1. Catéter Venoso Central (CVC) tipo Hickman o Broviac (Figura 7)
Su colocación es en quirófano, bajo anestesia y técnica estéril. Consisten en catéteres tuneli-zados de larga duración, flexibles y de silicona radiopaca, de una, dos o tres luces. Preferible-mente se implanta a nivel de tórax, por vena yugular o subclavia, para llegar a vena cava su-perior. Permiten una buena fijación aunque también tienen mayor incidencia de infecciones.
Figura 7. Hickman
Medidas a llevar a cabo
• Vigilancia diaria del punto de inserción
• Lavado de manos antes y después de manipular el catéter
• Material estéril y máxima asepsia a la hora del manteniendo del catéter
• Cura estéril de la zona de inserción catéter: gasas estériles, clorhexidina acuosa 2%
• Apósito transparente de clorhexidina con recambio cada 7-10 días; gasa o apósito clásico, cada 48-72h
• Recambio de equipos de infusión, sistemas y alargaderas cada 72h. Infundir nutri-ción parenteral (NPT) en luz exclusiva, con cambio de sistema cada 24h
• Aplicar alcohol 70% o clorhexidina alcohólica en conexiones antes de su manipulación

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
• Renovar el sellado de heparina del catéter cada 72h si no es utilizado
• Desechar 3 ml antes de las analíticas
• Lavar con suero fisiológico tras extraer sangre o tras administrar medicación
• Forma de heparinizar las luces del catéter: 1 ml Heparina 1% + 9 de suero fisiológico (SF). Infundir 3 ml por cada luz y clampar
Complicaciones que pueden aparecer
La oclusión del catéter puede deberse a una mala posición de la punta, vaina de fibrina en el extremo del catéter, catéter torcido o pinzado en algún punto, o complicaciones como una trombosis venosa.
Ante la imposibilidad de aspirar sangre pero poder infundir por la luz del catéter, ad-ministrar por medio de una jeringa 10 ml de SF e intentar aspirar probando diferentes posturas del paciente (levantar los brazos, ladear la cabeza, maniobras de vasalva como por ejemplo toser). Puede darse una oclusión parcial o total que no nos permita ni si-quiera infundir suero salino o que la administración de éste provoque dolor o molestias al paciente, lo que puede indicar que el catéter esté roto. Si no se resuelve, realizar Rx tórax y comprobar si es correcta su colocación y estado. Se podrá recurrir a la terapia trombolítica (Tabla 2).
• 2 ml SF + 1 ml heparina 1% en luz afectada. Clampar 10-30m
• Si no se resuelve, 2 ml SF + 5.000 UI de uroquinasa. Clampar 30m. Aspirar pasado ese tiempo. Si no refluye se puede repetir el procedimiento hasta en tres ocasiones, pudiéndose mantener la 3ª dosis hasta 24 horas
Tabla 2. Terapia trombolítica utilizada en caso de oclusión del catéter venoso central
EL NIÑO EN TRATAMIENTO CON RADIOTERAPIA
La astenia, náuseas, vómitos, pérdida de apetito, alteraciones en el gusto, cambios en la piel y alopecia son los efectos adversos más comunes. La sensación de cansancio es temporal, debien-do mantener el niño un equilibrio entre actividad y descanso. La radioterapia puede causar piel seca y descamada, prurito, enrojecimiento y cambios de coloración, volviéndose más oscura. Las recomendaciones a seguir se basan en la utilización de jabones neutros, secado suave de la piel, hidratación, proteger del sol y del frío, utilizar tejidos de algodón, lino o seda y ropa suelta que no oprima. En cuanto a las comidas, que sean de fácil digestión comiendo poca cantidad pero más frecuentemente. Importante la adecuada ingesta de líquidos, preferiblemente a temperatura am-biente. Si aparecen lesiones en boca o garganta o mucositis, seguir las mismas recomendaciones ya mencionadas en cuanto a higiene y cuidado.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
2.3. CUIDADOS Y ATENCIÓN DE ENFER-MERÍA EN LA FASE DE MANTENIMIENTO
INMUNOTERAPIA EN EL NEUROBLASTOMA DE RIESGO ALTO
A menudo, la causa principal de recaída es la presencia de enfermedad mínima residual. La terapia de posconsolidación o mantenimiento está diseñada para tratar la posible enfermedad mínima residual después de la etapa de consolidación. Los pacientes de riesgo alto en remisión después de un trasplante de células madre son tratados con anticuerpo monoclonal e Interleu-kina-2 (IL-2) junto con isotretinoína (ácido 13-cis retinoico), logrando mejorar la tasa de respuesta.
ATENCIÓN Y EDUCACIÓN AL PACIENTE Y FAMILIA DURANTE LA ADMINISTRACIÓN DE RETINOICO
El ácido 13-cis retinoico es tomado vía oral con las comidas, aconsejándose que sean ricas en grasas. Uno de los efectos más importantes a tener en cuenta es la sequedad de piel y mucosas que provoca su administración. De gran importancia es el uso de protector solar y ropa protectora debido al aumento de la sensibilidad a la luz solar, evitando o reduciendo la exposición al sol. La vitamina E aplicada en forma de lociones o aceites para la piel y labios proporciona hidratación además de actuar como defensa ante los efectos dañinos solares.
También puede provocar dolor en extremidades y espalda o aumento de las cifras de coles-terol y de calcio en sangre, requiriendo ajuste de la dosis. Menos frecuentes son el enrojecimiento de piel y ojos con prurito, cefalea, disminución de apetito, pérdida de peso, cambios en la visión, pitidos auditivos y retención de líquidos.
ATENCIÓN Y EDUCACIÓN AL PACIENTE Y FAMILIA DURANTE LA ADMINISTRACIÓN DE ANTICUERPO MONOCLONAL
Los GD2 son antígenos en la superficie de la membrana de las células del neuroblastoma. En esto se basa el desarrollo de anticuerpos monoclonales contra estos gangliósidos. La forma de tratamiento es en perfusión intravenosa, pudiendo variar los protocolos de administración de unos centros a otros.
Se enumeran a continuación efectos secundarios frecuentes que pueden aparecer y que el personal de enfermería debe conocer, además de educar al paciente y familia en su posible apari-ción con el objetivo de la identificación precoz y disminuir la ansiedad y miedo ante esta situación:
• Dolor generalizado que requiere la administración de analgésicos, incluyendo opioides como la utilización de morfina intravenosa, y el tratamiento con gabapentina
A. MIGUEL PELLÓN, L. MARGARITA ROMERO PINILLA Y M. CANTOS MUÑOZ

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
EFECTOS EN LA ADMINISTRACIÓN DE ANTI-GD2
Disminución de sodio, potasio y albúmina
Aumento de creatinina
Elevación de enzimas hepáticas
Disminución de plaquetas
Visión borrosa. Fotosensibilidad
Tos y dificultad respiratoria. Disnea
Neurotoxicidad: confusión. Neuropatía
Convulsiones
Síndrome de fuga capilar
Reacción alérgica severa
• Hormigueo en dedos de las manos y pies
• Hipo/hipertensión arterial. Taquicardia
• Hinchazón. Enrojecimiento de la piel
• Urticaria y/o prurito
• Fiebre
• Náuseas, vómitos y diarrea. Pérdida de apetito
• Fiebre
• Náuseas, vómitos y diarrea. Pérdida de apetito
Se recogen en la siguiente tabla otros efectos a tener en cuenta para el profesional de enfer-mería (Tabla 3):
Tabla 3. Algunos de los posibles efectos secundarios de la administración de anticuerpo monoclonal
ATENCIÓN Y EDUCACIÓN AL PACIENTE Y FAMILIA DURANTE LA ADMINISTRACIÓN DE IL-2
Con el mismo planteamiento que con la administración del anticuerpo monoclonal, se men-cionan los efectos más frecuentes que pueden aparecer con la IL-2, variando su forma de admi-nistración de unos protocolos a otros, pudiéndose ser una de las opciones la administración vía subcutánea:
• Fiebre y escalofríos
• Cuadro gripal con cefalea, cansancio y dolor articular
• Diarrea. Pérdida de apetito
• Hipotensión arterial

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
• Enrojecimiento cutáneo. Prurito
• Edemas. Aumento de peso
• Aumento de creatinina
• Disminución de la diuresis
• Aumento de enzimas hepáticas y bilirrubina
• Disminución de glóbulos rojos y plaquetas
Menos frecuentes pero también importantes:
• Náuseas y vómitos
• Disminución de sodio, calcio, magnesio y fosfato
• Síndrome de pérdida capilar
• Zumbidos en oídos. Visión borrosa
• Tos y moco nasal
• Cefalea
• Dolor abdominal
• Cambios de humor, somnolencia
• Reacciones graves: reacción alérgica grave, convulsiones, inflamación del colón con diarrea hemorrágica, parada cardiorrespiratoria

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
2.4. ATENCIÓN DOMICILIARIA AL NIÑO CON NEUROBLASTOMA
TRATAMIENTOS ADMINISTRADOS DE FORMA AMBULATORIA
Como hemos visto anteriormente el tratamiento con inmunoterapia del neuroblastoma en el paciente pediátrico consiste en la administración de 6 ciclos de varios fármacos: isotretinoína (13-cis-retinoico), aldesleukina (IL-2) y el anticuerpo monoclonal c14.18/CHO. El primero de los ciclos comienza con 14 días de ácido retinoico dividiendo la dosis total diaria en dos tomas. Al finalizar la infusión del anticuerpo monoclonal se inician los siguientes 14 días de retinoico. Es el tiempo que corresponde a la toma del ácido retinoico el que se llevará a cabo en el domicilio del paciente.
La visita domiciliaria es aquella que transcurre en el domicilio del paciente previo acuerdo con el paciente y en el caso del paciente pediátrico, previo acuerdo con sus padres.
La primera visita debe estructurarse la siguiente manera:
• Valoración del paciente. Siguiendo los patrones funcionales de Marjorie Gordon detectare-mos las necesidades de nuestro paciente
• Identificación de problemas
• Plan: tratamiento de las complicaciones, educación para la salud, adherencia terapeútica, resolución de dudas
En visitas sucesivas se valorará la evolución de las necesidades identificadas anteriormente, así como la detección de nuevas necesidades.
1. Percepción/mantenimiento de la salud
Dentro del primero de los patrones debemos valorar aquellas conductas que hace el pa-ciente (en nuestro caso sus padres ó cuidadores) para mantener la salud. Algunas de ellas ya habrán sido valoradas durante los ingresos.
• Hábitos tóxicos de los padres
• Estado de vacunación del niño/a
• Alergias
• Hábitos higiénicos: importantes en estos niños inmunodeprimidos para evitar las infecciones
• Ingresos hospitalarios
• Adherencia al tratamiento: en el caso del paciente pediátrico sometido a inmunoterapia,
A. MIGUEL PELLÓN, L. MARGARITA ROMERO PINILLA Y M. CANTOS MUÑOZ

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
el corroborar que sus cuidadores conocen a la perfección la medicación que debe tomar, así como la forma de administración, efectos secundarios más habituales (comentados en apartados anteriores) y precauciones a tener en cuenta durante el tratamiento es de vital importancia. Deben saber que durante el tratamiento con retinoico, el niño/a no debe tomar algunos fármacos como los derivados de la vitamina A y en el caso de los adolescentes tam-poco deben ingerir alcohol, todo ello por la alta hepatoxicidad del fármaco. También deberán ser instruidos en la forma de administración, siendo esta de manera oral y preferentemente junto con comidas con alto contenido en grasa. Deberán conservar el fármaco protegido de la luz y en nevera
2. Nutricional/metabólico
Dentro de este patrón debemos prestar atención a los siguientes:
• Número de comidas que realiza el paciente
• Presencia de náuseas, vómitos, problemas bucales, disfagia
• Aumento o disminución de la ingesta, ya que ambos pueden ser efectos secundarios del retinoico
• Pérdida de peso
• Estado de las encías pudiendo estas inflamarse
• Estado de la piel y mucosas, teniendo en cuenta que la sequedad es uno de los efectos se-cundarios más frecuentes del tratamiento con retinoico. Haremos especial hincapié en la importancia de mantener al niño hidratado. Instruiremos acerca de evitar la exposición a los rayos ultravioletas, debido a la mayor susceptibilidad a las quemaduras
• Picor de la piel
3. Eliminación
• Hábito intestinal: diarrea, estreñimiento, características de las heces…
• Disuria
• Presencia de edemas
4. Actividad/Ejercicio
Dentro de este patrón prestaremos atención a la presencia de:
• Debilidad, más frecuente durante la administración de la interleukina y el monoclonal
• Tolerancia a la actividad
• Deficiencias motoras
• Determinaremos las constantes vitales. Su alteración es más frecuente durante la adminis-tración de la interleukina y el monoclonal

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
5. Sueño/descanso
• Horas de sueño a lo largo del día
• Necesidad de fármacos para conciliar o mantener el sueño
• Pesadillas
• Somnolencia diurna
6. Cognitivo/perceptivo
• Nivel de consciencia
• Cambios de humor, depresión, nerviosismo…
• Alteraciones de los órganos de los sentidos, pudiendo aparece visión borrosa, fotofobia, difi-cultad para la visión nocturna, zumbidos en los oídos, disminución de la audición, pitidos…
• Presencia de dolor: cefalea, dolor abdominal o dolor en las extremidades son los más fre-cuentes
7. Autoconcepto/autopercepción
Indagaremos sobre la imagen que tiene el niño/a sobre sí mismo, cobrando mayor importan-cia durante la adolescencia.
8. Rol/relaciones
Valoraremos las relaciones que el paciente mantiene con su familia, tanto con sus padres como con sus hermanos u otros familiares relevantes en la vida del menor y también las re-laciones con otros niños.
9. Sexualidad/reproducción
En relación a la sexualidad y reproducción, es importante advertir a los padres que el trata-miento con retinoico tiene efectos teratogénicos , por lo que si es la madre quien administra el fármaco deberá hacerlo con unas medidas de seguridad que constan de guantes y mas-carilla y lavado de manos posterior.
En el caso de las adolescentes valoraremos sus ciclos menstruales si los tienen y explica-remos lo anteriormente descrito en cuanto a los efectos teratógenos del fármaco ante un posible embarazo.
10. Adaptación/tolerancia al estrés
Podemos indagar sobre cómo vive el niño la situación en la que se encuentra, si habla de ello o si por el contrario trata de evitar el tema.
11. Valores y creencias
Dentro de este patrón cobra importancia la religión y la relación con la muerte, no existiendo nada en especial a tener en cuenta durante la administración de la inmunoterapia.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
CONTINUACIÓN DE CUIDADOS EN EL DOMICILIO: ADAPTACIÓN TRAS EL TRATAMIENTO
Llegado el final del tratamiento y la vuelta del paciente y su familia a su vida habitual, es común que surjan sentimientos ambivalentes; por un lado, la alegría de haber superado la en-fermedad y por otro, sentimientos como el miedo a la recaída, la soledad, puesto que las visitas al hospital y el contacto con el personal sanitario disminuyen, la ansiedad ó la sensación de no sentirse integrado dentro de lo que antes era su día a día. Cada uno de los miembros de la unidad familiar, así como el conjunto de todos ellos debe readaptarse a la nueva situación, como ya lo hicieron anteriormente en el momento del diagnóstico. Es un proceso que implica tiempo y en el que la enfermería puede ayudar acompañando y promoviendo el autocuidado del paciente y su familia mediante la educación sanitaria.
Podría ser de utilidad concertar una visita domiciliaria al mes de haber terminado el trata-miento, y así poder identificar las necesidades que tiene cada familia. Algunas de las recomenda-ciones a realizar a las familias de estos niños irían encaminadas a:
• Prevenir infecciones: evitando, al menos los primeros meses, lugares muy concurridos y con poca ventilación, evitar el contacto con personas enfermas, prestar especial cuidado en la manipulación de alimentos, mantener una higiene personal y del entorno adecuada...
• Ámbito social: retomar las relaciones sociales y actividades de ocio puede resultar difícil al comienzo, por lo que debe ser algo progresivo
• Instruir a cerca de los signos y síntomas por los que deberían acudir a urgencias
• Es frecuente que durante algunos meses tras el tratamiento, el niño aún se sienta cansado o débil, por lo que sería conveniente programar períodos de descanso a lo largo del día

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
CONCLUSIONES
• El manejo seguro de citostáticos es de vital importancia tanto para el personal como para el paciente: comparación de la prescripción y la etiqueta del fármaco, equipo de protección in-dividual, comprobación del funcionamiento de la vía y administración y eliminación segura del fármaco
• Una adecuada asepsia en el manejo de las vías centrales proporciona una mayor seguridad al paciente
• Hinchazón, eritema, dificultad respiratoria y/o mareo son algunos de los signos de alarma a tener en cuenta durante la infusión de quimioterapia
• El aislamiento inverso consta de: correcta higiene de manos, habitación individual con filtro HEPA y presión positiva, y dispositivos de barrera (mascarilla tipo quirúrgica, guantes, bata y calzas antes de entrar a la habitación)
• Las principales complicaciones del transplante autólogo son la mucositis, cistitis hemorrági-ca, enfermedad veno-oclusiva hepática (EVO) y el síndrome del implante
• Una de las principales funciones de enfermería en la administración de inmunoterapia es la vigilancia de signos y síntomas derivados del tratamiento
• La educación sanitaria al entorno del paciente sobre los efectos secundarios o adversidades que pueden aparecer es importante para disminuir la ansiedad y mejorar la adherencia al tratamiento
• La aplicación del proceso de atención de enfermería en el domicilio ayuda a identificar las necesidades del paciente y su entorno que pueden pasar desapercibidas durante el ingreso hospitalario
BIBLIOGRAFÍA
• Garbin LM, Silveira RCCP, Braga FTMM, Carvalho EC. Medidas utilizadas en la prevención de infecciones en trasplante de
células tronco hematopoyéticas: evidencias para la práctica. Rev. Latino-Am. Enfermagem. Mayo-jun. 2011.
• Tejada Domínguez FJ, Ruiz Domínguez MR. Mucositis oral: decisiones sobre el cuidado bucal en pacientes sometidos a
radioterapia y quimioterapia conforme a la evidencia. Enfermería Global. Febrero 2010;18(18).
• Gómez-Candela C, Canales Albendea M. A., Palma Milla S, de Paz Arias R, Díaz Gómez J, Rodríguez-Durán D, Villari-
no-Sanz M, Arribas Hortigüela L, Burgos Peláez R. Intervención nutricional en el paciente oncohematológico. Nutrición
Hospitalaria. 2012; 27(3):669-680.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
• Carreras I Pons E., Rovira I Tarrats M., Zeberio Echechipia I., Valcárcel Ferreiras D. Manual de Trasplante Hematopoyético.
Quinta edición: 2016.
• Olaya Vargas A. Trasplante de células progenitoras hematopoyéticas en pediatría. Principios básicos. 2012.
• Sociedad Española de Hematología y Hemoterapia. Manual del Médico Residente en Hematología y Hemoterapia. c2014.
• Solà I, Izquierdo F, Paladio N. Inmunoterapia anti-GD2 en pacientes con neuroblastoma de alto riesgo. Actualización.
Agència de Qualitat i Avaluació Sanitàries de Catalunya. 2013.
• Pérez-García M, Olaya-Vargas A, Del Campo-Martínez A, Gaytán-Morales F, Mújica-Guzmán F, Juárez-Nicolás F, Mora-Ma-
gaña I, Augusto Alejandre Villar. Reconstitución inmunológica en niños receptores de trasplante de células progenitoras
hematopoyéticas. Alergia, Asma e Inmunología Pediátricas. Mayo-Agosto 2012; (21)2: 72-79.
• Rojas Baena P. Complicaciones en el TPH. Desde el Acondicionamiento hasta la recuperación hematológica. 2017.
• Comunidad de Madrid. Guía de recomendaciones al paciente. Radioterapia. Diciembre 2006.
• Comunidad autónoma de Euskadi. www.osakidetzaeuskadi.net. [En línea]. Disponible en:https://www.osakidetza.eus-
kadi.eus/contenidos/informacion/hd_publicaciones/es_hdon/adjuntos/Folleto_InmunodeprimidoC.pdf [Consultado el 15
de febrero de 2019].
• Serrano Barona D M., Sánchez-Izquierdo Castellanos S. Rev. Triaje. Enfermería Ciudad Real. Octubre. 2013.
• CICLOFOSFAMIDA [Internet]. Oncohealth Institute. 2019 [cited 15 February 2019]. Available from: http://www.oncohealth.
eu/es/area-paciente/cancer/informacion-soporte-paciente/informacion-general/tratamiento/quimioterapia/listado-far-
macos/ciclofosfamida.
• Peris Bonet R, Pardo Romaguera E, Muñoz López A, Sayas Sánchez N, Valero Poveda S. Cáncer infantil en España. Esta-
dísticas 1980-2016. Registro Español de Tumores Infantiles (RETI-SEHOP). Valencia: Universitat de València, 2017 (Edición
Preliminar, CD-Rom).

3HUMANIZACIÓN DE LOS CUIDADOS EN EL PACIENTE INFANTIL CON NEUROBLASTOMA
ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA MÓDULO 03

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
Además de tratar las enfermedades, es de gran importancia para los profesionales sanitarios proporcionar alivio a los problemas emocionales que presentan los pacientes, así como demos-trar respeto por la condición humana. Con este fin, afortunadamente se está centrado cada vez más atención en desarrollar programas de humanización hospitalaria, ofreciéndose así nuevas perspectivas de cuidado. Los programas de humanización son responsables de iniciar debates e intercambios de experiencia acerca de la vida diaria del hospital; de integrar el trabajo del día a día en proyectos concretos de humanización que se puedan estar llevando a cabo en cada centro, sensibilizando a las personas y animándoles a consolidar redes de colaboración y comunicación que contribuyen significativamente a mejorar la calidad de los cuidados sanitarios tanto para los pacientes como para los mismos profesionales.
La humanización de los cuidados debe desarrollarse a distintos niveles. Un primer nivel tiene lugar cuidando el entorno físico, arquitectónico, hospitalario. La consolidación de la humanización requiere un compromiso para construir entornos hospitalarios confortables y acogedores. Esto adquiere una especial importancia en pediatría oncológica. Los colores, olores, la luz del hospital, y el equilibrio entre ellos puede crear ambientes acogedores tanto para los profesionales como para los pacientes y sus familiares, pudiendo contribuir al proceso de promoción de la salud. El niño gravemente enfermo además de lidiar con la enfermedad, debe alejarse de su familia, de sus amigos y de su escuela, a la vez que se ha de someter a numerosos procedimientos invasivos do-lorosos, contribuyendo todo ello a que su experiencia hospitalaria se convierta en algo traumático. Así, se ha demostrado que el 50% de los niños pueden presentar alteraciones emocionales durante la hospitalización. Entre las causas que ellos mismos señalaban de tales alteraciones se incluían: los procedimientos médicos diagnósticos y el tratamiento, la separación de sus padres y amigos, y variables del entorno hospitalario. De este modo, el entorno hospitalario debe estar centrado en las necesidades del niño de jugar, aprender, explorar y comunicarse con otros de su misma edad, con el fin de facilitar la hospitalización al máximo.
3.1. INTRODUCCIÓN: QUÉ ES HUMANI-ZAR EL CUIDADO EN PEDIATRÍA ONCO-LÓGICA Y CÓMO SE CONSIGUEM. DIE TRILL Y F. MUÑOZ TORRES
Los avances de la Medicina y de la tecnología aplicada a la salud, los cambios sociales y otros factores han contribuido a la deshumanización del cuidado médico. Esto tiene implicaciones con-cretas y especiales en el cuidado de los niños gravemente enfermos y de sus familias. Reducir la distancia afectiva cuando transmitimos información médica a los pequeños pacientes y a sus pa-dres; facilitar su participación activa en el proceso de toma de decisiones médicas, de modo apro-piados a la edad del niño; resaltar su unicidad e individualidad, evitando la homogeneización con otros pacientes y familias; reduciendo su soledad durante el proceso de enfermedad; y ayudarles a dar sentido a su experiencia del cáncer, son parte del proceso de humanizar el cuidado.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
El desarrollo y la implementación de actividades lúdicas, musicales, culturales, etc. con los pequeños pacientes y sus familias, con el objetivo de buscar una mejor adaptación al entorno hos-pitalario, de aliviar el estrés, de reducir el tiempo de ingreso, y de facilitar la interacción entre pa-cientes, familias y personal sanitario, adquiere similar importancia en la humanización del cuidado.
Humanizar los cuidados implica también individualizarlos y adecuarlos a cada niño según su situación y sus necesidades. Se ha descrito, y así nos lo demuestra la práctica clínica diaria, que el acto de cuidar implica acompañamiento en todas las dimensiones de la persona y que la compren-sión, la implicación y la compasión, materializados a través de la ayuda, la promoción de la salud y la protección, son pilares básicos de la humanización. Con el fin de proporcionar cuidados con estas características, es de suma importancia que los profesionales sanitarios cuenten con una mí-nima formación en habilidades de comunicación. Poder entablar vínculos terapéuticos a través de la empatía es un requisito mínimo para humanizar el cuidado al paciente oncológico en pediatría. El personal de enfermería, cuyo ejercicio se basa en la relación con otros, adquiere un rol espe-cial en este sentido ya que está en primera línea de cara al paciente y además, son profesionales que mantienen relaciones personales y poco amenazantes con los pequeños enfermos y sus fami-lias. La empatía hace posible que puedan prestar ayuda en momentos de enorme vulnerabilidad emocional, física, social y psicológica, adaptando un papel de cada vez mayor protagonismo en el tratamiento psicoemocional del niño con cáncer y de su familia. Debido a su proximidad con los pacientes, los profesionales de la enfermería se encuentran en una posición perfecta para imple-mentar intervenciones psicológicas sencillas que puedan optimizar la calidad de vida del paciente y la adaptación de la familia al proceso de enfermedad.
Por todo ello podríamos decir que humanizar los cuidados con niños afectados de neuroblas-toma y sus familias implica cuidar con compasión y con comprensión en un entorno que inspire seguridad y tranquilidad al niño, con conocimiento de las necesidades del paciente y de su familia, desarrollando las propias competencias y autoconocimiento con objeto de proporcionar el mejor cuidado en cada momento, teniendo en cuenta la diversidad multicultural actual, y entendiendo en todo momento, el impacto emocional que tiene la enfermedad en el paciente, en la familia y en el personal sanitario.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
3.2. IMPACTO EMOCIONAL DEL NEUROBLASTOMA
IMPACTO EMOCIONAL SOBRE LOS PADRES DEL PACIENTE
Cuando los padres tienen conocimiento de que su hijo está afecto de un cáncer las reaccio-nes son múltiples e incluyen negación, un dolor profundo, sentimientos de impotencia, ira, tristeza, bloqueo, sentimientos de culpabilidad, duelo anticipado, sentimientos de fracaso como cuidado-res, ansiedad, dificultades para la comprensión y para realizar las actividades de la vida diaria, sensación de falta de recursos personales, e inseguridad ante todos los cuidados que deban pro-porcionar a su hijo. Estos sentimientos pueden ser oscilatorios y cambiantes desde el momento del diagnóstico hasta que alcanzan una aceptación, mayor o menor, de la realidad que les toca vivir.
Lo que está claro es que el diagnóstico de un neuroblastoma en un hijo es devastador y ge-nera una crisis en el seno de la vida familiar. La normalidad en la vida familiar requiere ahora una redefinición. Los padres que trabajan fuera del hogar deben tomarse el tiempo para cuidar de su hijo enfermo, que ahora se convierte en el foco principal del tiempo y la atención familiar. Los padres se suelen sentir desbordados por la enorme cantidad de información médica que reciben, por la necesidad de “digerirla”, y por tener que dar consentimiento para someter a su hijo a unos tratamientos altamente agresivos, en un periodo de tiempo muy limitado. El modo en que van a reaccionar ante esta nueva situación va a depender en gran parte de sus experiencias vitales, de sus creencias y valores culturales, y de sus respuestas de afrontamiento individuales a situaciones estresantes previas.
Nadie está inicialmente preparado para enfrentarse al diagnóstico de una enfermedad que amenaza la vida de un hijo. De ahí que la respuesta inicial de muchos padres sea una de negación: pueden cuestionar si los resultados de las pruebas son correctos, si son los de otro niño, o si los médicos se han confundido. Esta negación inicial puede servir para aliviar el enorme dolor que genera el enfrentamiento al diagnóstico. La negación no es un problema siempre y cuando no interfiera con la administración adecuada del tratamiento médico. La negación generalmente se va desmontando poco a poco, a medida que los padres van aceptando la cruda realidad de la en-fermedad y va dando lugar a la aparición de otros sentimientos. Los sentimientos de culpa son sig-nificativos: culpa por no haber podido proteger al hijo de la enfermedad: “¿Habrá sido porque he fumado?, ¿Serán mis genes? ¿De qué forma he contribuído yo a que esto le ocurriera a mi hijo?". La tristeza surge por las pérdidas a las que se enfrentan (pérdida de la salud del hijo, de los sueños y planes de vida que tenían para ese niño, etc), y por el dolor por el que pasa el pequeño enfermo. La ira es una respuesta a la crueldad que supone que el cáncer amenace la vida de un niño inocente y vulnerable, así como a los sentimientos de impotencia que aparecen en los padres.
El temor por la pérdida del hijo está siempre presente. No solamente se anticipa la pérdida del niño sino también, de todos los planes y fantasías que se habían proyectado sobre él desde el momento de su concepción.
M. DIE TRILL Y F. MUÑOZ TORRES

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
Toda esta convulsión dentro del seno familiar hace que los problemas concomitantes o ante-riores a este hecho se puedan ver agravados no siendo infrecuentes las desavenencias conyugales o los conflictos entre otros miembros de la familia.
La atención integral al niño con cáncer debe incluir intervenciones psicosociales dirigidas a los padres durante todo el proceso de enfermedad, siendo un indicador de excelencia en la aten-ción a los pacientes infantiles.
IMPACTO EMOCIONAL SOBRE EL PACIENTE PEDIÁTRICO Y ADOLESCENTE
Generalmente los niños con cáncer se sorprenden tanto como sus padres del nuevo diag-nóstico, del paso de un estado de salud a uno de enfermedad, y de las nuevas y poco bienvenidas pruebas médicas a las que ha de someterse. Genera mucho temor saber que tu cuerpo no está funcionando como debiera. Es difícil someterse a análisis de sangre, biopsias, aspiraciones de mé-dula, punciones lumbares, escáneres y otras pruebas ansiógenas e invasivas. La falta de colabo-ración con las pruebas médicas constituye una manifestación más del temor y ansiedad del niño ante la enfermedad y sus consecuencias (Die Trill, 2000). Es también fuente de angustia observar la ansiedad de tus padres sin entender muy bien lo que está pasando. La rabia y la culpa son reac-ciones normales ante el diagnóstico. Los pacientes se pueden preguntar por qué les está pasando ésto y sentir que no es justo. Sienten ira por todo aquello por lo que deben pasar en el hospital, por la necesidad de relacionarse con personas desconocidas, por sentir que su privacidad está siendo invadida, por tener que tragar pastillas que saben mal o tragan con dificultad y por tener que per-manecer en el hospital.
Los sentimientos de culpa son también frecuentes. Los niños y adolescentes pueden pre-guntarse si están enfermos por haber hecho algo malo: mentir, probar drogas, fumar, o por haber tenido malos pensamientos. También pueden sentirse culpables por haber generado una crisis familiar. Esto puede acentuarse en el caso de que haya conflictos familiares, los padres estén di-vorciados o haya algunos estresores adicionales.
La tristeza aparece generalmente al darse cuenta de las cosas importantes para ellos, que no pueden hacer a causa de la enfermedad o sus tratamientos: deporte, bailes. Sienten tristeza cuando piensan en todos los meses de tratamiento que tienen por delante y en cómo éste puede interferir con su actividad diaria. Sienten tristeza y vergüenza cuando observan las diferencias en-tre ellos y sus amigos y compañeros, y cuando observan los cambios que produce la enfermedad en su cuerpo y en su aspecto físico. Pueden sentir desesperanza y temer que los tratamientos pueden no funcionar como desean. La autoestima del pequeño se verá igualmente afectada: “No soy como los demás… No soy el de antes… Ya no querrán jugar conmigo… Estoy muy feo con la cara tan hinchada… No me puedo concentrar en la clase: ahora soy más tonto”, son algunos de los pensamientos que se cruzan por su cabeza.
Problemas con la alimentación no son poco frecuentes en niños con cáncer y en ocasiones pueden ser utilizados por los pacientes como medios para aumentar su control sobre la situación.
La adolescencia constituye un periodo caótico del desarrollo durante el cual el individuo lucha por desarrollar su propia identidad y auto-imagen, por ser independiente, por adaptarse a su sexualidad cambiante y a las modificaciones que sufre su cuerpo, y por establecer relaciones sociales y planificar su futuro. Es por ello que el cáncer sitúa al adolescente en una posición en la que ha de equilibrar sus necesidades de independencia con las exigencias de la enfermedad, que muy frecuentemente le obliga a depender de otros adultos de su entorno. En esta etapa evolutiva se acentúa el temor a perder el control sobre las funciones corporales y la vergüenza de “no ser

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
como los demás” de su edad. Los cambios físicos que se producen como resultado de la pubertad se añaden a las alteraciones en la imagen corporal producidas por el cáncer y sus tratamientos para acentuar la insatisfacción del adolescente con su propio cuerpo. La administración de tra-tamientos oncológicos generalmente interfiere con el desarrollo de actividades especialmente atractivas para el adolescente, como los deportes u otras actividades físicas en las que suele estar involucrado o interesado. El futuro se ve amenazado y surgen preguntas acerca de cómo va a poder vivirlo. Dudas acerca de su atractivo sexual, de la posibilidad de enamorarse y de contraer matrimonio, de la posible esterilidad inducida por el tratamiento oncológico, y en general, sobre la posibilidad de ser feliz haciendo lo mismo que los demás, asaltan con frecuencia la mente del adolescente enfermo generando altos niveles de angustia emocional que difícilmente comparte con sus superiores (Die Trill, 2003).
El impacto emocional que origina en un niño el conocimiento de que sufre una enfermedad oncológica como es un neuroblastoma va a depender en gran medida del estadio evolutivo en que se encuentre; del grado de madurez del paciente; de lo que significa el diagnóstico para él/ella; de su capacidad para expresar lo que siente; de sus habilidades para afrontar los cambios; de la dinámica y estructura familiar; de los apoyos y recursos con los que cuenta la familia, y de expe-riencias previas con la enfermedad, entre otras cosas.
Con el fin de mostrarle al enfermo su afecto y cuidados especiales, los padres frecuente-mente restringen la disciplina del niño y no ponen límites a su mal comportamiento. Ello impide la adaptación emocional del paciente provocando sensaciones aún mas intensas de pérdida de control. El niño necesita que alguien ponga un orden a su mundo ahora caótico, con el fin de nor-malizar su vida en la medida de lo posible (Die Trill, 2000).
Se ha observado que los supervivientes de neuroblastoma pueden tener un mayor riesgo de desarrollar alteraciones psicológicas debido a la edad temprana a la que se suele diagnosticar la enfermedad así como a la neurotoxicidad que producen los tratamientos administrados. Este ma-yor riesgo está asociado con un mayor uso de servicios de educación especial así como a un nivel de logro académico más bajo en la edad adulta. Se podría considerar que estos supervivientes de neuroblastoma consituyen un grupo de alto riesgo que se beneficiaría de cribajes continuados así como de recibir las intervenciones psicológicas y médicas necesarias en cada momento del proceso de superviviencia. Así, en el estudio de Zheng y sus colegas (2018), los supervivientes de neuroblastoma, comparados con sus hermanos sanos, presentaban con una prevalencia mayor de alteraciones en las áreas de ansiedad/depresión, déficits de atención, conflictos con los iguales/aislamiento social; comportamiento antisocial y cabezonería.
Los niños menores con neuroblastoma pueden:
• Temer la separación de sus padres
• Temer y angustiarse ante las pruebas médicas dolorosas
• Gritar, tener pataletas, negarse a cooperar, o aislarse
• Apegarse a los padres en exceso
• Comportarse de maneras agresivas o violentas
• Sentir enfado o tristeza cuando se ven limitados en sus actividades diarias
Los niños en edad escolar con neuroblastoma pueden:
• Mostrarse disgustados por la interrupción de su vida escolar

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
• Echar de menos a sus compañeros del colegio
• Mostrar ira y tristeza por la pérdida de su salud, de su actividad escolar y de su vida anterior
• Buscar más apoyo emocional y social de sus familiares y amigos
Los adolescentes con neuroblastoma pueden:
• Mostrarse disgustados por la interrupción que supone el diagnóstico en su funcio-namiento académico y en sus actividades sociales
• Sentir que su independencia está amenazada
• Mostrar reacciones emocionales intensas
• Requerir apoyo de amigos, contactos del colegio y otras personas importantes para ellos
• Centrarse en el significado que tiene la vida y en los efectos del cáncer sobre su identidad
• Hacer chistes acerca de su enfermedad, distraerse de ella, o intentar pensar “en po-sitivo”
• Rebelarse contra sus padres, los médicos y/o los tratamiento que reciben
IMPACTO EMOCIONAL SOBRE LOS HERMANOS SANOS DEL PACIENTE
Los hermanos del paciente generalmente sienten tristeza a medida que van tomando con-ciencia de que su hermano/a está realmente muy enfermo/a y va a requerir tratamiento impor-tante. Su tristeza surge también de ver tristes y preocupados a sus padres. Los hermanos menores del paciente echan en falta la presencia de los padres que ahora están centrados en cuidar del pe-queño paciente y en acompañarle en el hospital. Los hermanos adolescentes pueden comprender mejor los riesgos que corre su hermano enfermo, pero aumenta también su conciencia acerca de la fragilidad de la salud y de la vida, lo cual aumenta su angustia y temor.
Pensamientos de que a ellos les puede ocurrir algún día lo mismo que a su hermano enfermo son frecuentes en los hermanos de pacientes con neuroblastoma. Igualmente, preocupaciones re-lacionadas con la incapacidad de sus padres para proteger al enfermo del cáncer generan temor: los padres no han podido proteger al pequeño enfermo de ser diagnosticado de una enfermedad grave, de manera que tampoco me podrán proteger a mí si me ocurriera lo mismo.
Los hermanos de los pacientes pasan a ser en muchas ocasiones “los grandes olvidados” por lo que surgen sentimientos de abandono y fantasías sobre la enfermedad de su hermano. Senti-mientos de culpa por cuestionarse si han sido ellos los causantes de la enfermedad (quizás por haberse peleado con el enfermo, por no haber compartido sus juguetes, haberle mentido, etc.) no son poco comunes. De ahí que bajos resultados académicos, aislamiento del círculo de amigos, y en casos más extremos, comportamientos inadecuados, actitudes hostiles y negativas, y depre-sión, pueden aparecer también.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
Tabla 1. Aspectos psicosociales a valorar durante la primer encuentro con el personal de enfermería de referencia
CUÁNDO BUSCAR AYUDA DE UN PROFESIONAL PSICOONCÓLOGO PARA UN NIÑO CON NEUROBLASTOMNA O SUS HERMANOS
Si el niño no es capaz de gestionar sus sentimientos de tristeza
Si el niño se siente triste la mayor parte del tiempo
Si no se puede reconfortar al niño
Si el niño/adolescente refiera que ha pensado o piensa en suicidarse
Si el niño/adolescente siente extremadamente irritable
Si el niño se enfada con facilidad
Si el niño experimenta labilidad afectiva
Si el niño se aísla
Si el niño se comporta de manera diferente a como lo hacía antes del diagnóstico
Si el niño tiene cambios de apetito que no están causados por el tratamiento
Si el niño tiene niveles muy bajos de energía
Si el niño muestra poco interés en actividades
Si el niño tiene dificultades de concentración
Si el niño llora en exceso
Si el niño tiene dificultades para dormir

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
3.3. EL PRIMER ENCUENTRO: CÓMO LLEVAR A CABO LA ACOGIDA
El impacto emocional que supone un diagnóstico de cáncer en el niño y en la familia es de tal magnitud, complejidad y variabilidad que sería necesario implantar en las unidades de oncología pediátrica, un protocolo de intervención o actuación en estos primeros momentos iniciales, dife-rente al que se llevaría a cabo con un adulto.
En primer lugar, debe asegurarse el diagnóstico de neuroblastoma con cuantas pruebas diagnósticas sean necesarias antes de proporcionar la información médica a los padres y a los ni-ños, y antes de ingresar al paciente en la unidad hospitalaria. Todos los profesionales implicados en el cuidado deben consensuar y adecuar una estrategia de intervención con el objeto de minimizar en todo lo posible los efectos estresantes que este diagnóstico proporciona en todos los miembros de la familia. La comunicación del diagnóstico deberá ir seguida por una acogida en la unidad de hospitalización.
El proceso de transmisión de información médica debe llevarla a cabo el médico inicialmen-te. Es conveniente que la enfermera esté presente en este duro encuentro con los padres, con el fin de saber qué información exactamente ha recibido la familia y poder así reforzarla y responder a las preguntas que ésta le puede plantear posteriormente. La transmisión del diagnóstico debería llevarse a cabo en un entorno privado e íntimo, y sin interrupciones, debiéndose facilitar la expre-sión de emociones en los distintos miembros de la familia. Es importante que ambos progenitores estén presentes y que los profesiones sanitarios dispongan del tiempo que precise la familia para asumir el shock inicial y recabar toda la información médica que precisen en ese momento. La información debe transmitirse empleando un lenguaje claro, sencillo y con pocos tecnicismos, permitiendo a la familia articular las dudas y preguntas que deseen formular.
La importancia de la presencia de la enfermera referente que va a acoger posteriormente al paciente y a la familia en la unidad es primordial. El personal de enfermería es quien más tiempo pasa con los pacientes y con la familia, y está en una posición óptima para ofrecer la seguridad y la confianza necesarias para reforzar a la familia y al paciente, reforzando los esfuerzos del personal sanitario por proporcionar un cuidado lo más esmerado y profesional del niño posible, y asegu-rando a la familia que se van a poner a su alcance todos los medios de tratamiento disponibles en la actualidad. Esta actuación proporciona una visión de continuidad, refuerzo positivo, y cohesión entre los diferentes profesionales muy apreciada por las familias. La figura de la enfermera es me-nos amenazante, por regla general, que la del médico, sintiendo los pacientes y las familias más facilidad para plantear preguntas y dudas a la enfermera. Por ello es fundamental que el personal de enfermería cuente con una formación mínima en habilidades de comunicación (necesaria tam-bién en los profesionales médicos) que les permita empatizar con la familia y el paciente y emplear técnicas básicas de counselling en su comunicación con ellos.
A esta primera fase de transmisión de información diagnóstica le sigue la acogida en la uni-dad de hospitalización. Es conveniente que la habitación esté perfectamente acondicionada para
M. DIE TRILL Y F. MUÑOZ TORRES

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
el ingreso del niño y la acogida de sus padres con el fin de ofrecer una sensación de control y de seguridad. La enfermera referente que estuvo presente en el momento de transmisión del diag-nóstico, y la auxiliar de enfermería referente del paciente, recibirán a éste y a su familia en la uni-dad. Estos profesionales deben adecuar su tiempo para repetir toda la información médica que precisen el paciente y la familia. Deben asimismo, ofrecer información sobre la dinámica de la uni-dad hospitalaria: los horarios; la recogida de datos y confidencialidad; las comidas y alimentación adecuadas; los balances; la disponibilidad de otros servicios complementarios; la disponibilidad de otros profesionales, de personal de voluntariado y de la asistencia social que puedan requerir; etc., derivándoles a los profesionales cuyos servicios requieran en esos momentos. De nuevo la información deberá adaptarse lo máximo posible al paciente y a la dinámica familiar, y debe ser también sencilla y clara, repitiéndose y reforzándose en días posteriores.
La primera entrevista con el personal de enfermería debe incluir una valoración del funcio-namiento psicosocial del niño y de la familia. Dicha entrevista debería incluir los siguientes aspec-tos (Die Trill, 2000):
Tabla 2. Aspectos psicosociales a valorar durante la primer encuentro con el personal de enfermería de referencia
ASPECTOS PSICOSOCIALES A VALORAR DURANTE EL PRIMER ENCUENTRO CON EL PERSONAL DE ENFERMERÍA DE REFERENCIA
ASPECTOS PSICOSOCIALES RELACIONADOS CON LA FAMILIA Y SU ENTORNO SOCIAL
• Composición y funcionamiento familiar (relaciones entre los miembros, dificulta-des intergeneracionales, coaliciones entre diferentes miembros, rol del enfermo en la familia, etc). Hacer un genograma
• Bagaje cultural y creencias religiosas• Experiencia previa con enfermedades y pérdidas• Actitudes de la familia ante la enfermedad• Preocupaciones y temores• Sistemas de apoyo• Impacto de la enfermedad en los hermanos del paciente• Historia psicológica o psiquiátrica familiar, incluyendo historia de adicciones
PERFIL DE DESARROLLO BIOLÓGICO DEL NIÑO:
• Crecimiento: desarrollo físico y psicológico• Resultados de posibles evaluaciones neurológicas o psicológicas previamente
realizadas
VALORACIÓN PSICOLÓGICA DEL NIÑO:
• Funcionamiento psicológico premórbido y actual• Forma de actuar ante las dificultades• Historia psicológica o psiquiátrica personal• Estado psicosocial actual: temores, preocupaciones, sentimientos en torno a la
enfermedad, los tratamientos y el ingreso hospitalario; patrones de alimentación y sueño; comportamiento
• Necesidades emocionales del niño• Juegos y actividades favoritos• Entendimiento que tiene de la situación médica

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
El juego debe constituir un componente principal de la entrevista inicial infantil dado que la manipulación de objetos simbólicos puede ser una de las mejores maneras de obtener informa-ción acerca del funcionamiento afectivo y cognitivo del paciente infantil. Además, en muchas oca-siones, el niño con una enfermedad grave no tiene deseos de hablar pero sí de manipular deter-minados juegos y juguetes. Las preguntas directas deben realizarse con tacto. Comparen: “¿Tienes miedo de algo?” con “Algunas veces los niños que están enfermos y se encuentran en el hospital se asustan de ciertas cosas. Me estaba preguntando qué cosas te asustan a ti?” (Die Trill, 2003).
No hay que olvidar que la llegada a la Unidad de Oncología y el encuentro con otros pacien-tes oncológicos infantiles y adolescentes vuelve a constituir una fuente significativa de estrés, de desánimo y de tristeza, constituyendo éste otro de los momentos críticos en el abordaje del paciente infantil con neuroblastoma y de su familia. La valoración de aspectos psicosociales del niño y de la familia por parte del personal de enfermería va a transmitir un interés significativo por aspectos no médicos del niño, contribuyendo a una acogida más humana.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
3.4. CÓMO HABLAR CON LOS NIÑOS Y ADOLESCENTES GRAVEMENTE ENFERMOS
EL DESARROLLO EVOLUTIVO DE LOS CONCEPTOS DE ENFERMEDAD Y MUERTE
La humanización del cuidado en oncopediatría parte de la base de una comunicación eficaz con el paciente y su familia. No se pueden valorar las necesidades del pequeño enfermo ni de sus familiares adecuadamente a no ser que se establezca un vínculo terapéutico basado en la com-prensión, la confianza y la empatía. De ahí la importancia significativa de contar con pequeñas habilidades básicas de comunicación. El personal de enfermería está en primera fila en el cuidado del niño, y de ahí que sean estos profesionales en muchas ocasiones, los primeros en detectar ma-lestar emocional y necesidades no cubiertas del paciente o su familia.
Para poder comunicarnos con eficacia en oncopediatría, es necesario conocer cómo los ni-ños van aprendiendo a comprender los conceptos de enfermedad y muerte. Los niños alcanzan un entendimiento de ambos, enfermedad y muerte, en diferentes etapas, a través de un proceso que depende de su nivel evolutivo y madurez cognitiva y de factores socio-culturales y familiares, más que de su edad cronológica. Generalmente, entre los dos y los cinco años los niños comienzan a aprender lo que es la enfermedad, y entre los ocho y los diez años los niños poseen una noción madura de lo que significa morir, entendiendo la muerte como un hecho universal, irreversible y permanente. Los niños con enfermedades graves son conscientes de la gravedad de su condición a partir de los cinco años, incluso aunque nadie se lo haya comunicado, ya que observan los cam-bios que el cáncer produce en su cuerpo y las reacciones de sus familiares y de otros adultos de su alrededor (Die Trill, 1997, 1998, 2003).
Mientras que un niño entre los cero y los dos años no tiene la capacidad para comprender que está gravemente enfermo, aunque reacciona ante el dolor y la separación de sus progenito-res, a partir de los dieciocho meses el desarrollo lingüístico ha sido tal que a partir de los cuatro o cinco años comprende la mayor parte de lo que se le comunica, disfruta tomando decisiones por sí mismo y sientiéndose autosuficiente. Ya comienza a formarse algunas ideas acerca del funcio-namiento del cuerpo: aprende a nombrar sus partes principales, y a menudo conoce la localización del corazón y del estómago. También comienza a interpretar las señales que le envían las personas de su entorno acerca de cómo debe responder a la enfermedad. El cáncer en esta etapa se vive como algo causado por hechos o agentes externos, por ejemplo, accidentes.
M. DIE TRILL Y F. MUÑOZ TORRES
MK de casi cuatro años, al que se había diagnosticado un neuroblastoma. Al preguntarle a MK por el conocimiento que tenía de su enfermedad, indicó que tenía “… una piedra que se me ha metido en la cabeza”, aunque no entendía bien cómo había podido ocurrir esto (!), pues su capacidad de abstracción
estaba limitada debida a su nivel evolutivo.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
Entre el quinto y noveno año, el niño entiende que la enfermedad está causada por gérme-nes u otras fuerzas externas y comienzan a adquirir un entendimiento de las causas internas de la enfermedad. Comprenden que los organismos muertos no sólo permanecen inmóviles sino que también desaparecen. Piensan que la muerte es selectiva, y que solo afecta a los ancianos. Fan-tasía y realidad se confunden en la mente del niño, de modo que no es sorprendente que ahora relacione la muerte con el sueño, con un ser supernatural (p.e., un ángel o un espíritu), o que se personifique (Spinetta, 1974). Un adolescente gravemente enfermo se cuestiona el sentido de la vida, necesita ser escuchado y sus opiniones, creencias y rituales religiosos deben ser siempre respetados.
PAUTAS PARA HABLAR CON NIÑOS Y ADOLESCENTES GRAVEMENTE ENFERMOS ACERCA DE SU SITUACIÓN MÉDICA
El proceso de comunicar y hablar sobre la enfermedad grave y la muerte con los pacientes constituye quizás una de las intervenciones más complejas y difíciles que soportan los profesiona-les sanitarios que requiere no solo el desarrollo de habilidades concretas, sino también un esfuerzo personal que va a enfrentar a los profesionales a sus sistema de valores y creencias así como a sus propias ideas acerca de la vida y de la muerte. El arte de la comunicación es pues, una herramienta terapeútica indispensable para todos los miembros del equipo que trabajan con niños enfermos de neuroblastoma y sus padres.
Antes de hablar con los niños acerca de su situación médica y de la muerte, se debe mante-ner un diálogo con sus padres en el que se identifiquen creencias familiares, culturales, etc, que ellos quieran que se transmitan a sus hijos. Debemos igualmente explorar la información que ellos han transmitido a sus hijos enfermos y valorar el grado de comunicación que existe entre los diferentes miembros de la familia acerca de la enfermedad, con objeto de que la intervención constituya una acción terapeútica consensuada con ellos que de ninguna manera se viva de forma hostil o como una intromisión en sus derechos como padres. Además, debe favorecerse siempre que sean los padres quienes primero y de una forma continuada, hablen con sus hijos acerca de la situación, permitiendo que éste plantee sus dudas y temores de manera natural. Para todo ello el personal de enfermería juega un papel fundamental, por ejemplo, ofreciendo pautas a los padres de cómo comunicarse con los hijos y apoyándoles en todo el proceso.
Un lugar tranquilo, sin interrupciones, seguro para el niño y lo más acogedor posible para él será fundamental. El profesional debe colocarse a la altura del niño, hacer contacto visual con él y favorecer el contacto físico. Se le debe dar la oportunidad de indicar si quiere estar o no acom-pañado y por quién. A continuación se describen pautas para hablar con los niños acerca de la enfermedad y la muerte.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
PAUTAS PARA HABLAR CON LOS NIÑOS ACERCA DE LA ENFERMEDAD Y LA MUERTE
Emplear el lenguaje del niño y responder siempre con claridad y sencillez
No esperar una respuesta inmediata; el niño necesita tiempo para elaborar la información; es necesario respetar la capacidad del niño para tolerar la conversación
Dejar al niño preguntar y comentar con libertad, sin inhibirle ni juzgarle por sus pensamientos
No evitar el uso de las palabras muerte o morir. Por el contrario, evitar el uso de eufemismos y de palabras que puedan tener significados alternativos para el niño
Incorporar las creencias religiosas y sistemas de valores de los padres para explicar la finalidad de la muerte
Aclarar que ni la enfermedad ni la muerte son resultado de las acciones o pensamientos del niño
Nunca mentir
Recordar que generalmente los niños tienen mas información acerca de su condición de lo que creen los adultos
Ayudar al niño a reconocer sus sentimientos y emociones y a nombrarlas con el objeto de ayudarle a gestionarlas eficazmente
Antes de empezar a conversar, preguntar al niño qué piensa que le ocurre, explorar sus fantasías y corregir ideas erróneas acerca de la enfermedad y de la muerte
Expresar disponibilidad para responder a cualquier pregunta, duda, preocupación o temor que pueda te-ner el niño en el momento en el que él desee plantearla.
Identificar los conocimientos médicos que ya posee el niño acerca de la dolencia, identificando la presencia de esperanzas de curación, de miedos a la muerte, etc.
Adaptar la información transmitida al nivel cognitivo del niño, empleando siempre explicaciones médicas sencillas, honestas y esperanzadoras
Recordar que en condiciones óptimas, tanto el diagnóstico como información médica adicional la debería recibir el niño de sus progenitores
Transmitir la idea de que los enfermos generalmente se recuperan. Ayudar al niño a diferenciar entre varios tipos de enfermedad (graves versus leves, gripe o catarro versus cáncer, etc.)
Hacer contacto visual y físico con el niño mientras se conversa sobre la enfermedad y la muerte, pues favo-rece la cercanía, el apoyo y la empatía.
Guiarse por el comportamiento no verbal del niño, que nos indicarán hasta dónde quieren saber, si se que-dan con alguna duda, etc.
Incorporar las creencias religiosas de la familia en las explicaciones acerca de la muerte
Transmitir esperanzas realistas
Buscar ayuda de profesionales especializados cuando se tengan dudas o dificultades de comunicación con el niño
Respetar el derecho del niño a no querer saber o hablar de su condición médica, acabando el diálogo siempre con la expresión de disponibilidad por parte del profesional de enfermería, para hablar con el niño cuando él lo necesite
Tabla 3. Pautas para hablar con los niños acerca de la enfermedad y la muerte (Die Trill, 2000; 2003)

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
3.5. EL TRABAJO PSICOTERAPÉUTICO CON EL NIÑO Y ADOLESCENTE CON NEUROBLASTOMAM. DIE TRILL Y F. MUÑOZ TORRES
El trabajo psicoterapéutico con niños y adolescentes con cáncer deben llevarlo a cabo pro-fesionales de la salud mental formados para ello. Sin embargo, la implementación por parte del personal de enfermería, de técnicas psicológicas básicas, la comunicación, y el apoyo emocional al paciente y a la familia, son fundamentales a lo largo de todo el proceso oncológico, desde el diag-nóstico hasta la supervivencia o fallecimiento del niño. No solo humanizan el cuidado, sino que fa-cilitan una adaptación óptima del paciente y de su familia al neuroblastoma y a sus tratamientos. A continuación se describen técnicas psicoterapéuticas de gran utilidad en niños y adolescentes con neuroblastoma.
PAUTAS E INTERVENCIONES PSICOTERAPÉUTICAS
• Ayudar al niño a entender el comportamiento de las personas de su entorno (por ejemplo, los lloros, la ansiedad, la irritabilidad, o la preocupación de sus padres).
• Facilitar la expresión afectiva del niño y del adolescente, ayudarle a canalizar cómo se sien-te, ésto es, permitir manifestaciones de ira, tristeza y de preocupación y facilitar el diálogo acerca de estos sentimientos, normalizándolos y encauzándolos adecuadamente. Esto re-quiere una capacidad mínima para tolerar el mundo de sus emociones. Se pueden emplear diferentes medios para facilitar la expresión afectiva, por ejemplo, un mandala en el que el niño va coloreando sus diferentes partes con colores que previamente a asociado a emocio-nes concretas (por ejemplo, el verde significa esperanza, el rojo rabia, el azul tristeza, etc). A medida que el niño colorea se le puede preguntar por qué siente tristeza (si pinta en azul) y elaborar la tristeza a partir de aquí, por ejemplo: “Estás usando el color azul y ese color lo has escogido para representar la tristeza… ¿Qué cosas te hacen sentir trise últimamente?… ¿Qué haces cuando estás triste? ¿Lloras? ¿Se lo dices a alguien? ¿Pides ayuda?… ¿Cómo de triste te sientes: mucho, poco…?”. En otras ocasiones, cuando el niño encuentra dificultad en expresar lo que siente, se puede facilitar la expresión afectiva a través de juegos o muñecos. Por ejemplo, se puede jugar a que un muñeco está enfermo: “¿Qué le pasa al muñeco, está enfermo?... ¿Y cómo crees tú que se siente el muñeco ahora que está enfermo?… ¿Por qué se siente enfadado?... ¿Qué cosas le dan miedo al muñeco cuando va al hospital?...”
• Favorecer la participacion activa del niño y del adolescente en el proceso de toma de deci-siones médicas y en su cuidado, siempre que ésto sea posible y no añada tensión adicional al paciente. Por ejemplo, se le puede pedir que sea él quien cuente hasta tres antes de que la enfermera le pinche para administrar un tratamiento intravenoso, o podrá escoger en qué momento durante el transcurso de media hora quiere tomarse una medicación oral o realizar algún cuidado médico o de enfermería que le resulte desagradable o doloroso. Ello aumentará su percepción de control y facilitará su colaboración con los tratamientos. En

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
el caso de los adolescentes es importante negociar siempre de este modo pues con ello se evitarán las luchas de poder que frecuentemente generan como rebelión contra la depen-dencia que produce la enfermedad (Die Trill, 2000b).
• Facilitar la continuidad en el contacto con sus amigos, con el fin de reducir el aislamiento y los sentimientos de soledad. El personal de enfermería puede facilitar las visitas de los com-pañeros de clase o amigos al hospital, así como el intercambio con otros niños de la planta.
• Mantenerse en contacto con la escuela, informando a los responsables escolares del progre-so médico del niño y esperando que éste realice sus tareas escolares con continuidad mien-tras no pueda asistir a clase. Ello contribuirá a normalizar su vida y reducirá el sentimiento de ser diferente a los demás de su edad. Es necesario tener en cuenta que el niño o adolescente pueden presentar dificultades cognitivas, secundarias a la enfermedad y/o a sus tratamien-tos, que interfieran significativamente con el rendimiento académico, por lo que las tareas escolares deberán en muchos casos, adaptarse a las capacidades del paciente evitando que sus limitaciones interfieran con un desarrollo adecuado de su auto-estima.
• Aumentar la percepción de control del paciente sobre la enfermedad, sus tratamientos y otras áreas de su vida ofreciendo alternativas, haciéndole partícipe del cuidado médico, pi-diendo su opinión y colaboración, etc. Esto es especialmente importante en el contexto de una enfermedad que reduce significativamente la percepción del niño y del adolescente sobre su vida, y su entorno. Algo tan sencillo como ofrecer alternativas para tomarse la me-dicación oral con zumo, leche o agua, puede hacerle al niño sentir que puede escoger en un entorno en el que todo gira alrededor de las recomendaciones e indicaciones médicas y de enfermería y a las normas de los padres.
• Respetar el derecho del niño a permanecer infantil. Es fácil proyectar sobre el niño deseos y expectativas que o bien son propios de niños de edad más avanzada o bien surgen de al-guna necesidad afectiva del adulto. Por ejemplo, se puede esperar que el niño se comporte siempre de forma madura ante el dolor, las pruebas médicas, el tratamiento, etc. porque le resulte más fácil al adulto ver a un niño que controla sus emociones como si fuera un adulto, que a un niño que llora y patalea durante una aspiración de médula ósea.
• El uso de terapias cognitivo-conductuales por el personal de enfermería es fundamental. Estas técnicas incluyen RELAJACIÓN HIPNÓTICA, RELAJACIÓN MUSCULAR PROGRESIVA, VISUALIZACIÓN GUIADA, MODELAMIENTO, USO DE REFUERZOS POSITIVOS Y NEGATIVOS, DESENSIBILIZACIÓN SISTEMÁTICA, AUTO-AFIRMACIONES Y PARADA DE PENSAMIENTO. Así, en el caso de un niño con dolor, estas técnicas pueden ayudar a definir el grado de tole-rancia al mismo, a identificar aquello que le ha reconfortado en otras ocasiones, y a definir el tipo de comportamientos a través de los cuales el niño expresa el dolor tales como irrita-bilidad o aislamiento, y los que sugieren una reducción de éste. Por ejemplo, si el niño va a recibir un pinchazo para la administración del tratamiento o para obtener una muestra de sangre, se le puede entrenar en alguna técnica sencilla de respiración, y se le puede guiar a través de una visualización en la que imagine que su superhéroe favorito viene en su ayuda y le presta un guante mágico que le va a convertir la sensación dolorosa en una sensación de calor o frío, según la preferencia del paciente. En estos casos nunca se debe decir que va a desaparecer el dolor, puesto que no es cierto, sino que se va a transformar en otro tipo de sensación, o se va a aliviar. En otra situación, cuando un niño debe someterse a un TAC o resonancia o va a comenzar a recibir tratamiento con radioterapia y se resiste a quedarse solo en la sala, se le puede ayudar a imaginar que está en una nave espacial y guiarle a través de un viaje al espacio a través del interfono, durante la realización de la prueba o adminis-tración del tratamiento, mientras se intercalan sugerencias de relajación, tranquilidad y de respiración diafragmática. Se pueden emplear también técnicas de distracción cognitiva, cuyo uso se ha demostrado reduce la ansiedad y las náuseas y vómitos anticipatorios a la

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
quimioterapia (Redd, Jacobsen y Die Trill, 1987). Contar en orden ascendente y descendente del uno al diez con alguien, cantar durante una prueba médica, contar cuentos a medias con la enfermera o fijar la vista en un punto son técnicas sencillas que les ayudan a alejar la aten-ción de un síntoma o de un procedimiento doloroso o incómodo. Emplear un matasuegras mientras se obtiene una muestra de sangre ayuda a centrarse en la respiración, ofreciéndole al niño órdenes de soplar más o menos fuerte hasta alcanzar la nariz o dedo de su madre, que puede colocarse en frente del paciente, ayuda a reducir la ansiedad que se siente antes del pinchazo. El comportamiento del niño/adolescente en el hospital o clínica siempre debe ser reforzado con un caramelo, alabanzas a cómo se ha portado, pegatinas, etc. Incluso cuando un niño llora durante una prueba médica o se resiste inicialmente a ella, se debe reforzar su intento de realizarla y el hecho de haber pasado por ella. Nunca debe castigarse ni juzgarse la falta de colaboración. La desensibilización sistemática consiste en exponer gradualmente (en imaginación o en vivo) al paciente al estímulo o situación temida después de haberse inducido un estado de relajación. Por ejemplo, en el caso de un procedimiento médico dolo-roso, se le puede ayudar al niño primero, a que se imagine dicho procedimiento; después se le puede pedir que él lo administre a su peluche o muñeco favorito, y finalmente se le ayuda a ensayar el comportamiento durante una simulación del procedimiento en la misma sala en la que éste se vaya a administrar (Arteaga y Die Trill, 2000). En cuanto a las auto-afirmaciones positivas, se le puede instruir al niño en una serie de auto-afirmaciones que ellos mismos pueden repetirse y decirse a sí mismos cuando sientan dolor o miedo, por ejemplo: “Yo voy a poder con eso… Esto va a terminar pronto… Esto me va a ayudar a curarme…”. Generalmente se combina con la técnica de parada del pensamiento en la que se instruye al niño o adoles-cente a decirse a sí mismo “PARA” cuando empiece a pensar en el miedo o la angustia que le invade, y seguir inmediatamente después con autoverbalizaciones positivas.
• Utilizar el valor terapéutico del juego y el dibujo (Die Trill, 2000). Por medio del lenguaje sim-bólico de los dibujos (los colores, los motivos y los temas), y a través del juego, los niños pro-yectan sus miedos, sus fantasías y sus preocupaciones en torno a la enfermedad y la muerte, su ira, su tristeza, su ansiedad, sus deseos y sus esperanzas (Adams-Greenly 1989). La psi-coterapia con adolescentes se acerca más a la psicoterapia con adultos donde la palabra (o su ausencia, en el caso de los silencios) es el vehículo que guía el proceso terapéutico. No obstante, no debemos desechar la posibilidad de utilizar técnicas artísticas de potencial expresivo en adolescentes enfermos o incluso el juego en aquellos más jóvenes. Figuras de animales o personas; materiales de arte y dibujo; un conjunto de material médico; libros que relaten historias con las que el niño pueda identificarse; diarios o cartas al psicoterapeuta o a su peluche favorito; e historias incompletas son empleadas con eficacia en este contexto. En los casos en los que el paciente se encuentre demasiado cansado, deprimido, paralizado por el miedo, tenga dificultades para formar palabras o tenga limitaciones físicas que le impidan verbalizar, puede utilizarse la técnica del monólogo del terapeuta en la cual éste articula en alto lo que cree que piensa o siente el niño. El niño escucha las palabras que no puede decir enmarcadas en un contexto seguro, y se puede sentir comprendido y aliviado. Estos efectos terapéuticos se manifiestan con frecuencia dramáticamente a través del lenguaje corporal o de la conducta del paciente enfermo. El paciente sólo necesita escuchar o responder “Sí” o “No” a las preguntas que pueda formularle el terapeuta (Sourkes, 1998). El uso de música, películas, etc. Es igualmente terapéutico.
• No descartar la participación del niño o adolescente en terapias psicológicas por un psicoon-cólogo, especialmente cuando haya problemas específicos que se puedan beneficiar de ellas. Para ello es fundamental que el personal de enfermería conozca cuáles son las reac-ciones “normales” y adaptativas al proceso oncológico y cuales son desadaptadas o psicopa-tológicas, con el fin de que pueda realizar la derivación pertinente. Existen en la actualidad múltiples modalidades de psicoterapias que pueden facilitar la adaptación psicológica del paciente. La aplicación de una o de otra variará en función de las necesidades cambiantes

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
del paciente durante el curso de la enfermedad y del objetivo terapéutico. Así, las terapias de grupo sirven para fomentar el apoyo emocional, entrenar en habilidades sociales, favorecer el intercambio social, debatir cuestiones relacionadas con la enfermedad tales como dificul-tades escolares, familiares o personales, y para proporcionar información médica (Die Trill, 2003). Sería en estos casos, muy beneficioso para los pacientes contar con la participación de un miembro del personal de enfermería que colabore con el psicooncólogo y conduzca el grupo como co-terapeuta. Las psicoterapias familiares son necesarias por el impacto que tiene la enfermedad infantil en los diversos miembros de la familia, entre otras cosas. Las psicoterapias individuales de apoyo se emplean para explorar los temores y preocupaciones del niño o adolescente, aclarar malos entendidos y facilitar la expresión de sentimientos a la vez que se proporcionan pautas pata mejorar la adaptación psicosocial del paciente in-fantil a su enfermedad. La terapia de pareja dirigida a los padres del niño enfermo es con frecuencia, útil para abordar psicoterapéuticamente, las diferencias en el enfrentamiento a la enfermedad o a la inminente pérdida del niño y las consecuencias que ésto tiene sobre el funcionamiento de la pareja.
• Administrar psicofármacos y analgésicos siempre y cuando sea necesario por ejemplo en el caso de depresiones, ansiedad, dolor o trastornos orgánicos mentales. Transmitir a los padres del paciente la información necesaria para que acepten la administración de estos fármacos necesarios para el confort del paciente. Complementarlos con la aplicación de técnicas psi-cológicas. Por ejemplo, el entrenamiento en técnicas cognitivo-conductuales contribuye a aliviar la experiencia dolorosa. Mecer y acariciar puede aliviar el dolor en niños pre-verbales. La desensibilización sistemática, la distracción cognitiva y el refuerzo de conductas adaptati-vas son útiles en niños entre los dos y los siete años. A partir de los 8 años los niños se pueden beneficiar de técnicas psicoterapéuticas que además de las anteriores, incluyan la distrac-ción cognitiva y visual, ejercicios de relajación y respiración, el uso de cuentos y ejercicios de contar (Die Trill, 2003).
El personal de enfermería debe ser conocedor de las estrategias psicoterapéuticas básicas que ayuden a disminuir significativamente el impacto emocional negativo que suponen el diag-nóstico, los tratamientos y la hospitalización, y que faciliten la adherencia terapéutica al trata-miento y la adaptación emocional a todo el proceso oncológico.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
3.6. CÓMO TRABAJAR CON LA FAMILIA DEL NIÑO Y ADOLESCENTE CON NEUROBLASTOMAM. DIE TRILL Y F. MUÑOZ TORRES
INTRODUCCIÓN
El cáncer es una enfermedad familiar, afecta a todos los miembros de una familia de dife-rentes maneras, y tiene una connotación especial en el caso de pacientes pediátricos. Un diag-nóstico de neuroblastoma nunca deja indiferente a ningún miembro de la familia del pequeño paciente. La familia constituye el soporte que proporciona estabilidad y seguridad física y emo-cional al paciente. De ahí la importancia de poder identificar y atender a las necesidades de sus familiares a lo largo del proceso médico. La ayuda psicológica a la familia del paciente cumple dos funciones básicas. En primer lugar, contribuye y favorece el bienestar de la familia, y en segundo lugar, permite que la familia, si está adecuadamente atendida, pueda cuidar del niño de manera óptima. El primer paso es pues, establecer un vínculo terapéutico con los padres. Sin este vínculo, será imposible trabajar con los enfermos. La identificación previa de la dinámica familiar, de los conocimientos médicos y recursos con los que cuenta la familia permitirá adaptar la intervención psicológica a las necesidades de cada familia. A continuación, se ofrecen pautas concretas para que el personal de enfermería proporcione apoyo emocional a los padres y con los hermanos del niño diagnosticado con neuroblastoma.
PAUTAS PARA TRABAJAR CON LOS PADRES DEL PACIENTE CON NEU-ROBLASTOMA
• Reforzar el sentimiento de competencia de los padres para ayudar a su hijo durante las dife-rentes fases de la enfermedad. Ello evitará los sentimientos de culpa por tener un hijo grave-mente enfermo y el temor a no poder cuidar de él adecuadamente.
• Asegurar a los padres de que van a poder acompañar a su hijo en la mayoría de las inter-venciones, durante todo el tiempo que dure el proceso médico. Es frecuente que los pro-genitores teman no poder realizar este acompañamiento eficaz a su hijo al comienzo de la enfermedad. Con frecuencia temen volverse locos, no poder con la carga emocional que su-pone tener un hijo gravemente enfermo y posiblemente perderlo, o claudicar antes de que finalice el tratamiento médico.
• El personal de enfermería debe asegurarse de que la familia ha entendido y procesado la in-formación médica administrada de manera correcta, aclarando posibles dudas y reforzando de manera continuada, la transmisión de información que se les va suministrando en cada momento de la evolución de la enfermedad, aclarar posibles dudas y reforzar información previa.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
• Informar siempre a los padres de los síntomas tanto físicos como psíquicos que puedan ir desarrollándose en el niño a medida que avanza la enfermedad, con el fin de que puedan anticiparlos, reduciéndose así, parte de la angustia generada por la incertidumbre a la que se enfrentan.
• Recordar siempre que parte de la labor de enfermería es ayudar a los padres a tomar con-ciencia del papel protagonista que tienen en el cuidado y bienestar emocional de su hijo. Esto ayudará a reducir el sentimiento de impotencia ante la situación y reforzará el vínculo con el equipo sanitario.
• Facilitar la participación activa de los padres en los cuidados del niño, ya sea con la adminis-tración de tratamientos, el cambio de vendajes, o cualquier otra actividad que ellos puedan aprender a realizar. Su entrenamiento en el uso de técnicas cognitivo-conductuales para que las puedan practicar con su hijo (p.ej., relajación hipnótica) es asimismo, importante, ya que no solo contribuye a reducir los niveles de ansiedad del niño, sino la suya propia.
• Identificar el proceso afectivo de los padres e intentar desactivar sentimientos que no sean adaptativos, por ejemplo, los sentimientos de culpa que en muchas ocasiones desarrollan por no haber detectado antes la enfermedad o sentirse responsables de su diagnóstico.
• El personal de enfermería debe asegurarse de que los padres tienen las competencias nece-sarias para cumplir el régimen terapéutico. Para ello deben monitorizar a la familia durante todo el proceso de enfermedad, identificando y reforzando aquellas áreas en las que la fami-lia encuentre más dificultades para adherirse al tratamiento médico recomendado.
• El personal de enfermería debe valorar el impacto social y económico que supone la enfer-medad para el núcleo familiar, informando en todo momento de los recursos disponibles y facilitando el acceso a los servicios sociales existentes en cada comunidad sanitaria.
• El personal de enfermería debe igualmente valorar la aparición de posibles problemas en la pareja secundarios o acentuados por la enfermedad, con objeto de proporcionar la ofrecer la ayuda disponible en el centro sanitario e intentando que estos conflictos no interfieran en la comunicación con el personal sanitario o en la implementación de los tratamientos médicos y psicológicos que el niño necesite.
• Debe vigilarse la posible aparición de claudicación familiar ante procesos largos y dolorosos que exigen un elevado nivel de esfuerzo físico y emocional. Para ello se fomentarán los perio-dos de descanso y informará de la ayuda existente por parte de asociaciones y fundaciones, voluntariado, aula educativa, etc.
• El personal de enfermería debe asegurarse de que la familia cuenta con los recursos necesa-rios para el manejo de síntomas cuando el niño está en casa, proporcionando y asegurando la continuidad de la atención, facilitando un teléfono de contacto con el hospital y propor-cionando un seguimiento por parte del Servicio de Atención a Domicilio u otros recursos disponibles en la Unidad.
• Informar de recursos disponibles tanto en el hospital como en la comunidad, que faciliten la reintegración social, familiar, personal y académica del pequeño paciente una vez finalice los tratamientos.
• Reuniones con psicooncólogos que colaboren con el personal de enfermería pueden ayudar a los padres a poner en perspectiva sus vidas y las de sus familias. Asimismo, enfermería y psicología pueden proporcionar información acerca de cómo manejar situaciones concretas en la familia que surgen a consecuencia del desequilibrio que produce la enfermedad, y ayu-

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
dan a balancear los cuidados que la familia proporciona al enfermo con otras responsabilida-des personales y familiares.
En el caso de que la enfermedad progrese y el fallecimiento sea inminente:
• Proporcionar la información y apoyo necesarios para que los padres puedan anticipar el lugar donde prefieren que tenga lugar el fallecimiento del niño en el caso de que la enfermedad progrese y la muerte sea inminente. Explicarles detenidamente los beneficios y desventajas de proporcionar los últimos cuidados tanto en la casa como en el hospital. Siempre y cuando no haya limitaciones impuestas por la enfermedad, los padres deben sentirse libres para po-der escoger su preferencia.
• Permitir un grado adecuado de alejamiento emocional entre los padres y su hijo moribundo antes del fallecimiento que facilite el duelo posterior sin generar sentimientos de abandono en el paciente.
• Facilitar la presencia de los padres en el momento de la muerte. En caso de no haber sido posible, explicarles en detalle cómo ha ocurrido con el fin de facilitar el duelo posterior.
• Conocer y respetar las creencias religiosas de los padres y sus deseos de practicar cualquier tipo de tradiciones o rituales en torno a la muerte del niño.
• Los padres del enfermo necesitan saber que la vida de su hijo, una vez finalizada, ha sido importante. Describir las cualidades especiales del niño a sus padres, y proporcionar apoyo y recuerdos de los buenos momentos que existieron en el cuidado del enfermo.
• Proporcionar un apoyo o terapia si se necesitara, centrada en el duelo una vez se haya produ-cido el fallecimiento.
EL TRABAJO CON LOS HERMANOS DEL PACIENTE INFANTIL Y ADOLESCENTE CON NEUROBLASTOMA
• Averiguar qué conceptualización tienen los hermanos del enfermo acerca del cáncer y de su tratamiento, aclarando malos entendidos y manteniendo siempre una comunicación hones-ta y abierta con ellos.
• Explicar el porqué de la atención reducida que reciben de los padres sugiriendo a éstos que dediquen, en la medida de lo posible, unos momentos "especiales” del día o de la semana a realizar actividades con cada uno de los hermanos sanos del enfermo, de manera individual
• Fomentar las visitas de los hermanos del enfermo al hospital desmitifican el tratamiento y las admisiones hospitalarias.
• Los hermanos del paciente se benefician de una participación activa en los cuidados del en-fermo. Esto evita que se sientan apartados de la familia, y facilita que compartan su vivencia de la enfermedad.
• Evitar, siempre que sea posible, sobrecargar a los hijos sanos con responsabilidades adultas mientras los padres se dedican al cuidado del enfermo. Es preferible que éstos utilicen la ayuda de otros adultos.
• Fomentar la comunicación entre el enfermo y sus hermanos sanos así como entre los herma-nos sanos y sus padres.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
• Intentar que los hermanos del paciente limiten mínimamente sus actividades escolares y sociales, lo cual tenderán a hacer para evitar sentimientos de culpabilidad. Fomentar la inde-pendencia de los hermanos del enfermo disminuirá su identificación con éste.
• Explicar y anticipar los cambios físicos que va a sufrir el enfermo como consecuencia de los tratamientos con el fin de reducir el impacto emocional de estas alteraciones sobre los her-manos sanos.
• Organizar momentos y actividades que puedan compartir los hermanos sanos con los enfer-mos tanto durante las hospitalizaciones como cuando los niños son dados de alta.
• Disponer de personas que cuiden a los hijos sanos en la propia casa durante los ingresos hospitalarios, en lugar de llevarles a la casa de algún familiar o conocido, ayuda también a proporcionarles la continuidad en sus cuidados que la enfermedad ha interrumpido.
• Facilitar la despedida del hermano moribundo y respetar el deseo de participar en los ritua-les post-mortem en caso de fallecimiento del paciente.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
3.7. LOS PROFESIONALES SANITARIOS QUE TRABAJAN EN PEDIATRÍA ONCOLÓGICA
M. DIE TRILL Y F. MUÑOZ TORRES
CONSECUENCIAS DE TRABAJAR CON EL SUFRIMIENTO, EL DOLOR, LA ENFERMEDAD Y LA MUERTE
El enfrentamiento diario a la enfermedad grave de los niños y adolescentes, a su sufrimiento y deterioro, y a la muerte, genera con frecuencia, sentimientos de impotencia en los profesiona-les sanitarios y contribuye de una manera significativa a fomentar el enfrentamiento a la propia mortalidad. Si no se gestionan adecuadamente los cuestionamientos existenciales y las fuertes emociones que surgen de realizar la actividad diaria en estos entornos, se corre el riesgo de sufrir consecuencias que interfieren en el cuidado óptimo del paciente y de la familia. El burnout y la fatiga de compasión surgen con frecuencia en los profesionales sanitarios que trabajan en onco-pediatría y en concreto, con niños con neuroblastoma y sus familiares. Despersonalización, senti-miento de baja realización personal y agotamiento personal caracterizan al síndrome de Burnout, llevando a la falta de humanización de los cuidados que se puede tener manifestaciones físicas (cansancio, cefaleas, insomnio, problemas digestivos, asma, etc.); manifestaciones emocionales (irritabilidad, nerviosismo, hostilidad, sentimiento de fracaso o alienación, sentimientos de impo-tencia u omnipotencia, cambios de humor, tristeza y pesimismo, etc.); manifestaciones cognitivas (p.e., baja autoestima, indecisión, atención y memoria reducidas, suspicacia, hipersensibilidad a las críticas, dificultad de concentración, etc.), y manifestaciones comportamentales (conductas agresivas y de aislamiento, problemas de pareja, consumo de drogas, absentismo laboral, altera-ción en los patrones de alimentación, etc.) (Die Trill, 2018).
Por otra parte, los profesionales sanitarios que sufren fatiga de compasión pueden experi-mentar ansiedad, sentimientos de impotencia y enojo, apatía, depresión, errores en la práctica clínica, alteraciones de los biorritmos del sueño y pesadillas, pudiendo llegar a alterar gravemente la calidad de su práctica profesional y la calidad de su vida personal.
Los rasgos de personalidad y algunas variables intrapsíquicas pueden ser también fuentes de angustia para el profesional. Por ejemplo, el deseo de atender a las necesidades de todos los demás más que a las propias tendrá un impacto negativo sobre el profesional. Con frecuencia, esta actitud es generalizada y se mantiene también en las relaciones no profesionales entre los miembros del personal sanitario. Asimismo, no es poco frecuente que el profesional se convierta en un referente para familiares y amigos cuando éstos se encuentran con dificultades. En gene-ral, los profesionales suelen ser mucho más exigentes consigo mismos que con los demás. Como consecuencia, no son sólo cuidadores de sus pacientes, sino que probablemente tiendan a com-portarse como cuidadores en su vida personal cotidiana (Die Trill, 2015).
La formación de profesionales de la salud en habilidades de comunicación constituye un enfoque prometedor tanto para el cambio de actitudes negativas en el entorno laboral como para mejorar las relaciones con los pacientes. Sin embargo, el entrenamiento en habilidades de co-municación debe necesariamente ir acompañado de un ejercicio básico de introspección que el

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
profesional debe realizar, intentando encontrar respuestas honestas a preguntas básicas sobre situaciones complejas y delicadas que debe afrontar (Die Trill, 2013; 2015).
PAUTAS PARA EVITAR EL BURNOUT
Se han descrito estrategias de intervención individual, grupal y del sistema sanitario para prevenir o aliviar/reducir el burnout.
Entre las estrategias de intervención individuales se pueden incluir una formación adecuada en habilidades clínicas y de comunicación con el enfermo, con el fin de aumentar la percepción de control y eficacia del trabajo; un equilibrio entre la vida personal y la laboral; un establecimiento de metas objetivamente realistas en el entorno laboral; la práctica de técnicas sencillas de medita-ción, mindfulness y relajación durante el horario laboral; el respeto por los horarios laborales; y una mayor conciencia de nosotros mismos y de lo que sentimos ante diferentes situaciones que nos plantea la actividad laboral diaria. Así, el profesional será capaz de identificar aquellas situaciones que le impactan más y podrá buscar las formas más sanas de poder gestionarlas, sin ver compro-metida su labor asistencial. Esto requiere un mínimo conocimiento de uno mismo que permita identificar cuestiones del tipo: “¿Por qué he elegido este trabajo?... ¿Y esta especialidad?... ¿Qué experiencias previas he tenido con la enfermedad grave y con la muerte?... ¿Cómo las he gestio-nado?... ¿De qué manera influyen o se proyectan en mi trabajo actual?... ¿Qué tipo de pacientes me afectan más y por qué?”. Poder responder a estas cuestiones fomentará el auto-conocimiento y la gestión adecuada de nuestro propio flujo afectivo cuando nos enfrentamos a situaciones di-fíciles en el entorno sanitario.
Los grupos de ayuda guiados por profesionales ofrecen apoyo psicológico a los miembros del equipo y mejoran el cuidado del paciente y de su familia. El tema principal de trabajo en grupo debe centrarse en los aspectos relacionados con la labor diaria así como en las reacciones emo-cionales derivadas de ésta, los problemas que surgen y como resolverlos, y no en los conflictos o rencillas personales entre los diferentes miembros. Es importante asimismo, hacerles conscientes a los profesionales sanitarios que participen en el grupo de sus reacciones emocionales, ayudarles a encontrar nuevas formas de resolver los problemas que van surgiendo en su rutina diaria, y do-tarles de estrategias que puedan utilizar para disminuir el impacto del estrés y prevenir el burnout fomentando la cohesión y el apoyo entre los diferentes miembros del equipo. Una cuestión impor-tante sería ayudarles a buscar maneras que les permitan “cerrar” el trabajo realizado con los niños fallecidos a través de rituales o actividades que faciliten las despedidas. Por ejemplo, se pueden celebrar reuniones en las que los miembros pueden dialogar acerca de los niños fallecidos, identi-ficando los aspectos específicos al cuidado de cada paciente concreto. O por el contrario, se puede instruir a que cada miembro identifique su propia manera de “cerrar” cada caso. Ayudarles a iden-tificar los aspectos gratificantes del trabajo adquiere igual importancia (Papadatou et al., 2002).
El sistema sanitario podría facilitar cambios institucionales que favorecieran un entorno labo-ral agradable en el que el personal sanitario no se sienta quemado. Horarios flexibles, posibilidades de formación continuada y tiempo libre; jefaturas competentes que establezcan líneas directrices claras y apoyen al personal sanitario; cargas realistas de trabajo asistencial; y una clara definición de competencias y responsabilidades; son solo algunas de las actividades que deberían tener lugar de forma regular.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
CONCLUSIONES
• El diagnóstico de un neuroblastoma en la infancia y/o adolescencia tiene un impacto signifi-cativo no sólo sobre el pequeño paciente sino también sobre su familia y el personal sanita-rio.
• Los profesionales de Enfermería están un lugar prioritario para valorar las necesidades del enfermo y de su familia a lo largo de todo el proceso oncológico. Con el fin de optimizar y humanizar el cuidado es necesario contar con unas habilidades básicas de comunicación, así como con un conocimiento básico del proceso de adaptación emocional del niño a su enfer-medad y a los tratamientos. Ello implica no solo acompañar, sino también conocer e imple-mentar diferentes técnicas psicoterapéuticas adaptadas a cada niño y a cada situación, que puedan optimizar la calidad del vida del paciente y de su familia.
• El cuidado del profesional sanitario es igualmente importante, con el fin de evitar la apari-ción de un síndrome de burnout o de fatiga por compasión. La aplicación de distintas técni-cas individuales, grupales e institucionales es indispensable con el fin de facilitar que estos profesionales puedan humanizar el cuidado.
BIBLIOGRAFÍA
• Adams-Greenly M Psychosocial intervention in childhood cancer. En Holland J y Rowland J (eds) Handbook of Psy-
cho-Oncology New York: Oxford University Press, 1989:562-572.
• Die Trill M y Kovalcik R. The child with cancer: Influence of culture on truth-telling and patient care. En Surbone A y Zwit-
ter M (eds) Communication with the Cancer Patient. Information and Truth. Annals of the New York Academy of Science,
1997, 809:197-210.
• Die Trill M. Factores que influyen en el proceso de comunicación con los ninos acerca de la enfermedad y la muerte. En
M. Die Trill y E. López Imedio (eds), Aspectos Psicológicos en Cuidados Paliativos: La Comunicación con el Enfermo y su
Familia. Manual del curso a distancia: Aspectos Psicológicos en Cuidados Paliativos. Aula de Estudios Sanitarios, Madrid,
2000, pág. 117-124.
• Die Trill M El reto de enfrentarse a un cáncer infantil: Trastornos psicológicos y psiquiátricos más frecuentes y su trata-
miento. En F Gil: Manual de Psico-Oncología Nova Sidonia - Oncología, Barcelona, 2000b, pag. 109-136.
• Die Trill M Physician´s emotions in the cancer setting: A basic guide to improving well-being and doctor patient com-
munication. En A Surbone (ed) New Challenges in Communication with Cancer Patients Springer Science, 2013, pag
217-229.

ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA VOLVER AL ÍNDICE
• Die Trill M El trabajo personal del professional sanitaria en oncología: Guía básicapara mejorar el cuidado propio y el de
los pacientes. En F Gil (ed) Counselling y psicoterapia en Cáncer. Elsevier España, 2015, pag 39-44.
• Die Trill M y Redd W (1984) Aversiones condicionadas al tratamiento con quimioterapia en el paciente con cáncer. Revista
de Análisis del Comportamiento, 2:249-260.
• Die Trill M y Stuber M Psychological problems of curative cancer treatment. En Holland J (ed) Psychooncology New York:
Oxford University Press, 1998, pag. 897-906.
• Gonda TA y Ruark JE. Dying dignified. The health professional´s guide to care. Menko Park, Calif.:Addison Wesley P, Co.,
1984.
• Papadatou D, Bellali T, Papazoglou I y Petraki D Greek nurse and physician grief as a result of caring for children dying of
cancer Pediatr Nurs 2002 Jul-Aug; 28(4):345-353.
• Portella Ribeiro J, Calcagno Gomes G, Buss Thofehrn M Health facility environment as humanization strategy care in the
pediatric unit: systematic review Rev Esc Enferm USP 2014; 48(3):527-36.
• Redd W, Jacobsen P, Die Trill M et al. Cognitive/attentional distraction in the control of conditioned nausea in pediatric
cancer patients receiving chemotherapy J Cons and Clin Psychology 1987; 55(3):391-395.
• Sourkes B Psychotherapy En Holland J (ed) Psycho-Oncology New York: Oxford University Press, 1998:946-953.
• Spinetta JJ. The dying child´s awareness of death: A review. Psych Bull, 1974, 81:256-260.
• Rojas AKA, Machuca RPA. Factores ambientales y su incidencia en la experiencia emocional del niño Hospitalizado. Rev
Ped Elec [Internt]. 2009 [citado 2013 jul. 10]; 6(1):36-54.
• Zheng DJ; Krull K, Math YC, Diller L, et al. Long Term psychological and educational outcomes for survivors of neuroblas-
tomna: A report from the Childhood Cancer Survivor Study Cancer, 11 June, 2018.

4ACTUALIZACIÓN EN NEUROBLASTOMA PARA ENFERMERÍA
MÓDULO 04
CASOS CLÍNICOS

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
HISTORIA CLÍNICA
Lactante de sexo femenino de 9 meses de edad que es remitida para estudio desde otro hos-pital por presentar masa abdominal.
Es la tercera hija de una madre sana. En la familia por parte de madre existen antecedentes de cán-cer de mama y ovario (en la cuarta y quinta década de la vida). No refiere antecedentes previos de interés.
Refiere síndrome febril prolongado, de forma intermitente durante tres semanas previas, con temperatura máxima de 39ºC, anorexia y pérdida ponderal de 1.5 Kg de peso, motivo por el cual consulta en puerta de urgencias de hospital de origen.
EXPLORACIÓN Y PRUEBAS
En el examen físico inicial el peso era de 12 kg (p > 99) y la talla 77 cm (p 98), frecuencia cardia-ca 140 lpm, frecuencia respiratoria 30 rpm, tensión arterial 116/71 mm/Hg (p > 99). Destaca un estado general afectado, palidez de piel y mucosas, con abdomen distendido. Presenta masa palpable, que ocupa casi todo hemiabdomen izquierdo, y cruza línea media extendiéndose hasta hipocondrio dere-cho, dura y adherida a planos profundos, impresiona de dolorosa. El resto de la exploración física era normal.
Se realiza evaluación inicial con ecografía que demuestra una extensa masa de márgenes lobulados que ocupa el hemiabdomen derecho, con leve sobrepaso de la línea media hacia la izquierda. Desplaza superiormente al hígado y lateral al páncreas, aorta, tronco celíaco y arteria mesentérica. Parece comprimir el riñón derecho, desplazándolo medial e inferiormente, aunque no se puede descartar que dependa de él.
Engloba la vena cava inferior extrahepática, ejerciendo efecto de masa sobre su calibre. No identificamos trombosis. Es sólida, de ecogenicidad heterogénea con múltiples calcificaciones y muy vascularizada. Se observa otra lesión de similares características ecográficas localizada en el hilio renal izquierdo, sin poder identificar con claridad su continuidad con la masa descrita. No se identifican las glándulas suprarrenales.
Se realiza estudio bioquímico donde destaca anemia con Hb 6.8 mg/dl, con intensa reticu-locitosis, ferritina 959 ng/ml (VN 20-200), enolasa 1.380 ng/ml (VN < 20), LDH 6.947 U/L (VN < 300), catecolaminas en orina, Dopamina 1.046 mcg/gr Creat (0-1220), Ácido Vanilmandélico 34 mg/gr Creat (0-13), Ácido homovanílico 48 mg/gr Creat (5.4-15.5).
En RMN abdominal se demuestra extensa masa que ocupa el hipocondrio y el flanco derecho,
CASO 1. Niña de 9 meses con masa abdominal
M. BERMÚDEZ

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
parte del epigastrio y mesogastrio, y cruza la línea media hasta el flanco izquierdo. Mide 9.1 x 9.8 x 12 cm (AP x T x CC). Engloba la aorta regional, la salida del tronco celiaco, de la arteria mesentérica, y las arterias renales. Ejerce efecto de masa sobre la vena cava inferior, de morfología filiforme en el hilio hepático, y desplaza anteriormente a la vena renal derecha. Presenta calcificaciones y tras la administración de contraste i.v. realza homogéneamente el componente no calcificado. No se consigue identificar la glándula suprarrenal derecha.
Figuras 1. RMN abdominal
Se realiza gammagrafía con MIBG donde se observa hipercaptación heterogénea del traza-dor, de intensidad leve-moderada, en hemiabdomen izquierdo, más intenso en planos posteriores. No se observan otros depósitos patológicos del trazador en resto de localizaciones.
Se somete a biopsia de la tumoración mediante biopsia percutánea con aguja gruesa y estu-dio con aspirado y biopsia de médula ósea. El estudio anatomopatológico del tumor es compatible con Neuroblastoma (pobre en estroma schwanniano) indiferenciado INPC desfavorable. La biopsia y aspirado de médula ósea de ambas crestas iliacas es negativa para tumor.
La paciente durante su ingreso continúa con fiebre de forma esporádica, continua perdien-do peso, mantiene hipertensión con difícil control farmacológico e inicia oliguria con edema de miembros inferiores. Presenta anemización en dos ocasiones de forma brusca, subsidiarias de transfusión de concentrado de hematíes que atríbuímos a hemorragia intratumoral.
Se decide iniciar tratamiento quimioterápico según protocolo “LINES-SIOPEN” por la presencia de síntomas amenazantes para la vida recibiendo un curso de carboplatino y etopósido. Se recibe posterior-mente resultado de factores biológicos demostrando amplificación homogénea de gen MYC por FISH, no delección de brazo 11q, contenido triploide ADN y SNP con alteraciones cromosómicas segmentarias.
En dicho momento la paciente se encuentra recuperándose de una neumonía intersticial por un coronavirus, tras haber sufrido síndrome febril asociado a neutropenia sin documentación bacteriana. Presenta desaparición de hipertensión, oliguria y edema de miembros inferiores.
Posteriormente se sometió a resección casi completa de tumor abdominal, megaterapia con “BUMEL”, radioterapia sobre lecho tumoral, inmunoterapia con dinutuximab y terapia diferenciadora con ácido 13 cis retinoico. El tratamiento fue aceptablemente tolerado y actualmente la paciente se en-

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
El paciente es una niña de 5 años con una historia reciente de dolor en fosa iliaca derecha, febrícula y vómitos.
EXPLORACIÓN Y PRUEBAS
La palpación describe una masa abdominal indolora que ocupa el flanco derecho.
El estudio de RNM muestra una masa en glándula suprarrenal derecha que aparentemente se extiende al hilio renal y borde hepático.
Las catecolaminas son normales, la LDH presenta niveles de 1.660 UI/L. Existe captación tu-moral de MIBG-I123.
El estudio de extensión de medula ósea es normal.
Rx de tórax normal.
DIAGNÓSTICO
Neuroblastoma localizado estadio IIB se realiza resección quirúrgica de la masa.
Se remiten a nuestro laboratorio dos secciones tumorales para estudio molecular.
Las secciones histológicas corresponden a estos fragmentos.
CASO 2. Niña de 5 años con una historia reciente de dolor en fosa iliaca derecha
S. NAVARRO

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Anticuerpo Ø + ++ +++
NSE +++
HNK-1 +
S-100 Ø
CD-99 Ø
NB-84 +++
P-53 +
BCL-2 +++
Myc-n ++
KI-67 +++
TOP II-a +++
WT-1 Ø
CK(AE1-AE3) Ø
MYOD-1 Ø
MYOGENINA Ø
DESMINA Ø
CD-45 Ø
CD-20 Ø
CD-3 Ø
NEUROBLASTOMA CON AMPLIFICACIÓN DE MYCN
PCR

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Deleción de 1p36 Anaplásicoa1s2: MNA. (1p-,+17q). FSCA-10q
Ploidía
Confirmación del diagnóstico
• Neuroblastoma pleomórfico anaplásico
• Neuroblastoma indiferenciado de la clasificación INPC histopronóstico desfavorable
Diagnóstico diferencial
• WILMS WT-1(+), NB-84 (ø)
• T. Germinales αFP, PLAP, HCG, OCT-4
• Rabdomiosarcomas MyoD-1, Miogenina, Desmina
• Linfoma CD-45, ALK-1, CD-20, CD-3, etc.
• Feocromocitoma Cromogranina (+), Myc-n (ø)

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
FACTORES PRONÓSTICOS DE LOS TUMORES NEUROBLÁSTICOS
Edad: < 1 año (F)
Estadio: INSS
Factores biológicos:
• Expresión TrKA (F)
• Expresión TrKB (D)
• Amplificación de N-MYC (D)
• Diploidia/Tetraploidia (D)
• Triploidía (F)
• Ganancias/pérdidas cromosómicas: 1p-/11q-/14q-/17q+ (D)
Factores histopatológicos: Clasificación INPC (Sistema Shimada)
G.M. Brodeur. Nature Rev 2003; 3:203-216.
IMK Indiferenciado Pobremente diferenciado En diferenciación
Bajo D F F
Medio D F F
Alto D D D
INPC. Categorización, IMK, Edad
IMK Indiferenciado Pobremente diferenciado En diferenciación
Bajo D D F
Medio D D D
Alto D D D
IMK Indiferenciado Pobremente diferenciado En diferenciación
Bajo D D D
Medio D D D
Alto D D D
GNB EM (entremezclados) y GN (ganglioneuromas) - cualquier edad - F
IMK: Índice Mitosis Cariorrexis ; D: Desfavorable; F: Favorable
NB edad < 1,5 años
NB edad 1,5-5 años
NB edad > 5 años

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
CONCLUSIONES
• El fenotipo anaplasico-pleomorfico aparece también en casos de tumores neuroblásticos lo-calizados y confiere mal pronóstico
• El estudio de amplificación de MYC-N y de sobreexpresión de Myc-n posee valor no solo pro-nóstico sino que también ayuda en el diagnostico diferencial con otros tumores pleomorfi-cos de la infancia
BIBLIOGRAFÍA
• Harms D, Wilke H (1979). Neuroblastom-grading Klin Padiatr 191:228-233.
• Cozzutto C, Carboni A (1988). Pleomorphic (anaplastic) neuroblastoma. Arch. Pathol. Lab. Med. 112:621-625.
• Chatten J (1989). Anaplastic neuroblastomas. Arch . Pathol. Lab. Med. 113:9-10.
• Dehner LP (1989). Anaplasia in solid malignant tumors of childhood. Arch. Pathol. Lab. Med. 113:11-12.
• Cozzutto C, Cornaglia-Ferraris P (1991). Pleomorphic (anaplastic) neuroblastoma in nude mice. Arch. Pathol. Lab. Med.
115:68-73.
• Cowan JM, Dayal Y, Schwaitzberg S, Tischler AS (1997). Cytogenetic and immunohistochemical analysis of an adult ana-
plastic neuroblastoma. Am. J. Surg. Pathol. 21(8):957-63.
• Shimada H, Chatten J, Newton W (1984). Histopathologic prognostic factors in Neuroblastoma tumors: definition of
subtypes of Ganglioneuroblastoma and an age-linked classification of neuroblastomas. JNCI 73:405-416.
• Seeger R, Brodeur G, Shater H et al. (1985). Association of multiple copies of N-myc oncogene with rapid progression of
neuroblastoma. New Engl. J. Med 313:1111-1116.
• Caron H (1995). Allelic loss of chromosome 1 and additional chromosome 17 material are both infavorable prognostic
markers in neuroblastoma. Med. Pediatr. Oncol. 24:215-221.
• O Burgues, S Navarro, R Noguera, et al. (2006). Prognostic value of the International Neuroblastoma Pathology Classi-
fication in Neuroblastoma and comparison with other prognostic factors: a study of 182 cases from theSpanish Neuro-
blastoma Registry, Virchows Arch 449:410-420.
• S Navarro, G Amann, K Beiske, et al. (2006). Prognostic value of the International Neuroblastoma Classification in loca-
lised resectable peripheral neuroblastic tumors. A histopathologic study of LNESG 94.01 trial and protocol, J Clin Oncol,
24;695-699.
• S Navarro, R Noguera, A Pellín, et al. (2000). Brief Report: Pleomorphic anaplastic neuroblastoma. Medical and Pediatric
Oncology 35:498-502.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
CASO 3. Niña de 4 años de edad conepisodios de retención de orina en las últimas semanas
MOTIVO DE CONSULTA
Niña de 4 años de edad que acude a consulta refiriendo episodios de retención de orina en las últimas semanas.
EXPLORACIÓN Y PRUEBAS
Se solicita ecografía abdominal.
C. SANGÜESA NEBOT
Masa abdominal sólida retroperitoneal por delante de la bifurcación de los vasos iliacas hete-rogénea con múltiples y pequeñas imágenes ecogénicas correspondientes a calcificaciones.
Hallazgos de tumoración compatible con neuroblastoma del órgano de Zuckerkandl.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Pruebas de laboratorio:
• Enolasa: 60,15 ng/mL
• Catecolaminas en orina: normales
• LDH: 467 U/L
Otras pruebas de imagen:
• Se realiza estudio de RM para estudio local de la tumoración
RM muestra masa (flechas blancas) con captación irregular de contraste. Arterias iliacas (flechas discontinuas) rodeadas en más de un 50% de su circunferencia, por tanto criterio IDRF. Estadio L2.
• Estudio de extensión con MIBG + SPECT
Resulta negativo.
• Dado la negatividad se realiza estudio de PET-TC
La tumoración presenta una avidez por la FDG.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
Estudio histológico:
Biopsia percutánea de la masa: ganglioneuroblastoma nodular con pequeño nódulo consti-tuido por neuroblastoma en diferenciación.
• MKI bajo
• Nmyc no amplificado
• Médula ósea, biopsia sin infiltración
DIAGNÓSTICO
Neuroblastoma riesgo intermedio, grupo 7.
TRATAMIENTO
• Estadio L2 dado que presenta al menos un criterio IDRF
• MIBG negativo
• Realización del PET-TC que muestra avidez por FDG
• Ganglioneuroblastoma nodular

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
HISTORIA CLÍNICA
Niño de 3 años, remitido del Hospital Universitario de Puerto Real para estudio de masa ab-dominal. La familia refiere que hace 6 días inicia cuadro de dolor abdominal inicialmente intermi-tente y luego continuo sin deposiciones líquidas ni vómitos. Previamente había presentado dolor en hipocondrio izquierdo en las semanas previas cuando se tiraba a la piscina, sin otra focalidad. Desde hace 6 días presenta fiebre, con una temperatura máxima 39.2ºC, no presenta cuadro cata-rral ni otra sintomatología. En cuánto al peso, ha perdido 1 kg en la última semana.
Embarazo normal, controlado, parto con cesárea a término. No presenta incidencias en el periodo neonatal y mantiene un desarrollo psicomotor normal. Está en seguimiento de asma infantil en el Hos-pital de Getafe por el servicio de neumología. Asma infantil en seguimiento en Neumología en Getafe. No tiene ingresos hospitalarios y ni alergias conocidas previamente. El calendario vacunal lo lleva al día.
Los padres del paciente no tienen antecedentes patológicos de interés. Aún así, hay antece-dentes de cáncer de mama, próstata y colon en abuelos y tíos del niño.
EXPLORACIÓN Y PRUEBAS
Se queda ingresado para estudiar la situación, iniciándose sueroterapia a 100% de necesi-dades basales, antibioticoterapia y se inicia dieta de catecolaminas para recogida de orina. En la ecografía se observa una masa retroperitoneal. En el TAC de tórax no se haya nada significativo pero en el de abdomen, se observa una masa extensa en flanco izquierdo. En la RNM, se observa que hay un factor de riesgo al englobar el hilio renal izquierdo correspondiendo a un estadio L2. En la gammagrafía se observa que hay extensión localizada a hemiabdomen izquierdo.
DIAGNÓSTICO
Finalmente, se diagnostica neuroblastoma retroperitoneal izquierdo de alto riesgo y se deci-de comenzar con su tratamiento.
TRATAMIENTO
Durante la infusión de quimioterapia, presenta una reacción alérgica secundaria a la admi-nistración de etopósido. Esta se resuelve, y se decide continuar con la infusión sin incidencias a una velocidad reducida.
CASO 4. Niño de 3 años con masa abdominal
Á. MIGUEL PELLÓN, L. M. ROMERO PINILLA Y M. CANTOS MUÑOZ

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
CASO 5. Niña de 7 años con neuroblasto-ma de alto riesgo con metástasis óseas y en médula ósea
HISTORIA CLÍNICA Y SITUACIÓN ACTUAL
Niña de 7 años diagnosticada de neuroblastoma de alto riesgo con metástasis óseas y en médula ósea. Inicia quimioterapia de inducción. En remisión completa metastásica tras adminis-tración. Reducción de la masa tumoral, realizándose cirugía sin complicaciones postoperatorias a destacar.
Tras completar la terapia de inducción en el hospital de su ciudad, trasladada a la Unidad de Trasplantes para aféresis y autotrasplante de progenitores hematopoyéticos como consolidación del tratamiento de su enfermedad de base. Portadora de Port-A-Cath con buen funcionamiento del mismo.
PAUTAS DE INTERVENCIÓN EN LA UNIDAD DE TRASPLANTE
Se inicia movilización previa extracción de progenitores hematopoyéticos de sangre perifé-rica con G-CSF cada 24h subcutáneo durante cuatro días. Canalizado para procedimiento catéter femoral con dos luces. Escasa movilización. Se pospone recolecta y se retira catéter femoral.
Para segundo intento de aféresis, colocación de catéter Hickman y administración de G-CSF y Plerixafor. Se crioconservan dos bolsas.
Nuevo ingreso en la unidad para iniciar acondicionamiento con busulfán y melfalán, previa prehidratación para este último y requiriendo poshidratación, manteniendo buena respuesta con ritmos de diuresis abundantes. Se mantiene afebril, sin signos de infección ni necesitar transfu-siones.
El día 0 se procede a la descongelación de ambas bolsas y su infusión por la luz roja del caté-ter Hickman, previa administración de premedicación. Durante la infusión elevación de la PVC que se resuelve tras diurético (administración de furosemida con buena respuesta).
En los días postrasplante, el paciente se encuentra inapetente. Comienza pérdida de peso. Se coloca sondaje nasogástrico como primera opción por riesgo alto de enfermedad veno-oclusiva hepática (EVO). Se inicia nutrición enteral nocturna de 12h y seguimiento por nutrición.
En el día +5 desde la infusión aparece eritema en mucosa de cavidad bucal. Mantiene ingesta oral. En los tres días siguientes aumento de mucositis, no puede hablar y traga saliva con dificul-tad, precisando perfusión continua de morfina. Se modifica pauta a nutrición enteral de 24h.
Á. MIGUEL PELLÓN, L. M. ROMERO PINILLA Y M. CANTOS MUÑOZ

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
En el día +10, presenta ganancia de peso de 1.2 kg con respecto al peso basal al inicio del trasplante.
Se realiza ecografía abdominal sin claros criterios de EVO. Empeoramiento lento pero progre-sivo en los días posteriores con nuevo control ecográfico siendo compatible con EVO. La clínica se acompaña de hepatomegalia dolorosa, oliguria y escaso rendimiento de plaquetas.
Se inicia defibrotide intravenoso cada 6h, vigilando signos de sangrado. Requiere transfusio-nes de plaquetas cada 12h. Se lleva a cabo balance estricto por turno, con aportes hídricos restrin-gidos y forzando diuresis para conseguir balances negativos o neutros (en tratamiento con furose-mida y espironolactona). Control del perímetro abdominal y peso cada 12h.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
CASO 6. Gestión de la negación al final de la vida y sentimientos de impotencia en los profesionales sanitarios
HISTORIA CLÍNICA Y SITUACIÓN ACTUAL
María es una adolescente de 17 años. Fue diagnosticada de neuroblastoma a los 7 años y tratada en nuestro servicio de oncopediatría consiguiendo remisión de la enfermedad tras haber recibido el tratamiento protocolizado. Tres años después sufrió una recaída. Ha sido tratada con otras líneas de tratamiento en otros hospitales. Actualmente se encuentra en la fase terminal de la enfermedad.
Su familia responde a un perfil de familia cohesionada con creencias religiosas sólidas. La madre de María es su cuidadora principal estando enteramente dedicada al cuidado de su hija. Sus padres exhiben una dificultad significativa para asumir la gravedad de la enfermedad de María. Niegan la gravedad de la condición médica de su hija. Esto se manifiesta en sus solicitudes con-tinuadas por mantener a María hospitalizada así como en sus peticiones para que le administren “…todo lo que puedan darle…”. Rechazan ayuda psico-oncológica alegando que “…María es muy fuerte y vamos a salir de ésta, como en otras ocasiones”. Evitan que los profesionales sanitarios, en concreto, el personal de Enfermería, pueda estar a solas con ella y hablar sobre la situación actual o el final de su vida. María tiene una hermana menor de 14 años que apenas acude al hospital a visitarla. Los padres justifican su ausencia refiriendo que no quieren que lo pase mal viendo a su hermana enferma: “Ya tendrá tiempo para estar con ella en casa… Además, debe seguir con sus estudios”.
Tras diez años desde su diagnóstico, María está muy cansada de tratamientos, hospitaliza-ciones repetidas, procedimientos médicos y otras cuestiones relacionadas con su enfermedad. Cuando sus padres no están presentes, expresa al personal sanitario su deseo de estar en casa y pasar ahí sus últimos días; sin embargo, no transmite estos deseos a sus padres con el fin de evi-tarles sufrir.
El equipo de enfermería ha compartido muchos momentos de gran intensidad emocional con María y su familia a lo largo del tiempo y desde la confirmación de su diagnóstico, lo cual ha generado reacciones de diferente índole en los distintos profesionales. Mientras que algunos intentan evitar, en la medida de lo posible, la entrada en la habitación de María, otros han reac-cionado con profunda tristeza y con expresiones relacionadas con las injusticias de la vida. Para el equipo de enfermería las principales dificultades giran en torno a cómo gestionar la actitud de negación mantenida por los padres de María, así como conseguir que ellos acepten la situación de terminalidad de su hija y permitan y se preparen para poder despedir a María en casa, como ella quiere. La negación de los padres de María impide que el personal sanitario ponga a su disposición todos los recursos disponibles para facilitar una muerte sin dolor y sin sufrimiento. Esto provoca además, fuertes sentimientos de impotencia en los profesionales, que consideran que podrían estar prestando mejores servicios a su pequeña paciente.
M. DIE TRILL Y F. MUÑOZ TORRES

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
PAUTAS DE INTERVENCIÓN
Manejo de la negación en una situación clínica como aquella en la que se encuentran los pa-dres de María.
• ¿Hay que permitirles seguir negando la situación para protegerse del dolor o hay que inter-venir de alguna manera? En caso afirmativo, ¿cómo habría que intervenir?
La negación es un mecanismo de defensa psicológico. Los mecanismos de defensa son pro-cesos psicológicos inconscientes (esto es, la persona que niega no es consciente de que está negando) que sirven para proteger al yo de una situación amenazante. Hay diferen-tes mecanismos de defensa que empleamos todos ante situaciones dolorosas y ansiógenas, siendo la negación el más frecuente en Oncología y estando provocada ésta por la angustia que genera el enfrentamiento a la muerte. Por regla general, la negación en Oncología no se desmonta cuando no interfiere en la administración del tratamiento médico requerido. Esto es, no se confronta al paciente o a la familia con el hecho de estar negando a no ser que impida que se le administre al paciente el tratamiento médico recomendado, como ocurre en el caso descrito. En estos casos, la negación se confronta con suavidad y con respuestas empáticas. Cuando la negación no interfiere con la administración del tratamiento médico recomendado, se “deja estar” y se va desmontando por sí sola a medida que el paciente va deteriorándose y ella/su familia van tomando conciencia del deterioro y el mayor acerca-miento de la muerte.
La respuesta empática es una que permite ver la realidad desde la perspectiva del paciente/familia, desde sus experiencias, sus creencias, sus sistemas de valores, etc. La respuesta em-pática se puede aprender.
Consta de tres pasos que consisten en:
- Identificar el sentimiento que transmite el paciente/familia.
- Identificar la fuente de la emoción.
- Responder de manera que el profesional demuestre al paciente/familiar la conexión entre los dos pasos anteriores.
Para ser empático no es necesario sentir lo mismo que siente el paciente ni tampoco lo es es-tar de acuerdo con su punto de vista. Lo que es necesario, es identificar cómo se siente y por qué, y dejarle saber que hemos identificado ambos. Así, cuando los padres de María solicitan prolongar la hospitalización de María con el fin de seguir administrando tratamientos cuya eficacia terapéutica es nula, la respuesta empática correcta por parte del personal sanitario sería:
Enfermera: “Tiene que ser profundamente doloroso (identificación del sentimiento) encon-trarse en una situación en la que uno sabe que ya no quedan alternativas terapéuticas po-sibles para su hija (identificación de la fuente de dolor: ya no quedan tratamientos dispo-nibles)” o “Entiendo que es muy duro/triste (identificación del sentimiento) aceptar que los médicos no pueden ofrecerles más tratamientos para María (identificación de la fuente de dolor: ya no quedan tratamientos disponibles)”.
Estas respuestas empáticas emitidas de manera continuada acabarán ayudando a los padres de María a tomar conciencia de su inminente muerte y a adoptar las medidas pertinentes.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
• Identificar en qué áreas intervenir
Se debería intervenir en las siguientes áreas con María y su familia:
- Tratar el tema de la negación según las pautas arriba descritas.
- Facilitar la expresión afectiva, tanto por parte de María como de sus padres y hermana.
- Facilitar la comunicación abierta y sincera entre los miembros de la familia, evitando barreras que aíslen a los diferentes miembros unos de otros, y permitiendo que cada miembro de la familia conozca los deseos, necesidades y preocupaciones/temores de los demás, con el fin de potenciar la ayuda y el apoyo mutuo.
- Proporcionar pautas a los padres de María, para hablar con sus hijas acerca de la muerte incorporando sus sistemas de valores y creencias y explicando los beneficios que esto tiene sobre la adaptación emocional de todos los miembros de la familia.
- Favorecer el cumplimiento de los deseos de María con respecto a cómo quiere pasar la etapa final de su vida.
- Favorecer la despedida con el fin de facilitar la adecuada gestión del duelo posterior al falle-cimiento.
- Permitir la participación activa de la hermana de María en los cuidados a la paciente, poten-ciando las visitas al hospital y aumentando su implicación en el proceso de enfermedad, en la medida en la que ella lo desee.
• ¿Habría que intervenir con el equipo sanitario? Formas de intervención con el equipo sanita-rio que faciliten la gestión afectiva de la situación y permitan actuar de una forma óptima con María y su familia
Sería muy importante intervenir con el equipo sanitario, especialmente con el equipo de En-fermería que atiende a María debido a su estrecha vinculación con la paciente y su familia a lo largo de tantos años y a las dificultades que la situación plantea en un momento tan crítico como lo es el enfrentamiento a la muerte de la pequeña paciente.
El motivo de intervenir sería reducir los sentimientos de impotencia que experimentan las enfermeras, aumentar su sensación de logro y satisfacción con respecto a la gestión del caso, y favorecer una actuación eficaz optimizando la adaptación familiar a la situación.
Se intervendría con el equipo:
- Ayudándoles a llevar a cabo las intervenciones familiares antes descritas (p.e., entrenando a las enfermeras en técnicas de comunicación, por ejemplo, en cómo ser empático, etc.
- Ayudándoles a centrarse en aquellas áreas en las que han podido ser eficaces con la familia y con María a lo largo de todo el tratamiento, aquellas áreas que ellas pueden controlar, con el fin de reducir la sensación de fracaso.
- Ayudando a las enfermeras a tomar conciencia de las enormes limitaciones con las que se enfrentan en muchas situaciones, y a aceptarlas.
- Ofreciendo un espacio estructurado (por ejemplo, durante una sesión clínica) para compartir lo que el personal siente con respecto a este caso y cómo gestionar lo que sienten adecuada-mente, apoyándose y ofreciendo pautas concretas de actuación que se pueden definir entre los miembros del equipo.

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
CASO 7. Conflictos familiares y su interferencia en la administración del tratamiento médico adecuado
HISTORIA CLÍNICA Y PERSONAL
Miguel es un niño de 7 años diagnosticado de neuroblastoma a los 3 años. Sigue aún en tra-tamiento porque su enfermedad no ha remitido.
Miguel se muestra con un alto nivel de ansiedad y un comportamiento muy hostil (caracte-rizado por regla general, por gritos, llantos, resistencia, insultos) cuando ingresa durante las inter-venciones asistenciales que se le realizan. Esto supone verdaderos episodios de angustia para el niño, sus padres y para el personal sanitario.
A los ingresos siempre acude acompañado por sus padres, a pesar de que ellos se han divor-ciado durante el periodo de enfermedad. Aunque intentan mantener una fachada de cordialidad ante el personal de Enfermería, muestran una actitud de frialdad y distancia entre ellos. Cada uno verbaliza por separado criterios de actuación muy diferentes en las distintas situaciones que de-ben ir afrontando con su hijo. El padre de Miguel tiene una nueva pareja que no es bien recibida en el hospital por parte de su ex-mujer. El acompañamiento de su hijo durante las estancias hos-pitalarias lo hacen tanto el padre como la madre, alternándose un día cada uno.
Mientras permanece ingresado, Miguel se muestra muy retraído. Apenas quiere salir de la habitación. Tampoco quiere hablar ni establecer contacto visual con nadie que no sean sus padres. No quiere jugar con otros niños en la sala de juegos hospitalaria ni implicarse en ninguna actividad con los voluntarios. Los padres de Miguel refieren que está triste solamente en el hospital y que en casa muestra un comportamiento y actitud diferente.
Además, Miguel exhibe problemas con la comida. No le gusta comer en el hospital a pesar de que con los niños se realiza una dieta hospitalaria personalizada y se permite a los padres traer comida de casa.
Cuando Miguel está acompañado por su madre, demanda continuamente analgesia porque refiere que su hijo tiene dolor; se le realizan, por parte del equipo, valoraciones del dolor de manera continuada, existiendo en muchas ocasiones, una contradicción entre la valoración objetiva y lo que la madre manifiesta y demanda con gran exigencia a los profesionales. Por otra parte, cuestio-na y discute con los oncólogos casi a diario las líneas de tratamiento porque dice ella “…estar muy bien informada de la enfermedad de su hijo, de los últimos avances alcanzados”.
Esto último plantea dificultades importantes de comunicación y se observa que ejerce una presión en los médicos que propicia la distancia y empeora las relaciones.
M. DIE TRILL Y F. MUÑOZ TORRES

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
PAUTAS DE INTERVENCIÓN
Aspectos del funcionamiento psicológico de Miguel y de sus padres en profundidad
Sería importante, con el fin de comprender el comportamiento de Miguel y de sus padres y de poder desarrollar así, la intervención psicológica que más ayudara a este pequeño pacien-te y a su familia, a adaptarse al proceso de enfermedad, evaluar en profundidad los siguien-tes aspectos del funcionamiento psicosocial:
Funcionamiento psicológico:
• ¿Cuál ha sido el funcionamiento psicológico y comportamiento de Miguel antes de la enfermedad?
• ¿Cómo ha afectado el diagnóstico a Miguel? ¿Ha cambiado su comportamiento o su forma de sentir, expresarse, jugar, estudiar, relacionarse, etc. de alguna manera? ¿Cómo?
• Cuál es el estado afectivo de Miguel: ¿está triste o deprimido?, ¿temeroso?, ¿preocupado?, ¿asustado? En caso afirmativo, ¿a qué se debe?
• Cuáles son los hábitos alimentarios y los patrones de sueño de Miguel: ¿come con apetito?, ¿ha perdido/ganado peso?; ¿duerme bien por la noche?, ¿hay insomnio de conciliación o mantenimiento?, ¿tiene pesadillas?
Funcionamiento social:
• ¿Tiene amigos Miguel?
• ¿Mantiene sus relaciones sociales con los amigos desde el diagnóstico?, ¿van a visitarle los amigos?
• ¿Acude al colegio cuando la enfermedad y tratamientos se lo permite?
• ¿Cómo han reaccionado los amigos ante su enfermedad?
• ¿Qué apoyos tiene Miguel?
• ¿De qué manera la cuidan su padre y su madre?
Funcionamiento familiar:
• ¿Miguel tiene hermanos? En caso afirmativo, ¿qué lugar de orden ocupa él entre los hermanos?
• ¿Fue un niño deseado y buscado por sus padres?
• Describe relación con padre, madre y con hermanos si los hubiere
• ¿Qué edad tenía Miguel cuando se separaron sus padres?
• ¿Cómo le afectó la ruptura conyugal de sus padres?
• ¿Qué mensajes recibe Miguel de su padre acerca de su madre, y viceversa?
• ¿Qué relación tiene Miguel con la nueva pareja de su padre?
• ¿Es diferente el comportamiento de Miguel con su padre que con su madre?
• ¿Qué expresa y entiende Miguel acerca de la separación de sus padres?
• Evaluar al padre de Miguel y a la madre por separado: sus rasgos de personalidad, temores, preocupaciones, formas de afrontar la enfermedad y la vida en general, puntos de conflicto,

NEUROBLASTOMA enfocado a ENFERMERÍA VOLVER AL ÍNDICE
puntos en común, grado de satisfacción con la vida en general, expectativas de Miguel, ex-pectativas y esperanzas con respecto al curso de la enfermedad, etc.
Pautas a adoptar para trabajar aspectos emocionales con estos padres
• Ayudarles a tomar conciencia sobre el impacto que tiene su comportamiento y falta de acuerdo ante el niño, sobre el comportamiento y malestar general del paciente.
• Identificar puntos en común y centrarles en su objetivo compartido: comparten el objetivo de cuidar del niño, optimizar su vida, ofrecerle el mejor tratamiento médico y facilitarle la adaptación al proceso de enfermedad.
• Impedir los desacuerdos delante del niño.
• Facilitar la aceptación por parte de la madre de Miguel, de la pareja de su exmarido y buscar formas en las que ésta pudiera participar de una forma óptima en el cuidado de Miguel.
• Trabajar con la pareja para que ayuden a Miguel a aceptar y respetar al equipo médico, mostrándose respetuosos ellos siempre con los profesionales y sus opiniones, y transmitiendo a Miguel la impor-tancia que tiene colaborar con el equipo sanitario, modelando ellos mismos dicho comportamiento.
• Dar a los padres de Miguel alternativas: acudir a un psicólogo con experiencia en terapia de pareja para ayudarles a resolver los conflictos que parece que aún no han resuelto a pesar de haberse separado, o pedir que en el hospital muestren acuerdo y “mantengan las formas” delante de Miguel, ayudándole así a mejorar su comportamiento.
• Empoderar a la madre de Miguel. No parece sentirse con mucho poder en el cuidado de su hijo, motivo por el cual quizás cuestione los criterios y tratamientos médicos y solicite medicación para el dolor constantemente. Darle un papel “especial” en el cuidado de Miguel sería impor-tante para que ella sepa que, como madre, es quien mejor puede cuidar del pequeño paciente. Esto facilitará el que ella no se sienta “desplazada” por la nueva pareja de su exmarido.
• Los padres tienen que facilitar que Miguel se relacione con el personal sanitario y con otras personas del hospital durante sus ingresos.
• Celebrar reuniones familiares (padres de Miguel y equipo sanitario que trata a Miguel) con un mediador que puede ser una enfermera o un psicooncólogo, con el fin de facilitar y optimizar la comunicación entre el equipo y los padres, y de proporcionar un entorno estructurado y seguro en el que los padres puedan verbalizar sus preocupaciones, temores, dudas, etc. so-bre el tratamiento y la enfermedad de Miguel.
Estrategias de intervención para ayudar al paciente y profesionales que deben llevarlas a cabo
• Deberían utilizarse intervenciones cognitivo-conductuales con Miguel para reducir su an-siedad y eliminar su comportamiento hostil cuando ingresa en el hospital. Entrenamiento en técnicas de relajación, respiración, visualización guiada, distracción cognitiva, y uso de refuerzos contingentes al comportamiento deberían implantarse. El personal de enfermería debería poder realizar este tipo de intervenciones. En el caso de que el comportamiento de Miguel no respondiera, se debería derivar a un psico-oncólogo.
• Se debería evaluar el dolor de Miguel de forma sistemática y periódica durante los ingresos de Miguel (por ejemplo, cada 3h inicialmente), anticipándonos a las peticiones de analgesia por parte de la madre. Esto evitaría o reduciría sus peticiones. Además, se debería poner el control del dolor en manos de un experto de la Unidad del Dolor, o de un anestesista. Un profesional de fuera del servicio de oncopediatría debería manejar el tema del dolor. Con ésto se evitarían las luchas entre la madre de Miguel y el personal sanitario sobre el dolor de Miguel.

AVALADO POR
PATROCINADO POR