UNIVERSIDAD PERUANA CAYETANO HEREDIA - … LUCIA... · La irrigación en el tratamiento de...
Transcript of UNIVERSIDAD PERUANA CAYETANO HEREDIA - … LUCIA... · La irrigación en el tratamiento de...

1
“SOLUCIONES IRRIGANTES EN ENDODONCIA”
INVESTIGACIÓN BIBLIOGRÁFICA DEL PROCESO DE SUFICIENCIA
PROFESIONAL PARA OBTENER EL TÍTULO DE CIRUJANO DENTISTA
Viviana Lucía Magallanes Aguilar
LIMA – PERÚ
2010
UNIVERSIDAD PERUANA CAYETANO HEREDIA
Facultad de Estomatología Roberto Beltrán

2
JURADO EXAMINADOR
PRESIDENTE: Dr. Felipe Hernández Añaños
SECRETARIO: Raúl Villanueva Kcomt
ASESOR(A): Dra. Allison Chávez Alayo
FECHA DE SUSTENTACION: 11 DE MARZO DEL 2010
CALIFICATIVO: APROBADO

3
A mis padres, por darme su amor y apoyo durante toda
mi vida y ser las personas en las que siempre voy a
poder confiar.
A mi hermana, por su apoyo incondicional y amor que me
demuestra día a día.
A mis amigos, por permanecer siempre a mi lado.

4
AGRADECIMIENTOS
A la dra. Allison Chávez Alayo por su apoyo, dedicación, amistad y paciencia

5
RESUMEN
La irrigación en el tratamiento de conductos radiculares consiste en el lavado y la
aspiración de todos los restos y sustancias que puedan estar contenidos en la cámara
o conductos radiculares. Y formará parte fundamental de la preparación
biomecánica, ya que facilitará la instrumentación al lubricar las paredes del
conducto radicular.
En la actualidad existen distintos tipos de soluciones irrigantes utilizadas para el
tratamiento de conducto radiculares.
El presente trabajo tendrá como finalidad evaluar cada una de estas soluciones
irrigantes utilizadas en endodoncia, para así determinar cuáles son las más
adecuadas para cada tipo de tratamiento. Además se dará a conocer las novedades
en sistemas de irrigación que hay en el mercado y si su uso es ventajoso o no.
Palabras claves: irrigación, soluciones irrigantes, sistemas de irrigación.

6
ÍNDICE DE GRÁFICOS
Página
Gráfico 1: Reacción de Saponificación 11
Gráfico 2: Reacción de Neutralización aminoácido 11
Gráfico 3: Reacción de Cloraminación 11
Gráfico 4: Fórmula de molécula de clorhexidina 22

7
ÍNDICE DE FIGURAS
Página
Figura 1: Irrigación – lavado y aspiración 3
Figura 2: EDTA al 17% 32
Figura 3: Remoción de barro dentinario al minuto de aplicar
NaOCl al 5.25% + EDTA al 17% 35
Figura 4: Remoción del barro dentinario a los 10 minutos de aplicar
NaOCl al 5.25% + EDTA al 17% 35
Figura 5: Jeringas utilizadas durante la terapia endodontica 40
Figura 6: Agujas utilizadas durante la terapia endodóntica 41
Figura 7: Cánulas de succión utilizadas durante la terapia endodóntica 42
Figura 8: Pre y post tratamiento de accidente con extravasación de
hipoclorito de sodio. 46
Figura 9: Extravasación de NaOCl al 5.25% hacia los tejidos periapicales 47
Figura 10: Extravasación de NaOCl al 5.25% hacia los tejidos periapicales 48
Figura 11: Extravasación de NaOCl al 5.25% hacia los tejidos periapicales 48
Figura 12: Extravasación de NaOCl al 5.25% hacia los tejidos periapicales 48
Figura 13: Extravasación de NaOCl al 5.25% hacia los tejidos periapicales 48
Figura 14: Extravasación de NaOCl al 5.25% hacia los tejidos periapicales 48
Figura 15: Salida del NaOCl a través del dique de goma 49
Figura 16: Inyección de solución de NaOCl cuando se cambian los tubos
de anestésico, por tubos previamente llenados con dicha
solución irrigante. 52
Figura 17: Inyección de solución de NaOCl cuando se cambian los tubos
de anestésico, por tubos previamente llenados con esa
solución de irrigación 52
Figura 18: Sistema Endoactivador 55
Figura 19: Activación Ultrasónica Pasiva 57
Figura 20: Equipo de agujas de desinfección fotoactivada (PAD) 58
Figura 21: Agujas y equipo de irrigación con gas Ozono (O3) 60
Figura 20: Sistema Endovac 61

8
ÍNDICE DE CONTENIDOS
Página
I. INTRODUCCIÓN 1
II. MARCO TEÓRICO 3
II.1 DEFINICIÓN 3
II.2 OBJETIVOS 4
II.3 PROPIEDADES IDEALES DE LOS IRRIGANTES 5
II.4 CLASIFICACIÓN DE SOLUCIONES IRRIGANTES 7
II.4.1 COMPUESTOS HALOGENADOS 9
II.4.2 DETERGENTES SINTÉTICOS 30
II.4.3 QUELANTES 31
II.4.4 ASOCIACIONES 36
II.4.5 OTRAS SOLUCIONES DE IRRIGACIÓN 39
II.5 MATERIAL E INSTRUMENTAL PARA LA IRRIGACIÓN
INTRACANAL 40
II.6 MECANISMO Y TÉCNICA DE IRRIGACIÓN 43
II.7 COMPLICACIONES MÁS FRECUENTES CON EL USO DE
SOLUCIONES IRRIGANTES EN ENDODONCIA. 45
II.8 PROTOCOLO FARMACOLÓGICO FRENTE
INTOXICACIÓN POR IRRIGACIÓN DE HIPOCLORITO
DE SODIO EN LOS TEJIDOS BLANDOS
DURANTE UN PROCEDIMIENTO ENDODÓNTICO 54
II.9 NOVEDADES EN IRRIGACIÓN 55
III. CONCLUSIONES 62
IV. REFERENCIAS BIBLIOGRÁFICAS 64

1
I. INTRODUCCIÓN
Los microorganismos juegan un rol fundamental en la etiología de las enfermedades
pulpares y periapicales, por lo que su control y eliminación antes, durante y después
del tratamiento endodóntico van a ser muy importantes.
Las bacterias comúnmente asociadas a signos y síntomas de inflamación pulpar, son
las bacterias aerobias gram negativas. Sin embargo, las anaerobias facultativas,
como el Enterococcus faecalis, Staphylococcus aureus, e incluso la Candida
albicans son consideradas por muchos autores, como una de las especies más
resistentes de la cavidad oral.
El Enterococcus faecalis es un microorganismo gram positivo anaerobio
facultativo, el cual posee la habilidad de crecer en presencia o ausencia de oxígeno,
comúnmente detectado en infecciones endodónticas persistentes asintomáticas. Su
prevalencia en tales infecciones oscila entre el 24% - 77%. Este hallazgo puede ser
explicado gracias a sus factores de virulencia y supervivencia, incluyendo su
habilidad de competir contra otros microorganismos, invadir túbulos dentinarios y
resistir a la privación nutricional.
Varios autores consideran al E. faecalis como una de las especies más resistentes y
como tal una de las principales causas de fracasos en los tratamientos endodónticos.
Es por eso que uno de los objetivos principales de los tratamientos de conductos es
la reducción de microorganismos.
Ya que los microorganismos van a ser uno de los principales causantes de fracasos
en los tratamientos de conductos radiculares, el procedimiento clínico de rutina para
la eliminación de estos microorganismos va a consistir en realizar una meticulosa
instrumentación mecánica, acompañada de irrigación con sustancias químicas.
Va a ser importante realizar una correcta preparación biomecánica del conducto
radicular. Sin embargo, la instrumentación mecánica por si sola no llega a obtener
conductos radiculares libres de bacterias, ya que existen ciertas variaciones en la
anatomía de los conductos radiculares tales como presencia de conductos en forma
de C, S, elípticos, conductos accesorios y laterales, los cuales no son evidentes a
simple vista y en donde se alojan dichos microorganismos Por lo que la irrigación
va a ser complementaria a la instrumentación, facilitando la remoción o arrastre
físico de trozos de tejido pulpar, sangre líquida o coagulada, virutas de dentina,

2
polvo de cemento, bacterias, plasma, exudado, restos alimenticios y medicación
anterior, especialmente en las áreas en las que el instrumento manual no logra
llegar.
La irrigación debe ser abundante para el funcionamiento efectivo de las limas. Sin
irrigación, los instrumentos perderían rápidamente su eficacia debido a la
acumulación de residuos. El irrigante se va a encargar de limpiar el instrumento,
aumentando su efectividad. La irrigación va ha facilitar la instrumentación al
lubricar las paredes de los conductos y suspender el polvo de la dentina.
La sustancia irrigante escogida debe permitir la neutralización e inactivación de las
toxinas bacterianas mediante un completo desbridamiento y desinfección del
espacio del conducto radicular, lo cual es fundamental para el éxito del tratamiento,
al igual que una completa obturación de éste.

3
II. MARCO TEÓRICO
II.1 DEFINICIÓN DE LA IRRIGACIÓN
La irrigación, en endodoncia, se define como el lavado y aspiración de todos los
restos contenidos en la cámara y conductos radiculares. (1)
Este acto operatorio consiste en irrigar las paredes del conducto radicular con una
solución química, que al mismo tiempo al ser sometida a la aspiración, promoverá la
limpieza del espacio endodóntico. (2) La irrigación juega un rol importante en el
desbridamiento y desinfección del conducto radicular y por lo tanto, forma parte
importante de los procedimientos de la preparación biomecánica. (1) Va a ser un
complemento fundamental de la instrumentación, puesto que residuos de tejido
pulpar, bacterias y restos de dentina pueden permanecer en el conducto aún después
de haber hecho una meticulosa preparación biomecánica. (3)
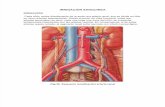
Figura 1: Irrigación – lavado y aspiración
Cortesía de la Dra. Allison Chávez

4
II.2 OBJETIVOS DE LA IRRIGACIÓN:
Los objetivos de la irrigación de los conductos radiculares consisten en realizar una
limpieza o arrastre físico de tejido orgánico e inorgánico, con el fin de evitar el
taponamiento del conducto, reducir las bacterias existentes en los conductos
radiculares por el acto mecánico del lavado y por la acción antibacteriana de la
sustancia utilizada, mantener las paredes dentinarias hidratadas y ejercer una acción
lubricante facilitando la acción conformadora de los instrumentos endodónticos. (3)

5
II.3 PROPIEDADES DEL IRRIGANTE IDEAL
Es por esa razón que la solución irrigante ideal debe tener propiedades que le
permitan cumplir con la mayoría de los objetivos. (3, 4, 5)
1. Desinfectante
Efecto antimicrobiano; bactericida y/o bacteriostático
La irrigación depende de la vulnerabilidad de las especies involucradas. Se ha
demostrado que los microorganismos y sus productos, toxinas y subproductos son la
principal causa para el desarrollo y persistencia de una lesión pulpar y periapical.
Algunos microorganismos como el Enterococos faecalis han sido relacionados con
los signos y síntomas de las patologías endodónticas, considerándolo una de las
especies resistentes en la cavidad oral y una de las posibles causas del fracaso
endodóntico. En infecciones endodónticas persistentes, estos microorganismo
invaden canales dentinales y laterales del conducto principal, por lo tanto para lograr
una completa desinfección de las paredes, la aplicación local de las sustancias
irrigantes deben penetrar dentro de la dentina a altas concentraciones para eliminar las
bacterias invasoras.
Bactericida:
Un efecto bactericida es aquel que produce la muerte a una bacteria.
Bacteriostático:
Un efecto bacteriostático es aquel que aunque no produce la muerte a una bacteria,
impide su reproducción; la bacteria envejece y muere sin dejar descendencia.
2. Baja toxicidad
El irrigante ideal no debería ser tóxico, para que no sea agresivo con los tejidos
apicales y periapicales.
3. Solvente de tejidos o de residuos orgánicos e inorgánicos
En las regiones inaccesibles para los instrumentos, el irrigante puede disolver o
romper remanentes de tejido blando o duro para permitir su eliminación.

6
4. Baja tensión superficial
Esta propiedad fomenta el flujo a las áreas inaccesibles. Cuanto menor sea la
tensión superficial de un irrigante, mejor será su propiedad de permeabilidad
dentinaria del irrigante, podrá penetrar en zonas de difícil acceso como son los
conductos laterales y túbulos dentinarios.
El alcohol agregado a un irrigante va a disminuir la tensión superficial y por lo
tanto aumentará su penetrabilidad; se desconoce si mejora la limpieza.
5. Lubricante
La lubricación ayuda a que los instrumentos se deslicen dentro del conducto;
todos los líquidos tienen este efecto, algunos más que otros.
6. Fácil aplicación
Es aquel irrigante que requiere de una técnica sencilla para ser aplicado dentro del
conducto radicular.
7. Acción rápida
Será aquel irrigante, el cual no requiera de un largo periodo de tiempo dentro del
conducto radicular para hacer efectivas sus propiedades.

7
II.4 CLASIFICACIÓN DE SOLUCIONES IRRIGANTES
IV.1. COMPUESTOS HALOGENADOS (2)
IV.1.1. Solución de Hipoclorito de Sodio al 0.5 % (solución de Dakin)
IV.1.2. Solución de Hipoclorito de Sodio al 1% + ácido bórico
(solución de Milton)
IV.1.3. Solución de Hipoclorito de Sodio al 2.5 % (solución de Labarraque)
IV.1.4. Solución de Hipoclorito de Sodio al 4-6, 5%
(soda clorada doblemente concentrada)
IV.1.5. Solución de Hipoclorito de Sodio al 5.25% (preparación oficial, USP)
IV.1.6. Solución de Gluconato de Clorhexidina al 2%
IV.2 DETERGENTES SINTÉTICOS (2)
IV.2.1. Duponol C – al 1% (alquil- sulfato de Sodio)
IV.2.2. Zefirol – Cloruro de alquidimetil- bencilamonio (cloruro de Benzalconium)
IV.2.3 Dehyquart- A (cloruro de cetiltrimetilamonio)
IV.2.4. Tween – 80 (polisorbato 80)
IV.3. QUELANTES (2)
IV.3.1. Soluciones de ácido etilenodiaminotetracético – EDTA
IV.3.2. Largal ultra (agente quelante comercial)
IV.3.3. Redta (agente quelante comercial)
IV.4. ASOCIACIONES (2)
IV.4.1 RC Prep (ácido eltilenodiaminotetracético + peróxido de urea + base
hidrosoluble y polietilenoglicol – Carbowax)
IV.4.2. Glyde File Prep
IV.4.3. MTAD (asociación de una tetraciclina isométrica, ácido cítrico y un
detergente - Tween 80)
IV.4.4. Endo – PTC (peróxido de urea + Tween 80 + Carbowax)
IV.4.5 Smear Clear

8
IV.5. OTRAS SOLUCIONES DE IRRIGACIÓN (2)
IV.5.1. Agua Destilada esterilizada
IV.5.2. Agua de hidróxido de calcio – 0.14 g%
IV.5.3. Peróxido de Hidrógeno - 10 volúmenes
IV.5.4. Suero Fisiológico
IV.5.5. Solución de ácido cítrico

9
II.4.1 COMPUESTOS HALÓGENADOS
II.4.1.1 HIPOCLORITO DE SODIO
RESEÑA HISTÓRICA:
El Hipoclorito de Sodio, fue introducido durante la primera guerra mundial. (2, 3)
En 1915, 1916, 1917, gracias a las investigaciones realizadas por Dakin y
Dunham, los compuestos de cloro comenzaron a ser ampliamente utilizados en
medicina, en cirugía y también en odontología, pues el bajo costo del producto,
era una importante razón que justificaba su popularidad. Éstos introdujeron el uso
del hipoclorito de sodio al 0.5% y 0.6% como antiséptico en heridas infectadas.
En 1919, basado en este reporte de Dakin y Dunham, el hipoclorito de sodio fue
recomendado como irrigante por Coolidge.
En 1936, Walker inició el uso del NaOCl al 5% como irrigante de conductos
radiculares.
En 1941, Grossman y Meiman evaluaron varios químicos utilizados durante la
preparación biomecánica de los conductos radiculares y comprobaron que la
solución de hipoclorito de sodio del 4% - 6% (soda doblemente clorada) fue el
disolvente más eficaz del tejido pulpar.
En 1960, Marshall y colaboradores mostraron que los antisépticos acuosos
penetraban más fácilmente en los túbulos dentinarios que las sustancias no
acuosas, siendo que la solución de hipoclorito de sodio al 5%, como consecuencia
de esa penetración, aumentaba la permeabilidad dentaria.
Desde entonces el NaOCl se ha postulado como el irrigante más popular en
endodoncia por su capacidad para disolver tejido y por su amplio espectro
antimicrobiano, ya que elimina rápidamente formas vegetativas de bacterias,
esporas, hongos y virus.

10
ESTRUCTURA QUÍMICA:
El Hipoclorito de sodio, cuya fórmula química es: (6, 7)
NaOCl +H2O = NaOH + HOCl
Es una sal formada de la unión de dos compuestos químicos, el ácido hipocloroso
y el hidróxido de sodio, el cual presenta propiedades oxidantes. Según Dakin y
Dunham, el cloro es uno de los más potentes germicidas conocidos, ejerciendo
acción antibacteriana en forma de ácido hipocloroso no disociado. Al estar en
solución neutra o ácido hipocloroso no se disocia y su acción bactericida es
efectiva. (2) El hipoclorito de sodio es hipertónico (2800mOsmol/kg) y muy
alcalino (pH=11 a 12). (5) Por su pH alcalino (11-12), el NaOCl neutraliza la
acidez del medio, evitando el desarrollo bacteriano. (3)
MECANISMO DE ACCIÓN:
Según Estrela y col. los mecanismos de acción del hipoclorito de Sodio (NaOCl)
son tres: (6, 7)
1) SAPONIFICACIÓN, donde el hipoclorito de sodio actúa como un solvente
orgánico que degrada los ácidos grasos para convertirlos en sales ácidas
grasosas (jabón) y glicerol (alcohol), lo cual reduce la tensión superficial de la
solución remanente. (Ver tabla 1)
2) NEUTRALIZACÍON, donde el Hipoclorito de sodio neutraliza los
aminoácidos formando agua y sal. (Ver Tabla 2)
3) CLORAMINIZACIÓN. Con la reducción de los iones hidroxilo, va a haber
una reducción del pH. El ácido Hipocloroso, una sustancia presente en el
hipoclorito de sodio, cuando está en contacto con el tejido orgánico, actúa
como un solvente, lo cual va hacer que haya una reacción entre el cloro y el
grupo amino, formando cloraminas, las cuales se encargarán de interferir en el
metabolismo celular de los microorganismos, dando como resultado la muerte
celular de las bacterias. El cloro, que es un oxidante fuerte posee una acción
antimicrobiana inhibiendo enzimas esenciales de las bacterias por medio de
oxidación, formando complejos tóxicos que las destruyen. (Ver Tabla 3)

11
Gráfico 1. REACCIÓN DE SAPONIFICACIÓN (6)
O O
|| ||
R – C – O – R + NaOH ↔ R – C – O – Na + R – OH
ácidos hidróxido de jabón glicerol
sodio
Gráfico 2. REACCIÓN DE NEUTRALIZACIÓN AMINOÁCIDA (6)
H O H O
| // | //
R – C – O – C + NaOH ↔ R – C – O – C + H2O
| |
NH2 OH NH2 ONa
Amino ácido hidróxido de sal agua
sodio
Gráfico 3. REACCIÓN DE CLORAMINACIÓN (6)
H O Cl O
| // | //
R – C – O – C + HOCl ↔ R – C – O – C + H2O
| |
NH2 OH NH2 OH
amino ácido ácido cloramina agua
hipocloroso

12
VENTAJAS Y DESVENTAJAS DEL USO DE HIPOCLORITO DE SODIO
VENTAJAS:
En la actualidad, el hipoclorito de Sodio (NaOCl) sigue siendo uno de las
soluciones irrigantes más usadas en la endodoncia de estos tiempos, por presentar
excelentes propiedades como: (2, 5, 8, 9, 10)
1. Acción antimicrobiana (bactericida)
Cuando el hipoclorito de sodio entra en contacto con el tejido y los restos
orgánicos pulpares, libera oxígeno y cloro. El cloro es uno de los más potentes
germicidas conocidos, ejerce acción antibacteriana en la forma de ácido
hipocloroso, no se disocia y su acción bactericida es efectiva y acentuada.
Byström y Sundvist (1985) consideran al E. faecalis como el microorganismo más
resistente a las terapias endodónticas. (11)
Estrela y col (2003) comparan la eficacia antimicrobiana del NaOCl con la de
clorhexidina al 2%, contra 5 microorganismos (Staphylococcus aureus,
Enterococcus faecalis, Pseudomonas, Aeruginosa, Bacillus subtilis, Candida
albicans, y una mezcla de todas) mediante 2 pruebas: Prueba de difusión de agar
y prueba de exposición directa. Los resultados mostraron que ambas tuvieron
acción antimicrobiana contra estos microorganismos. La magnitud de esta eficacia
esta influenciada por el método experimental, las características de los
microorganismos y el tiempo de exposición. La solución de hipoclorito de sodio
al 5.25% y la clorhexidina al 2% mostraron ser los mejores antimicrobianos
eliminando el E. faecalis (12)
Sassone y col (2008) comparan la actividad antimicrobiana del hipoclorito de
Sodio al (1% y 5%) y la Clorhexidina al (0.12%, 0.5%, 1%) contra 3
microorganismos facultativos (S. Auresus, E. faecalis y E. Coli) y 2
microorganismos anaerobios (P. Gingivalis y F. Nucleatum). El NaOCl al 1% y
5% y la Clorhexidina al 1% mostraron una efectiva acción antimicrobiana contra
estos microorganismos a diferencia de la Clorhexidina al 0.12% y 0.5%, los
cuales mostraron ser inefectivos contra la E .faecalis. (13, 14)

13
2. Acción disolvente
De acuerdo a las investigaciones de Grossman y Meiman, el hipoclorito de sodio
es el disolvente más eficaz del tejido pulpar. Una pulpa puede demorar entre 20
minutos hasta dos horas, para disolverse por completo con este agente.
Türkün y Cenguiz (1997) comparan la efectividad de disolución de tejido
necrótico y de limpieza del hipoclorito de sodio al 0.5% y 5% con una previa
aplicación de hidróxido de calcio en pasta, media hora antes del tratamiento. Los
resultados muestran que el hidróxido de calcio pretratamiento mejoran la eficacia
del NaOCl al 0.5%. En algunas ocasiones se podría utilizar hidróxido de calcio y
luego NaOCl al 0.5% en vez de utilizar NaOCl al 5%, el cual tiene efectos
altamente citotóxicos en contacto con los tejidos periapicales. (15)
3. Deshidrata y solubiliza las sustancias proteicas
Los restos pulpares y alimentarios, así como los microorganismos de la luz del
conducto radicular, las bacterias alojadas en los túbulos dentinarios, laterales,
colaterales y accesorios, están constituidos en gran proporción por prótidos. Estas
sustancias proteicas se deshidratan y solubilizan por la acción de la solución de
hipoclorito de sodio, que las transforma en materia fáciles de eliminar, del interior
del sistema de conductos radiculares.
4. Acción lubricante.
La solución de hipoclorito de sodio, químicamente se considera un alcali, que
actúa sobre los ácidos grasos de los tejidos, los saponifica y los transforma en
jabón soluble y de fácil eliminación. Esta transformación química hace que la
solución de hipoclorito de sodio lubrique el conducto radicular desempeñando la
función de sustancias cremosas también indicadas como coadyuvantes a la
preparación biomecánica.
5. Auxilia en la instrumentación
Por el humedecimiento de las paredes del conducto radicular y por la reacción de
saponificación, facilita la acción de los instrumentos.

14
6. Baja la tensión superficial
En razón de esta propiedad, la solución de hipoclorito de sodio, penetra en todas
las concavidades del sistema de conductos radiculares, y también crea
condiciones para mejorar la eficiencia del medicamento de uso tópico que se
aplica entre sesiones.
7. Neutraliza parcialmente productos tóxicos.
Esta propiedad de la solución de hipoclorito de sodio al 5.25% es de fundamental
importancia, pues permite neutralizar parcialmente y remover todo el contenido
tóxico del conducto radicular en la sesión inicial de tratamiento, sin correr el
riesgo de las desagradables agudizaciones de los procesos periapicales crónicos,
permitiendo una penetración quirúrgica en medio del ambiente antiséptico en la
misma sesión.
8. Tiene doble acción detergente
Los álcalis actúan sobre los ácidos grasos, saponificándolos, es decir,
transformándolos en jabones solubles y de fácil eliminación lo que facilita la
acción de los instrumentos. Los álcalis así como los jabones, disminuyen la
tensión superficial de los líquidos, suministrándole al hipoclorito de sodio el doble
poder de ser humectante y detergente.
9. Tiene acción rápida
La interacción del hipoclorito de sodio/agua oxigenada o hipoclorito de
sodio/restos orgánicos se hace rápidamente y con enérgica efervescencia,
presionando la sangre, los residuos y las bacterias hacia fuera de la masa
dentinaria y llevándolos hacia la luz del conducto radicular.
10. Acción de limpieza (arrastre mecánico)
La solución de hipoclorito de sodio presenta una baja tensión superficial, siendo
considerada como una sustancia doblemente detergente. En razón de su baja
tensión superficial, en los casos de necrosis pulpar y lesión periapical crónica,
ésta solución penetra en las concavidades del sistema de conductos radiculares
(túbulos dentinarios, ramificaciones, deltas apicales, erosiones cementarias

15
apicales), reacciona con los restos necróticos y se deshace en cloro y oxígeno;
éstos por ser volátiles, buscan un área de escape (luz del conducto radicular)
llevando consigo, por arrastre mecánico, restos necróticos, bacterias etc.
Además, promueve el aumento de la permeabilidad dentinaria.
11. No es irritante en las condiciones de uso
La solución de hipoclorito de sodio al 2.5% o al 5.25% no es irritante en
condiciones de uso clínico, especialmente en tratamiento de conductos
radiculares de dientes con necrosis pulpar y lesión periapical crónica.
12. pH alcalino
Gracias a su pH alcalino (11.8) la solución de hipoclorito de sodio neutraliza la
acidez del medio dejando el ambiente impropio para el desarrollo bacteriano.
DESVENTAJAS:
La principal desventaja y la menos desseable de la solución de hipoclorito de sodio
(NaOCl) es causar efectos altamente citotóxicos cuando es inyectado a nivel de los
tejidos periapicales.
Es de vital importancia que el irrigante a usar sea biocompatible con los tejidos. El
hipoclorito de sodio (NaOCl) ha sido utilizado durante muchos años a diferentes
concentraciones (0.5% - 5%) como solución irrigante en el conducto radicular. A
altas concentraciones (5.25%) el hipoclorito de sodio causa efectos altamente
citotóxicos cuando es inyectado a nivel de los tejidos periapicales, mientras que a
una concentración mas baja (NaOCl al 0.5%) sus efectos a nivel de los tejidos
periapicales no serán tan citotóxicos, pero en cuanto a su efectividad
antimicrobiana, microorganismos como el E. faecalis serán resistentes. Es por esta
razón, deben seguirse ciertas pautas de prevención en el manejo del hipoclorito de
sodio y una técnica adecuada de irrigación, evitaran que el líquido irrigante alcance
los tejidos periapicales. (3)
Además de otras desventajas como; mal olor y sabor, blanquear la ropa, alto
potencial corrosivo del instrumental endodóntico y reacciones alérgicas. (3)

16
FACTORES QUE PUEDEN MODIFICAR LAS PROPIEDADES DEL
HIPOCLORITO DE SODIO (NaOCl)
La acción bactericida y de disolución de tejidos del hipoclorito de sodio pueden estar
modificadas por tres factores: Concentración, temperatura, estabilidad química y pH
de la solución. (5)
1.- CONCENTRACIÓN:
Las soluciones de hipoclorito de sodio (NaOCl) según su concentración se
clasifican de la siguiente manera: (9)
1.1 Solución de Hipoclorito de Sodio al 0.5 % (Solución de Dakin)
1.2. Solución de Hipoclorito de Sodio al 1% + ácido bórico (Solución de Milton)
1.3. Solución de Hipoclorito de Sodio al 2.5 % (Solución de Labarraque)
1.4. Solución de Hipoclorito de Sodio al 4-6, 5% (Soda clorada doblemente
concentrada)
1.5. Solución de Hipoclorito de Sodio al 5.25% (Preparación oficial, USP)
En la actualidad, tanto endodoncistas, como clínicos generales que practican la
endodoncia, utilizan durante la preparación biomecánica, diferentes concentraciones
de hipoclorito de sodio, sin que haya unanimidad en la elección. (2)
Su efecto será lo necesariamente dañino para eliminar las bacterias que comúnmente
están presentes en el conducto radicular, pero a su vez, ésta concentración será
altamente tóxica e irritante. (3)
1.1 Solución de Hipoclorito de sodio al 0.5% ( Solución de Dakin)
Esta solución de hipoclorito de sodio al 0.5% posee un tiempo de vida muy corto
y una concentración de cloro muy baja, por lo que sus propiedades
antimicrobianas contra microorganismos como el E. faecalis y de disolución de
tejido pulpar van a ser muy pobres. (2) Su efecto bactericida no será tan eficaz
como una solución de NaOCl a mayor concentración, ya que al ser diluido
disminuye su efecto antimicrobiano (3) y le tomará un mayor tiempo en disolver
el tejido orgánico. Es por esta razón que muchos autores no la recomiendan para
los tratamientos de dientes con necrosis pulpar y lesión periapical. (2)

17
1.2 Solución de hipoclorito de sodio al 1% (solución de Milton)
La solución de hipoclorito de sodio al 1%, está indicado para el tratamiento de
conductos radiculares de dientes con vitalidad y necrosis pulpar, pero sin lesión
apical. (2)
Según Cohen y Burns (2001) el NaOCl al 1% posee propiedades antimicrobianas
y de disolución de tejido muy buenas si es utilizada en abundancia. A diferencia
de las soluciones de NaOCl a mayor concentración afectan a los tejidos apicales y
periapicales. (8)
1.3 Solución de hipoclorito de sodio al 2.5 % (solución de Labarraque)
La solución de hipoclorito de sodio al 2.5% está indicado para el tratamiento de
conductos radiculares con necrosis y lesión periapical. (2)
1.4 Solución al 5.25% (preparación oficial, USP)
La solución de hipoclorito de sodio al 5.25% es una de las mas utilizadas por los
endodoncistas, ya que presenta buena acción antimicrobiana y disolvente. Su
efecto será lo necesariamente dañino para eliminar las bacterias que comúnmente
están presentes en el conducto radicular, pero a su vez, ésta concentración será
altamente tóxica e irritante. (3)
Spangberg y col. (1972) evalúan tanto in vivo como in vitro el NaOCl al 5.25% y
reportan que éste presentaba excelentes propiedades antimicrobianas pero a su
vez, esta concentración era altamente tóxica e irritante. Hand y col. también
demuestran que el NaOCl al 5.25% aparte de ser un potente antimicrobiano, es un
disolvente de tejido pulpar muy eficaz. El porcentaje y el grado de acción
antimicrobiana y de disolución de tejido orgánico están en función de la
concentración del irrigante. (3)
Según Johnson y col. cuanto mas concentrada sea la solución de hipoclorito de
sodio, mejor será su poder de disolución tisular (tejido vivo o necrótico) y mayor
su capacidad de neutralización del contenido tóxico del conducto radicular. Sin
embargo, cuanto más concentrada sea esa solución, mayor será su efecto irritante
cuando esté en contacto con los tejidos vivos apicales y periapicales.

18
Compararon las soluciones de hipoclorito de sodio al 3%, 6%, 8% y 10% y
concluyeron que al aumentar la concentración de las soluciones de hipoclorito de
sodio de forma que supere el 6%, no determinaba que su capacidad solvente
aumentaría. (2)
Siqueira y col. (2000) comparan la efectividad antimicrobiana del hipoclorito de
sodio a diferentes concentraciones (1%, 2.5% y 5.25%) y la solución salina contra
el E. faecalis en un estudio in vitro. Las tres concentraciones de hipoclorito de
sodio, fueron significativamente más efectivas que la solución salina en cuanto a
reducir el número de bacterias de E. faecalis en el conducto radicular. Se alcanzó
una reducción considerable de bacterias usando NaOCl en sus diferentes
concentraciones. Las soluciones de mayor concentración tuvieron mejores efectos
antimicrobianos que las soluciones de menos concentración. No obstante no se
logro eliminar totalmente las bacterias del conducto radicular. (16)
Vianna y col. (2004) refieren que cuanto mayor concentración tenga el NaOCl
menor será el tiempo que requiera en eliminar microorganismos aerobios (S.
aureus, C. albicans), anaerobios (P. endodontalis, P. gingivalis, P intermedia) y
facultativos (E. faecalis). El NaOCl al 5.25% mata los microorganismos en 15 s,
mientras las soluciones de NaOCl al 0.5% y 1% requieren de un mayor tiempo
para matar estos mismos microorganismos, entre 20-30 min. (4)
2.- TEMPERATURA
El aumento de temperatura del hipoclorito de sodio (NaOCl), será un factor
importante que ayudará a la solución, a mejorar su acción disolvente de tejido
orgánico. El aumento de temperatura, disminuye la tensión superficial del NaOCl
y como consecuencia habra una mejor penetración de la solución a través de los
túbulos dentinarios. (3)
Según Cunninghan y Balekjian (1980) el NaOCl al 5,25% y 2,6% tuvieron la
habilidad de disolver el colágeno del tejido pulpar tanto a temperatura ambiente
(21°C) como a temperatura corporal (37°C). Sin embargo, demostraron que la
solución de NaOCl al 2.6% era un agente igual de efectivo disolviendo el
colágeno que la solución de NaOCl al 5.25% tanto a 21°C como a 37°C. Este
efecto fue únicamente válido para la disolución del colágeno. 24 horas después se
demostró que hubo pérdida de los iones cloro, por lo que no se recomienda

19
calentar la solución de hipoclorito de sodio por un periodo prolongado, porque
pierde sus propiedades. (7, 17,18)
Según Sirtes y col (2005) el NaOCl al 1% a 45°C disuelve el tejido pulpar tan
efectivamente como el NaOCl al 5.25% a temperatura ambiente (20°C). Sin
embargo el NaOCl al 1% a 60°C disolvía el tejido pulpar de una manera mucho
más efectiva. (10)
Rossi-Fedele y col (2008) evalúan la habilidad y velocidad del NaOCl al 4% para
disolver el tejido pulpar, para lo cual lo dividen en cuatro grupos a diferentes
temperaturas: Grupo C: NaOCl al 4% a temperatura ambiente (20.5°C – control),
Grupo T1: NaOCl al 4% a 45°C, Grupo T2: NaOCl al 4% a 60°C y Grupo T3:
NaOCl al 4% a 75°C. Los 4 grupos mostraron ser eficaces al diluir el tejido
pulpar bobino. Sin embargo, hubo un incremento significativo en la velocidad de
disolución del tejido pulpar del grupo T1 en comparación del grupo C. Y de los
grupos T2 y T3 en comparación del grupo T1. Los grupos T1 y T2 mostraron
tiempos de disolución del tejido pulpar similares. (19)
3.- ESTABILIDAD QUÍMICA
Las soluciones de hipoclorito de sodio comerciales son más alcalinas,
hipertónicas y tienen una concentración de cloro entre 10% a 14%. Y por lo tanto,
van ha ser más fácil que se deterioren con el tiempo, a la exposición a la luz, a la
temperatura y a la contaminación con iones metálicos. La alta concentración de
cloro en las soluciones irrigantes de hipoclorito de sodio hace que éste se
transforme en una solución ácida, y por lo tanto menos inestables. Cuanta mayor
concentración tenga la solución de hipoclorito de sodio, mayor inestabilidad va a
tener. Algunos autores reportan que la estabilidad química y las propiedades del
hipoclorito de sodio se van a ver afectadas por la exposición a altas temperaturas.
Se cree que la falta de estabilidad química es un factor importante que puede
afectar negativamente a las propiedades bactericidas, disolventes de tejidos vivos
y/o necróticos, como también pueden disminuir la capacidad de detoxificación,
por lo que se deben almacenar en periodos cortos de tiempo y en ambientes
apropiados.
(2, 20)

20
Gambarini (1998) evalúa la estabilidad química del hipoclorito de sodio después
de ser calentada durante 30 días. El estudio consistía en calentar dos botellas de
hipoclorito de sodio cada 12 horas durante 30 min a 50°C con el fin de medir el
contenido de cloro remanente, pH y densidad a los 3, 7, 14, 21 y 30 días; se
encontró que no hubo efecto adverso en la estabilidad química de la solución
después de 30 días, ya que el pH se mantuvo con una disminución mínima, la
densidad no aumentó significativamente y la disminución de cloro en la solución
fue baja. Estos hallazgos nos demuestran que al calentar la solución de hipoclorito
de sodio, se mantiene la estabilidad química, y se mejora la acción disolvente de
tejido orgánico y se mantienen las propiedades de disolución de tejido orgánico,
debido a que al aumentar la temperatura se logra una disminución en la tensión
superficial del hipoclorito de sodio, permitiendo que éste tenga mayor penetración
en los tejidos.
Al aumentar la temperatura se mejora el desbridamiento, las propiedades
bactericidas y de disolución de tejido orgánico. No refieren que este aumento de
temperatura afecte la estabilidad química de la solución, aunque recomienda
cierta precaución ya que no se sabe que daño puede causar a los tejidos
periapicales. (20)
4.- PH DE LA SOLUCIÓN
Gracias a su pH alcalino 11 -12, la solución de hipoclorito de sodio neutraliza la
acidez del medio dejando el ambiente impropio para el desarrollo bacteriano. (2)
Pécora y col. encontraron que la solución de hipoclorito de sodio pierde 4,6% de
cloro cuando se almacena a temperatura ambiente durante 60 días y conforme
aumenta el tiempo de almacenamiento también aumenta la pérdida de cloro.
Clarkson y col. (2001) refieren que cuanto menor contenido de cloro tenga la
solución de hipoclorito de sodio, menor será el pH del irrigante. Por tal razón, es
importante, el lugar de almacenaje del NaOCl. Aquel NaOCl de menor
concentración va ser que el contenido del hipoclorito de sodio caiga más
fácilmente que uno de mayor concentración. (21)

21
II.4.1.2 GLUCONATO DE CLORHEXIDINA
RESEÑA HISTÓRICA:
El Gluconato de Clorhexidina fue desarrollada en la década de 1940 en Inglaterra
y se comercializó en 1954 como antiséptico para heridas de piel. Más adelante, el
antiséptico empezó a utilizarse mas ampliamente en medicina y cirugía, incluidas
las ramas de obstetricia, ginecología, urología y preparación prequirúrgica de la
piel, tanto para el paciente como para el cirujano. La Clorhexidina en Odontología
inicialmente se empleó para desinfectar la boca. A partir de 1970, gracias a los
estudios realizados por Loe y Schiott, se popularizó como enjuague bucal, capaz
de inhibir la neoformación de placa y el desarrollo de gingivitis. En 1975, Baker y
col. Ya consideraban viable el uso de Clorhexidina como irrigante en endodoncia.
En 1982, Delany y col. concluyeron que la clorhexidina es un agente
antibacteriano efectivo al utilizarse como irrigante durante la terapia endodóntica.
(22)
Gracias a sus propiedades antibacterianas y antifúngicas, la solución de clorhexidina
(CHX), es usada actualmente como antiséptico bucal a diferentes concentraciones, ya
sea en forma enjuagues, irrigación subgingival, gels, dentífricos o chiclets, (2) con el
fin de prevenir y tratar las enfermedades periodontales y de caries dental. Sin
embargo, también es ampliamente usada en los tratamientos de conductos radiculares
como solución irrigante y medicamento intraconducto. (4)
Este agente antimicrobiano ha sido utilizado de manera eficaz en el control de
enfermedades bucales en pacientes de edad y minusválidos, ya que al ser ingerido se
elimina casi totalmente por las ese fecales. De esta manera, la cantidad mínima
absorbida por el tracto intestinal, va a ser eliminada por los riñones y el hígado, y no
hay evidencia de que pueda permanecer retenida en el organismo. (2)

22
ESTRUCTURA QUÍMICA
La Clorhexidina (CHX) es una biguanida catiónica, compuesta por dos anillos
simétricos 4-clorofenólicos y dos grupos biguanida conectados por un puente
central de hexametileno, con dos cargas positivas en cada extremo del puente.
(23)
Contiene 0.12% de gluconato de clorhexidina en una base que contiene agua,
11.6% de alcohol, glicerina y agentes saborizantes. (3)
Grafico 4. FÓRMULA DE MOLÉCULA DE CLORHEXIDINA
MECANISMO DE ACCIÓN:
La clorhexidina es una molécula con carga positiva hidrofóbica y lipofílica, la
cual presenta un amplio espectro contra bacterias gram positivas y negativas,
esporas bacterias, virus lipofílicos y dermatofitos. Ésta interactúa con los
fosfolípidos y lipopolisacáridos de la membrana celular de las bacterias a un pH
de 5.0 -8.0 y posteriormente entra a la bacteria por algún tipo de mecanismo de
transporte activo o pasivo. Su eficacia se da gracias a la interacción de la carga
positiva de la molécula y la carga negativa de los grupos fosfatos en la pared de
las células microbianas, alterando de esta manera el equilibrio osmótico de la
célula, lo cual va a permitir el incremento en la permeabilidad de la pared celular
de la bacteria, y la molécula de clorhexidina podrá entrar dentro de la bacteria.
(24)
A bajas concentraciones de Clorhexidina, las sustancias de bajo peso molecular
salen, especialmente potasio y fósforo, provocando de esta forma el efecto
bacteriostático. Por el contrario, a altas concentraciones, la Clorhexidina tiene
efecto bactericida debido a la precipitación y/o coagulación del citoplasma. (3)

23
VENTAJAS Y DESVENTAJAS DEL USO DE CLORHEXIDINA (CHX)
VENTAJAS:
Por presentar propiedades antibacterianas, antifúngicas y antivirales, es uno de las
soluciones irrigantes más utilizadas en endodoncia. Como irrigante endodóntico, la
clorhexidina es utilizada al 0.12% o 2%, demostrando propiedades antibacterianas
similares a las del hipoclorito de sodio (NaOCl). En bajas concentraciones actúa
como bacteriostático y en altas concentraciones como bactericida. (2)
1.- ACCIÓN ANTIMICROBIANA
La actividad antimicrobiana de esta solución comprende un amplio espectro
contra los microorganismo, incluyendo el E. faecalis y la C. albicans; sin
embargo para lograr el efecto letal contra estos microorganismos la
concentración debe ser cuanto menos al 1%, preferentemente al 2%. (22)
Siqueira y col. (1998) comparan la acción antimicrobiana del NaOCl al 0.5%,
2.5% y 4%, el gluconato de CHX al 0.2% y 2%, el ácido cítrico al 10% y el
EDTA al 17%, contra contra cuatro anaerobios gram negativo negro-
pigmentados (P. endodontalis, P. gingivalis, P. intermedia, P. nigrescens) y
cuatro anaerobios facultativos (E. faecalis, S. mutans, S. sanguis, S. sabrinus). Y
encontraron que todos los irrigantes mencionados tuvieron una acción
antibacteriana contra las cepas analizadas. E hicieron un ranking de acción
antibacterial desde la solución más fuerte a la más débil y va como sigue:
NaOCl al 4%, NaOCl al 2.5, gluconato de CHX al 2 %, gluconato de CHX al
0.2 %, EDTA al 17%, ácido cítrico al 10% y el NaOCl al 0.5%. Se demostró
que el NaOCl al 4% era estadísticamente mejor que la CHX al 0,2% y 2%
contra los cuatro anaerobios gram negativo negro- pigmentados y los cuatro
anaerobios facultativos. (25)
Vianna y col (2004) comparan la efectividad antimicrobiana de la clorhexidina
gel y líquida en sus diferentes concentraciones (0.2%, 1% y 2%) en relación al
tiempo que requieren para matar microorganismos aerobios (S. aureus, C.
albicans), anaerobios (P. endodontalis, P. gingivalis, P intermedia) y
facultativos (E. faecalis).

24
La CHX liquida al 0.2%, 1% y 2% y la CHX gel al 2% eliminaron
microorganismos facultativos y aerobios en 1 minuto o menos. Mientras que a
la CHX gel al 0.2% le tomo hasta 2 horas para matar estos mismos
microorganismos.
A pesar que todos los irrigantes probados poseían actividad antimicrobiana, el
tiempo necesario para eliminar E. faecalis depende de la concentración y el tipo
de irrigante utilizado. (4)
2.- SUSTANTIVIDAD
Después de la obturación final y antes de la restauración definitiva, hay
diferentes situaciones en las que el conducto radicular puede volverse a infectar,
como son el momento en el que el diente esta temporalmente restaurado o
cuando no se utiliza aislamiento absoluto mientras se realiza la restauración
final. Por otra parte, la reinfección del conducto radicular puede ocurrir cuando
hay un nuevo crecimiento de microorganismos residuales que han sobrevivido a
los procedimientos durante el tratamiento de conductos radiculares.
La clorhexidina tiene una propiedad única, la cual es prevenir la colonización
microbiana de la superficie dentinaria durante un periodo prolongado. (26) Su
prolongada presencia dentro del conducto puede favorecer la acción
antibacteriana en caso que fuera necesario dejarlo como medicamento
intraconducto, demostrando así eficientes características clínicas debido a que
va a estar mayor tiempo en contacto con el tejido, esto, en el caso que la
endodoncia no pueda ser realizada en una sola cita. (3)
La Clorhexidina absorbida gradualmente es liberada durante más de 24 horas,
por eso se cree que reduce la colonización bacteriana en la superficie de los
dientes.
Weber y col. encontraron in vitro que la clorhexidina posee un amplio espectro
antibacteriano residual hasta por 168 horas posteriores a su aplicación. (15)
Rosenthal y col. reportan que la sustantividad de la clorhexidina perdura hasta
por 2 semanas. (27)
Khademi y col (2006) evaluaron la sustantividad de la CHX al 2%, del NaOCl
al 2.6% y 10 ml -1 de doxiciclina durante 28 días (4 semanas). El NaOCl al
2.6% mostró la mejor eficacia antibacteriana al primer día, pero conforme fue

25
pasando el tiempo, su acción antibacteriana fue decayendo rápidamente. A
diferencia de la clorhexidina que no mostró acción antibacteriana al inicio, sin
embargo con el paso de los días y semanas mantuvo una buena acción
antibacteriana contra el E.faecalis. La sustantividad de la clorhexidina fue
mucho mejor que la de la doxiciclina, mientras que el hipoclorito de sodio no
llegó a presentar sustantividad con el paso de los días. (27)
3.- BAJA TOXICIDAD
Ya que la clorhexidina es significativamente menos tóxica que el hipoclorito de
sodio, va poder ser utilizada en dientes con perforaciones o ápices abiertos.
Otra de las ventajas de la Clorhexidina es que va a poder ser usada en pacientes
que son alérgicos al hipoclorito de sodio. Si es utilizada al 0.2% causa mínima
toxicidad al tejido. (3)

26
DESVENTAJAS:
El Gluconato de clorhexidina es una solución relativamente no tóxica, posee amplio
espectro antibacteriano residual, no afecta el comportamiento de los cementos
selladores a corto ni largo plazo, sin embargo y a diferencia del hipoclorito de
sodio, (15) su principal desventaja será no tener la capacidad de disolver tejido
orgánico (ni vital ni necrótico). (2,3)
Okino y col (2004) evalúan la capacidad de disolución de tejido orgánico del
NaOCl al 0.5%, 1% y 2.5%, del digluconato de CHX líquida al 2%, digluconato de
CHX gel al 2% y del agua destilada como control. Fragmentos de pulpa bovina
fueron pesados y colocados junto con 20 ml de cada solución en un tubo de ensayo
y centrifugados a 150 rpm hasta su total disolución. El tiempo de velocidad de
disolución de la pulpa se calculó dividiendo el peso de la pulpa entre el tiempo de
disolución. El agua destilada y los distintos tipos de CHX no tuvieron la capacidad
de disolver la pulpa en un periodo mayor a 6 horas. Mientras que el periodo de
disolución de tejido pulpar del NaOCl al 0.5%, 1%, 2.5% fue 0.31, 0.43 y 0.55 mg
min -1 respectivamente. (28)
Además, su uso a larga escala va ha tener restricciones en razón de sus defectos
colaterales que son reversibles, tales como pigmentación de la lengua, dientes y
restauraciones, descamación de la mucosa oral, además de síntomas subjetivos
como sabor amargo, sensación de quemadura (ardor) e interferencia en la sensación
gustativa. (2)

27
ESTUDIOS COMPARATIVOS DEL HIPOCLORITO DE SODIO (NaOCl) Y
LA CLORHEXIDINA (CHX)
1.- ACTIVIDAD ANTIMICROBIANA
Siqueira y col (1998) reportan que todos las soluciones irrigantes utilizadas para
el estudio tuvieron acción antibacteriana contra las cepas analizadas. Sin embargo,
se demostró que el NaOCl al 4% era estadísticamente mejor que la CHX al 0,2%
y 2% eliminando a los cuatro anaerobios gram negativo negro- pigmentados y los
cuatro anaerobios facultativos. (25)
Vianna y col (2004) reportan que la CHX liquida al 0.2%, 1% y 2% y la CHX gel
al 2% eliminaban microorganismos facultativos y aerobios en 1 minuto o menos.
Mientras que a la CHX gel al 0.2% le tomo hasta 2 horas para matar estos
mismos microorganismos. Por otro lado, el NaOCl al 5.25% mató los
microorganismos en 15 segundos, mientras que las soluciones de NaOCl al 0.5%
y 1% requirieron de un mayor tiempo para matar estos mismos microorganismos,
entre 20-30 minutos. (4)
Sassonei y col (2008) reportan que el NaOCl al 1% y 5% y la Clorhexidina al 1%
muestran una efectiva acción antimicrobiana contra el E. faecalis a diferencia del
la Clorhexidina al 0.12% y 0.5% que muestran ser inefectivos contra estos
mismos microorganismos. (13, 14)
2.- DISOLUCIÓN DE TEJIDO PULPAR
La clorhexidina a diferencia de la solcuión de hipoclorito no tiene la capacidad de
disolver tejido orgánico (vital ni necrótico), lo cual se considera como su mayor
desventaja.
Según Cunninghan y Balekjian (1980) el NaOCl al 5,25% y 2,6% tuvieron la
habilidad de disolver el colágeno del tejido pulpar tanto a temperatura ambiente
(21°C) como a temperatura corporal (37°C). Sin embargo, encontraron que la
solución de NaOCl al 2.6% era un agente igual de efectivo disolviendo el
colágeno que la solución de NaOCl al 5.25% tanto a 21°C como a 37°C. (17, 18)
Okino y col (2004) reportaron que el agua destilada y los distintos tipos de
digluconato de CHX gel y líquida al 2% no tuvieron la capacidad de disolver la
pulpa en un periodo de 6 horas. Mientras que el tiempo de velocidad de

28
disolución de tejido pulpar del NaOCl al 0.5%, 1%, 2.5% fue 0.31, 0.43 y 0.55
mg min -1 respectivamente. (28)
3.- SUSTANTIVIDAD
El hipoclorito de sodio no presenta ninguna actividad antimicrobiana residual
hasta después de la obturación final, como es el caso de la clorhexidina. La
clorhexidina a diferencia del hipoclorito de sodio continúa su liberación por un
periodo posterior a la instrumentación. (26)
Según Khademi y col (2006) el hipoclorito de sodio no presenta sustantividad. A
diferencia de la clorhexidina que no muestra acción antimicrobiana al inicio, sin
embargo mantuvo su sustantividad contra el E. faecalis hasta por 4 semanas,
mostrando mejor acción antimicrobiana las dos primeras semanas. Esto
confirmaría la teoría de Rosenthal y col. quienes demuestran la sustantividad de la
clorhexidina hasta por 2 semanas. (27)

29
INTERACCIÓN DEL HIPOCLORITO DE SODIO (NaOCl) Y LA
CLORHEXIDINA (CHX)
Estudios realizados en ratas mezclan las soluciones de hipoclorito de sodio y
clorhexidina con el fin de aprovechar ambas propiedades. Y concluyen diciendo que
al juntar estas dos, se forma un precipitado, el cual tiene efectos cancerígenos.
Basrani y col (2007) mezcla estas dos soluciones irrigantes para determinar cual es la
concentración mínima de hipoclorito de sodio que se requiere para formar este
precipitado. Mezcla clorhexidina con diferentes concentraciones de de hipoclorito de
sodio ( NaOCl al 6% hasta 0.023%). Y determina que la solución de hipoclorito de
sodio mínima requerida para que se forme este precipitado denominado
paracloranilina (PCA) era NaOCl al 0.023%. Esta reacción se va a dar gracias a la
sustitución de un grupo guanidina de la molécula de clorhexidina. La CHX es una
acido dicatiónico (pH 5.5-6.0) que tiene la habilidad de donar protones, mientras que
el NaOCl es alcalino y puede aceptar protones. Como una amina aromática, el
principal efecto tóxico sera la formación de meta globulina. El incremento de PCA va
a estar correlacionado con altas concentraciones de NaOCl. (29)
Delany y col (2003) indican el uso de hipoclorito de sodio al 2.5% en las primeras
irrigaciones, aprovechando su capacidad de disolver tejido orgánico, continuando con
la Clorhexidina al 0.2%, la cual posee acción antibacterial sumada a la adecuada
sustantividad y bio-compatibilidad de este compuesto. De esta manera se
aprovecharía la propiedad de disolución de tejido orgánico del NaOCl y la propiedad
antibacterial y de sustantividad de la CHX, con menor riesgo a efectos citotóxicos en
los tejido periapicales. (30)

30
II.4.2 DETERGENTES SINTÉTICOS
Los detergentes son sustancias químicas semejantes al jabón, que se emplean con
frecuencia como soluciones de irrigación, debido a que son muy efectivos para
eliminar los residuos del tejido graso, que quedan como productos colaterales de la
necrosis pulpar. (8) Por la baja tensión superficial, los detergentes desarrollan una
acción de limpieza, penetrando más profundamente en los túbulos dentinarios,
laterales, colaterales, secundarios y accesorios, humedeciendo las paredes del
conducto radicular, combinándose con los restos orgánicos, virutas de dentina y
bacterias que se encuentran en su interior, atrayéndolos a la superficie o
manteniéndolas en suspensión. (2)
Estas sustancias actúan en los procesos de: lubricación, humectación (riego),
formación de espuma, emulsificación; dispersión, diseminación, solubilización,
además de que reducen la tensión superficial de los sustratos por ejemplo; las paredes
dentinarias (para un mejor contacto entre la medicación tópica entre sesiones y el
material de obturación.)
Los productos utilizados con mayor frecuencia pertenecen a la familia de compuestos
de amonio cuaternario. Los antisépticos derivados del amonio cuaternario se emplean
en solución acuosa a concentraciones entre 0.1% y 1%.
Estos productos tienen una toxicidad muy similar a la de otras soluciones de
irrigación y su espectro bactericida va a ser bastante limitado. (8)
El Zephiran Chloride se ha empleado frecuentemente como solución irrigante en
endodoncia. Si se tiene en cuenta su toxicidad y su baja eficacia microbiana, no
tendría sentido utilizar este detergente cuando se podría utilizar una solución irrigante
con mejores propiedades como el NaOCl < al 1%. (8)

31
II.4.3 QUELANTES
Se denomina quelantes a las sustancias que tienen la propiedad de fijar los iones
metálicos de un determinado complejo molecular. El término quelar es derivado del
griego “Khele” que significa garra, así como de la palabra quelípodo pata de ciertas
especies de crustáceos que terminan en pinza o garra como el cangrejo y que sirven
para aprisionar a sus alimentos. (2)
Los quelantes presentan en la extremidad de sus moléculas, radicales libres que se
unen a los iones metálicos actuando de manera similar a los cangrejos. Estas
sustancias roban los iones metálicos del complejo molecular en que se encuentran
entrelazados, fijándolos por una unión coordinada, a la cual se le denomina quelación.
Por lo tanto, la quelación es un fenómeno físico químico, por el cual ciertos iones
metálicos son secuestrados de los complejos de lo que participan, sin constituir una
unión química con las sustancia quelante sino una combinación. Este proceso se
repite hasta que se agota la acción quelante, y no se realiza por el mecanismo clásico
de la disolución.
La dentina es un complejo molecular que tiene en su composición los iones de calcio
y sobre la cual se aplica el quelante; lo que puede resultar en una deficiencia de iones
calcio que le dará más facilidad de desintegración.
No todos los quelantes fijan cualquier ion metálico, hay una cierta especificidad para
determinados iones, que pueden ser secuestrados sin que el quelante actúe sobre otros
iones presentes en un determinado complejo molecular.
El ácido etilenodiaminotetracético, el EDTA, es un quelante específico para el ión
calcio y por consiguiente para la dentina. (2)
INDICACIONES:
Las soluciones quelantes se indican para la preparación biomecánica de conductos
radiculares atrésicos y/o calcificados.
A pesar de los excelentes resultados obtenidos con ese producto en lo que se refiere a
la limpieza de los conductos radiculares, no se indica como solución de irrigación,
sino como un auxiliar para ensanchar conductos atrésicos o calcificados y remover el

32
barro dentinario (“smear layer”) en el lavado quirúrgico final de la preparación
biomecánica. (2)
II.4.3.1 EDTA ( Sal disódica del ácido etilendiaminotetracético)
El EDTA fue presentado por primera vez por Nygaard-Ostby en 1957. Es una
sustancia fluida con un pH neutro de 7,3, la cual se emplea en una concentración de
10 - 17%. Con esta solución se logra reducir a siete el grado de dureza Knoop de la
dentina, que normalmente tiene una dureza de cuarenta y dos cerca de la luz del
conducto no tratado. Posee un pequeño efecto antibacterial sobre ciertas especies
bacterianas como Streptococcus alfa-hemolíticos y Staphylococcus aureus, y tiene un
alto efecto antimicótico. Produce una reacción inflamatoria leve al contacto con tejido
blando y al contacto con tejido óseo reacciona en forma similar al de la dentina.
Entre las soluciones quelantes utilizadas con mayor frecuencia para la irrigación se
incluyen EDTA, EDTAC y RC-Prep, en las que el ingrediente activo es el ácido
diaminoetilentetracético. (9)
Figura 2: EDTA al 17%
Cortesía de la Dra. Allison Chávez

33
EDTA - REMOCIÓN DE BARRO DENTINARIO
Cada vez que la dentina del conducto radicular es removida ya sea con instrumentos
manuales o rotatorios, se va producir una fina capa de materia orgánica e inorgánica a
la cual se le va a llamar barro dentinario. El barro dentinario es una mezcla de
bacterias, dentina, predentina, residuos pulpares, procesos odontoblásticos y restos de
irrigante.
Erick y col (1970) reportaron por primera vez la existencia de barro dentinario en el
conducto radicular, mediante la microsonda electrónica con microscopio electrónico
de barrido (SEM), y demostraron que su espesor era de aproximadamente 0.5% -15
micras.
Brännström & Johnson (1974) demostraron mediante estudios de microscopía
electrónica escaneada que la capa de barro dentinario no era tan delgada como se
suponía, sino que su espesor era de 2-5 micras. (31)
Lester & Boyde (1977) refieren que como el barro dentinario no pudo ser removido
por completo con el EDTA, su composición principal debía ser dentina orgánica.
Goldman y col. (1981) estuvieron de acuerdo con las investigaciones pasadas,
quienes describían que el espesor del barro dentinario era de 1 micra, y concordaban
que la composición principal del barro dentinario era de dentina orgánica.
Mader y col. (1984) reportan que el espesor del barro dentinario era de 1-2. (31)
La remoción del barro dentinario sigue siendo un tema controversial. Ya que algunos
autores, refieren que el barro dentinario actúa como una barrera de metabolitos
bacteriales, previniendo la invasión bacteriana a través de los túbulos dentinarios. Sin
embargo, los microorganismos se va a poder multiplicar en el barro dentinario y van a
poder penetrar a través de los túbulos dentinarios.
Muchos autores mencionan que la impermeabilidad del diente después de la
obturación es mucho mayor después de la remoción del barro dentinario, mientras
que otros autores no mostraron diferencias estadísticamente significativas. (32)
El EDTA se aconseja con frecuencia como solución irrigante, puesto que tiene la
capacidad de quelar y eliminar la porción mineralizada de la capa de barro dentinario.
Si se emplea en mucha cantidad puede descalcificar una capa de hasta 50 mm de
pared del conducto radicular. (8)
Numerosos estudios han demostrado que la irrigación con EDTA al 17% tiene un
buen efecto de limpieza en las paredes del canal radicular. (32)

34
EDTA E HIPOCLORITO DE SODIO
El barro dentinario evita la penetración de irrigantes, medicamentos o materiales a
través de los túbulos dentinarios. No hay irrigante que haya demostrado ser capaz de
disolver tejido orgánico y a su vez desmineralizar el tejido calcificado. (5) Ya que el
barro dentinario comprende de un componente orgánico y otro inorgánico, para
eliminar el barro dentinario, el EDTA no suele ser suficiente por sí solo, ya que éste
solo elimina el componente inorgánico. Se le debe añadir un componente proteolítico
como el hipoclorito de sodio, para eliminar el componente orgánico de la capa de
barro dentinario. (8) para lo cual se han desarrollado técnicas que consisten en alterar
de manera secuencial los agentes de irrigación. Irrigar el conducto radicular con
NaOCl al 5.25%, seguida de una irrigación final con EDTA entre 3% - 17%, nos
permite obtener una efectiva acción quelante sobre la hidroxiapatita de los túbulos
dentinarios, actuar sobre los microorganismos presentes y favorecer el contacto
íntimo del cemento sellador. (5)
Yamashita y col (2003) comparan la efectividad en la remoción de barro dentinario
de 4 soluciones irrigantes: 1. Solución salina, 2. clorhexidina al 2%, 3.hipoclorito de
sodio al 2.5% e 4. hipoclorito de sodio al 2.5 % + EDTA. La mejor limpieza del
conducto radicular la obtuvieron el hipoclorito de sodio al 2.5 % +EDTA, seguido
del hipoclorito de sodio al 2.5 %. El tercio apical de los conductos radiculares no fue
limpiado tan bien como el tercio medio y coronal. La limpieza de la solución salina y
la clorhexidina fue inferior en comparación a la limpieza que tuvo el hipoclorito de
sodio + EDTA. (33)

35
A continuación se presentan dos imágenes con microscopia electrónica de barrida.
La figura 1 nos muestra como los túbulos de la dentina peri e intertubular quedan
tapados por una fina capa de barrillo dentinario después de la instrumentación y en la
figura 2, como se erocionan estos túbulos peri e intertubulares, luego de aplicarles
NaOCl al 5.25% + EDTA al 17% por 10 minutos. (31)
Figura 3: Remoción parcial Del barro dentinario
al minuto de la aplicación de NaOCl al
5.25% + EDTA al 17%
Figura 4: Remoción parcial Del barro dentinario
a los 10 minutos de la aplicación de
NaOCl al 5.25% + EDTA al 17%

36
II.4.4 ASOCIACIONES
II.4.4.1 RC - Prep
La unión de EDTA + el peróxido de urea, desarrollan una nueva fórmula que tiene
por nombre comercial RC-Prep.
Stewart y col. unieron el peróxido de urea (bactericida) y el EDTA (quelante)
asociados a una base estable, con la finalidad de ofrecer las ventajas de cada uno de
ellos y proporcionar una rápida y completa preparación biomecánica.
Comprobaron que la mejor y más estable asociación fue la que se preparó triturando
el polvo de EDTA en peróxido de urea, homogenizado en una base carbowax
(polietilenglicol). Esta sustancia, de consistencia cremosa, además de servir de
vehículo, presenta según sus autores otras propiedades deseables: es totalmente
soluble en agua, se licuefacciona a la temperatura corporal, es más resistente e
indefinidamente estable y finalmente actúa en el conducto radicular como lubricante
para los instrumentos.
La fórmula Del RC-Prep es la siguiente: (2)
EDTA………………………………..15%
Peróxido de urea……………............. 10%
Carbowax……………………. Como base
II.4.4.2 Glyde File Prep
El Glyde File Prep es un nuevo agente quelante producido por la casa
DENTSPLY/MAILLEFER – Ballaigues, Suiza, que contiene EDTA con vehículo de
gel. Este producto se lleva al conducto radicular como un auxiliar de la
instrumentación y se usa alteradamente con las irrigaciones con solución de
hipoclorito de sodio. Se recomienda utilizar el Glyde File prep como solución
complementaria al hipoclorito de sodio en la remoción de barro dentinario. (2)
Lim y col (2003) evaluaron por microscopía electrónica y óptica, la capacidad de
remover el barro dentinario del conducto radicular de dientes humanos extraídos, con
las siguientes soluciones de irrigación que se utilizaron durante la instrumentación.

37
Grupo A: Irrigación con 0.5 ml de solución de hipoclorito de sodio al 1%, después de
cada lima utilizada, complementando con irrigación final de 10 ml de solución de
hipoclorito de sodio al 1%.
Grupo B: Irrigación con 0.5 ml de solución de NaOCl al 1%, después de cada lima
utilizada, completando con una irrigación final con 10 ml de EDTA al 17%.
Grupo C: Utilización de “Glyde File prep” para recubrir cada lima utilizada,
irrigación con 0.5 ml de solución de NaOCl al 1% completando con una irrigación
final, de 10 ml de solución de NaOCl al 1%.
Los resultados mostraron que los conductos radiculares sometidos a la acción del
EDTA y del “Glyde File prep resultaron significativamente más limpios que los
sometidos a la acción de la solución de NaOCl usada aisladamente. La irrigación con
la solución de NaOCl, en los casos en que el “Glyde File prep” se utilizó, fue más
eficaz para remover el barro dentinario. (34)
II.4.4.3 MTAD – Doxicilina
El MTAD (4 metil – 1, 24 triazoline-3, 5-dione) es una solución irrigante constituida
por tetraciclina isómera, ácido cítrico y un detergente aniónico denominado Tween
80.
El protocolo para el uso clínico de MTAD es 20 minutos con NaOCl al 1.3% seguido
por 5 minutos de MTAD. Los efectos de solubilización del MTAD en la pulpa y el
esmalte dental son algo similares a los del EDTA.
Varios estudios han demostrado buena propiedad antimicrobiana, sin ser
necesariamente citotóxica. Además, remueve barro dentinario cuando es utilizado
como irrigación final en el tratamiento.
Estudios recientemente realizados en cultivo de células (fibroblastos L929)
demostraron que el MTAD, es menos citotóxico que el eugenol, el agua oxigenada al
3%, pasta de hidróxido de calcio, solución de hipoclorito de sodio al 5.25% y que el
EDTA. Sin embargo, demostró ser más citotóxico que las soluciones de hipoclorito
de sodio al 0.66%, 1.31% y 2.63%.

38
Estudios realizados in vitro comprobaron que el MTAD posee una eficaz acción
antimicrobiana contra el E. faecalis y que es una solución irrigante tan efectiva como
el NaOCl al 5.25%. (2)
Sin embargo, Krause y col (2007) compararon la eficacia antimicrobiana in vitro del
hipoclorito de sodio, MTAD, y dos de sus componentes, doxiciclina y ácido cítrico
contra el E. faecalis. Y obtuvieron que en modelo de difusión del agar, el hipoclorito
y la doxiciclina fueron los que mejor eficacia tuvieron eliminando E. faecalis, en
comparación al MTAD y el ácido cítrico. A pesar que ninguna de las soluciones logro
eliminar el E. faecalis al 100%, el hipoclorito de sodio demostró la mejor eficacia
antimicrobiana. (35)
El MTAD presenta propiedades antimicrobianas, sin embargo su efectividad no es tan
buena como la del hipoclorito de sodio, por lo que este último sigue siendo el
irrigante más utilizado en los tratamientos de conductos radiculares.

39
II.4.5. OTRAS SOLUCIONES DE IRRIGACIÓN
En el mercado existen otras soluciones irrigantes para el tratamiento de conductos
radiculares, las cuales sólo vamos a mencionar ya que la literatura no reporta estudios
en los cuales se demuestre su eficacia antimicrobiana, de disolución de tejido o restos
orgánicos e inorgánicos, de remoción de detritus, substantividad, lubricación ni baja
tensión superficial. (2)
Las otras soluciones de irrigación son las siguientes:
Agua Destilada esterilizada
Agua de hidróxido de calcio – 0.14 g%
Peróxido de Hidrógeno - 10 vol
Suero Fisiológico
Solución de ácido cítrico

40
II.5 MATERIAL E INSTRUMENTL PARA LA IRRIGACIÓN INTRACANAL
JERINGA HIPODÉRMICA
La jeringa hipodérmica es un tubo de plástico descartable, que posee un émbolo
en la parte inferior y una cavidad pequeña en la parte superior por donde se
inserta la aguja. El émbolo se debe jalar cuando uno desea llenar la jeringa y se
presiona para dejar salir el líquido de irrigación. Son fácilmente accesibles y se
van a encontrar en el mercado en sus diferentes tamaños y presentaciones.
Figura 5: Jeringas utilizadas durante la terapia endodóntica
Cortesía de la Dra. Allison Chávez

41
AGUJAS DE IRRIGACIÓN
Durante la irrigación es fundamental que las agujas irrigadoras sean precurvadas y
que se introduzcan profundamente en el conducto radicular. Es preciso disponer
de diferentes calibres (“gauge” G). La industria Ultradent ofrece por el sistema
“Deliver Eze”, aguja con 27 G, 30 G y 31 G de calibre, las cuales son las que se
prefieren para irrigar conductos multirradiculares. (2) Es importante considerar el
largo de la aguja de irrigación, en relación con el conducto radicular. (1) Agujas
de mayor calibre pueden obstruir el conducto e impedir el reflujo normal de la
solución de irrigación. (2)
Se debe tener en cuenta la técnica de irrigación seleccionando la aguja adecuada,
preferiblemente de calibre 27 ya que posee el potencial de penetrar con mayor
profundidad en el conducto, proporcionando una mayor distribución de la
solución; a medida que la preparación se acerca a la constricción apical, la
frecuencia de irrigación debe aumentar realizando siempre movimientos de
bombeo. (3)
Las agujas pueden ser de diferentes tipos aunque se recomiendan las de Max I
Probe, las cuales limpian el conducto hasta el nivel del ápice; ésta es con punta
cerrada y ventana lateral que sin duda es la más segura. (36)
Monseur y Heur recomiendan el sistema monojet, el cual consiste en un sistema
de agujas largas, de extremo abierto y romo que se insertan a toda longitud del
conducto, suministrando un mayor volumen de solución irrigante. (36)
Figura 6: Agujas utilizadas durante la terapia endodóntica.
Cortesía de la Dra. Allison Chávez

42
CANULAS PARA ASPIRACIÓN
En el inicio de la preparación biomecánica, se deben usar las cánulas de mayor
calibre (30-10, 30-08), en razón de la gran cantidad de restos necróticos, etc, que
hay inicialmente en el conducto. En el transcurso de la instrumentación, se pueden
sustituir por cánulas de menor calibre, que pueden entrar más profundamente en
el conducto radicular. Cuanto menos calibre tengan y haya un mayor
ensanchamiento del conducto radicular, habrá una mejor limpieza principalmente
en el tercio apical. Además las cánulas de mayor calibre vana poder ser utilizadas
para conducto más anchos, mientras que las de menor calibre para conductos más
estrechos. (2)
Figura 7: Cánulas de succión
Cortesía de la Dra. Allison Chávez

43
II.6 MECANISMO Y TÉCNICA DE IRRIGACIÓN
El sistema para irrigación endodóntica más simple que existe es: jeringa desechable
de plástico y aguja. Esta técnica de irrigación es simple, rápida y eficaz. Después del
procedimiento de instrumentación con cada una de las limas debe realizarse la
irrigación de los conductos radiculares. (36)
Puede emplearse una de varias jeringas de plástico desechables. La solución irrigante
se coloca en un vasito de vidrio o plástico, el cual se debe mantener lleno para ahorrar
tiempo, el cual nos sirve para ir llenando la jeringa con el líquido irrigante. La jeringa
se llena introduciendo el vástago en la solución y tirando del émbolo. (9) Para evitar
que la solución irrigante sea forzada hacia la región periapical, la presión sobre el
émbolo de la jeringa debe ser leve. (2)
Luego de llenar la jeringa con la solución irrigante se procede a colocar la aguja. La
aguja puede ser de varios tipos y debe doblarse para permitir el suministro fácil de la
solución irrigante. (9) Se recomienda mucho que la aguja penetre en el conducto en
forma pasiva sin hacer contacto con las paredes, mientras se vanr realizando
movimientos de vaivén. Al sentir la resistencia de la punta de la aguja en las paredes
del conducto radicular, aún con el movimiento de vaivén, es preciso remover la aguja.
(2) Ya que se han informado complicaciones graves provocadas al forzar las
soluciones irrigantes más allá del ápice, no se debe introducir la aguja en el conducto
con demasiada fuerza, para que haya un reflujo adecuado. La cinemática del uso de
aguja (vaivén) disminuye la frecuencia de accidentes operatorios. (9)
Se ha encontrado que el volumen apropiado del irrigante debe ser de 1 a 2 ml cada
vez que es irrigado el conducto. Se sabe que durante la irrigación si se usa una
excelente técnica no se van afectar los tejidos periapicales puesto que el irrigante no
debería sobrepasar el ápice radicular.
Una vez irrigados los conductos radiculares se secan con conos de papel estériles,
para ser posteriormente obturados. (9)

44
Abou- rass y col. sugieren que la proximidad de la aguja al ápice desempeña un
cometido importante en la eliminación de los residuos de los conductos radiculares.
(9)
La eficacia en la irrigación del canal radicular en términos de remoción de desechos y
erradicación de bacterias depende de varios factores: (1)
1. Profundidad de penetración de la aguja.
2. Diámetro del canal radicular.
3. Diámetro interno y externo de la aguja.
4. Presión de la irrigación.
5. Viscosidad del irrigante.
6. Velocidad del irrigante en la punta de la aguja.
7. Tipo y orientación del bisel de la aguja.

45
II.7 COMPLICACIONES MÁS FRECUENTES
La literatura especializada, describe muchos incidentes que ocurren durante el
tratamiento de conductos radiculares durante el uso clínico de esas soluciones,
principalmente cuando eran concentradas.
DAÑO A LA ROPA
Es probablemente uno de los accidentes más comunes durante la irrigación del
canal radicular. Ya que el NaOCl es un agente blanqueador doméstico, aún en
pequeñas cantidades en contacto de la ropa va a causar grandes daños,
destiñéndola y tornándola de color blanco. (37)
DAÑO A LOS OJOS
Cuando alguna solución irrigante salpica a los ojos del paciente u operador puede
producir una pérdida de células epiteliales de la capa externa de la córnea. Por lo
que el profesional deberá lavar profusamente con agua y referir al paciente al
oftalmólogo para evaluación y tratamiento. Las manifestaciones clínicas pueden
ser: dolor, abundante lagrimeo, quemazón y eritema. (37)
INYECCIÓN DE LA SOLUCIÓN DE HIPOCLORITO DE SODIO EN LA
REGIÓN PERIAPICAL
Las soluciones de hipoclorito de sodio, tienen un pH de aproximadamente 11-12,
por esta razón, cuando entran en contacto con los tejidos vivos apicales y
periapicales, promueven primeramente una injuria por la oxidación de sus
proteínas. (2) Conductos radiculares con foramen apical amplio, o cuando las
constricción apical ha sido destruida durante la preparación del canal radicular o
por reabsorción, permiten la salida de gran volumen de solución de hipoclorito de
sodio hacia la región periapical, principalmente cuando se presiona demasiado el
émbolo de la jeringa en el momento de la irrigación. Si esto ocurriese, por la gran
capacidad del NaOCl para disolver el tejido orgánico, se produciría necrosis del
tejido. (1, 37)
Este incidente operatorio determina una reacción inmediata del paciente, que
relata ardor y dolor intenso. En pocos segundos pueden aparecer señales de

46
hematoma y equímosis, siendo que el desaparecimiento del dolor y del edema en
pocas horas, es la tendencia normal de este proceso. (2)
Witton y col (2005) reportan el caso de una paciente de sexo femenino de 43 años
de edad, quien acude a consulta por dolor de la pza 12. Se le realiza el tratamiento
de conductos radiculares y se le irriga con 10 ml de NaOCl con una concentración
desconocida. En este caso hubo una quemadura de los tejidos blandos, después de
la extrusión del NaOCl hacia los tejidos periapicales. Clínicamente, la paciente
presentaba dolor, hinchazón de la cara y parestesia del nervio infraorbitario.
Aparentemente, la anatomía del diente era normal, pero por la destrucción del
hueso alrededor del ápice, combinada con la infección crónica y la presión de
irrigación permitieron que haya un ingreso del NaOCl hacia los tejidos
periapicales y con él los microorganismos del canal radicular, produciendo una
infección. (38)
Hay muy pocos casos que ha reportado la literatura de complicaciones
postoperatorias a la piel y alteración en la sensación del nervio, por la utilización
de NaOCl en los tratamientos endodónticos. Y este sería uno de esos pocos casos.
(38)
Figura 8: Pre y post tratamiento de conducto donde ocurrió extravasación de
hipoclorito de sodio.

47
Gernhardt y col (2010) publicaron un caso clínico, con severas consecuencias a
causa de la extrusión hacia la región periapical de la solución concentrada de
hipoclorito de sodio al 5.25%.
Paciente de sexo femenino de 49 años de edad, sometida al tratamiento de
conductos radiculares de la pza 34, que en el examen clínico no reveló indicios de
fístula o de posible cicatrización de la misma. El diagnostico clínico fue de
pulpitis aguda irreversible. Después de remover la pulpa, el conducto se irrigó
abundantemente con solución de hipoclorito de sodio al 5.25%, con jeringas sin
excesiva presión. Dos minutos después, la paciente relató un dolor difuso con
sensación de ardor en el labio inferior y en la región mandibular izquierda.
Después de la remoción inmediata del dique de goma, se observó un edema
intenso del labio. En pocos minutos un edema disperso surgió en la mucosa
próxima al diente en tratamiento, desarrollándose del lado izquierdo de la mejilla
una alteración netamente visible. Después de irrigar el conducto radicular con
solución fisiológica y secarlo, se colocó ledermix y el acceso coronal se obturó
con Cavit. Después de un pequeño intervalo de tiempo, el edema extraoral
diminuyó, dejando un color azul violeta en la piel. Se observó una pequeña
perforación necrótica en la mucosa bucal adyacente a la pza 34. Para evitar una
posible superinfección local de la zona, se recetó una terapéutica antibiótica
sistémica (Doxicilina -100mg) diariamente durante 10 días. Cuatro días después
el tratamiento endodóntico fue reiniciado. Los autores demostraron por el relato
de este caso clínico, que las soluciones concentradas de hipoclorito de sodio
cuando se extruyen inadvertidamente hacia la región periapical, causan severos
daños tisulares, gran molestia para el paciente y por consiguiente, dudas sobre la
habilidad del profesional. Por tal razón es importante confirmar la longitud e
integridad del conducto radicular antes de utilizar NaOCl en altas
concentraciones. (39).

48
Figura 9: Rx de diagnóstico antes del tratamiento
Figura 10: Marcada hinchazón del labio inferior, minutos
después de irrigar el conducto radicular con
altas concentraciones de hipoclorito de sodio
Figura 11: Se evidencia una hinchazón difusa a nivel de fondo de surco de la
premolar. (Figura derecha)
Figura 12: Se evidencia una perforación a nivel del ápice de la premolar
(Figura izquierda)
Figura 13: 5 días después del accidente, se evidencia amplio hematoma que se
extiende desde la región labial en toda la región mandibular
hasta el cuello. (Figura izquierda)
Figura 14: 5 días después de la complicación, se evidencia incremento de la
perforación a nivel del ápice de la premolar y necrosis de la mucosa
oral. (Figura derecha)

49
LESIONES DE PIEL CAUSADAS POR LA SALIDA DE HIPOCLORITO
DE SODIO A TRAVÉS DEL DIQUE DE GOMA
Serper y col (2004) reportan el caso de una paciente de sexo femenino de 54 años
de edad, a la cual se le realiza el tratamiento de conductos radiculares de la pieza
25. Durante la irrigación del conducto con NaOCl al 2.5%, la paciente se queja de
una sensación de quemazón, pero el operador ignora las quejas y continúa con el
tratamiento hasta concluirlo. Al retirar el dique de goma, se evidencia una extensa
quemazón en la piel de la paciente que se extendía desde el labio inferior hasta la
barbilla. La paciente fue tratada con un extracto tropical Hamamelis virginiana
por dos semanas hasta su completa recuperación. (40)
Figura 15: Apariencia facial de la paciente después de
del accidente con el hipoclorito de sodio.
DAÑO DEL NERVIO DENTARIO INFERIOR
La extrusión apical de microorganismos y sustancias irrigantes del canal
radicular de dientes inferiores, puede producir daños severos a nivel del nervio
dentario inferior como anestesia temporal o permanente del nervio, hiperestesia,
parestesia o en raros casos hiperestesia. El mayor riesgo de daño al nervio
dentario inferior puede ocurrir durante el tratamiento de conductos radiculares de
la segunda molar inferior.
Littner y col. investigaron la relación entre los ápices de la 3ra, 2da y 1ra molar en
relación al nervio dentario inferior y dedujeron que la menor distancia fue de 3.45
mm para la raíz distal de la segunda molar y la mayor distancia fue de 5.47 mm
para la raíz mesial de la primera molar. (1)

50
REACCIONES ALÉRGICAS
La literatura refiere que aunque no muy común, existen pacientes alérgicos a
algunos materiales contenidos en el NaOCl. No obstante, puede ocurrir
hipersensibilidad y dermatitis de contacto en algunos casos. En casos de
hipersensibilidad contra el hipoclorito de sodio, la clorhexidina no debería ser
usada por el contenido de cloro que tiene, por lo que se debería usar un irrigante
alternativo con altas propiedades antimicrobianas como agua de hidróxido de
calcio o detergentes aniónicos, dependiendo del caso clínico. (1)
La literatura endodóntica relata casos de hipersensibilidad a las soluciones de
hipoclorito de sodio. Las reacciones alérgicas varían desde una sensación de ardor
hasta un dolor intenso, pudiendo llegar a una hinchazón del labio o mejilla, con
equimosis, hematoma y hemorragia vía conducto radicular. El dolor y la
sensación de falta de aire disminuyen normalmente en corto periodo de tiempo,
aunque la parestesia del lado de la cara del diente sometido a tratamiento puede
permanecer por varios días. Para estos casos se prescriben medicamentos
antihistamínicos. Se recomienda que el paciente sea encaminado a un médico
alergista que podrá confirmar la hipersensibilidad a productos de limpieza casera
que contengan hipoclorito de sodio.
Caliskan y col (1994) reportan el caso de un paciente femenino de 32 años de
edad, quien presentaba fractura radicular del incisivo central superior, para lo cual
se le decide realizar tratamiento de conductos radiculares de dicha pieza dentaria.
Al irrigar el conducto radicular con NaOCl al 1 %, inmediatamente a la paciente
se le formó un edema severo y generalizado, eritema, dificultad para respirar,
seguida de hipotensión. Se le indicó tomar corticoides y un antihistamínico para
prevenir una reacción anafiláctica y mejorar estos severos signos y síntomas. La
presencia de estos síntomas clínicos los dirigió a diagnosticar Urticaria de
contacto. (41)
La urticaria de contacto se define como una reacción de edema y aumento de
calor cuando una sustancia es aplicada a piel intacta. (41)
A pesar que se ha reportado que la CHX es una solución relativamente segura,
puede producir reacciones alérgicas. Las reacciones alérgicas a la clorhexidina
pueden ser las siguientes: anafilaxis, dermatitis de contacto y urticaria en contacto
con mucosa oral y heridas abiertas. (1)

51
EXTRUSIÓN DE SOLUCIONES IRIRGANTES HACIA EL SENO
MAXILAR
El seno maxilar es una cavidad neumatizada, cubierta por una membrana mucosa
respiratoria muy cerca a las puntas de las raíces de dientes postero-superiores. En
el 50% de las personas, el piso del seno maxilar se expande en el proceso alveolar
del maxilar. Los ápices, principalmente de la segunda premolar y la primera y
segunda molar, aunque incluso los de la primera premolar y el canino pueden
extenderse dentro del seno maxilar o están separados por una fina capa de hueso.
Ehrich y col. reportan el caso de una paciente a la cual se le inyecta NaOCl al
5.25% a través de la raíz palatina de la primera molar superior hacia el seno
maxilar. La paciente solo se quejó de un sabor a lejía, pero no hubo signos de
dolor, edema ni hemorragia. Se le irrigó con 30 ml de agua estéril y se le indico
tomar antibióticos. (1)
ENFISEMA ( AIRE EN LOS TEJIDOS)
El enfisema durante el tratamiento endodóntico, es producido como consecuencia
del uso de aire comprimido para secar el conducto radicular, lo cual puede
producir la constricción apical de los tejidos. (37) Sin embargo, este accidente
operatorio puede ocurrir cuando se usan soluciones de irrigación que desprenden
gran cantidad de oxígeno naciente, como las concentraciones de hipoclorito de
sodio y el agua oxigenada a 10 volúmenes. Al ejercer excesiva presión sobre el
émbolo de la jeringa durante la irrigación de los conductos radiculares, el
profesional podrá llevar esas soluciones a la región periapical, generando el
enfisema. La primera señal de enfisema es el aumento inmediato del volumen de
los tejido blandos, próximo al diente que está siendo tratado; esto le ocasiona
importante malestar al paciente, principalmente en su apariencia. En la mayoría
de casos, el enfisema no requiere indicación de analgésicos ni de antibióticos,
porque en pocos días el edema se disemina por los tejidos circunvecinos y
desaparece en corto periodo de tiempo. (2)

52
INYECCIÓN DE SOLUCIÓN DE NaOCl CUANDO SE CAMBIAN LOS
TUBOS DE ANESTÉSICO, POR TUBOS PREVIAMENTE LLENADOS
CON ESA SOLUCIÓN DE IRRIGACIÓN.
Para conductos radiculares atrésicos rectos y/o curvos de molares, se recomienda
el uso de jeringa cárpule y la utilización de tubos de anestésicos vacíos,
previamente esterilizados y llenados con soluciones de NaOCl. Esa
recomendación es adecuada para los profesionales y auxiliares responsables, que
nunca utilizarían inadvertidamente los tubos con solución de NaOCl como
anestesia. (2)
Gursoy y col (2006) reportan el caso de un paciente de sexo masculino de 21 años
de edad, quien acude a consulta particular por dolor en una premolar superior
derecha, para lo cual se decide realizar un tratamiento de conductos radiculares.
Durante el tratamiento como el paciente continuaba experimentando dolor, el
operador decide colocarle más anestesia en la mucosa del paladar. Pero en vez de
colocar lidocaína al 2%, inyecta NaOCl al 2.5% y esto fue suficiente para
producir necrosis del tejido. Esta equivocación ocurrió porque ambas soluciones
fueron dispensadas en cartuchos idénticos y porque el dentista no tuvo la
precaución de verificar que solución estaba inyectando. Esto le produjo al
paciente 1-2 mm de área de necrosis del tejido palatino, con pérdida de hueso. El
área estaba muy adolorida y el tejido necrótico tuvo que ser reemplazado por
tejido conectivo nuevo. (42)
Figura 16: Radiografía de diagnostico
Figura 17: Apariencia clínica de la mucosa del paladar después de la inyección
con hipoclorito de sodio.

53
En este tipo de casos, la inyección de NaOCl en el tejido gingival y/o tejidos
blandos de la cavidad bucal, dependiendo de la concentración del producto, podrá
producir una necrosis tisular, en razón de su excelente capacidad de disolución y
acción cáustica sobre los tejidos. En cuestión de segundos se observarán señales
de equimosis y hematomas acompañados de una sensación de ardor.
Se recomienda la aplicación local de un producto a base de corticoides y
analgésicos antiinflamatorios, por vía sistémica. (2)
INGESTIÓN DE SOLUCIONES IRRIGANTES Y OBSTRUCCIÓN
DE LAS VÍAS AÉREAS.
A pesar que el tratamiento del canal radicular necesita ser realizado con dique de
goma, las soluciones irrigantes pueden ser ingeridas y entrar en contacto con las
vías aéreas inadvertidamente.
En la ingesta de NaOCl en altas concentraciones (5.25%), se ha reportado que
produce irritación de la mucosa oral. En caso de ingestión de mayor cantidad de
NaOCl podría ocasionar problemas esofágicos como quemazón o edema. Y en el
peor de los casos este edema de los tejidos podría producir la obstrucción de las
vías aéreas. (1)

54
II.8 PROTOCOLO FARMACOLÓGICO FRENTE INTOXICACIÓN POR
IRRIGACIÓN DE HIPOCLORITO DE SODIO EN LOS TEJIDOS BLANDOS
DURANTE UN PROCEDIMIENTO ENDODÓNTICO
(22, 40,42,43)
Lo primero que se debe hacer inmediatamente después que haya ocurrido
extravasación de hipoclorito de sodio hacia los tejidos periapicales es:
Mantener la calma y apoyar al paciente en mantener la calma, explicarle lo
sucedido y qué esperar de antemano, asegurándole que la apariencia normal
regresará luego de un corto periodo de tiempo si ocurre hinchazón.
Inmediatamente hay que irrigar el conducto radicular con abundante suero y tapar
el conducto con un cemento provisional.
Para evitar el dolor se inicia un tratamiento con corticoesteroides por vía
parenteral como dosis inicial (dexametasona 8 mg IM) e irlo manejarlo con dosis
horarias por 1 a 2 días (dexametasona 8 mg im c/8 h).
Conjuntamente se debe administrar antibióticos beta - lactámicos a base de PNC
de gran espectro, (amoxicilina + ácido clavulámico 625 mg c/8 h x 7 días), para
evitar un proceso infeccioso agudo frente a la necrosis tisular posiblemente
diseminada en pocos minutos.
El mismo día del incidente se deben colocar paños de agua fría.
Durante los 3días siguientes colocar paños de agua tibia intercaladamente cada 8
horas por una hora como ayuda complementaria al aumento de la capilaridad
vascular periférica y asimismo a la mejor cobertura antibiótica de la zona.
Finalmente ir realizando llamadas para monitorear el progreso hasta que haya
habido una recuperación del paciente. Esta recuperación puede tardar entre 1- 3
semanas.

55
II.9 NOVEDADES EN IRRIGACIÓN
Recientemente, han sido introducidos nuevos dispositivos de irrigación y/ o
desinfección en endodoncia, entre ellos el Sistema Endoactivador (DENTSPLY Tulsa
Dental Specialties), Irrigación ultrasónica pasiva, EndoVac (Discus, Culver City, CA,
USA), Irrigación Vista (Vista Dental Products, Racine, WI, USA), Desinfección por
foto activación y gas de Ozono, entre otros. Estos nuevos sistemas usan presión,
vacío, oscilación y/o una combinación con succión. Por el momento no existe una
evidencia científica clara con respecto a la eficacia de estos sistemas, y/o los riesgos
de extrusión del irrigante durante su utilización. En el siguiente resumen se
presentaran los diferentes sistemas con sus características de uso.
ENDOACTIVATOR SYSTEM
El Sistema EndoActivator de DENTSPLY, Tulsa Dental Specialties, usa de
manera segura una punta de polímero no cortante en una pieza de mano. En forma
rápida y vigorosa, agita las soluciones de irrigación durante el tratamiento
endodóntico.
En un estudio reciente (Desai 2009), fue analizada la seguridad de varios sistemas
de irrigación intraconducto con respecto a la extrusión del irrigante. La conclusión
del artículo señala que el EndoActivador tiene un mínimo de extrusión en
comparación con la irrigación manual, ultrasónica y el sistema rinse endo. (44)
Jiang y col (2010), evalúan la capacidad de remover el detritus dentinario del
conducto radicular, mediante la activación de un sistema sónico y ultrasónico. Los
resultados mostraron que la activación ultrasónica fue más eficiente en remover
detritus dentinario que la activación sónica. La activación ultrasónico removió el
89% de detritus, mientras que la activación sónica solo el 5.5% - 6.7%. (45)
Figura 18: Sistema Endoactivator

56
ACTIVACIONES ULTRASÓNICAS PASIVAS
Los sistemas sónicos y ultrasónicos fueron introducidos por primera vez por
Richman en (1957). Son aparatos que se basan en la acción vibratoria de
instrumentos energizados dentro del conducto radicular.
En la actualidad se ha demostrado que estos sistemas sónicos y ultrasonido son
incapaces de afrontar individualmente los pasos de la preparación del conducto
radicular. Siempre será necesario iniciar la instrumentación con la técnica manual
y culminarla de la misma manera. De otro lado, donde una lima o escariador no
puedan ingresar por dificultades de calcificación o curvatura del canal, los
instrumentos sónicos y ultrasónicos tampoco podrán penetrar, lo cual nos
demuestra serias deficiencias de estos sistemas. (46)
Por otro lado se ha demostrado que las limas activadas por ultrasonido irrigación
por ultrasonido son capaces de ayudar con la irrigación y desinfección del
conducto radicular. La literatura ha descrito dos tipos de irrigación ultrasónica: la
primera, en la cual, la irrigación es combinada con la instrumentación simultánea
con ultrasonido (UI) y la segunda en la cual, no se combina con instrumentación
ultrasónica, conocida por irrigación ultrasónica pasiva (PIU). Durante IU la lima
es intencionalmente puesta en contacto con la pared del conducto radicular y ha
demostrado ser menos eficaz en la eliminación de tejido pulpar del sistema de
conductos radiculares o capa de barro dentinario de la pared del conducto
radicular que la PUI (Weller et al. 1980, Ahmad et al. 1987a). Esto se explica por
la reducción de la cavitación acústica que se produce cuando la lima entra en
contacto con la pared del diente. (Ahmad et al.). Como la anatomía del conducto
radicular es compleja (Peters, 2004) un instrumento nunca podrá estar en contacto
con toda la pared del conducto radicular (Wu et al. 2003). De este modo UI,
podría resultar en el corte no controlado de la pared del conducto radicular sin una
limpieza efectiva. (44)
La Irrigación pasiva por ultrasonido fue descrita por Weller y col. (1980). El
término "pasivo" no describe adecuadamente el proceso, ya que es en realidad
activo, sin embargo, cuando se introdujo por primera vez el término pasivo fue
relacionado con la acción no cortante de la lima activada por el ultrasonido. PUI
se basa en la transmisión de energía acústica desde una lima oscilante o alambre

57
liso a una solución de irrigación en el conducto radicular. La energía se transmite
por medio de ondas de ultrasonido y puede inducir la transmisión acústica y la
cavitación de la irrigación (Ahmad et al. 1987a). Después de que el conducto
radicular se ha conformado hasta la lima apical maestra (independientemente de
la técnica de preparación utilizada), una pequeña lima o alambre liso (por ejemplo
el tamaño 15) se introduce en el centro del conducto radicular, hasta la región
apical. El conducto radicular se llena con una solución de irrigación y la lima de
ultrasonido oscilante activa la irrigación. A medida que el conducto radicular ya
se ha conformado, la lima o el alambre se puede mover libremente y la irrigación
pueda penetrar más fácilmente en la parte apical del conducto radicular (Krell, et
al. 1988), siendo el efecto de limpieza será más poderoso (Lumley et al. 1991).
Con esta metodología no cortante, la posibilidad de crear formas aberrantes dentro
del conducto radicular se reducirá al mínimo. (47)
Cunningham y col. utilizando dientes extraídos, compararon las técnicas de
irrigación convencionales con un sistema ultrasonido en el que se utilizó flujo
constante del irrigante junto con una lima ensanchadora. A los niveles de 1, 3 y 5
mm del ápice, los conductos preparados con ultrasonido estaban
significativamente más limpios. Al parecer este sistema mejora significativamente
la acción del irrigante. (9)
Al-Jadaa y col (2009) realizan un estudio en la cual utilizan la técnica de
activación ultrasónica pasiva con hipoclorito de sodio al 2.5%. Los resultados
muestran que después de 5 minutos, la temperatura del irrigante aumenta 53.5 °C
± 2.7 °C, aumentando de esta manera las propiedades de disolución de tejidos del
irrigante. Después de usarlo entre (12-14 minutos) la temperatura no sigue
aumentando sino que empieza disminuir, indicando una pérdida de energía
ultrasónica trasmitida a la solución de irrigación en el canal. (48)
Figura 19: Activaciones ultrasónicas pasivas (PUI)

58
DESINFECCIÓN FOTO ACTIVADA (PAD)
Recientemente ha aparecido un nuevo método para la desinfección de caries y
para el tratamiento de conductos radiculares, llamada desinfección fotoactivada
(PAD). El PAD es un método láser que sirve para controlar los microorganismos
patógenos de la cavidad oral. (29) Éste actúa a través de la fotosensibilización,
emitiendo una radiación láser de poca energía (100 mW)¸ con una longitud de
onda de 635 nanómetro activando un tinte (cloruro del tolonium) donde una luz
es transferida a través de los túbulos dentinarios emitiendo dicha radiación
uniforme y periférica. El líquido que es parte del sistema, consiste en un tinte
(azul de la toluidina, TBO). Ni el tinte de cloruro de tolonium, ni el oxígeno
reactivo producido de él son tóxicos para el paciente. (23, 49)
La activación de moléculas fotosensibilizantes por longitud de onda específica
producen entidades químicas perjudiciales para matar bacterias. El oxidante fuerte
generado durante el proceso, puede actuar a varios niveles de la bacteria: a nivel
de la membrana celular, en la inactivación enzimática, genómica y daños en el
ADN plasmático que dan como resultado la muerte inmediata del
microorganismo. Además, la luz reduce relativamente, las posibilidades de dar
lugar a una población resistente, por lo que es un tratamiento ideal. (44)
Bergmans y col (2008) evalúan la efectividad antimicrobiana del PAD y el láser
contra tres microorganismos (Streptococcus anginosus, Enterococcus faecalis y
Fusobacterium nucleatum). La desinfección fotoactiva (PAD) en los conductos
radiculares produjo una reducción significativa de bacterias. Eliminó el 93.8% de
S. anginosus (P < 0.0001), el 88.4% de E. faecalis (P < 0.05) y el 98.5% de F.
nucleatum (P < 0.0001), pero no llegó a esterilizar el 100% del conducto
radicular. Mientras que el láser no tuvo ningún efecto antimicrobiano
significativo. (50)
Figura 20: Equipo y agujas de desinfección fotoactivada

59
GAS OZONO
El Ozono (O3) es un compuesto natural formado por tres átomos de oxígeno. Se
encuentra en la naturaleza, en la forma de gas en la estratósfera, en una
concentración de 1.10 ppm, siendo continuamente creados y destruidos en el O2
molecular.
La microbiología fiable y propiedades metabólicas del ozono, en cualquiera de las
fases gaseosa o acuosa, lo convierten en un desinfectante útil con una amplia
gama de actividades. El ozono, en la fase gaseosa o acuosa, ha demostrado ser un
agente antimicrobiano de gran alcance y confiable contra las bacterias, hongos,
protozoos y virus. Es generalmente aceptado que el potencial oxidante del ozono
induce la destrucción de las paredes de las células y las membranas
citoplasmáticas de las bacterias y hongos. Durante este proceso, el ozono ataca las
glicoproteínas, glucolípidos, y otros aminoácidos e inhibe y bloquea el sistema de
control enzimático de la célula. Esto resulta en un aumento de la permeabilidad de
la membrana; el elemento clave de la viabilidad celular, conduciendo a la
interrupción funcional inmediata. Entonces, las moléculas de ozono pueden
fácilmente entrar en la célula causando la muerte de los microorganismos.
Además, el ozono puede atacar muchas biomoléculas, como la cisteína,
metionina, histidina y los residuos de las proteínas. El ozono tiene un efecto muy
perjudicial sobre las bacterias cariogénicas, resultando en la eliminación de
bacterias acidogénicas. El ácido pirúvico es el ácido más fuerte que aparece
naturalmente, producido por las bacterias durante la cariogénesis acidogénica. El
ozono puede descarboxilar este ácido a ácido acético. Se ha demostrado que la
remineralización de lesiones de caries incipientes puede ser fomentada con la
producción de ácido acético, o de otros ácidos pKa alto que se encuentran en
reposo en la placa, amortiguadores de fluido de la placa. (Azarpazhooh 2008).
(44)
Los peligros del ozono cuando se utilizan en la endodoncia no han sido
investigados hasta ahora. Se debe tener cuidado con respecto al paciente y al
odontólogo a la exposición del gas. (Figura 6 muestra el equipo de ozono con una
punta especial para la aplicación intraconducto). (1)

60
Figura 21: Equipo y agujas especiales de irrigación con ozono
Hezlozono (Kavo)
ENDOVAC
El Endovac es un sistema de irrigación-evacuación combinados. La irrigación es
expulsada del sistema en el orificio del conducto radicular, con presión. La
evacuación, se hace por medio de una micro-cánula que se extiende a la región
apical del conducto radicular; las dimensiones de la aguja son de calibre #55 con
un 2% conicidad. Del alto volumen de aspiración de la unidad dental resulta una
presión apical negativa y por lo tanto de forma pasiva absorbe la irrigación desde
el orificio de la parte apical del conducto radicular. La extrusión apical
probablemente se reducirá en la medida que disminuya la presión apical. (Nielsen,
BA, 2007).
Un dispositivo similar se ha presentado por Fukumoto et al. (Fukumoto Y, 2006:
Fukumoto Y.2005). La irrigación se liberada por una aguja (diámetro exterior de
0,41 mm, diámetro interior de 0,19 mm) y un tubo de aspiración (Masterflex,
Cole Palmer Instruments, Vernon Hills, IL, EE.UU.) conectado a la parte
coronaria o media del conducto radicular y aspirada por una segunda aguja
(diámetro exterior de 0,55 mm, 0,30 mm de diámetro interior), que se introduce a
la parte apical del conducto radicular. La presión de aspiración es de -20 kPa. La

61
irrigación se aspira desde la parte coronal a la parte apical del conducto radicular
y finalmente se succiona. En un experimento in vitro en dientes con ápices
cortados, Esta técnica resultó en un significativo menor exceso de extrusión de
irrigación que una técnica de irrigación convencional, con la punta de la aguja
colocada a 2 mm del ápice. Cuando la aguja se coloca a 3 mm del ápice, los
resultados no difieren significativamente. (44)
Figura 22: Endovac

62
III. CONCLUSIONES
El hipoclorito de sodio sigue siendo la solución irrigante mas utilizada de estos
tiempos gracias a sus propiedades bactericidas y de limpieza. (1, 10, 5)
La concentración adecuada de hipoclorito de sodio (NaOCl) que se debería
utilizar para el tratamiento de conductos radiculares sigue siendo tema de debate.
Ya que a mayor concentración de la solución, mayores efectos citotóxicos tendrá
en contacto de los tejidos periapicales. Sin embargo, mientras más concentrada
(5.25%) sea la solución, mejores propiedades tendrá en comparación a una
solución de menor concentración. (3, 9, 2)
La temperatura va ha ser un factor importante que va ayudar a mejorar las
propiedades del hipoclorito de sodio. El aumento de la temperatura de la solución
de hipoclorito de sodio disminuye su tensión superficial permitiendo una mayor
penetración en el conducto. Cuando se aumenta la temperatura de una solución de
NaOClal 2.5% hasta 37°C, se van a obtener las mismas propiedades de limpieza
que el NaOCl al 5.25%, pero con menos efectos citotóxicos. (3,10)
La clorhexidina al 2% presenta buenas propiedades antibacterianas, de
substantividad y lo principal, sus efectos al estar en contacto con los tejidos
periapicales no serán tan citotóxicos como la solución de hipoclorito de sodio. Sin
embargo, su mayor desventaja será su incapacidad para disolver tejido o
remanentes orgánicos e inorgánicos. (24, 8, 2, 15, 31)
Tanto la solución de hipoclorito de sodio al 5.25% como la clorhexidina al 2%
tendrán efectos bactericidas, eliminando el el E.faecalis.
Se han realizado estudios en los cuales mezclan dos irrigantes muy usados en
endodoncia, hipoclorito de sodio + clorhexidina con el fin de aprovechar ambas
propiedades en una misma solución. A pesar que el PCA tenga un amplio
espectro antimicrobiano, esto va a ser irrelevante ya que es altamente tóxico.
Estudios realizados en ratas muestran que es carcinogénico. (30)
El EDTA al 17% (agente quelante) que tiene la propiedad de remover el barro
dentinario de las paredes del conducto radicular y que junto con ayuda del
hipoclorito de sodio (solvente orgánico) va ha mejorar esta propiedad. (5, 8)
Aunque muchos estudios muestran resultados bastante satisfactorios en lo
referente a la capacidad antibacteriana de la CHX al 2%, muchos otros autores

63
siguen mostrando preferencia por el hipoclorito de sodio, no sólo porque ofrece
excelentes propiedades bactericida, sino también por la acción mecánica de
disolver tejido orgánico.
Es por tal razón, que la clorhexidina podría utilizarse como una segunda
alternativa en dientes con necrosis pulpar, en los cuales no se requiera disolver el
tejido orgánico. (2)
La literatura endodóntica reporta deferentes complicaciones que podrían ocurrir
durante la irrigación del conducto radicular. Muchos de éstos, se dan por una mala
determinación de la longitud de trabajo del conducto radicular, perforaciones
iatrogénicas del foramen apical, perforaciones laterales. Para evitar estas
complicaciones es importante realizar una adecuada historia clínica para averiguar
si hubiese historia de alergia en los pacientes, determinar de manera correcta la
longitud de trabajo del conducto radicular y seguir una buena técnica de irrigación
del conducto radicular. (1)
En la actualidad hay nuevas técnicas de irrigación tales como; sistema
endoactivador, activación pasiva de ultrasonido, desinfección foto activada
(PAD), Gas Ozono y Endovac, que serán complementarias a las técnicas de
irrigación ya existentes. (44)
El sistema de activación ultrasónica pasiva, al vibrar dentro del conducto va
ayudar al irrigante a penetrar de una forma más efectiva a través de los túbulos
dentinarios, en comparación del sistema sónico, sistema endoactivador. (9, 47, 48)
La desinfección fotactivada (PAD) no es una alternativa pero si un posible
suplemento para protocolos ya existentes en la desinfección del canal radicular.
Este sistema va ayudar a desinfectar de una manera efectiva en conducto
radicular, sin embargo, no ayudara a la esterilización de éste. (50)
El Ozono ha sido propuesto para la desinfección del conducto radicular, auque no
se hayan hecho investigaciones muy a fondo. Sin embargo, se debe tener
precaución en cuanto la exposición al gas tanto del paciente como del profesional
y el personal asistente. (1)

64
IV REFERENCIAS BIBLIOGRÁFICAS
1. Hülsmann M, Rödig T, Nordmeyer S. Complications during root canal
irrigation. Endod Top 2009; 16: 27-63.
2. Leonardo MR. Endodoncia “Tratamiento de los conductos radiculares”
Principios técnicos y biológicos 2008.
3. Azuero MM, Ordóñez AF, Tinjacá V. Comparación de tres soluciones
irrigantes utilizadas en endodoncia. Rev odont Javer 2004; 13: 45-56.
4. Vianna ME, Gomes B, Bellocchio Berber V, Zaia A.A, Randi Ferraz CC, de
Souza-Filho F.J. In vitro evaluation of the antimicrobial activity of
chlorhexidine and sodium hypochlorite. Oral Surg 2004; 97: 79 -84.
5. Rodríguez I, Rodríguez MI, Rodriguez E. Uso de sustancias irrigadoras
complementarias en endodoncia para la eliminación de la capa de barro
dentinario propuesta de un protocolo de irrigación. Rev odont Javer 2003; 10:
14-17.
6. Estrella C, Estrellla C, Barbin EL, Spanó JC, Marchesan M, de Pécora J.
Mechanism of Action of Sodium Hypochlorite. Braz Dent J. 2202; 13(2):113 –
117.
7. Spanó JC, Barbin EL, Santos TC, Guimaräes
LF, Pécora JD. Solvent Action of
Sodium Hypochlorite on Bovine Pulp and Physico-Chemical Properties of
Resulting Liquid. Braz Dent J 2001; 12 (3): 154-79
8. Cohen S, Burns RC. Vías de la pulpa 8va Edición 2001.
9. Ingle JI, Rainsor J.F. Endodoncia 3ra edición 1993.
10. Sirtes G, Waltimo T, Schaetzle M, Zehnder M. The Effects of Temperature on
Sodium Hypochlorite, short-Term Stability, Pulp Dissolution Capacity, and
Antimicrobial Efficacy. J endod 2005; 31(9): 669- 671.
11. Byström A, Claesson R, Sundqvist G. The antibacterial effect of camphorated
paramonochlorophenol, camphorated phenol and calcium hydroxide in the
treatment of infected root Canals. Endod Dent Traumatol 1985; 1: 170-175.
12. Estrela C, Ribeiro RG, Estrela CRA, Pécora JD, Sousa-Neto MD. Antimicrobial
Effect of 2% Sodium Hypochlorite and 2% Chlorhexidine Tested by Different
Methods. Braz Dent J 2003; 14(1): 58-62.

65
13. Sassone LM, Fidel RS, Francescutti Murad S, Rivera Fidel S, Hirata R Jr.
Antimicrobial Activity of Sodium Hypochlorite and chlorhexidine by two
different tests. Aust Endod J 2008; 34: 19-24.
14. Sassonei LM, Fidel RAS, Fidel SR, Diaz PD, Hirata R Jr. Antimicrobial
Activity of Different Concentrations of NaOCl and Chlorhexidine Using a
Contact Test. Braz Dent J 2003; 14(2): 100-104.
15. Türkün M, Cengiz T. The effects of sodium hypochlorite and calcium
hydroxide on tissue dissolution and root canal cleanliness. Inter endod J 1997;
30: 335–342.
16. Siqueira JF, Rocas IN, Favieri A, Lima KC. Chemomechanical reduction of the
bacterial population in the root canal after instrumentation and irrigation with
1%, 2.5% and 5.25% sodium hypochlorite. J endod 2000; 26(6):331-334.
17. Cunninghan WT, Balekgian AY. Effect of temperature on collagen-dissolving
ability of sodium hypoclorite endodontic irrigant. Oral Surg 1980; 4:175-177.
18. Cunninghan WT, Joseph SV. Effect of temperature on the bactericidal action of
sodium hypoclorite endodontic irrigant. Oral Surg 1980; 50:569-569.
19. Rossi-Fedele GP, de Figueiredo JAP. Use of a bottle warmer to increase 4%
sodium hypochlorite tissue dissolution ability on bovine pulp. Aust Endod J
2008; 34: 39–42.
20. Gambarini G. Chemical Stability of Heated Sodium Hypochlorite Endodontic
irrigants. J endod 1998; 24: 432 – 432.
21. Clarkson RM, Moule AJ, Podlich HM. The shelf-life of sodium hypochlorite
irrigating solutions. Aust Dent J 2001; 46:(4):269-276.
22. Balandro Pinal F. Soluciones para la irrigación en endodoncia: Hipoclorito de
sodio y Gluconato de Clorhexidina. 2007; 3: 11-14.
23. Bergmans L, Moisiadis P, Huybrechts B, Van Meerbeek B, Quirynen M. Effect
of photo – activated disinfection on endodontic pathogens ex vivo. Int endod J
2008; 41: 227-239.
24. Mohammadi Z, Abbott PV. The properties and applications of chlorhexidine in
endodontics. Int endod J 2009; 42: 288 -302.
25. Siqueira JF, Batista MD, Fraga RC, Uzeda M. Antibacterial effects of
endodontics irrigants on black–pigmented gram negative anaerobes and
facultative bacteria. J endod 1998; 24(6): 414 – 416.

66
26. Mohammadi Z, Abbott PV. Antimicrobial substantivity of root canal irrigants
and medicaments: A review. Aust endod J 2009; 35: 13-139.
27. Khademi AA, Mohammadi Z, Havaee A. Evaluation of the antibacterial
substantivity of several intra-canal agents. Aust endod J 2006; 32: 112-115.
28. Okino LA, Siqueira EL, Santos M, Bombana AC, Figueiredo JA. Dossolution
of pulp tissue by aqueous solution of chlorhexidine digluconate and
chlorhexidine digluconate gel. Int endod J 2004; 37: 38-41.
29. Basrani BR, Manek S, Sodbi R, Fillery E, Manzur A. Interaction between
Sodium Hypochlorite and Clorhexidine Gluconate. J Endod 2007; 33 (8): 966-
969.
30. Pappen F, Bolzani L, Rodríguez S, Amaral M.R, Tanumaru Filho M. In Vitro
antimicrobial effect of irrigating solution used in endodontics. Rev. Estomatol
Hered 2003; 13 (1-2):9-11.
31. Violich DR, Chandler NP. The smear layer in endodontics - a review. Int endod
J 2010; 43: 2-15.
32. Hülsmann M, Heckendorff M, Lennon A. Chelating agents in root canal
treatment: mode of action and indications for their use. Int endod J 2003;
36(12): 810-830.
33. Yamashita JC, Tanomaru Filho M, Leonardo MR, Rossi MA, Silva LA.
Scanning electron microscopic study of the cleaning ability of chlorhexidine as
a root–canal irrigant. Int endod J 2003; 36: 391- 394.
34. Lim TS, Wee TY, Choy MY, Koh C, Sae-Lim V. Light and scanning electron
microscopic evaluation of Glyde File Prep in smear layer removal. Int endod J
2003; 26: 336-346.
35. Krause TA, Liewehr FR, Chin.Lo Hahn. The antimicrobial effect of MTAD,
sodium hypochlorite, doxycicline, and citric acid on E. faecalis. J endod 2007;
33(1): 28-30.
36. Milena D. Agentes irrigantes y quelantes en endodoncia. Rev. Bibliográfica.
Rev odont Javer 2005; 17: 32-38.
37. Hülsmann M, Hahn W. Complications during root canal irrigation – literature
review and case report. Int endod J 2000; 33: 186-193.

67
38. Witton R, Brennan PA. Severe tissue damage and neurological deficit following
extravasation of sodium hypochlorite solution during routine endodontic
treatment. Brit Dent J 2005; 198(12): 749 – 750.
39. Gernhardt CR, Eppendorf K, Kozlowski A, Brandt M. Toxity of concentrated
Sodium Hypochlorite as an endodontic irrigant. Case Report. Inter Endod J
2004; 37: 272-280.
40. Serper A, Zbek MÖ, Calt S. Accidental Sodium Hypochlorite- Induced skin
injury during endodontic treatment. J endod 2004;30 (3): 180-181.
41. Caliskan MK, Turkün M, Alper S. Allergy to sodium Hypochlorite during canal
therapy: a case report. Int endod J 1994; 27: 163-167.
42. Gursoy UK, Bostanci V, Kosger HH. Palatal mucosa necrosis because of
accidental sodium hypochlorite injection instead of anaesthesic solution. Int
endod J 2006; 39: 157-161.
43. Isaza O, Reyes E, Rojas, P. Accidentes con hipoclorito de sodio. Rev odont
Javer 2004; 11: 26-18.
44. http://www.endodoncia-sae.com.ar/info_articulos02.htm
45. Jiang LM, Verbaagen B, Versluis M, van der Sluis L. Evaluation of a sonic
device designed to activate irrigant in the root canal. J endod 2010; 36 (1): 143-
146.
46. Villena H. Preparación biomecánica del conducto radicular. 2001
47. Van der Sluis LWM, Versluis M, Wu MK, Wesselink PR. Passive ultrasonic
irrigation of the root canal: a review of the literature. Int endod J 2007; 40: 415-
426.
48. Al-Jadaa A, Paqué F, Attin T, Zehnder M. Necrotic pulp tissue dissolution by
passive ultrasonic irrigation in simulated accessory canals: impact of canal
location and angulation. Int endod J. 2009; 42: 59-65.
49. Bonsor SJ, Nichol R, Reid TMS, Pearson GJ. Microbiological evaluation of
photo-activated in endodontics (In vitro study). Brit Dent J 2006; 200(6): 337-
341.
50. Bergmans L, Moisiadis P, Huybrechts B, Van Meerbeek B, Quirynen2 M,
Lambrechts P. Effect of photo-activated disinfection on endodontic pathogens
ex vivo. Inter Endod J 2008; 41: 227–239.

68