Tratamientos por membranas. Filtración convencional vs. Filtración por membranas.
Membranas clase 2012
-
Upload
andres-esquercia-fontana -
Category
Documents
-
view
184 -
download
1
Transcript of Membranas clase 2012

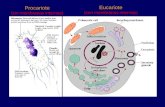
MEMBRANASMEMBRANAS
CONCEPTOS BASICOSCONCEPTOS BASICOS

MEMBRANA PLASMATICAMEMBRANA PLASMATICA
Estructura elástica delgada, laminar, formada por Estructura elástica delgada, laminar, formada por bicapa lipídica, proteínas y glúcidos, que recubre bicapa lipídica, proteínas y glúcidos, que recubre a las células y define sus límites.a las células y define sus límites.
Regula el intercambio de sustancias entre las Regula el intercambio de sustancias entre las células y su medio externo, manteniendo células y su medio externo, manteniendo constante la composición de estos espacios.constante la composición de estos espacios.
Las proteínas pueden actuar como poros o Las proteínas pueden actuar como poros o canales; carrier; enzimas; receptores. canales; carrier; enzimas; receptores.
Permioselectividad: Permioselectividad: libre pasaje de agualibre pasaje de agua : : limita el pasaje de iones y limita el pasaje de iones y
otras otras sustanciassustancias

Agua coporal y membranasAgua coporal y membranas
El agua es el solvente en el que ocurren casi todas El agua es el solvente en el que ocurren casi todas las reacciones químicas. las reacciones químicas.
Es el 60 % del peso corporal: 40% el LIC y 20 % es Es el 60 % del peso corporal: 40% el LIC y 20 % es LECLEC
El agua en los distintos compartimientos líquidos (LIC, El agua en los distintos compartimientos líquidos (LIC, LIS, plasma) no está estable, hay movimiento LIS, plasma) no está estable, hay movimiento contínuo.contínuo.
El movimiento de agua es por ósmosis y se genera por El movimiento de agua es por ósmosis y se genera por la existencia de gradientes osmóticos. Estos se la existencia de gradientes osmóticos. Estos se producen cuando a ambos lados de una membrana producen cuando a ambos lados de una membrana hay distinta osmolaridad.hay distinta osmolaridad.

ConceptosConceptos OSMOSIS: movimiento pasivo de agua a través de OSMOSIS: movimiento pasivo de agua a través de
una membrana semipermeable, desde zonas de baja una membrana semipermeable, desde zonas de baja cc de soluto a zonas de alta cc de soluto cc de soluto a zonas de alta cc de soluto (gradiente).(gradiente). Es difusión simple a través de poros proteicos.Es difusión simple a través de poros proteicos.
agua
A BA = B = 2 particulas/l
5 particulas/l 2 particulas/l

ConceptosConceptos OSMOLARIDAD: forma de expresar cc, referida a OSMOLARIDAD: forma de expresar cc, referida a
sustancias osmoticamente activas en un solvente.sustancias osmoticamente activas en un solvente. Es el nro de osmoles por litro de soluciónEs el nro de osmoles por litro de solución
Osm= n. M Osm= n. M
n: nro de particulas osmoticamente activas* = nro de partículas por n: nro de particulas osmoticamente activas* = nro de partículas por molécula, que se mueven libremente al disociarse en soluciónmolécula, que se mueven libremente al disociarse en solución
M: molaridad (mol/l) mol: PM (g/mol)M: molaridad (mol/l) mol: PM (g/mol)
• * : iones (Na+, K+, Cl-,etc), glucosa, urea..* : iones (Na+, K+, Cl-,etc), glucosa, urea..• Por ej: 1 mol de ClNa (58,5 g) = 2 osmoles de ClNaPor ej: 1 mol de ClNa (58,5 g) = 2 osmoles de ClNa• En solución ClNa Cl- + Na+ n= 2 En solución ClNa Cl- + Na+ n= 2 • 1 mol de glucosa (180 g) = 1 osmol de glucosa (no se ioniza) n=11 mol de glucosa (180 g) = 1 osmol de glucosa (no se ioniza) n=1

OsmolaridadOsmolaridad
Osmolaridad plasmática= 300 mosm/lOsmolaridad plasmática= 300 mosm/l VN: 280-300 mOsmVN: 280-300 mOsm Cálculo Cálculo osm plasm = Nax2 + Glu/18 + urea/6osm plasm = Nax2 + Glu/18 + urea/6
Na+= 137-145 mOsm
Glu= 70-110 mg/dl
Urea= 15-50 mg/dl
Osm pl = (140 x2) + 100/18 + 30/6 = 280
Para evitar desequilibrios que afecten a los compartimientos líquidos del organismo las osmolaridades de éstos espacios deben ser iguales

Conceptos Conceptos PRESIÓN OSMÓTICA: fuerza necesaria PRESIÓN OSMÓTICA: fuerza necesaria
para detener la ósmosis (fuerza osmotica) para detener la ósmosis (fuerza osmotica) Está determinada por el nro de partículasEstá determinada por el nro de partículas
agua
Presión osmótica

ConceptosConceptos En el intravascular la presencia de En el intravascular la presencia de proteínasproteínas genera genera
fza osmótica llamada fza osmótica llamada presión oncóticapresión oncótica. . Las proteínas no pueden salir del IV y retienen agua dentro Las proteínas no pueden salir del IV y retienen agua dentro
de los capilares, oponiendose a la presión hidrostática de los capilares, oponiendose a la presión hidrostática (presión dependiente del peso de la columna de líquido) (presión dependiente del peso de la columna de líquido) impartida por el bombeo cardíaco impartida por el bombeo cardíaco
Presion hidrostática
Proteinas
LIS
H2O
CAPILAR LINFÁTICO

Osmolaridad vs TonicidadOsmolaridad vs Tonicidad Comparar osmolaridades = solo tengo en cuenta Comparar osmolaridades = solo tengo en cuenta
la concentración osmolar la concentración osmolar
300
300
LIC y LEC son isoosmolares
ClNa
300 mosm
isoosmolar
ClNa 400 mosm
hiperosmolar
ClNa 200 mosm hipoosmolar

Osmolaridad vs TonicidadOsmolaridad vs Tonicidad
300
300
LIC y LEC son isotonicas
ClNa
300 mosm
isotónica
ClNa 400 mosm
hipertónica
ClNa 200 mosm hipotónica
Comparar Tonicidad: tengo en cuenta la presión osmótica generada
Vol cteEdema celular hemolisis
Deshidratación cel crenación
Hb

Tonicidad Tonicidad Es la fuerza que ejerce la p. osmótica de una sc. sobre Es la fuerza que ejerce la p. osmótica de una sc. sobre
la mb celular, causando cambio en el volumen y la mb celular, causando cambio en el volumen y composición cel.composición cel.
Es la propiedad fisicoquímica que tiene una solución Es la propiedad fisicoquímica que tiene una solución de provocar cambios en el volumen y tamaño de una de provocar cambios en el volumen y tamaño de una celula suspendida en dicha solucion; a causa de un celula suspendida en dicha solucion; a causa de un gradiente electroquímico o desequilibrio osmótico para gradiente electroquímico o desequilibrio osmótico para algún componente de dicha soluciónalgún componente de dicha solución
Depende de cada soluto en particular y la Depende de cada soluto en particular y la permeabilidad de la membranapermeabilidad de la membrana

TonicidadTonicidad
Solución isotónicaSolución isotónica: en ella es posible colocar : en ella es posible colocar células sin que varíe su tamaño dado que no células sin que varíe su tamaño dado que no se produce pasaje neto de agua. se produce pasaje neto de agua.
Por ej: ClNa 0.9 g% (sc fisiologica) y sc Por ej: ClNa 0.9 g% (sc fisiologica) y sc glucosa 5% glucosa 5%
Solución hipotónica:Solución hipotónica: determina entrada neta de determina entrada neta de agua a la célula. (agua, ClNa hipoosmolar, agua a la célula. (agua, ClNa hipoosmolar, urea a cualquier concentración)urea a cualquier concentración)
Solución hipertónicaSolución hipertónica: determina salida neta de : determina salida neta de agua hacia el extracelular (ClNa hiperosmolar)agua hacia el extracelular (ClNa hiperosmolar)

TonicidadTonicidad Solamente para las soluciones de ClNa (ppal soluto del Solamente para las soluciones de ClNa (ppal soluto del
extracelular) la osmolaridad y la tonicidad coinciden.extracelular) la osmolaridad y la tonicidad coinciden. Para las soluciones de otro soluto, depende si éste se Para las soluciones de otro soluto, depende si éste se
encuentra o no dentro de la célula y si la membrana encuentra o no dentro de la célula y si la membrana permite su pasaje.permite su pasaje.
Sc de urea 300 mosm
300
300
isoosmolar
300 mosm de urea
600
300
hipotónica
300

Efectos de ingerir Efectos de ingerir liquidos de diferente liquidos de diferente tonicidadtonicidad
Hiperhidratación isotónica
No cambia

efectos de ingerir liquidos de diferente efectos de ingerir liquidos de diferente tonicidadtonicidad
intersticial
al LIC

Efectos de ingerir liquidos de diferente Efectos de ingerir liquidos de diferente tonicidadtonicidad
intersticial