Calorimetría
-
Upload
david-andres-quezada-espinosa -
Category
Documents
-
view
22 -
download
4
description
Transcript of Calorimetría
-
UNIVERSIDAD CENTRAL DEL ECUADOR
FACULTAD DE INGENIERA EN GEOLOGA, MINAS, PETRLEOS Y
AMBIENTAL
ESCUELA DE PETRLEOS
INFORME DE LABORATORIO N 3
NOMBRE: Quezada Espinosa David Andrs. FECHA: 2014_05_21
PROFESOR: Dr. Bolvar Enrquez. CURSO: Cuarto
1. Tema: Calorimetra
2. Objetivos:
2.1. Objetivo General
Establecer el equivalente trmico del calormetro
2.2. Objetivos Especficos
Especificar el equilibrio trmico experimental.
Averiguar los mtodos de deduccin del equivalente trmico.
Inducir el equivalente trmico del calormetro aplicando la ecuacin
existente para la definicin del mismo con los resultados determinados
experimentalmente.
Investigar acerca de los cambios trmicos y los procesos de
intercambio trmico.
3. Marco Terico
Cambio Trmico.
Concurrir un cambio trmico cuando dos objetos o cuerpos se fusionen
o se junten y cada uno posea una temperatura distinta, la energa
calorfica ser desigual, esta se transferir del de mayor temperatura
hacia el de menor temperatura, hasta el punto en que ambos cuerpos
tengan la misma temperatura, es decir, adquieran el equilibrio trmico.
-
Cuando dos porciones cualesquiera de un sistema se encuentran en
equilibrio trmico se dice que el sistema mismo est en equilibrio trmico
o que es trmicamente homogneo. Experimentalmente se encuentra
que, en un sistema en equilibrio trmico, la temperatura en cualquier
punto del cuerpo es la misma.
Equivalente Trmico
El equivalente en agua del calormetro es la masa de agua que se
comportara igual que el calormetro y que perdera igual calor en las
mismas circunstancias. De esta forma, solo hay que sumar al agua la
cantidad de equivalentes.
Deduccin de equivalente trmico y su ecuacin.
Sea 0 la temperatura del termo vaco y la temperatura del agua en el
momento de verterla en el recipiente aislado.
Igualando ambos calores se tiene:
=( + )
E es el equivalente buscado y ma es la masa de agua.
Admitiendo que el calor cedido por el agua es absorbido ntegramente por
el calormetro, se puede aplicar la formula anterior donde es la
temperatura de equilibrio, es la inicial del agua y 0 la inicial del
calormetro.
Unidades:
o La calora (cal), que es la cantidad de energa que hay que suministrar a
un gramo de agua para elevar su temperatura 1.
o Joule, tras mltiples experimentaciones en las que le movimiento de unas
palas, impulsadas por un juego de pesas, se movan en el interior de un
recipiente con agua, estableci el equivalente mecnico del calor,
-
determinando el incremento de temperatura que se produca en el fluido
como consecuencia de los rozamientos producidos por la agitacin de las
palas: 1cal = 4,187 J
o El BTU se define como la cantidad de calor que se debe agregar a una
libra de agua para aumentar se temperatura en un grado farenheit, y
equivale a 252 caloras.
Deduccin del equivalente trmico.
=
+ =
. ( ) + . ( )
= . ( )
. = =
=( ) ( )
( )
=( + )
( )
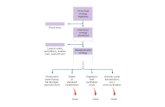
4. Montaje del equipo.
4.1. Diagrama del experimento
2
3 4
5
1 6
1
4.2. Materiales.
1. Calormetro.
2. Vaso trmico.
3. Termmetro.
4. Embudo.
5. Reverbera.
6. Agua.
-
5. Datos experimentales
CALORMETRO
Tiempo (s) Tf (C) Tc (C) Tm (C)
0 20 40 29
30 20 39,9 29
60 20 39,7 29
90 20 39,5 29
120 20 39,2 29
150 20 39 29
180 20 38,9 29
210 20 38,6 29
240 20 38,1 29
270 20 38 29
300 20 38 29
6. Procedimiento
Medimos una cantidad prudencial de agua, de tal manera que al mezclar
los volmenes de agua frio y caliente no exista exceso y se rebote del vaso.
Medimos la temperatura de este volumen.
Calentamos este volumen medido hasta que llegue a una temperatura de
40 y retiramos el envase con agua del fuego.
Introducimos el termmetro y realizamos mediciones de temperatura cada
30 segundos, hasta completar 5 minutos.
Mezclamos este volumen de agua calentado con el agua fra en el vaso
trmico y realizamos las mismas mediciones de temperatura cada 30
segundos hasta alcanzar los 5 minutos.
Anotamos los valores obtenidos en esta etapa de la prctica.
Realizamos los mismos pasos, pero en esta ocasin mezclaremos los
volmenes en el calormetro.
Realizar las tablas de resultados acompaadas de sus grficos.
7. Clculos
7.1. Calcular el equivalente trmico del vaso
=( + )
( )
VASO TRMICO
Tiempo (s) Tf (C) Tc (C) Tm (C)
0 19 40 28
30 19 39,9 28
60 19 39,5 28
90 19 39,2 28
120 19 38,5 28
150 19 38 28
180 19 37,8 28
210 19 37,5 28
240 19 37,2 28
270 19 37 28
300 19 37 28
-
=0.3(38,33 28 28 + 19)
(28 19)
= 0,0443
7.2. Calcular el equivalente trmico del calormetro de madera
=( + )
( )
=0.3(38,99 29 29 + 20)
(29 20)
= 0,033
7.3. Grficos de la temperatura Tf, Tc, Tm, f (t).
0
10
20
30
40
50
0 50 100 150 200 250 300 350
Tem
era
tura
(C
)
Tiempo (s)
CALORMETRO
Tf Tc Tm
-
7.4. Comparar valores obtenidos
Segn las grficas se puede afirmar que existe mayor prdida de energa o
calor en el vaso trmico que en calormetro de madera.
8. Resultados
0
10
20
30
40
50
0 50 100 150 200 250 300 350
Tem
pe
ratu
ra (
C)
Tiempo (s)
VASO TRMICO
Tf Tc Tm
VASO TRMICO
Tiempo (s) Tf (C) Tc (C) Tm (C)
0 19 40 28
30 19 39,9 28
60 19 39,5 28
90 19 39,2 28
120 19 38,5 28
150 19 38 28
180 19 37,8 28
210 19 37,5 28
240 19 37,2 28
270 19 37 28
300 19 37 28
Suma 209 421,6 308
Promedio 19 38,3272727 28
T (K) 292 311,327273 301
CALORMETRO
Tiempo (s) Tf (C) Tc (C) Tm (C)
0 20 40 29
30 20 39,9 29
60 20 39,7 29
90 20 39,5 29
120 20 39,2 29
150 20 39 29
180 20 38,9 29
210 20 38,6 29
240 20 38,1 29
270 20 38 29
300 20 38 29
Suma 220 428,9 319
Promedio 20 38,9909091 29
T (K) 293 311,990909 302
-
9. Conclusiones
El equivalente en agua del calormetro es la masa de agua que se
comportara igual que el calormetro y que perdera igual calor en las
mismas circunstancias, por ende, el vaso trmico presentar una mayor
disipacin de la energa o calor que le calormetro.
Cuando se mezclan dos sustancias de distinta temperatura, existe un
intercambio de calor o energa que cesar hasta que se llegue al equilibrio
trmico.
La prdida de calor estar directamente relacionada con el material
aislante.
10. Recomendaciones.
Que se tenga precaucin al momento de calentar el agua.
Que se tome con precisin las mediciones de temperatura, procurando ser
exacto en el tiempo.
Que se cierre de manera correcta el vaso trmico al momento de equilibrar
la temperatura del lquido contenido.
11. Bibliografa
BOLIVAR E, Gua de laboratorio Fisicoqumica. Universidad Central del
Ecuador, Facultad de Ingeniera en Geologa, Minas, Petrleos y Ambiental,
Quito Ecuador.
CALORMETRO, http://es.wikipedia.org/wiki/Calor%C3%ADmetro
CA
LOR
MET
RO
E 0,033 kg
Tf promedio 20 C
Tc promedio 38,99 C
Tm promedio 29 C
VA
SO T
RM
ICO
E 0,044 kg
Tf promedio 19 C
Tc promedio 38,33 C
Tm promedio 28 C
-
12. Anexos.
CUESTIONARIO
1. 100 g de una aleacin de oro y cobre, a la temperatura de 75.5C se introducen
en un calormetro con 502 g de agua a 25C, la temperatura del equilibrio
es de 25.5C. Calcular la composicin de la aleacin sabiendo que los calores
especficos del oro y del cobre son 130 J/kg C y 397 J/kg C respectivamente.
= 130
0 = 75,5
= 25,5
= 397
= 0,502
= 4180
=
= (0 ) + (0 )
= ( 0)
(0 ) + (0 ) = ( 0)
[130
] (75,5 25,5) + [397
] (75,5 25,5) = 0,502 [4180
] (25,5 25
6500
+ 19850
= 1049,18
+ = 0,1
= 0,1
-
6500
(0,1 ) + 19850
= 1049,18
= 0,0299
= 0,0701
2. Qu altura tendra que tener una cascada para que el agua aumentase 1C su
temperatura. (Suponiendo que toda su energa potencial se transformase en
calor que va a calentar al lquido).
= 1
= 4180
=
=
=4180
1
9.82
= 423,5306
3. Explica en qu situacin al calentar un cuerpo no aumenta su temperatura.
Cuando agregamos calor a un cuerpo, este no sufrir elevacin de temperatura si
como consecuencia existe un cambio de estado, por ende se puede afirmar que el
cambio de estado es un proceso isotrmico.
4. En un calormetro que contiene 440 g de agua a 9C se introduce un trozo de
hierro de masa 50g a 90C. Una vez alcanzado el equilibrio la temperatura
es de 10C. Cul es el calor especfico del hierro? Dato: calor especfico del
agua 4180 J/kg.K.
= 440
= 9
-
= 50
= 90
= 10
=?
=
(0 ) = (0 )
=(0 )
(0 )
=0.440 4180
(10 9)
0.05(90 10)
= 459,8
5. Una masa de mercurio cae libremente desde un recipiente superior a otro
inferior separados entre s un metro, aumentando su temperatura 0.7C.
Suponiendo que es despreciable todo el intercambio trmico entre el mercurio y
el exterior, calcula el calor especfico del mercurio.
= 0,7
= 1
=?
=
=
-
=9,8
2
1
0,07
= 14
6. Mezclamos 1kg de agua a 95C con 1kg de hielo a 5C. Se fundir todo el
hielo? Indica cules sern las condiciones finales de la mezcla. Datos: Calor
especfico del hielo: 0.5 cal/gC, Calor de fusin del hielo 80 cal/g, Calor
especfico del agua: 1 cal/gC.
= 1
= 95
= 1
= 5
= 0,5
= 1
= 80
.
|| = ||
+ =
=
=1 4180 9 1 2090 5
334400
= 1,15
.
-
.
|| = + + ( 0)
|| = (95 )
|| = ||
+ + ( 0) = (95 )
1 2090 5 + 1 334400 + 1 4180 = 1 4180(95 )
= 6,25