BOLILLA 8: Metabolismo de Aminoácidos. Digestión y absorción. Catabolismo. Transaminación....
-
Upload
estefania-zamora -
Category
Documents
-
view
56 -
download
5
Transcript of BOLILLA 8: Metabolismo de Aminoácidos. Digestión y absorción. Catabolismo. Transaminación....

BOLILLA 8: Metabolismo de Aminoácidos. Digestión y absorción. Catabolismo. Transaminación. Desaminación oxidativa y no oxidativa. Descarboxilación. Transporte de amoníaco: síntesis de glutamina. Glutaminasa. Organismos ureotélicos, uricotélicos y amoniotélicos. Ciclo de la urea. Costo energético. Destino del esqueleto carbonado. Aminoácidos cetogénicos y glucogénicos. Compuestos nitrogenados de importancia biológica derivados de aminoácidos.
QUIMICA BIOLOGICA Lic. y Prof. en Ciencias Biológicas

ME
TA
BO
LIS
MO
IN
TE
RM
ED
IO
Conjunto de reacciones químicas que tienen lugar en las células y tejidos.

Conocimientos previos:
- Ciclo del nitrógeno.
- Sistemas digestivo, circulatorio, endocrino.
- Estructura química de proteínas y aminoácidos. Nomenclatura.
-Transporte mediado activo. Difusión facilitada.
- Actividad enzimática y su regulación. Acción de cofactores y moduladores.
- Metabolismo. Regulación. Balance energético.
- Glucólisis.
- Ciclo de Krebs.
Química Biológica METABOLISMO DE AMINOACIDOS

Objetivos
- Que al finalizar la clase, sean capaces de:
1) Definir y distinguir aminoácidos esenciales y no esenciales.
2) Diferenciar y formular las reacciones de transaminación y desaminación, comprendiendo su significado biológico.
3) Fundamentar la toxicidad del amoníaco. Explicar su metabolización y excreción en los distintos organismos.
Química Biológica METABOLISMO DE AMINOACIDOS

Química Biológica METABOLISMO DE AMINOACIDOS
Quimotripsina
Diversidad de Proteínas
Extraído de Lehninger, 2008.
Proteínas de membrana Luciferasa
HemoglobinaQueratina

AMINOACIDOAMINOACIDO
Química Biológica METABOLISMO DE AMINOACIDOS
COO-
C
R
H3N+ H
Grupo carboxilo(disociado)
Cadenalateral
Carbono
Grupo amino(protonado)
Repasemos…Repasemos…

H2N C
H
R1
CO NH C
H
CO
R2-n
NH C
H
R3
COOH
n
Repasemos…
AA amino terminal AA carboxilo terminal
Uniones peptídicas

AMINOACIDOSAMINOACIDOS##
Aminoácidos esenciales en roedores, insectos, peces*, aves* y humanos**
Aminoácidos no esenciales
Química Biológica METABOLISMO DE AMINOACIDOS
- No son sintetizados por el organismo. Deben ser incorporados con la dieta. -Mantener el crecimiento y el equilibrio nitrogenado.
Valina Fenilalanina
Leucina Triptofano
IsoleucinaTreonina
Lisina Histidina**
Metionina Arginina**
Alanina Glicina
Serina Tirosina
Cisteína Ac. Aspártico
Ac. Glutámico Glutamina
Asparagina Prolina
- Sintetizados por el organismo.
# Los 20 AAs pueden ser sintetizados por los vegetales.* Peces y aves poseen además otros aminoácidos esenciales.** En humanos, Histidina es esencial en niños y Arginina es parcialmente esencial.

Química Biológica METABOLISMO DE AMINOACIDOS
COO-
CH3N+ H
CH3
AlaninaAla
Algunos aminoácidos que veremos en esta clase
COO-
CH3N+ H
CH2
COO-
AspartatoAsp
COO-
CH3N+ H
CH2
CH2
COO-
GlutamatoGlu
COO-
CH3N+ H
CH2
CH2
CONH2
GlutaminaGln
AA neutro o alifático
AAs ácidos
AA amida

Química Biológica METABOLISMO DE AMINOACIDOS
COO-
CH3N+ H
CH2
COO-
CH3N+ H
CH2
OH
Fenilalanina Tirosina
COO-
CH3N+ H
CH2OH
SerinaSer
COO-
CH3N+ H
C OHH
CH3
TreoninaThr
AAs hidroxilados
Aminoácidos aromáticos

Recordemos como funciona el Ciclo del N2
en la naturaleza…

N2
N2
N2
NH4+
AAsNO3-
Absorción del nitrógeno por las plantasAbsorción del nitrógeno por las plantas
N2 N2
N2
N2
NH4+
NO3-
NO3-
AAs
NH4+
AAs

Fijación del Nitrógeno en las plantasFijación del Nitrógeno en las plantas
N2 NH4+
Nódulo radicalNódulo radical: bacteria, u otro microorganismo en asociación simbiótica con raíz.

NHNH44++
Fijación del Nitrógeno en las plantasFijación del Nitrógeno en las plantas
Nitrogenasa
N2 NH4+
NADHNADPH

Oxidación de CH (Ej. Glu y Fru)
NADHNADPH
Ferredoxina reducida
Ferredoxina oxidada
Fe-Proteinaoxidada
Fe-Proteinareducida
Fe-Mo-Proteinareducida
Fe-Mo-Proteinaoxidada
2ATP
2ADP + 2Pi
N2 +10H+
2 NH4+ + H2
COMPLEJO NITROGENASA
AMINOACIDOS PROTEINAS
Fijación del Nitrógeno en las plantasFijación del Nitrógeno en las plantas
Flavodoxina red.
e- e- e-

N2
N2
N2
NH4+
AAsNO3-
Absorción del nitrógeno por las plantasAbsorción del nitrógeno por las plantas
N2 N2
N2
N2
NH4+
NO3-
NO3-
AAs
NH4+
AAs

La absorción de NO3- esta mediada por un
mecanismo de simporte 2H+/NO3

Plantas que no pueden fijar N2 Plantas que no pueden fijar N2 (mayoría de los cultivos excepto leguminosas)(mayoría de los cultivos excepto leguminosas)
Fuentes importantes de nitrógeno: NO3- y NH4
+
NO3- NO2
- + H2O
NAD(P)H + H+ NAD(P)+
Nitrato reductasa
NO2- + 3H2O + 2H+
Nitrito reductasa
LUZFerredoxina
NH4+ + 2H2O + 1.5 O2
AMINOACIDOS PROTEINAS
Citosol
Cloroplastos o Protoplastidios

Fuentes exógenas Fuentes endógenas
Proteínas de la dieta ANIMALES Proteínas de membranas, (vegetales o animales) enzimas, hormonas, etc.
Digestión y absorción Degradación
AMINOACIDOS
Transaminación y/ó Desaminación
- Proteínas- Aminoácidos No esenciales- Constituyentes nitrogenados no proteicos: purinas, pirimidinas, porfirinas, ácidos biliares.
Degradación Biosíntesis
α - cetoácido amoníaco

Química Biológica METABOLISMO DE AMINOACIDOS
¿Cómo se digieren las proteínas de la dieta en el humano?
Extraído de Lehninger, 2008.
SecretinaCO3H-
Colecistoquinina

Pepsinógeno
Digestión de ProteínasI) En el estómago
pH 1,5-2,5 Proenzima
-NH2
GASTRINA
Células Parietales
Células Principales
HCl
Pepsinógeno
Pepsina + resto de 42 Aa.HCl
Enzima activa
-NH2-NH2

Digestión de proteínas en el estómagoDigestión de proteínas en el estómagopor acción de la Pepsinapor acción de la Pepsina
COOCOO--
NHNH33++
Arg
Phe
Leu
PepsinaPepsina
Péptidos de alto PMPéptidos de alto PM
COOCOO --
Phe
Leu
NHNH33
++
NHNH 33++
Arg
COOCOO--
• ES UNA ENDOPEPTIDASA.
• HIDROLIZA UNIONES PEPTIDICAS.
• ACTUA SOBRE GRUPOS AMINO DE AMINOACIDOS AROMATICOS HIDROLIZANDO LAS PROTEINAS A POLIPEPTIDOS DE ALTO PM.

Química Biológica METABOLISMO DE AMINOACIDOS
¿Cómo se digieren las proteínas de la dieta en el humano?
Extraído de Lehninger, 2008.
Secretina
CO3H-Colecistoquinina

SECRECION PANCREATICA
Secretina
Colecistoquinina
Contenido estomacal acido
HCO3-
Proenzimas
o zimógenos
pH

Química Biológica METABOLISMO DE AMINOACIDOS
¿Cómo se digieren las proteínas de la dieta en el humano?
Extraído de Lehninger, 2008.
SecretinaCO3H-
Colecistoquinina

Digestión de ProteínasII) En Duodeno e Intestino
Tripsinógeno
Tripsina
Quimotripsinógeno
Procarboxipeptidasas A y B
Enteroquinasa
Proelastasa
Quimotripsina
Carboxipeptidasas A y B
Elastasa
TRIPSINA
INACTIVOS ACTIVOS

QUE TIPO DE ENLACES PEPTIDICOS HIDROLIZAN ??
• Tripsina (endopeptidasa) : grupos carbonilo de lisina y arginina
• Quimotripsina (endopeptidasa) grupos carboxilo de fenilalanina, tirosina, triptofano
• Las carboxipeptidasas (exopeptidasas) eliminan restos carboxilos terminales.

Digestión intraluminal de proteínasDigestión intraluminal de proteínaspor acción de proteasas pancreáticaspor acción de proteasas pancreáticas
COOCOO--
NHNH33++
Arg
Phe
Leu
TripsinaTripsina
QuimotripsinaQuimotripsina
ElastasaElastasa
NHNH33++
Arg
COOCOO--
Phe
NHNH33++
COOCOO--
Leu
NHNH33++
COOCOO--
NHNH33++
COOCOO--
NHNH33++
COOCOO--
OligopéptidosOligopéptidos
Arg COOCOO--NHNH22
AA BásicosAA Básicos
Leu COOCOO--NHNH22
Phe COOCOO--NHNH22
AA NeutrosAA Neutros
Carboxi-Carboxi-Peptidasa BPeptidasa B
Carboxi-Carboxi-Peptidasa APeptidasa A
PeptidasasPeptidasas

Química Biológica METABOLISMO DE AMINOACIDOS
¿Cómo se digieren las proteínas de la dieta en el humano?
Extraído de Lehninger, 2008.
SecretinaCO3H-
Colecistoquinina
AminoácidosDipéptidosTripéptidos

Absorción intestinal de aminoácidos y péptidosAbsorción intestinal de aminoácidos y péptidos
- Ocurre por - Ocurre por transportadores de aminoácidos y péptidostransportadores de aminoácidos y péptidos del borde en cepillo de las células intestinales.del borde en cepillo de las células intestinales.
- Transporte - Transporte activo Naactivo Na++-dependiente-dependiente y transporte y transporte pasivo pasivo NaNa++-independiente-independiente..
- Necesidad de múltiples transportadores determinados - Necesidad de múltiples transportadores determinados por la por la diferencia de tamaño y cargadiferencia de tamaño y carga de los aminoácidos y de los aminoácidos y péptidos.péptidos.

Transporte intestinal de aminoácidosTransporte intestinal de aminoácidos
Ocurre por varios mecanismos:Ocurre por varios mecanismos: % Relativo para% Relativo para AlaninaAlanina
T. activo dependiente de NaT. activo dependiente de Na++ 75% 75%T. facilitado independiente de NaT. facilitado independiente de Na++ 20% 20%Difusión pasivaDifusión pasiva < 5% < 5%
AminoácidosAminoácidosLUMENLUMENINTESTINALINTESTINAL
ENTEROCITOENTEROCITO
SANGRE SANGRE PORTALPORTAL
AminoácidosAminoácidos
AminoácidosAminoácidos
NaNa++
NaNa++
AminoácidosAminoácidos
NaNa++ KK++
KK++ATP → ADP+Pi
AminoácidosAminoácidos AminoácidosAminoácidos

PéptidosPéptidosLUMENLUMENINTESTINALINTESTINAL
ENTEROCITOENTEROCITO
SANGRE SANGRE PORTALPORTAL
PeptidasasPeptidasascitosólicascitosólicas
AminoácidosAminoácidos
Transporte intestinal de péptidos pequenosTransporte intestinal de péptidos pequenos
AminoácidosAminoácidosPéptidosPéptidos
Transporte activo de di- y tripéptidos acoplado a Transporte activo de di- y tripéptidos acoplado a hidrogenioneshidrogeniones
2H2H++
PéptidosPéptidos HH++
NaNa++
NaNa++
NaNa++KK++
ATP → ADP+Pi

Distribución de los aminoácidos en el período Distribución de los aminoácidos en el período post-prandialpost-prandial
• La mayor parte de los aminoácidos: Hígado.• Glutamina y Asparragina: Intestino y riñón. • Aminoácidos de cadena ramificada: Músculo y cerebro.
¿¿CCóómo son incorporados los aminoácidos en las mo son incorporados los aminoácidos en las células de los distintos tejidos?células de los distintos tejidos?
Difusión facilitada
-Los transportadores se encuentran en todas las células.- Son específicos para grupos de aminoácidos (neutros, catiónicos y de glutamato).

Química Biológica METABOLISMO DE AMINOACIDOS
AMINOACIDOS (fondo metabólico
común)
UTILIZACION
Síntesis de proteínas
Síntesis de compuestos nitrogenados no proteicos
Degradación y producción de
Energía
ORIGENORIGEN
Absorción en intestino
Degradación de proteínas
endógenas (Proteasas)
Síntesis de aminoácidos (principalmente
en hígado)

Química Biológica METABOLISMO DE AMINOACIDOS
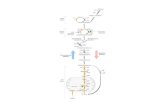
Catabolismo de aminoácidosCatabolismo de aminoácidos
Proteínas intracelulares
Proteínas dietarias Aminoácidos
Esqueleto carbonadoNH4+
Biosíntesis de aminoácidos, nucleótidos y aminas biológicas
Carbamil fosfato α-cetoacidos
CICLO DE LA UREA
CICLO DE KREBS
Interconexión Aspartato-arginino
succinato
CO2 + H2O + ATP
OxalacetatoUREA
(producto de excreción del nitrógeno)
Glucosa(gluconeogénesis)C
atab
oli
smo
del
nit
róg
eno
d
e am
ino
ácid
os

Vías de eliminación del grupo Vías de eliminación del grupo αα-amino-amino
Química Biológica METABOLISMO DE AMINOACIDOS
- Reacciones de Transaminación
- Reacciones de Desaminación
Oxidativa
No Oxidativa

Química Biológica METABOLISMO DE AMINOACIDOS
TransaminaciónTransaminación
α-aminoácido (R’)α-cetoácido (R)α-aminoácido (R) α-cetoácido (R’)
PLP
Aminotransferasa o Transaminasa
PLP: piridoxal fosfato piridoxamina fosfato

• Las reacciones de transaminación son fácilmente reversiblesreversibles y son muy importantes en el metabolismo proteico.
• Todos los aminoácidos (excepto lisina y treonina) participan en reacciones de transaminación con los α-cetoácidosα-cetoácidos:
• α-cetoglutarato
• oxaloacetato
• piruvato

Química Biológica METABOLISMO DE AMINOACIDOS
Principales reacciones de transaminación
PLP
Alanina aminotransferasa
(ALT)
Glutámico pirúvico transaminasa (GPT)
COO-
CH3N+ H
CH3
Alanina
+
COO-
C
CH2
CH2
COO-
O
α-cetoglutarato
COO-
C
CH3
O
Piruvato
COO-
CH3N+ H
CH2
CH2
COO-
+
Glutamato
GPTGPT- Localización citoplasmática.- Particularmente abundante en hígado, corazón y músculo.

Química Biológica METABOLISMO DE AMINOACIDOS
PLP
Aspartato aminotransferasa
(AST)
Glutámico oxalacético transaminasa (GOT)
Principales reacciones de transaminación
COO-
C
CH2
CH2
COO-
O
+
α-cetoglutarato
COO-
CH3N+ H
CH2
COO-
Aspartato
+
COO-
CH3N+ H
CH2
CH2
COO-
Glutamato
COO-
C
CH2
COO-
O
Oxalacetato
GOTGOT- Localización >> mitocondrial y < citoplasmática.- Particularmente abundante en hígado y corazón.

Vías de eliminación del grupo Vías de eliminación del grupo αα-amino-amino
Química Biológica METABOLISMO DE AMINOACIDOS
- Reacciones de Transaminación
- Reacciones de Desaminación
Oxidativa
No Oxidativa

Glutamato α-cetoglutarato
Glutamato deshidrogenasa
Química Biológica METABOLISMO DE AMINOACIDOS
Desaminación oxidativa del glutamatoDesaminación oxidativa del glutamato
(+) ADP y GDP
(-) ATP y GTP

GDH
TRANSDESAMINACION
TRANSAMINACION DESAMINACION OXIDATIVA
Aminoácido cetoglutarato
Glutamatocetoácido
NADH + H+
NAD+
NH4++
Transaminasa

Química Biológica METABOLISMO DE AMINOACIDOS
Desaminación oxidativa por Desaminación oxidativa por aminoácido oxidasasaminoácido oxidasas peroxisomales peroxisomales
D-aminoácido + H2O + E-FAD
E-FADH2 + O2
D-aminoácido oxidasa
D-aminoácido oxidasaE-FAD + H2O2
-cetoácido + NH4+
+ E-FADH2
L-aminoácido oxidasa
L-aminoácido oxidasaE-FMNH2 + O2 E-FMN + H2O2
L-aminoácido + H2O + E-FMN -cetoácido + NH4+
+ E-FMNH2
2 H2O2 2 H2O + O2
Catalasa

Vías de eliminación del grupo Vías de eliminación del grupo αα-amino-amino
Química Biológica METABOLISMO DE AMINOACIDOS
- Reacciones de Transaminación
- Reacciones de Desaminación
Oxidativa
No Oxidativa

Química Biológica METABOLISMO DE AMINOACIDOS
Desaminación no oxidativaDesaminación no oxidativa
COO-
CH3N+ H
CH2OH
Serina
COO-
C
CH3
O
Piruvato
+ NH4+
PLP
Serina deshidratasa
H2O H2O
COO-
CH3N+ H
C OHH
CH3
Treonina
PLP
Treonina deshidratasa
H2O H2O
COO-
C
CH2
CH3
O
α-cetobutirato
+ NH4+

Química Biológica METABOLISMO DE AMINOACIDOS
Bibliografía
1- BLANCO A., “Química Biológica”, Ed. El Ateneo, 8a edic., Bs. As. (2007).2- LEHNINGER, A.L., "Principios de Bioquímica", Ed. Omega, 4ª ed. (2008).
Bibliografía Complementaria
1- CAMPBELL Y FARREL, “Bioquimica”, Thomson Eds., 4ta. Ed., (2005).2- SALISBURY Y ROSS, “Fisiología vegetal”, Grupo Ed. Iberoamericana, (1994).3- HILL, WYSE Y ANDERSON, “Fisiología animal”, Ed. Med. Panamericana,(2006), Madrid, España.4- LIM M.Y., “ Lo esencial en Metabolismo y Nutrición”, Ed. Elsevier, 3ra. ed., Barcelona (2010).