VALIDACIÓN DE UN MÉTODO PARA … · DLLME Microextracción líquido-líquido dispersiva ......
Transcript of VALIDACIÓN DE UN MÉTODO PARA … · DLLME Microextracción líquido-líquido dispersiva ......
IV Edición del Máster en
Gestión Sostenible y Tecnologías del Agua
Trabajo fin de Máster:
VALIDACIÓN DE UN MÉTODO PARA IDENTIFICACIÓN DE SILOXANOS EN AGUAS RESIDUALES
Autor: Luciana Costa dos Reis Cruz
Tutora (Universidad de Alicante): Nuria Boluda Botella
Tutores (Empresa): Julio Llorca Pórcel
Carol Cortada Cortes
Alicante, septiembre de 2012
3
Agradecimientos
Primeramente Dios, por darme salud y fuerzas para seguir mis sueños.
A mis padres, Sérgio y Maria Goretti, por estar siempre presentes en mi vida,
por vibrar en cada conquista y darme los consejos correctos en los momentos
oportunos.
A la Universidad de Alicante, por elegir a mí entre los estudiantes de la
Universidad de São Paulo para hacer el máster de Aguas, perfecto para mi
desarrollo académico y científico.
Al director del máster, Daniel Prats y mi tutora en la universidad, Nuria Boluda
Botella, por disponer su tiempo y su atención en favor de los estudiantes del
máster y por brindarnos con un máster completo en el área ambiental.
A la Empresa AQUALOGY Medio Ambiental, por la oportunidad de hacer las
prácticas.
A Julio Llorca y Carol Cortada por sus enseñanzas y buena voluntad durante mi
estancia en el Laboratorio de Cromatografía.
A mi novio Jorge Garcia, por su apoyo y cariño mientras hacía este trabajo, y a
mi gran amiga Valeiry Vega, por su confianza y compañía.
Por fin, a todos mis compañeros de trabajo de la Empresa, gracias por cada
favor, dudas contestadas, sonrisas y saludos, pues lo que nos mueve en el
trabajo son las ganas de aprender cada vez más y eso se logra compartiendo
nuestras habilidades con los demás en un ambiente donde uno se siente bien.
4
ÍNDICE DE CAPÍTULOS Y APARTADOS
1. INTRODUCCIÓN ........................................................................................... 7 2. REVISIÓN BIBLIOGRÁFICA ........................................................................ 9 2.1 Siloxanos – Conceptos Generales ......................................................... 9
2.1.1 Definición .................................................................................... 9
2.1.2 Propiedades de los siloxanos ...................................................... 9 2.1.3 Aplicación de siloxanos .............................................................. 12 2.1.4 Precursores de los siloxanos ..................................................... 13
2.2 Siloxanos en el Biogás ……………………………………………………..13
2.2.1 Eliminación de siloxanos ………………………………………….. 16
2.2.2 Importancia del biogás y necesidad de incrementar su rendimiento …………………………………………………………………………. 20 2.3 Presencia de Siloxanos en el Medio Ambiente …………………………….. 21 2.4 Siloxanos en Agua, Sedimento y Lodo ……………………………………… 21 2.5 Bioacumulación de Siloxanos ………………………………………………… 23 2.6 Estudio de la Toma de Muestra para Determinación de Siloxanos ……… 24 2.6.1 Muestras de agua ………………………………………………….. 24 2.6.2 Muestras de lodo …………………………………………………... 24 2.6.3 Muestras de biogás ……………………………………………….. 24 2.7 Caracterización de los Métodos de Análisis – Determinación Analítica … 27 2.7.1 Determinación de siloxanos en el lodo ………………………….. 27 2.7.2 Determinación de siloxanos en el suelo ………………………… 28
2.7.3 Determinación de siloxanos en el biogás ………………………. 28
2.7.4 Determinación de los siloxanos en el agua …………………….. 29
3. OBJETO Y ALCANCE DEL TRABAJO ……………………………………… 30
4. PROCEDIMIENTO ……………………………………………………………… 31
4.1 Reactivos y Disoluciones ………………………………………………… 31
4.2 Cromatografía de Gases Acoplada a Espectrometría de Masas ……. 33
4.2.1 Condiciones previas ………………………………………………. 33
4.2.2 Instrumentación ……………………………………………………. 36
4.2.3 Identificación de los siloxanos ……………………………………. 38
4.3 Curvas de Calibrado ……………………………………………………… 41
4.4 Identificación de los Picos Cromatográficos …………………………… 43
4.5 Estudio r&R – Repetibilidad y Reproducibilidad ………………………. 45
4.5.1 Repetibilidad ……………………………………………………….. 46
4.5.2 Reproducibilidad …………………………………………………... 46
4.6 Límite de Detección ………………………………………………………. 47
4.7 Estudio de la Extracción de Siloxanos con Solventes en Muestras de
Aguas Residuales ………………………………………………………………….. 47
4.8 Análisis de Agua Residual ……………………………………………… 51
4.9 Repetibilidad para Análisis de Siloxanos en una Muestra de Agua
Residual …………………………………………………………………………….. 51
5. RESULTADOS Y DISCUSIÓN ………………………………………………... 52
5.1 Rectas de Calibrado …………………………………………………….. 52
5
5.2 Comparación Valor Calculado y Valor Experimental ………………… 64
5.3 Estudio r&R – Repetibilidad y Reproducibilidad ……………………… 65
5.3.1 Repetibilidad ……………………………………………………….. 65
5.3.2 Reproducibilidad …………………………………………………... 66
5.4 Análisis de Agua Residual ……………………………………………… 67
5.5 Análisis Cromatográfico de Muestra de Agua Residual Pretratada con
LLE y DLLME ………………………………………………………………………. 68
5.6 Repetibilidad para Análisis Cromatográfico de Agua Residual …….. 69
6. CONCLUSIONES ………………………………………………………………. 71
7. ACCIONES FUTURAS ………………………………………………………… 71
BIBLIOGRAFIA …………………………………………………………………….. 72
PUBLICACIÓN …………………………………………………………………….. 78
6
RESUMEN
El aprovechamiento eficaz de la energía producida por la quema del biogás enfrenta problemas cuando hay presencia significativa de siloxanos y otros compuestos en los lodos de depuradoras de aguas residuales. Debido a la volatilidad de algunos siloxanos, es evidente su presencia en el gas resultante del proceso de digestión anaerobia de los lodos. En la quema del biocombustible se forma dióxido de silicio sólido, depositándose en los motores y otros equipos. Los daños físicos y el bajo rendimiento del biogás son los motivos por los cuales se busca alternativas para la eliminación de los siloxanos antes que lleguen al gas de los vertederos. Siloxanos son utilizados en diversos productos, como los cosméticos, resultando evidente su presencia en las aguas residuales urbanas e industriales. Por lo tanto, es necesario disponer de un método de análisis fiable para la determinación de los siloxanos volátiles, cuyo destino final es el biogás. En este trabajo se describió y se validó un método para análisis de siloxanos en aguas residuales, que consiste en la preparación de solución-madre con siloxanos comerciales a partir de la cual se prepararon soluciones diluidas para estudiar la repetibilidad y reproducibilidad. Los análisis mediante GC-MS fueron considerados válidos, confirmación dada por la excelente repetibilidad del método propuesto, que también resultó reproducible. Se obtuvo una recta de calibrado con buen coeficiente de correlación para cada siloxano comercial estudiado (0,99). La precisión está reflejada en los bajos coeficientes de variación, que para la Cromatotografía Gaseosa se acepta hasta un 15%. Este trabajo obtuvo como coeficiente de variación más alto un 5,4%. Validado el método propuesto por la empresa, se analizó la repetibilidad para una muestra de agua residual de una EDAR.
7
1.INTRODUCCIÓN
El creciente consumo de siloxanos y siliconas en los procesos
industriales produce un incremento de estos compuestos en las aguas
residuales. En las plantas de tratamiento de aguas muchas veces se prohíbe la
presencia de los derivados de siloxanos, pues perjudican el rendimiento del
biogás producido en las instalaciones de digestión anaerobia de lodos.
Siloxanos a altas temperaturas se convierten en óxidos de silicio, que
deterioran con rapidez las instalaciones de recuperación de energía de biogás
(generación de potencia del motor, la cogeneración, pilas de combustible, etc)
(Ricaurte Ortega, D., 2009).
Los análisis de siloxanos son frecuentemente realizados con
cromatografía de gases acoplada a espectrómetro de masas (GC-MS) y la
toma de muestra de gases incluye varios métodos, como adsorción, absorción
y el uso de bolsas Tedlar. El procedimiento más sensible es el muestreo del
biogás con tubos adsorbentes Dewil et al. (2007).
Hay varios factores a considerar al elegir un método analítico para
determinación de siloxanos en una muestra, como la selectividad del detector,
su disponibilidad y costes asociados con la determinación y sensibilidad de los
compuestos a analizar.
Actualmente se ve muy necesario detectar y cuantificar los siloxanos en
el agua y lodo, así como en el destino final que es el biogás, para estudiar
métodos de eliminación de estos compuestos antes que se incorporen al
combustible. Se busca maneras de mejorar el aprovechamiento del biogás,
fuente renovable de energía, y por lo tanto, se debe eliminar los elementos que
deterioran los equipos usados en la quema de este gas. De los contaminantes
presentes en el biogás, los siloxanos son los más difíciles de eliminar (Cabirta
Branco, M. S., 2010).
8
LISTA DE SIGLAS
AED Detector de emisión atómica
ATD Vaporizador térmico automático
DMSD Dimetilsilanodiol
DLLME Microextracción líquido-líquido dispersiva
EDAR Estación Depuradora de Aguas Residuales
EPA Agencia de Protección Ambiental
EPS Sustancias extracelulares
FID Detector por ionización de llama
GC Cromatografía de gases
GC-MS Cromatografía de gases acoplada a
espectrometría de masas
GC-FID Cromatografía de gases con detector de
ionización de llama
HRGC Cromatografía de gases de alta resolución
HS-SPME Microextracción en fase sólida del espacio
de cabeza
LLE Extracción líquido-líquido
MS Espectrometría de masas
PAH Hidrocarburos aromáticos policíclicos
PCB Policlorobifenil
PDMS Polidimetilsiloxanos
uma unidad de masa atómica
VMS Metilsiloxanos volátiles
VOC Compuestos orgánicos volátiles
9
2. REVISIÓN BIBLIOGRÁFICA
2.1 Siloxanos – Conceptos Generales
2.1.1 Definición
Descubiertos por Frederick S. Kipping en el siglo XX, son los siloxanos un sub-grupo de siliconas. El nombre "siloxano" es la abreviatura de silicio, oxígeno y alcano (Mckim, J. M. et al., 2001).
Los polímeros de cadenas saturadas de hidruros de silicio-oxígeno se
presentan lineales o ramificados, con alternancia de silicio y átomos de oxígeno
(cada átomo de silicio se separa de sus vecinos más próximos de silicio por
átomos de oxígeno individuales).
La estructura general de siloxanos lineales es H3Si [OSiH2]nOSiH3. Como ejemplo de siloxano cíclico se puede destacar la fórmula H3Si[OSiH2]nOSiH [OSiH2OSiH3]2 (IUPAC, 2012).
Los siloxanos hacen parte del ensamblaje de moléculas denominadas poliorganosiloxanos, de nombre genérico, silicona. Enlaces Si-O-Si de los siloxanos unidos a varias unidades CH3, constituyen las siliconas. Un polímero de siloxano de estructura consistente en átomos de oxígeno y silicio alternados, con varios radicales orgánicos unidos a los átomos de silicio, es una silicona. Con diversas aplicaciones, las siliconas suelen ser utilizadas como aceites y grasas para vacío, como agentes de impermeabilizado y como disolventes para las pinturas.
En el caso de los siloxanos, los átomos de silicio están unidos a través de átomos de oxígeno. También es posible unirlos por medio de átomos de carbono formando cadenas silico-carbono. Los siloxanos son preparados a partir de esqueletos Si-O de los silicatos minerales. El mineral es molido con una mezcla de HCl concentrado y frío, alcohol isopropílico y hexametildisiloxano. Se separa la capa de siloxano y se analiza cromatográficamente. Los trimetilsililderivados corresponden al tipo de complejo Si-O del silicato original.
Solubles en la mayoría de disolventes orgánicos, los siloxanos son combustibles. Esta familia de compuestos de organosilicio polimérico son de naturaleza inerte e impermeables al agua (López López, L. et al., 2002). 2.1.2 Propiedades de los siloxanos
Los metilsiloxanos volátiles (VMS), muy utilizados industrialmente, preferentemente tienen un punto de ebullición inferior a 250 ºC. VMS lineales tienen la fórmula general (CH3)3-SiO{(CH3)2SiO}xSi(CH3)3, y los VMS cíclicos {(CH3)2SiO}y en la que “x” es 0-5 e “y” es 3-6 (OFICINA ESPAÑOLA DE PATENTES Y MARCAS, 2002).
Las figuras 2.1 a 2.4 representan la fórmula estructural de algunos VMS.
10
Figura 2.1. VMS lineal.
Figura 2.2. VMS cíclico.
Figura 2.3. VMS lineal ramificado.
Figura 2.4. VMS cíclico ramificado.
Fuente: (OFICINA ESPAÑOLA DE PATENTES Y MARCAS, 2002)
Los polidimetilsiloxanos (PDMS), polímeros con unidades repetitivas de
sílice (dióxido de silicio), tienen en los extremos, trimetilsilano. En términos comerciales, los PDMS más importantes en la industria son los que presentan bajo peso molecular y son insolubles en agua. Los PDMS se convierten por hidrólisis en compuestos de cadena más pequeñas, los VMS, tales como octametilciclotetrasiloxano (D4) y decametilciclopentasiloxano (D5) (Stevens, 1998).
Con una polaridad distinta de los siloxanos citados, el trimetilsilanol es un compuesto con un grupo –O-Si-(CH3)2- y su estructura se completa con los grupos –OH y CH3-. La presencia del grupo –OH lo hace polar (OFICINA ESPAÑOLA DE PATENTES Y MARCAS, 2002).
11
Figura 2.5. Estructura del trimetilsilanol.
En la siguiente tabla se presentan algunas propiedades físico-químicas
de los compuestos lineales y cíclicos (Tabla 2.1). Tabla 2.1. Propiedades de los siloxanos.
Compuesto Abreviatura Fórmula
Química Masa Molar Punto
Fusión Punto Ebullición
Densidad Presión de Vapor
Solubilidad en H2O 25ºC
(g.mol-1
) (ºC) (ºC) (g.ml-1
) (KPa, 25 ºC)
(mg.L-1
)
Trimetilsilanol TMS C3H9SiOH 90,20 - 99 0,810 2,13 35000 Hexametil-disiloxano
L2 C6H18OSi2 162,38 -59 100 0,764 4,12 0,93
Hexametilciclo-trisiloxano
D3 C6H18O3Si3 222,46 50-64 134 - 1,14 1,56
Octametil-trisiloxano
L3 C8H24O2Si3 236,54 -82 152 0,820 0,52 0,035
Octametilciclo-tetrasiloxano
D4 C8H24O4Si4 296,62 17-18 176 0,956 0,13 0,056
Decametil-tetrasiloxano
L4 C10H30O3Si4 310,69 -68 194 0,854 0,07 0,00674
Decametilciclo-pentasiloxano
D5 C10H30O5Si5 370,77 -44 210 0,958 0,02 0,017
Dodecametil-pentasiloxano
L5 C12H36O4Si5 384,84 -81 229 - 0,009 -
Dodecametilciclo-hexasiloxano
D6 C12H36O6Si6 444,92 -3 245 - 0,003 0,005
Polidimetilsiloxanos
PDMS >606 - - - <0,13 -
Fuentes: (OFICINA ESPAÑOLA DE PATENTES Y MARCAS, 2002; Schweigkofler, M. & Niessner, R., 1999)
Con la tabla 2.1, se puede ver que la solubilidad es menor, cuanto mayor es el peso molecular, por lo que se puede concluir que los PDMS son compuestos más insolubles. Los valores de la presión de vapor reflejan la volatilidad de cada sustancia y, por lo tanto, cuanto mayor sea el valor, más volátil es la sustancia, siendo L2 el siloxano lineal más volátil, mientras que D3 es el más volátil entre los cíclicos.
Una evaluación del impacto de siloxanos en la utilización de la energía de biogás, concluye que el D6 es el compuesto de mayor tendencia a ser retenido por la fase sólida, por presentar alto peso molecular y la más baja presión de vapor.
Como resultado de la degradación de dimetilsiloxanos, el trimetilsilanol, no es clasificado como un siloxano, por ser muy volátil y presentar una altísima solubilidad en agua. De esta forma, en términos de solubilidad no se espera que el trimetilsilanol se acumule en el agua (Schweigkofler & Niesser, 2001).
Los siloxanos son productos sintéticos, químicamente inertes, que normalmente no se encuentran en la naturaleza. Los metilsiloxanos volátiles son muy utilizados por sus características físico-químicas, tales como:
Densidad baja, Ligera solubilidad en agua, Baja viscosidad,
12
Alto peso molecular, Punto de ebullición alto, Ligeramente volátil a temperatura ambiente, Alta compresibilidad, Buena estabilidad térmica, Pequeña tendencia a oxidación, Toxicidad muy baja.
Debido a estas propiedades, son ampliamente utilizados en la fabricación de polímeros de siliconas y para modificar las propiedades físicas de muchos materiales (Mckim, J. M. et al., 2001). 2.1.3 Aplicación de siloxanos
Una de las principales aplicaciones de los siloxanos es en la industria cosmética como sustancia vehículo volátil, donde metilsiloxanos volátiles (VMS) de bajo calor de vaporización tienen una rápida evaporación debido a la alta presión de vapor. La ventaja de su uso en productos cosméticos, es que no dejan residuos en el lugar de aplicación. En la mayoría de los casos se empleaba siloxanos cíclicos con grupos metilos de cuatro a seis grupos siloxanos (D4, D5, D6). Sin embargo, los compuestos D4 exhiben efecto tóxico para el ser humano y actualmente hay alternativas con el uso de organosiloxanos lineales (OFICINA ESPAÑOLA DE PATENTES Y MARCAS, 2006).
Otra importante utilidad de los siloxanos es en la sustitución de cloro-fluoro-carbono CFC-113 (C2Cl3F3) y de metilcloroformo (CH3CCl3) en limpieza de sistemas cerrados, limpieza de metales y componentes electrónicos, además de aplicaciones de limpieza de precisión. Bajo la Significant New Alternatives Policy (SNAP) de la EPA, se autorizó la sustitución de contaminantes atmosféricos peligrosos (HAP - hazardous air pollutants) usados para los fines de limpieza por los VMS, tales como octametilciclotetrasiloxano, decametilciclopentasiloxano, hexametildisiloxano, octametiltrisiloxano y decametiltetrasiloxano. Según el Título I de la Ley de Limpieza Atmosférica, los VMS satisfacen la necesidad de desarrollar sustitutos para sustancias reductoras de ozono (ODS - ozone depleting substances) y permiten alcanzar los Niveles de Calidad del Aire Ambiente para el ozono. EPA excluyó los VMS como componentes orgánicos volátiles (VOC), basándose en que la contribución de los compuestos de VMS es insignificante para la formación de ozono troposférico (USEPA, 1994).
Otras aplicaciones de los siloxanos están ilustradas en la Tabla 2.2.
13
Tabla 2.2. Uso de siloxanos (adaptado de Dewil et al., 2006; Varaprath et al., 2006).
Aplicación Productos
Implantes utilizados en cirugía estética Medicinal Recubrimiento de agujas hipodérmicas Revestimiento de Marcapasos
Elastómero Componente de silicona y de tubería
Cremas Gel de sílice Pañales
Productos a prueba de agua Champús, suavizantes, spray, crema de afeitar Pinturas y aceites Productos de papel Aditivos Antiespumante Productos cosméticos Desodorantes antitranspirantes Alimentos (como antiespumante, antiaglutinante y emulsionante) Productos farmacéuticos
Retardante de combustión
2.1.4 Precursores de los siloxanos
Se puede sintetizar polimetil siloxanos por hidrosililación (interconversión
de grupos funcionales) cuantitativa de los derivados de alilo (éter alil fenil, alil
glicidil éter, metacrilato de alilo, cloruro de alilo, alilamina) y 1-octeno con poli
(metilhidro) siloxanos catalizada por platino [Pt(PPh3)2(CH2=CH2), PtCl2(PPh3)2,
H2PtCl6 ciclohexanona] y rutenio (Ru3(CO)12) complejos (Marciniec, B. et al.,
1997).
Siloxanos de hidratos de carbono funcionales (CHFSs) que exhiben altas
interacciones intermoleculares han sido sintetizados por trans-acetilación ácido-
catalizada entre un siloxano de acetal-funcional y glucosa en disolventes mixtos
dimetilformamida/dioxano. Arcilla activada suele ser un buen catalizador,
debido a su alta actividad y su fácil extracción del producto. Acetal-funcionales
siloxanos como materiales de partida se pueden sintetizar fácilmente con
buenos rendimientos por hidrosililación entre siloxanos funcionales Si-H y
acroleína dietil acetal. Este método posee bajo coste y alto rendimiento. Los
CHFSs presentan alta viscosidad en comparación a los correspondientes
siloxanos acetales-funcionales y buena solubilidad en disolventes polares como
dimetilformamida y dimetilsulfóxido (Ogawa, T., 2003).
2.2 Siloxanos en el Biogás
Los siloxanos se mezclan a la variedad de materia orgánica de las aguas
residuales pues están presentes en residuos de fuentes industriales y
domésticas en los vertederos y plantas de tratamiento de aguas. La materia
orgánica en los residuos se descompone para producir biogás que contienen
14
diversos compuestos orgánicos volátiles, como el metano (Mason, J. et al.,
2006).
El biogás, mezcla de metano (CH4), dióxido de carbono (CO2), vapor de
agua y trazas de otros compuestos como sulfuro de hidrógeno (H2S), amoníaco
(NH3), siloxanos, hidrocarburos halogenados, oxígeno (O2), partículas y
espumas, requiere acondicionamiento/limpieza para adecuado uso. Es
necesario reducir/eliminar su contenido en humedad y separar de él todos los
compuestos perjudiciales en la vida útil de los equipos involucrados en su
aprovechamiento como biocombustible.
Entre los compuestos que disminuyen la calidad del biogás como
combustible o como materia prima para la elaboración de productos químicos
como metanol e hidrógeno, están los siloxanos.
En la combustión del biogás que se produce en la parte interna de motores, hay deposición de sílice, causando efecto abrasivo y reduciendo la vida útil de los motores (Reina, J., 2005).
Cuando un motor de combustión de biogás está contaminado con siloxanos, los precipitados de dióxido de silicio (sílice) se depositan sobre las piezas del motor, tales como paletas de turbinas, cilindros, intercambiadores de calor y equipos de control de emisiones. La abrasión de las superficies del motor genera una pérdida de eficiencia del motor y su fallo prematuro. Los depósitos también envenenan los catalizadores (Mason, J. et al., 2006).
La presencia de siloxanos, incluso en cantidades muy pequeñas (unos pocos mg m-3) tiene consecuencias desastrosas para las plantas que utilizan biogás como combustible.
Los compuestos más comunes presentes en el biogás son D4 y D5, dispuestos en diferentes concentraciones.
Wheless & Gary (2002) analizaron la concentración de siloxanos en 15 diferentes digestores anaerobios, obteniendo una concentración promedio de 27,7 mg m-3, siendo que los valores oscilaron de 3,8 a 122 mg m-3 para D4 y D5. Otros estudios han informado de una concentración entre 1,6 y 6,23 mg m-3 (McBean et al., 2002).
El compuesto L2 puede ser encontrado en grandes cantidades en el biogás, debido a su estabilidad química.
En la quema del biocombustible ocurre la descomposición natural de otros compuestos tales como el L4.
Moléculas más pesadas tales como D6 no se volatilizan durante la digestión anaerobia a causa de su presión de vapor muy baja.
Durante el proceso de digestión anaerobia, la mayoría de los siloxanos son liberados de los flóculos de lodo debido a la descomposición de la materia orgánica provocada por el aumento de temperatura. Estos compuestos acaban en el biogás, particularmente los cíclicos D4 y D5 (Accettola et al., 2008; McBean, 2008). Las moléculas más pequeñas, como D3, se volatilizan rápidamente y se quedan retenidas en la fase sólida las moléculas más grandes, como D6 y PDMS (Dewil et al., 2007).
En efecto, durante la combustión del biogás, el silicio se libera en forma de óxido de silicio mediante la combinación de siloxano con el oxígeno. La reacción es dada en la ecuación I (Tower, P., 2003).
15
Los residuos formados en esta combustión son de color blanco o marrón
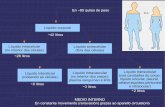
claro y se presentan en la forma de un polvo muy fino o granos más gruesos. A menudo, se forma sílice (SiO2), pero también puede haber contenido de calcio, cobre, sodio, azufre o zinc. Se adhieren rápidamente a las superficies metálicas, como una capa hasta varios milímetros de espesor (Figura 2.6). Un motor, por ejemplo, que trabaje con combustión interna para producir 0,19 normales metros cúbicos por segundo (Nm3 s-1) de biogás que contienen sólo 1mL m-3 de siloxano puede generar aproximadamente 59 kg de óxido de silicio al año. Observación: N es de Normal metro cúbico, pues como el volumen de un gas depende de su presión y temperatura, para no tener que poner estos parámetros lo que se hace es llevar la masa de gas a las condiciones normales para un gas: 0 °C y 1 atm.
Algunos ejemplos de los daños conocidos en diferentes aplicaciones que utilizan el biogás:
Aumento de la temperatura y la disminución de la transferencia de calor en intercambiadores de calor.
En el equipo generador de energía, silicatos (SiO2, SiO3, etc) se unen a las paredes de la cámara de combustión del motor, reduciendo el volumen de esta cámara y, a su vez, aumentando la relación de compresión y la tendencia a detonación. A veces, estos depósitos se forman bajo la válvula de escape, dando lugar a fugas de gas y la quema de válvulas. Esto reduce la eficiencia de la compresión del motor. Al mismo tiempo, se produce un enriquecimiento del aceite del motor con partículas finas de silicatos.
En las turbinas de gas, los silicatos pueden causar abrasión severa del rotor y se depositan sobre la boquilla de combustible.
Todos estos fenómenos conducen a un aprovechamiento más bajo de energía y calor. Debido a los constantes fallos del motor, los fabricantes de motores han venido disminuyendo constantemente el contenido aceptable de siloxanos en el biogás. Se acepta concentraciones entre 10 y 25 mg m-3 y algunos fabricantes han fijado el límite en 5 mg m-3. (Chao, S., 2002; UKEA, 2002).
De esta manera, las Estaciones Depuradoras de Aguas Residuales (EDAR), al producir biogás en la digestión anaerobia de fangos, necesitan eliminar los siloxanos y otros componentes perjudiciales presentes en el biocombustible.
Ecuación I
16
Figura 2.6. Efecto de desgaste de un motor provocado por siloxanos.
En la Tabla 3 se presenta una simulación de datos de la empresa AFT,
en términos de sílice producida, considerando una tasa de flujo de biogás de 0,07 N m3 s-1 para un motor con potencia de 1 MW. Se puede ver con más detalles, en términos numéricos, los graves problemas provocados por la deposición de dióxido de silicio en los equipos (Cabirta Branco, M. S., 2010). Tabla 2.3. Simulación de deposición de dióxido de silicio (SO2) (Cabirta Branco, M. S., 2010).
Especies Peso
Molecular % Sílice
Concentración de cada siloxano en el biogás
Sílice producida (SiO2)
mL m-3 mg m-3 Kg h-1 Kg año-1
Tetrametilsilano 88,2 31,84 1,0 3,66 0,0006 5,2
Trimetilsilanol 90,2 31,14 1,0 3,74 0,0006 5,2
Tetrametildisiloxano 134,3 41,82 1,0 5,57 0,0012 10,4
Pentametildisiloxano 148,4 37,87 1,0 6,15 0,0012 10,4
L2 162,4 34,60 1,0 6,73 0,0012 10,4
Hexametiltrisiloxano 208,5 40,42 1,0 8,64 0,0018 15,6
L3 236,5 35,63 1,0 9,80 0,0018 15,6
L4 310,7 36,17 1,0 12,88 0,0024 20,7
L5 384,9 36,50 1,0 15,95 0,0030 25,9
D3 222,5 37,88 1,0 9,22 0,0018 15,6
D4 296,6 37,88 1,0 12,29 0,0024 20,7
D5 370,8 37,88 1,0 15,37 0,0030 25,9
D6 444,9 37,88 1,0 18,44 0,0036 31,1
2.2.1 Eliminación de siloxanos
Un método para eliminar siloxanos constituye de un conjunto de equipos que interconectados entre sí, permite la remoción por medio físico (térmico y adsorción) el contenido en humedad, siloxanos, compuestos halogenados y H2S, así como reducir la temperatura del gas hasta valores permisibles para la entrada a motores o para la elaboración de productos químicos. El método es una etapa previa para la producción de biogás utilizado en la automoción o inyectado a la red de gas natural (Reina, J., 2005).
17
Intentos anteriores de eliminación de contaminantes de siloxano a partir de biogás han utilizado adsorbentes tales como carbón activado, tamices moleculares y gel de sílice. Se necesitan mejoras en las técnicas para la eliminación de siloxanos del biogás (Mason, J. et al., 2006).
La remoción estudiada por Reina, J. (2007) puede utilizar una de las técnicas siguientes o combinarlas para eliminar siloxanos antes que se utilice el biogás:
1. Refrigeración hasta 4 ºC. 2. Sub-enfriamiento hasta –25 ºC. 3. Adsorción en carbón activo. 4. Adsorción en sílica gel. 5. Lavado con hidrocarburos. 6. Combinación de técnicas.
Se realiza diferentes operaciones en un orden preestablecido: enfriamiento (reducción de temperatura), condensación (eliminación de humedad, siloxanos, ácido sulfhídrico) y adsorción (reducción de componentes indeseables, tales como siloxanos, H2S e hidrocarburos).
La planta para esta remoción, trabaja tanto en aspiración (vacío) como en impulsión (carga) de la corriente de biogás y está automatizada y optimizada en cuanto a consumo energético y al uso del carbón activo como partes elementales de su funcionamiento (Reina, J., 2007).
Otra manera de eliminar los siloxanos del biogás liberado de vertederos y plantas de tratamiento de aguas residuales es hacer pasar el biogás a través de un lecho que contiene alúmina activada, que absorbe los siloxanos. Al saturarse con siloxanos, la capacidad de absorción de la alúmina activada puede ser recuperada haciendo pasar un gas de regeneración a través del lecho de alúmina activada. Se puede utilizar un sistema de dos o más lechos de alúmina activada para eliminar siloxanos del biogás, mientras que uno o más de los otros lechos están siendo regenerados. Además de eliminar los siloxanos, la alúmina activada puede actuar como un desecante y eliminar el agua del biogás. Varios otros componentes de biogás (por ejemplo, dióxido de carbono) también pueden ser adsorbidos en la alúmina activada y retirados del biogás. Los lechos pueden incluir alúmina activada mezclada con otros materiales, como sílice activada. El gas de regeneración puede ser cualquier gas que no reaccione con alúmina activada, preferiblemente aire o nitrógeno, libre de agua.
A continuación se ilustra en la Figura 2.7 un sistema de lecho individual de extracción de siloxanos.
11
18
Figura 2.7. Sistema de eliminación de siloxanos con una cámara de lecho de alúmina activada.
El sistema de eliminación de siloxanos representado en la Figura 2.7
incluye una sola cámara (7) que contiene un lecho de alúmina activada. La cámara 7 incluye una entrada de biogás (6), una salida de biogás (10), una entrada de gas de regeneración 5 y una salida de gas de regeneración (9). Biogás a partir de la fuente de biogás (1) entra en la cámara (7) a través de una entrada de biogás (6). Si la diferencia de presión entre la fuente de biogás (1) y la cámara (7) no proporciona un flujo suficiente de biogás, se puede forzar el biogás desde la fuente (1) en la cámara (7) mediante técnicas conocidas utilizando un motor de gas, tal como un ventilador, un compresor o una bomba de vacío. En la cámara (7), los contaminantes de siloxanos en el biogás se adsorben en la alúmina activada. Purificado, el biogás deja la cámara (7) a través de biogás output (10). El biogás purificado puede ser quemado inmediatamente en el quemador de biogás (11) y como alternativa, puede ser recogido en un tanque de almacenamiento para su uso posterior. Cuando el lecho de alúmina activada en la cámara (7) se satura con siloxano, el lecho de alúmina activada es regenerado, siendo aislado de la fuente de biogás (1). Preferiblemente, el lecho se lleva entonces a las condiciones de presión atmosférica. La regeneración puede llevarse a cabo en una variedad de formas en las que un gas de regeneración es forzado a través del lecho de alúmina activada saturado con siloxano, mediante un motor de gas que puede ser uno o más ventiladores, un compresor y una bomba de vacío (Mason, J. et al., 2006). Es necesario proporcionar métodos de purificación técnicamente eficaces y económicamente viables. Los métodos de eliminación de siloxanos en biogás no son específicos, pero resultan tener eficiencia aceptable.
1
4
3
2
5 6
7
8
9 10
19
Hay otras formas de eliminar los siloxanos detalladas a continuación, donde se debe tener en cuenta también el coste del proceso: • Absorción: es posible transferir los siloxanos de la fase gaseosa a una fase líquida (por ejemplo, tetradecano). La dificultad radica en la baja capacidad de absorción y la generación de productos. • La condensación criogénica del biogás: difícil de implementar debido a complejidad de la matriz de gas. Alto coste energético. Para alcanzar 99% de eliminación de siloxanos, es necesaria una temperatura de condensación de -70°C. • Separación por membranas: el proceso es muy caro y resulta problemático debido al ensuciamiento de las membranas. • Adsorción: barato, pero difícil por la complejidad del gas de matriz y las capacidades de procesamiento que son bajas (Huppman, R. et al., 1996).
Schweigkofler & Niessner (2001) estudiaron la degradación química de los siloxanos. Siloxanos lineales y cíclicos presentes en el gas de vertedero son compuestos llamados inertes. Sin embargo, los ácidos o bases fuertes, rompen el enlace Si-O. Se han utilizado para degradar L2 (hexametildisiloxano) y D5 (decametilciclopentasiloxano). La tasa de eliminación es luego de 95%, utilizando ácido nítrico en exceso (concentración 65%) o ácido sulfúrico (concentración 48%) a una temperatura de 60 °C. Estos rendimientos disminuyen rápidamente con la temperatura y la concentración de ácido. El hidróxido de sodio mezclado con ácido sulfúrico ha dado muy buenos resultados en la degradación de la categoría D4 (octametilciclotetrasiloxano) (Huppmann et al., 1996). Se elimina un 99% para este siloxano a una temperatura de 60 °C, utilizando altas concentraciones de ácido sulfúrico. En los procesos de degradación, también se puede citar la peroxidación (Appels et al., 2008), que se utiliza para la eliminación de siloxanos en los biosólidos.
Otra manera de eliminar siloxanos es a partir de su degradación biológica. La eliminación biológica de D4 haciendo pasar el biogás en biofiltros fue estudiado por Sudeep et al. (2008). Estos experimentos se realizaron con filtros anaeróbicos o aeróbicos fortificados con mezclas (soluciones de Biogene, Prodex, NaCl, etc.). La eliminación es baja (43%) y el tiempo de degradación de siloxanos, muy lento. Estudios recientes realizados por Ohannessian et al. (2008), utilizaron microorganismos para degradar polidimetilsiloxano (PDMS) de lodos de depuradora. Se mide silicio en la fase acuosa para conocer el grado de degradación biológico de los siloxanos.
En general, una sustancia química que entra en una estación de tratamiento de aguas residuales se puede eliminar a través de los siguientes procesos: (I) por adsorción a sólidos suspendidos, eliminados como parte de los lodos, en tanque de sedimentación primaria y secundaria; (II) por emisión a la atmósfera, en el tratamiento primario y secundario, a través de la volatilización superficial, o por el efecto de aireación forzada; (III) por la biodegradación en el tanque de aireación, o en decantador primario y secundario.
20
Los siloxanos D4 y D5 no son biodegradables durante el tratamiento, pero tienen una menor solubilidad en agua y son menos adsorbentes que la mayoría de los compuestos orgánicos (Cabirta Branco, M. S., 2010).
Parker et al. (1999), desarrollaron estudios sobre la eficiencia en la eliminación de los compuestos D4 y D5 en una estación de tratamiento de aguas residuales. En escala piloto, la eliminación es de 86,4% para D4 y 95,8 para D5. En relación al lodo, permanece un 9,1% de D4 y un 8,2% de D5. De acuerdo con Mueller et al. (1995), aproximadamente el 95% de D4 presente en el agua residual se elimina a través de los procesos de tratamiento.
Los compuestos de siloxano son químicamente inertes y por eso su tratamiento químico es muy difícil (Huppmann et al., 1996). 2.2.2 Importancia del biogás y necesidad de incrementar su rendimiento
El biogás es producido por la fermentación de la materia orgánica en ausencia de oxígeno, siendo compuesto en su mayor parte por el metano y el dióxido de carbono.
Actualmente, se enfrenta una crisis de energía y problemas de contaminación. De esta manera es de urgente necesidad adoptar nuevas fuentes de energía eficaces y sencillas para el medio ambiente. La energía renovable obtenida de la biomasa, o sea, el biogás, genera pocos residuos y emisiones, además de ser obtenida de residuos, y por lo tanto, constituye una alternativa eficaz y ecológica (Poulleau, J., 2002).
La barrera para el uso de esta fuente de combustible es ciertamente la gestión de las plantas de biogás y la ausencia de un tratamiento de residuos real y de purificación adaptada al biogás. Se necesita aumentar la pureza del biogás en relación a cantidad de metano y por lo tanto se debe eliminar otros productos de la digestión anaerobia de la materia orgánica, como es el caso de compuestos clorados (gas de relleno sanitario), haluros de hidrocarburos y siloxanos que producen ácidos y derivados halogenados de silicio (Schweigkofler, M. & Niessner, R., 2001).
Dependiendo del método de producción del biogás y de la naturaleza y composición de los residuos utilizados, el biogás está compuesto de un volumen de metano de 50 a 70%, siguiendo una variación de 10 a 30% para dióxido de carbono.
Hay también algo de vapor de nitrógeno, muy poco oxígeno y agua. También contiene en cantidades muy variables, H2S, y más de 140 otras sustancias. Entre estas sustancias se encuentran todo tipo de compuestos orgánicos volátiles (VOC), hidrocarburos aromáticos policíclicos (PAH), compuestos halogenados, metales pesados, y siloxanos, en cantidades que varían ampliamente. Su contenido depende estrechamente de los residuos tratados y de la etapa de terminación de la digestión.
Raramente se utiliza el biogás en su estado natural, sin ningún tipo de tratamiento y pre-acondicionamiento. Los principales productos a ser eliminados para garantizar el rendimiento del biogás en procesos térmicos de recuperación son: el ácido sulfhídrico, compuestos halogenados y siloxanos. La desulfuración (eliminación de H2S) disminuye problemas de corrosión de las instalaciones. Durante la oxidación térmica del biogás se forman subproductos tales como SO2 y SO3 y, en presencia de humedad, se produce ácido sulfuroso
21
(H2SO3) altamente corrosivo. Así, la deshumidificación del gas evita la acumulación de condensación y la formación de solución de ácido corrosivo. En algunos casos en la recuperación del biogás, no siempre es necesario separar CO2 de metano, pues muchos motores estacionarios son capaces de funcionar con una mezcla. Sólo la eficiencia energética es afectada. Siloxanos (compuestos de silicio) deben ser eliminados absolutamente para los usos del biogás como combustible de motor. En efecto, se forman depósitos de sílice en el motor cuando los siloxanos son oxidados a alta temperatura (Poulleau, J., 2002). 2.3 Presencia de Siloxanos en el Medio Ambiente
Las buenas propiedades físico-químicas de los siloxanos, permiten su amplia utilización en la fabricación de productos comerciales diversos, tales como cosméticos, productos de limpieza y mantenimiento, resinas y pinturas, colas y adhesivos, textiles, máscaras, aparatos eléctricos y electrónicos, además de productos farmacéuticos.
Debido a este intenso uso, los siloxanos llegan fácilmente al medio ambiente, presentes en la mayoría de los residuos domésticos e industriales (Biron, M., 2007).
Su origen en las aguas residuales es también debido a la degradación aparente de los compuestos utilizados para el sellado de techos, en las construcciones.
La deposición total de los siloxanos en las aguas residuales de Estados Unidos se estima en 17.000 toneladas/año, siendo que las perspectivas son de aumento de 5% a 8% por año, en relación a la producción/uso de estos compuestos (Dewil et al., 2006; Torre & Wetzel, 2006).
En el medio acuático, la presencia de los siloxanos no llega a ser ecológicamente significativa debido a sus propiedades físicas (densidad baja, baja solubilidad en agua, volatilización rápida y su corta vida). Los siloxanos no se descomponen con el lodo activado, pero sin embargo, son adsorbidos en las sustancias extracelulares (EPS) de los lodos (Watts et al., 1995). Si el lodo es utilizado como fertilizante, por ejemplo, los siloxanos pueden estar presentes en el suelo.
Durante la digestión anaerobia de los lodos, la temperatura se eleva por encima de 40 °C (fermentación mesófila), siloxanos se volatilizan y pasan a formar parte del biogás (Dewil et al., 2007).
La producción anual de siloxanos se estima en cerca de dos millones de toneladas (Hagmann, M. et al, 2001). Sin embargo el proceso aún está creciendo (5% año, de acuerdo con el centro europeo de siliconas - CES) y por lo tanto también la cantidad de siloxanos recuperada en el biogás. 2.4 Siloxanos en Agua, Sedimento y Lodo
Estudio del método HS-SPME (microextracción en fase sólida del espacio de cabeza) acoplado a GC-MS (cromatografía de gases-espectrometría de masas) para analizar metilsiloxanos lineales y cíclicos en muestras de ríos de Cataluña (NE de España) encontró límites bajos de cuantificación. Los resultados mostraron concentraciones de siloxanos lineales
22
que van desde 0,09 hasta 3,94 ng L-1 y de siloxanos cíclicos desde 22,2 a 58,5 ng L -1 (Companioni-Damas, E. Y. et al., 2011).
En Reino Unido se hizo un estudio que determinó niveles de D5 en el rango <10-29 ng L-1 en el río Ouse Grande, y niveles ligeramente más altos en el río Nene. La concentración medida de D5 en el agua residual tratada varió entre 31 y 400 ng L-1, dependiendo del tipo de proceso de tratamiento empleado (Sparham, C. et al., 2008).
En el agua, los siloxanos sufren degradación que depende del porcentaje de los siloxanos en el agua, las condiciones de pH, temperatura, velocidad de la absorción/desorción y disponibilidad de oxígeno y nutrientes. Los cíclicos D4, D5 y D6 tienen una solubilidad muy limitada en agua y presentan enlaces intermoleculares muy débiles. Cuando estos compuestos son transportados al agua rápidamente se depositan en la película aceitosa sobre la superficie de la fase acuosa, pasando luego a la atmósfera. El agua, por lo tanto, es una fase meramente transitoria para estos compuestos, lo que significa que constituyen un riesgo reducido para el ecosistema (Graiver et al., 2003). De acuerdo con Mueller et al. (1995), los compuestos D4 y D5, muy utilizados en bienes de consumo, son principalmente emitidos a la atmósfera, y sólo el 3,3% del D4 llega a la planta depuradora.
Zhang, Z. et al. (2011) estudiaron la concentración de cuatro siloxanos cíclicos, octametilciclotetrasiloxano (D4), decametilciclopentasiloxano (D5), dodecametilciclohexasiloxano (D6), y tetradecametilcicloheptasiloxano (D7) así como 13 siloxanos lineales (L4 a L16 ), en los sedimentos muestreados del río Songhua y en muestras de lodos de aguas residuales de plantas de tratamiento de aguas residuales que descargan en el río Songhua en el noreste de China. Los siloxanos se encuentran en todas las muestras de sedimentos en las concentraciones totales (suma de todos los siloxanos cíclicos y lineales) de hasta 2050 ng g-1 de peso seco. Los rangos de concentración para los respectivos totales cíclico (D4, D5, D6 y D7) y lineal (L4 y L16) siloxanos en los lodos de depuradora son de 602 a 2360 y de 98 a 3310 ng g-1 de peso seco. Siloxanos cíclicos se encuentran en mayores concentraciones que los siloxanos lineales en las muestras de sedimentos. Sin embargo, las concentraciones sumadas de siloxanos lineales fueron superiores a las concentraciones sumadas de siloxanos cíclicos en muestras de lodos. Entre los siloxanos cíclicos, D5 y D7 fueron los compuestos dominantes, tanto en sedimentos como en lodos. Entre los siloxanos lineales, L10 y L11 en conjunto representaron el 55% de las concentraciones totales en muestras de lodos, y L6, el 30% de la concentración total en muestras de sedimentos.
En la digestión de lodos, solamente siloxanos volátiles, VMS, son detectados en el biogás, mientras que los polidimetilsiloxanos (PDMS), de peso molecular más alto, se adsorben en el lodo (Dewil et al., 2006).
Se espera que los PDMS tengan una alta movilidad en los compartimentos terrestres y acuáticos, siendo que no transitan a la atmósfera por tener baja presión de vapor y alto peso molecular. Cuando entran en la fase acuosa, rápidamente son transportados a la película sobre el agua o a las partículas en suspensión (Cabirta Branco, M. S., 2010). Aproximadamente 97% de los PDMS terminan en los lodos resultantes del tratamiento de aguas residuales. Esta teoría está apoyada en datos de monitorización de efluentes tratados de varias estaciones de tratamiento (Graiver et al., 2003; Fendinger et al., 1997). Por los estudios realizados, se concluye que los PDMS no se
23
degradan o se descomponen en el tratamiento de aguas residuales, no afectando a ninguno de los procesos (Graiver et al., 2003).
Los dimetilsiloxanos, compuestos de bajo peso molecular, son bastante volátiles, evaporando para la atmósfera y siendo degradados por reacciones de oxidación (Griessbach & Lenhmann, 1999).
En cuanto al destino de los siloxanos en el suelo, muchos estudios anteriores apoyan la hipótesis de que los PDMS sufren una despolimerización por hidrólisis, resultando en la rotura de las conexiones siloxanos y generando compuestos de bajo peso molecular, PDMS oligoméricos (Lehmann et al., 1994, 1995) (Figura 2.8).
Figura 2.8. Mecanismo de hidrólisis de los siloxanos en el suelo (Griessbach & Lenhmann,1999).
El primer producto de esta hidrólisis, dimetilsilanodiol (DMSD), tiene dos formas de ser eliminado; por volatilización para la atmósfera o por biodegradación en el suelo (hidrólisis). Los productos finales de estas descomposiciones suelen ser el dióxido de carbono (CO2), dióxido de sílice (SiO2) y agua (H2O) (Griessbach & Lenhmann, 1999). 2.5 Bioacumulación de Siloxanos
Los metilsiloxanos volátiles (VMS) fueron detectados en niveles tróficos de biota acuática. Octametilciclotetrasiloxano (D4), decametilciclopentasiloxano (D5), y dodecametilciclohexasiloxano (D6) se estudiaron junto con los bifenilos policlorados (PCB) en poliqueta y pez del estuario de Humber, Reino Unido. La bioacumulación se evaluó utilizando los factores de bioacumulación que cuantifica la fracción de la presencia de un contaminante en el medio acuático que se transfiere a la biota. PCB 180, una sustancia química de alta bioacumulación, se utilizó como punto de referencia. La media de mmBAF (factor de bioacumulación multimedia) para D5 fue aproximadamente el doble que el de PCB 180 en dos poliquetos y en el pez platija, mientras que para D4 era 6 y 14 veces mayor, respectivamente. El mmBAF de D6 era un factor de 5-10 menor que la de PCB 180. La bioacumulación multimedia comparativamente fuerte de D4 y D5, se explica porque ambos compuestos (D4 y D5) tienen una tendencia 100 veces más fuerte a la partición en lípidos en lugar de en carbono orgánico, mientras PCB 180 tiene particiones en un grado similar en ambas matrices (Kierkegaard, A. et al., 2011).
Debido al alto peso molecular de los PDMS, éstos no se difunden a las células y por lo tanto se espera que no sean bioacumulativos (Cabirta Branco, M. S., 2010).
24
2.6 Estudio de la Toma de Muestra para Determinación de Siloxanos 2.6.1 Muestras de agua
Los puntos de toma de muestra en una Estación Depuradora de Aguas Residuales (EDAR) deben ser representativos del influente, al corresponder con la mezcla de todos los colectores de la red unitaria de la población.
Para la toma de las muestras compuestas, de acuerdo con la normativa legal (Directiva 91/271/CEE, sobre el tratamiento de aguas residuales urbanas), se utilizan toma-muestras automáticos portátiles. Las muestras individuales, recogidas a diferentes intervalos de tiempo, son homogeneizadas y se hace los análisis lo más pronto posible para que no se pierda la composición real de siloxanos.
Las muestras generalmente son tomadas en el decantador secundario y son conservadas en frascos estériles a 4 ºC (APHA, 1992). 2.6.2 Muestras de lodo
En lodos procedentes de plantas de tratamiento de agua residual urbana e industrial, un muestreo puntual de una masa de lodo suele ser realizado con válvula de muestreo limpia y sin corrosión. Las muestras pueden ser almacenadas en recipientes de polietileno, polipropileno, policarbonato y vidrio debido a la estabilidad química de estos materiales. Se debe tomar precauciones para que no haya explosiones provocadas por gases producidos por el lodo sometido a presión en el recipiente, como por ejemplo, un sistema de apertura periódico del recipiente para liberar presión. Si existe riesgo de liberación de gases, se debe envolver el recipiente con cinta adhesiva resistente al agua o con mallas plásticas.
El almacenamiento de las muestras de lodo así como el transporte debe mantenerlas a temperaturas de 4 ºC ± 2 ºC para evitar pérdidas de material volátil y minimizar cambios inducidos biológicamente. Conviene también mantener las muestras en la oscuridad para evitar estimulación de la actividad biológica o reacciones de degradación de compuestos. 2.6.3 Muestras de biogás
Las técnicas de recolección del biogás para análisis de siloxanos son muchas y se pueden simplificar como tres más importantes y utilizadas: adsorción sólida, adsorción líquida y recepción con el uso de diferentes materiales (Tabla 2.4).
25
Tabla 2.4. Materiales utilizados en las diferentes técnicas de muestreo (adaptado de Dewil et al., 2006).
Técnica de Muestreo Materiales Usados en el Muestreo
Adsorción sólida Carbón activado.
Resinas iónicas-XAD 2, XAD 4.
Adsorción líquida Metanol, hexano y diesel
Bolsas Tedlar
Recogida en recipientes Botella de vidrio
Recipientes de acero (Canister)
En la adsorción sólida, se utiliza un tubo relleno de un adsorbente sólido,
como carbón activado o resina iónica. Se hace necesario crear una presión negativa para que el biogás pase por el tubo. Se debe controlar el flujo de biogás de entrada al sistema y la duración de la prueba con el fin de determinar el volumen de biogás analizado. Se extraen los compuestos de la matriz adsorbente para análisis de los siloxanos (Hayes et al., 2003).
Según Dewil et al. (2006) para la adsorción de los siloxanos a través de tubos con carbones activados (origen natural o sintético) y adsorbente polimérico, se aspira el biogás a un flujo de 1 L min-1 durante 10 minutos. El cerrado debe ser hermético con tapones de plástico, siendo la conservación en nevera a 4 °C.
La adsorción líquida implica el paso del biogás por dos o más vasos llenos con metanol (disolvente), utilizando una bomba. Los siloxanos se disuelven en el disolvente enfriado. Al comienzo del sistema hay una válvula de aguja que permite el ajuste del flujo del biogás, registrando la medida en el medidor de flujo de volumen de gas (Figura 2.9). El sistema se cierra transcurrido el tiempo necesario, y se hacen los análisis de los siloxanos presentes en el disolvente (Tower, 2003).
Figura 2.9. Representación del muestreo por adsorción con metanol (Tower, 2003).
El biogás puede ser almacenado en 3 tipos de bolsas de diferentes
volúmenes (1 y 3 litros) y materiales (Tedlar y Flexfilm) y en 1 tipo de minicanister (0,4 litros).
En la recogida por Bolsas Tedlar, se recoge la muestra en una bolsa comunicada a una bomba a volúmenes de 1, 3 o 5 L, permitiendo detecciones en el orden de mg L-1 (Air Toxics, 2008) (Figura 2.10).
26
Figura 2.10. Representación de la bolsa de recogida de muestra (Bolsa Tedlar) (Air Toxics, 2008).
Otro ejemplo de recipiente de muestreo, el canister se mantiene bajo
vacío para que el biogás sea recogido de forma pasiva. Se puede recoger diferentes volúmenes de muestra dependiendo de la capacidad del canister (Figura 2.11).
Figura 2.11. Representación de canister (Air Toxics, 2008).
El canister es fiable en relación a fuentes de contaminación. En las
bolsas se demostró presencia de silicona en tests con blancos y en los recipientes de vidrio se detectó adsorción de siloxanos a la pared del vidrio (Hayes et al., 2003). Como desventaja, este método proporciona poca información, dando apenas una pequeña idea de la concentración, pues el canister se queda relleno por solo algunos segundos.
De esta manera, la muestra puede no ser representativa de las concentraciones de siloxanos en el biogás, siendo alto el grado de incertidumbre (Wheless & Pierce, 2004, Hayes et al., 2003).
En relación a la tasa de recuperación, la adsorción con metanol presenta un mejor rendimiento que los canisters para los siloxanos cíclicos tales como D4, D5 y D6. Para recuperar pentametildisiloxano y D3, el canister presenta mejores resultados (Hayes et al., 2003; Saeed et al., 2002).
27
2.7 Caracterización de los Métodos de Análisis – Determinación Analítica 2.7.1 Determinación de siloxanos en el lodo
Para el análisis de siloxanos en los lodos, R. Huppmann et al. (1996) describen un método que consiste en despojar los siloxanos de las muestras por el helio. Posteriormente, la mezcla de gas se pasa a través de una resina XAD-para adsorber los siloxanos, seguido por una desorción. La cuantificación se hace por GC-FID.
Dewil et al. (2007) hicieron un estudio para determinar siloxanos en una planta de aguas residuales de Bélgica, con muestras de lodos tomadas del decantador secundario. Se determinó el contenido de sólidos secos del lodo. El disolvente elegido fue n-hexano para análisis en cromatógrafo de gases con inyector automático. La temperatura del inyector se estableció a 125 °C, la inicial del horno a 60 °C, mantenida durante 4 minutos, cuando se incrementó hasta 250 °C a una velocidad de 8 °C/min. El detector FID se mantuvo a temperatura de 250 °C. En la Figura 2.12 se puede apreciar el cromatograma de una muestra de lodos sobrecargada con D4, siendo que este siloxano suele salir entre los 5 y 6 minutos. Este método presentó buena recuperación y repetibilidad.
Figura 2.12. Cromatograma de muestra de lodo sobrecargada con D4.
La repetibilidad es importante en análisis con cromatografía gaseosa
para garantizar la confiabilidad del método utilizado, pues se hace determinado
número de inyecciones en el mismo día de muestras a fin de obtener buen
coeficiente de variación. Como existe una relación significativa entre la
concentración y el área de pico, se obtiene los coeficientes de variación que
evalúan la precisión de los análisis repetidos de una misma muestra (Granda,
F. et al., 2011).
28
2.7.2 Determinación de siloxanos en el suelo
Sánchez-Brunete et al. (2010) analizaron los siloxanos lineales L4 y L14
y los siloxanos cíclicos D4, D5 y D6, en diferentes muestras de suelo de
campos agrícolas e industriales de la región de Madrid, Albacete, Badajoz y
Toledo (España). Para la extracción de muestra se utilizó columna de vidrio con
papel Whatman, añadiéndose sulfato de sodio anhidro al filtro de papel. Se
prepararon dos soluciones estándar; una con L4, D4, D5, D6, L5 y silano a 500
ng mL-1 y otra con PDMS y silano a 500 ng mL-1. Las muestras de suelo fueron
enriquecidas con las soluciones estándar de siloxanos y se hizo extracción del
suelo con 5 mL de n-hexano durante 15 minutos en baño de ultrasonido a
temperatura ambiente. La recuperación de todos los siloxanos con hexano es
mayor que 92%, nivel más alto que otros disolventes orgánicos. Al utilizar baño
de ultrasonido además se incrementó en un 20% la recuperación de siloxanos.
De las quince muestras analizadas, todas contenían D5 y D6, siendo que en
los suelos agrícolas las concentraciones variaron de 9,2 hasta 56,9 ng g-1 y 5,8
a 27,1 ng g-1, respectivamente. En contraste, D4 no se encontró en ninguna de
las muestras de suelos agrícolas. Debido a su uso extendido, siloxanos pueden
entrar en el suelo a través de rutas directas e indirectas, incluyendo los
derrames de biosólidos y la deposición de la atmósfera gaseosa. En el suelo
enmendado con lodos de aguas residuales, D5 y D6 se detectaron en
concentraciones que van del 30,8 al 37,5 ng g-1 y 22,5 a 32,0 ng g-1,
respectivamente. En cuanto a los suelos industriales, todas las muestras
examinadas mostraron cantidades detectables de los siloxanos D5 y D6, con
concentraciones que van desde 22,3 a 482,6 ng g-1. D4 se detectó en sólo un
suelo en una concentración de 58,6 ng g-1 (Sánchez-Brunete et al., 2010).
2.7.3 Determinación de siloxanos en el biogás
Narros, A. (2009) et al. determinaron siloxanos en el biogás por técnica
GC-MS. Se hicieron tomas de muestras de gas en la propia tubería de una
estación de tratamiento de aguas residuales. Las muestras gaseosas fueron
recogidas por tubos tipo Tenax TA y Carbosieve III y por el método impinger se
hace burbujear 10 L de biogas a través de 20 mL de un líquido absorbente,
metanol. También se muestrearon con bolsas Tedlar. Una curva de calibración
con soluciones patrones de los siloxanos fue construida a partir de soluciones
de hexametildisiloxano (L2), hexametilciclotrisiloxano (D3), octametiltrisiloxano
(L3), octametilciclotetrasiloxano (D4), decametilciclopentasiloxano (D5) y
trimetilsilanol. Los compuestos orgánicos volátiles adsorbidos por los tubos
Tenax y Carbosieve fueron desorbidos por trampa enfriada de tenax (fijada a -
30 °C) dentro de una matriz ATD (automatic thermal desorber) y analisados por
cromatografía de gases acoplada a espectrometría de masas. De acuerdo con
los resultados obtenidos, concluyeron que la adsorción con tubos Tenax es
más fácil y rápida, además de tener menores riesgos de pérdidas y tener la
29
ventaja de permitir el análisis de trimetilsilanol. Se encontraron mayores
concentraciones de los siloxanos D4 y D5 en las muestras de biogás.
2.7.4 Determinación de los siloxanos en el agua
Huppmann, R. et al. (1996) estudiaron la determinación de siloxanos en
aguas residuales, haciendo extracción de estos compuestos volátiles con gas
helio burbujeado en muestras líquidas de un proceso de tratamiento de aguas
residuales. La adsorción se procede con resinas XAD, que elimina
cuantitativamente los siloxanos de las muestras de agua residual. El agua
atraviesa la resina a un flujo de 300 mL min-1 y después es sometida a una
extracción en soxhlet con 200 mL de acetona por 6 horas. Posteriormente el
residuo acuoso (acetona y el agua con siloxanos) es llevado a evaporación a
40 °C. Se extrae con cloroformo y se pasa el extracto a través de sulfato de
sodio anhidro. El residuo es seco y para analizarlo por cromatografía se hace
una dilución. La desventaja de la resina XAD es la necesidad de regeneración
con solución de ácido sulfúrico concentrado a temperatura de 60 °C.
30
3. OBJETO Y ALCANCE DEL TRABAJO
El proyecto tiene como objeto poner a punto un método cromatográfico
para análisis de muestras de agua de Estaciones Depuradoras de Aguas
Residuales (EDAR) en España, identificando y cuantificando siloxanos
volátiles, perjudiciales al proceso de producción del biogás.
Los métodos utilizados en la detección de los siloxanos están descritos
por procedimientos internos de la empresa AQUALOGY Medio Ambiente y de
manera general consisten en análisis de las muestras por Cromatografía de
Gases acoplada a Espectrometría de Masas (GC-MS).
Como prácticas realizadas dentro del máster oficial de Gestión
Sostenible y Tecnologías del Agua, el presente proyecto también tiene la
finalidad de aplicar los conocimientos adquiridos durante las clases y permitir el
desarrollo científico en el área de cromatografía de compuestos volátiles.
La identificación de los siloxanos volátiles de las muestras de agua de la
depuradora, posibilitará evaluar la presencia de siloxanos en las estaciones de
tratamiento que producen el biogás. Otros trabajos científicos han estudiado la
presencia de siloxanos lineales y cíclicos bien como trimetilsilanol en muestras
de gases de depuradoras, pero identificar la presencia de los siloxanos y de las
especies formadoras en el agua residual también es importante. De esta forma,
se podrá buscar técnicas de inhibición de siloxanos presentes en el agua
residual, previniendo su posterior deposición en el lodo y consecuente
aparición de los mismos en el gas formado con la digestión anaerobia de este
lodo.
Solucionar el problema de bajo rendimiento del biogás producido en las
plantas depuradoras a causa de la presencia de siloxanos es evitar que se
formen precipitados de dióxido de silicio en la quema del combustible, lo que
conlleva a daños en las piezas del motor de combustión.
31
4. PROCEDIMIENTO 4.1 Reactivos y Disoluciones
A partir de siloxanos comerciales de grado analítico se prepararon dos soluciones madres con concentración aproximada de 10 g L-1 de cada uno de los siloxanos disueltos en metanol Baker HPLC Analyzed marca J.T. Baker. Utlizándose una balanza analítica marca Mettler Toledo modelo AG204 con precisión de 4 cifras decimales, se pesó masa cercana a 0,1000 g de trimetilsilanol marca Sigma (Alemania), hexametildisiloxano Fluka Analytical (Alemania), hexametilciclotrisiloxano Aldrich Chemistry (Reino Unido), octametiltrisiloxano Aldrich Chemistry (EE. UU.), octametilciclotetrasiloxano Aldrich (Alemania), decametiltetrasiloxano Aldrich Chemistry (EE. UU.), decametilciclopentasiloxano Aldrich Chemistry (EE.UU), dodecametilpentasiloxano Aldrich Chemistry (EE.UU), dodecametilciclohexasiloxano Aldrich Chemistry (Alemania).
El pesaje de cada siloxano se hizo en relación a un volúmen aproximado de 100 µL, con excepción del hexametilciclotrisiloxano (sólido), pesado separadamente en un vaso y totalmente disuelto en metanol. Se pesaron los siloxanos dentro de un matraz aforado de 10 mL completado con metanol hasta enrase (Figura 4.1).
Figura 4.1. Preparación de las soluciones madre.
Las masas exactas de cada siloxano en las dos soluciones madres preparadas y las respectivas concentraciones están señaladas en la tabla 4.1. Las soluciones fueron preparadas en días distintos para que una pudiese ser de calibrado y otra de verificación para estudio de la reproducibilidad del método de análisis cromatográfico para los siloxanos (Figura 4.2).
32
Figura 4.2. Soluciones madre para reproducibilidad del método cromatográfico.
Tabla 4.1. Masas y concentraciones de las soluciones madre.
Compuesto comercial Masa en la
solución
madre
(g)
Concentración
en el matraz de
calibrado
(g L-1
)
Masa en la
solución
madre de
verificación
(g)
Concentración
en el matraz de
verificación
(g L-1
)
trimetilsilanol 0,1181 11,81 0,0948 9,48
hexametildisiloxano 0,1112 11,12 0,1066 10,66
hexametilciclotrisiloxano 0,1236 12,36 0,1067 10,67
octametiltrisiloxano 0,1270 12,70 0,0991 9,91
octametilciclotetrasiloxano 0,1366 13,66 0,1083 10,83
decametiltetrasiloxano 0,1262 12,62 0,1006 10,06
decametilciclopentasiloxano 0,1526 15,26 0,1155 11,55
dodecametilpentasiloxano 0,1237 12,37 0,1035 10,35
dodecametilciclohexasiloxano 0,1198 11,98 * -
*La solución comercial no estaba disponible cuando se preparó la concentración
madre de verificación.
33
4.2 Cromatografía de Gases Acoplada a Espectrometría de Masas
La mayoría de los métodos de análisis para siloxanos utiliza la técnica de cromatografía de gases (GC) con columna capilar.
Como detectores para cromatógrafo de gases, se puede hacer uso del detector por ionización de llama (FID), detector de emisión atómica (AED) o detector espectrómetro de masas (MS).
De acuerdo con Hayes et al. (2003), el detector por espectrometría de masas es muy selectivo una vez que permite el conocimiento de la información estructural del compuesto basada en picos de fragmentación patrón y masa de los iones. La masa específica de los iones posibilita la cuantificación de un determinado compuesto en presencia de otro que esté co-eluído. En la espectrometría de masas se obtiene alta sensibilidad para la identificación y cuantificación de componentes minoritarios en matrices complejas. El análisis por GC/MS resulta en una cuantificación directa de las especies presentes, con recurso a la calibración directa. Este método de calibración se constituye de un análisis directo de las especies de siloxanos, haciendo variar sus concentraciones. Se construye una curva de calibración para cada compuesto y con base en esta curva se puede calcular la concentración de siloxanos presentes en la muestra. La calibración directa permite al usuario obtener información sobre la muestra, de forma exacta y detallada de diversos tipos de siloxanos (Hayes et al., 2003; Saeed et al., 2002).
De esta forma, se preparó de forma adecuada los equipos utilizados para los análisis de este trabajo, haciéndose la instalación de la columna cromatográfica adecuada para separación de siloxanos volátiles, bien como limpieza de los componentes del espectrómetro de masas, conexiones, estabilizaciones y configuraciones del método de detección y cuantificación en el software NIST MS Search 2.0. 4.2.1 Condiciones previas
Antes de utilizar los equipos analíticos GC-MS, se instaló la columna
para análisis de siloxanos en el cromatógrafo de gases. La columna instalada
fue una DB-624 de 60 m de longitud x 0,250 mm de diámetro x 1,40 µm de
espesor de filme o superficie rellena (Figura 4.3). El cromatógrafo de gases era
de la marca Varian 3900 (Figura 4.4) con inyector 1177 (Figura 4.5).
34
Figura 4.3. Columna capilar instalada en el horno del cromatógrafo gaseoso.
Figura 4.4. Purga-trampa y cromatógrafo de gases acoplado al espectrómetro de
masas
35
Figura 4.5. Inyector del cromatógrafo de gases.
Las piezas que componen el espectrómetro de masas Varian Saturn
2100T (Figura 4.4) fueron limpias con solución de diclorometano, dentro de
vasos inmersos en baño de ultrasonido J.P. Selecta durante 15 minutos.
Se configuró el Software de control del análisis cromatográfico con las
especificaciones de la columna (Figura 4.6) y se hizo pasar el gas portador,
helio, a diferentes temperaturas, a fin de eliminar impurezas. Para la
verificación del buen funcionamiento del cromatógrafo, no se conectó al
detector MS (Figura 4.7). Se confirmó la entrada y salida del gas de arrastre
helio en la columna cromatográfica, poniéndose la extremidad de la columna en
un vaso con n-hexano grado analítico marca Panreac, verificándose la
formación del burbujeo.
Figura 4.6. Configuración de las Figura 4.7. GC desconectado del MS.
condiciones cromatográficas.
36
Con la exposición de las piezas del espectrómetro de masas a la
atmósfera al hacer limpieza e instalación, agua y aire se quedan en el interior y
por eso hay que hacer una eliminación para que las cantidades detectadas H2O
y aire (O2 y N2) no interfieran en los picos de las muestras analizadas. Con el
cromatógrafo conectado al espectrómetro, se dejó de un día para el otro, un
flujo de helio pasando por el conjunto GC/MS, siendo que la temperatura de la
columna y la trampa del MS fueron mantenidas a 200 °C. El manifold que
intercomunica la columna al MS fue mantenido a 120 °C. De este modo, se
logró eliminación adecuada de agua y aire.
4.2.2 Instrumentación
La calibración del espectrómetro de masas se llevó a cabo
separadamente, sin estar acoplado al GC. Las condiciones de calibración
fueron voltaje para el multiplicador de MS de 1350 V como mínima y de 1400 V
como máxima.
El espectrómetro de masas (MS) fue calibrado con una solución patrón
de gases del propio equipo. Lo que se verificó, fueron las masas
correspondientes a los picos de los fragmentos de los gases estándares. De
esta manera se garantiza que la fragmentación en los análisis posteriores se
hará de manera correcta.
El cromatógrafo de gases fue calibrado haciéndose pasar por la
columna, una solución patrón de benzeno-deuterado, cogidos por el equipo de
purga y trampa ARCHON, marca Varian (Figura 4.4). Se puede utilizar el
equipo de purga-trampa comunicado al conjunto GC/MS para análisis de
muestras líquidas o sólidas. Los constituyentes orgánicos volátiles se purgan o
extraen haciéndose pasar una corriente de helio por la muestra. El helio hace
que los compuestos volátiles se volatilicen (Figura 4.8).
37
Figura 4.8. Burbujas de helio arrastrando compuestos volátiles.
Los vapores van a una columna-trampa (Tenax, sílica gel y carbón) que
retiene los compuestos afines que luego son arrastrados por el gas helio a la
columna cromatográfica. Después de la separación de los compuestos en el
cromatógrafo, aquellos gaseosos son llevados al Trap del detector MS (Figura
4.9), donde reciben un bombardeo de electrones fragmentándose en partículas
de masas identificables, ion-fragmento (Gomis Yagües, V., 2008). De esta
forma, comunicados purga/trampa y GC/MS se verificó en los cromatogramas
obtenidos, si la separación de los compuestos volátiles dentro de la columna se
realizaba correctamente. En los análisis posteriores no se utilizó el equipo de
purga y trampa.
38
Figura 4.9. Trap del detector espectrómetro de masas.
4.2.3 Identificación de los siloxanos
Con el objetivo de verificar el estado de separación e identificación de
los siloxanos por la columna DB-624 se inyectó la solución madre de calibrado
diluida 1000 veces en hexano (10 mg L-1).
A continuación se encuentra la rampa de temperatura de la columna DB-
624 basada en estudios de la empresa (Tabla 4.2), con almacenaje de iones
con masas de 60 a 445 unidades de masa atómica (uma).
Tabla 4.2. Programa de temperatura.
Temperatura
(°C)
Velocidad de calentamiento
(°C/min)
Tiempo
(min)
40 0 2
120 6 5
150 8 0
220 20 5
Cuando se utiliza un programa de temperatura para resolver la
separación de las sustancias presentes en una mezcla, si se mantiene la
presión constante en la cabeza de la columna, al aumentar la temperatura, la
viscosidad del gas portador aumenta y el flujo que pasa por la columna
disminuye (Gomis Yagües, V., 2008). En este trabajo se fijó el flujo de helio en
20 mL min-1 para permitir una mejor eficacia y resolución, bien como un menor
tiempo de análisis.
El cromatograma del análisis de los 9 siloxanos comerciales de la
solución madre diluida tuvo un tiempo total de retención de 32,58 minutos.
El inyector del cromatógrafo alcanza una temperatura de 250 °C lo que garantiza la volatilización de todos los siloxanos de la solución visto que la mayor temperatura de ebullición corresponde al dodecametilciclohexasiloxano con un 245 °C.
39
Resulta importante hacer una verificación sobre la posición de la aguja del inyector, visualizando si se encuentra encima del agujero, pues de lo contrario se puede perder la aguja de inyección cuando en vez de entrar en el agujero que va hacia la columna, se choca contra el equipo (Figura 4.10).
Figura 4.10. Aguja del inyector.
La inyección en modo Split es activada en el Software para 12, lo que
significa que 1 parte en 12 partes de muestra cogidas por la aguja del equipo pasa por la columna capilar, siendo el resto arrastrado por el gas portador helio. Para obtener menor cantidad de volumen, se utiliza un divisor de flujo (la inyección se conoce como modo "Split") a la entrada de la columna, que desecha parte del analito introducido (McNair, H. M. & Miller, J. M., 1998). Antes de cada inyección, la aguja del inyector coge varias veces el eluyente hexano grado analítico, inyectándolo en la columna para su limpieza. También como solución blanco, formando la línea de base en el cromatograma, se usa el hexano.
El volúmen de muestra cogido por el inyector fue de 2 µL y el flujo en la columna correspodiente a 0,2 mL min-1.
En la figura 4.11 se muestra los picos cromatográficos de cada siloxano
encontrado en la solución madre diluida, permitiendo verificar los tiempos de
retención de cada polímero de silício, oxígeno y carbono.
40
Figura 4.11. Cromatograma de una solución patrón de siloxanos.
La tabla 4.3 refleja los tiempos de retención de cada siloxano y la unidad
de masa atómica (uma) correspondiente a cada uno.
MS Data Review Active Chromatogram Plot - 7/17/2012 1:31 PM
5 10 15 20 25 30minutes
0
100
200
300
400
500
600
700
kCounts Ions: RIC Ignore Patroncalprueba17-7.SMS 2000 CENTROID RAW
41
Tabla 4.3. Tiempo de retención y unidad de masa atómica para cada siloxano en la
columna DB-624.
Siloxano Tiempo de retención Unidad de masa atómica
(uma)
TMS 11,022 75
L2 12,865 147
D3 17,822 207
L3 20,455 221
D4 25,126 281
L4 27,063 208-295
D5 28,884 355-267+73
L5 30,408 282-360
D6 32,240 342
4.3 Curvas de Calibrado
La validación de un método cromatográfico depende de una buena curva
de calibrado para cada compuesto que se pretende identificar.
A partir de la solución madre de calibrado de la tabla 5, se preparó una
solución-madre de 20 mg L-1 usada para las diluciones necesarias para
construcción de las curvas de calibrado.
Se añadieron 10 µL de la solución madre de calibrado en un matraz de 5
mL con metanol para obtener la concentración aproximada de 20 mg L-1 de
cada siloxano.
Partiendo de esta nueva solución madre se hicieron diluciones con
hexano, obteniéndose concentraciones de siloxanos de 0,1; 0,5; 1; 2; 5; 10 y 20
mg L-1 para construcción de curvas con 7 puntos de calibrado. El hexano
permite una desorción cuantitativa de los siloxanos de la solución y hace que
volatilicen con rapidez a la hora de la inyección en la columna cromatográfica
(Relea, F. et al., 2009). Para evitar la pérdida de alguno de los siloxanos, las
muestras preparadas con hexano son transferidas a los viales para inyección
inmediata (Figura 4.12).
En las soluciones madres de calibrado y verificación preparadas al inicio de este trabajo, los siloxanos comerciales fueron disueltos en metanol, que debido a su polaridad posibilita una mejor extracción de los siloxanos, permitiendo el almacenaje en frascos de vidrio cerrados hermeticamente, mantenidos en refrigeración.
42
Según Marigorta, A. M. (1997), a través de un estudio sobre modelización termodinámica de sistemas de mezclas binarias que contienen metanol con n-alcanos (C5, C6) y esteres alquílicos, este disolvente se caracteriza por el carácter fuertemente polar, con gran capacidad para formar/destruir enlaces de hidrógeno.
Figura 4.12. Preparación de las diluciones para curvas de calibrado.
Las curvas de calibrado son construidas a partir de las áreas de los picos cromatográficos originados al final de las inyecciones, proporcionales a determinada concentración. Cada solución diluida tenía un cromatograma con los picos correspondientes a los 9 siloxanos. La integración de cada área generaba una concentración correspondiente.
Antes de proseguir, se analizaron los coeficientes de correlación de las curvas para garantizar precisión adecuada en el método de estudio. Para aumentar el coeficiente de correlación de las curvas de calibrado, también se prepararon diluciones a partir de la solución madre de verificación, con concentraciones de 0,5; 1; 2; 5; 10 y 20 mg L-1. De esta manera, utilizando el Software, era posible usar en la construcción de las rectas los valores de concentraciones producidos, a partir de la solución madre de calibrado y a partir de la solución madre de verificación para mejorar los coeficientes de correlación. Las curvas fueron usadas como referencia en el método de identificación y cuantificación de los siguientes análisis.
También tiene importancia una verificación sobre cuán cerca del valor de referencia que hemos usado para calibrar el instrumento se encuentra el valor medido (ASTM, 1999). De esta forma también se calcularon los valores de las concentraciones para las diluciones preparadas a partir de la solución madre de verificación para comparar con los valores reales obtenidos por cromatografía.
43
4.4 Identificación de los Picos Cromatográficos
La identificación de cada pico en el cromatograma se hace mediante la búsqueda de los valores de fragmentos de masas (Figura 4.13) anteriormente conocidos en el apartado 4.2.3. Se identifica el tiempo en lo cual sale cada siloxano y se crea un método en el Software para análisis de los 9 siloxanos del trabajo. Se guardan informaciones sobre el rango de integración, ancho del pico cromatográfico, sensibilidad o señal ruido, cuentas de área y lo que se debe descartar de área en la lectura realizada por el detector.
Se comproba la eficiencia del hexano en la desorción de los siloxanos cuando se obtiene una curva de calibrado con buen coeficiente de correlación y poco señal ruido en los cromatogramas.
El método de análisis de siloxanos grabado en el Software es usado en todos los análisis de este proyecto y se puede extender su uso a cualquier análisis de agua contaminada por siloxanos.
Existe siempre un banco de datos en el Software, donde se encuentran compuestos analisados por el laboratório en su cotidiano. En el programa informático se encuentran datos de otros análisis y se puede utilizar la información para identificar los picos cromatográficos dudosos. Con la información del rango de los fragmentos de masas de cada siloxano y los valores de concentración obtenidos en las curvas de calibrado, el própio Software correlaciona los datos recibidos por el detector, de las masas de fragmento, con el banco de datos guardado en la carpeta de trabajo. Al final de las inyecciones de cada día, se usa la función cuantificación del programa para producir una tabla con los valores de áreas de los picos cromatográficos y la concentración correspondiente para cada siloxano.
El programa dispone de informaciones sobre cada compuesto identificado, como fórmulas y detalles sobre los fragmentos de masa (Figura 4.14).
44
Figura 4.13. Cromatograma y espectro de masas de una solución diluída a 10 mg L-1 de siloxanos.
MS Data Review Active Chromatogram and Spectrum Plots - 8/10/2012 2:16 PM
5 10 15 20 25 30minutes
0
25
50
75
kCounts RIC Merged 10ppm-cal.sms 2000 CENTROID RAW
1A
TMS
L2
D3
L3
D4
L4
D5
L5
D6
100 200 300 400 500m/z
0%
25%
50%
75%
100%
73
221
222
223
Spectrum 1A20.515 min. Scan: 1619 Channel: Merged Ion: 12253 us RIC: 30003BP 221 (12091=100%) 10ppm-cal.sms
45
Name: Trisiloxane, octamethyl-
Formula: C8H24O2Si3
MW: 236 CAS#: 107-51-7 NIST#: 11382 ID#: 131657 DB: mainlib
Other DBs: Fine, TSCA, HODOC, EINECS
Contributor: R.W.CRAWFORD UNIV. OF CALIFORNIA, LIVERMORE, CALIFORNIA, USA
10 largest peaks:
221 999 | 73 479 | 222 253 | 103 127 | 223 126 |
147 94 | 133 64 | 59 64 | 45 63 | 205 57 |
Synonyms:
1.Octamethyltrisiloxane
2.Silane, dimethylbis(trimethylsiloxy)-
3.1,1,1,3,3,5,5,5-Octamethyltrisiloxane
4.[(CH3)3SiO]2Si(CH3)2
5.Dimethylbis(trimethylsiloxy)silane
6.CO9816
7.O9816
Figura 4.14. Espectro de masas, fórmula estructural e informaciones dadas por el
software sobre el siloxano octametiltrisiloxano.
4.5 Estudio r&R – Repetibilidad y Reproducibilidad
El estudio r&R se le conoce como la variabilidad entre las condiciones (ISO 5725-2, 1994).
(mainlib) Trisiloxane, octamethyl-
0 20 40 60 80 100 120 140 160 180 200 220 2400
50
100
2 15 29
45
51
5966
73
80 87 95
103
115133
147
159 175189 205
221
Si
OSiO
Si
46
4.5.1 Repetibilidad
Un método es repetitivo cuando hay proximidad de concordancia entre
los resultados de mediciones sucesivas mensuradas en las mismas condiciones
de medición. Las condiciones de repetibilidad incluyen: el mismo procedimiento de
medición, el mismo observador, el mismo instrumento de medición utilizado bajo
las mismas condiciones, el mismo lugar y repetición en un periodo corto de
tiempo. Se expresa cuantitativamente la repetibilidad en términos de la dispersión
característica de los resultados, calculándose la desviación estándar muestral y
el coeficiente de variación estándar (ISO 5725-2, 1994):
σ= Ecuación II.Desviación estándar muestral.
Ecuación III. Coeficiente de variación.
Un volumen de 500 µL de la solución madre de calibrado fue diluido en
metanol, obteniéndose una solución intermedia de 1 g L-1 en matraz de 5 mL. A partir de la solución intermedia, se prepararon en hexano, diluciones de 2 mg L-1 y de 10 mg L-1. Se hicieron 5 inyecciones consecutivas con cada una de las soluciones diluidas y, a partir de las cuentas de área obtenidas al final de cada análisis cromatográfico, se calcularon las desviaciones estándares y coeficientes de variación para comprobar la repetibilidad del método. 4.5.2 Reproducibilidad
Se conoce por reproducibilidad, la proximidad de concordancia entre los
resultados de mediciones sucesivas mensuradas bajo condiciones de medición que
cambian donde:
-Una declaración válida de reproducibilidad requiere que se especifique la
condición que cambia.
-Las condiciones que cambian pueden incluir: principio de medición, método de
medición, observador, instrumento de medición, patrón de referencia, lugar,
condiciones de uso y tiempo.
-La reproducibilidad puede ser expresada cuantitativamente en términos de la
dispersión característica de los resultados.
-Se entiende que los resultados usualmente son resultados corregidos (ISO
5725-2, 1994).
47
En la tabla 4.1 del apartado 4.1, están los valores de concentraciones de
cada siloxano comercial en las soluciones madres preparadas en días distintos
e instrumentos de medición de volúmen diferentes. No se disponía del
dodecametilciclohexasiloxano para la preparación de la solución madre de
verificación, pero aún así, se pudo hacer una comparación de las
concentraciones obtenidas por el análisis cuantitativo GC/MS de las dos
soluciones madres.
Se prepararon soluciones diluidas a partir de la solución madre de
verificación, con el objetivo de inyectar 5 veces sucesivamente las mismas
concentraciones de 2 mg L-1 y de 10 mg L-1. Como fueron análisis
cromatográficos realizados en días diferentes, se pudo calcular los coeficientes
de variación para cada siloxano de las diluciones de verificación y las
diluciones de calibrado para verificar la reproducibilidad del método de
identificación de siloxanos.
4.6 Límite de Detección
En la construcción de la curva de calibrado descrita anteriormente en el
apartado 4.3, se hicieron primeramente 6 inyecciones sucesivas, de
concentraciones 0,5; 1; 2; 5; 10 y 20 mg L-1, pues no se conocía el límite de
detección del conjunto GC/MS para siloxanos.
Una solución de concentración 0,1 mg L-1 fue preparada en otro día para
comprobar la capacidad del detector en relación a esta baja concentración de
siloxanos volátiles. Se confirmó que las áreas de los picos cromatográficos
eran 3 veces el área del ruido de la línea base. Los valores de concentraciones
de siloxanos para la dilución de 0,1 mg L-1 fueron utilizados en la construcción
de las curvas de calibrado a fin de aumentar el coeficiente de correlación.
4.7 Estudio de la Extracción de Siloxanos con Solventes en Muestras de
Aguas Residuales
Una muestra de agua residual de Aguas de Valladolid fue utilizada para un
test en el GC/MS en la identificación y detección de siloxanos según el método
estudiado en este proyecto.
La solución madre de calibrado fue diluida 1000 veces con el agua residual
de Aguas de Valladolid, en matraz de 10 mL. Otro matraz de 10 mL fue
completado hasta enrase con esta misma agua residual, correspondiendo a la
solución blanco del test.
Fueron añadidos a los dos matraces, 500 µL de hexano para verificar el
comportamiento de la solución con siloxanos y del agua residual sin siloxanos.
El hexano extrae los siloxanos del agua residual y para eso, los matraces
fueron agitados manualmente durante 1 minuto y dejados en reposo. En este
procedimiento de extracción líquido-líquido (LLE), el solvente orgánico hexano
48
forma una fase orgánica en la parte superior del matraz y el agua residual
corresponde a la fase líquida.
La extracción líquido-líquido es una de las técnicas más antiguas para
pre-tratamientos en cromatografía, debido a su simplicidad y bajo coste
(Cortada, C. et al., 2009).
En este test con muestra de agua residual, en la extracción se formó una
emulsión en la fase orgánica. Para la inyección en el cromatógrafo gaseoso es
necesario coger la fase orgánica formada por el hexano en la parte superior del
matraz, pero esta fase no puede contener burbujas de aire, visto que no se
puede entrar aire en la columna cromatográfica. La formación de emulsión
impide extraer el hexano sin que la pipeta Pasteur coja la fase líquida (agua
residual) o burbujas de aire (Figura 4.15).
Figura 4.15. Formación de emulsión en la fase orgánica de la extracción líquido-
líquido con hexano.
Se hizo la inyección en el cromatógrafo de las dos soluciones, agua
residual con hexano libre de siloxanos y otra análoga con siloxanos, pero éstos
no fueron detectados.
La extracción líquido-líquido fue utilizada como pre-tratamiento en el
método de análisis de siloxanos con GC/MS, esta vez con agua Milli-Q
sustituyendo el agua residual.
Con la solución madre de calibrado diluida 1000 veces en agua Milli-Q,
la extracción con 500 µL de hexano, seguida de agitacón y reposo, resultó en
buena separación de fases. Se obtuvo un cromatograma con los 9 picos
correspondientes a los siloxanos, comprobando ser la formación de emulsión lo
que dificultaba la extracción de los siloxanos por el hexano, siendo estos
compuestos no identificados en GC/MS.
49
La alternativa fue realizar un test en otras muestras de agua residual de
la empresa hasta que se pudiera obtener mejor separación entre la fase
orgánica (hexano) y la fase líquida (agua residual).
Utilizándose la técnica LLE descrita anteriormente, una de las muestras
de agua testadas resultaron en formación mínima de emulsión (Figura 4.16).
Con la ayuda de una pipeta Pasteur, un pequeño volumen de la fase orgánica
de la solución de siloxanos diluida con agua residual y de la solución agua
residual (blanco) fue añadido a 2 viales de cromatografía. Los cromatogramas
tenían mala separación entre los picos y era difícil identificar cada siloxano,
debido a presencia, aún mínima, de emulsión en la fase orgánica.
Figura 4.16. Formación mínima de emulsión en la extracción líquido-líquido con
hexano de una muestra de agua residual.
Buscando otro disolvente que produjera una separación de fases donde
la fase orgánica fuera totalmente homogénea, se experimentó una
microextracción líquido-líquido dispersiva (DLLME).
De acuerdo con Azcárate, F. et al. (2000), la microextracción líquido-
líquido dispersiva DLLME consiste en una buena alternativa para la extracción
de compuestos en matriz acuosa. Esta extracción, comparada con el
tratamiento tradicional, representa un ahorro en solvente (pocos µL); ahorro en
50
tiempo de procesamiento (de unas 4 horas a pocos minutos), y disminución de
los desechos producidos.
Nuevamente se prepararon dos matraces, uno con 10 mL de agua
residual (muestra 1589342 que produjo mínima emulsión con hexano) y otro
con 10 mL de solución de siloxanos diluída a 1:1000 por la misma agua
residual. El contenido de cada matraz fue transferido a dos tubos de ensayo de
fondo cónico y se añadieron 50 µL del nuevo disolvente. La agitación procedió
en baño de ultrasonidos Selecta durante 2 minutos.
Con respecto al uso del ultrasonido para la extracción de los siloxanos
por el disolvente usado para dispersión y extracción, la sonicación intensa de
líquidos genera ondas sonoras que se propagan en el medio líquido resultando
en ciclos alternos de alta presión y baja presión. Durante el ciclo de baja
presión, se crean pequeñas burbujas de vacío de alta intensidad en el líquido
que se colapsan violentamente durante el ciclo de alta presión, la cavitación.
Durante la implosión se producen localmente flujos de líquido de alta presión y
velocidad (Hielscher-Ultrasound Technology, 2011).
Posteriormente se hizo una centrifugación de los tubos en centrífuga
Beckman modelo GS-6R durante 5 minutos a 320 rpm. En este tipo de
extracción, el disolvente usado era más denso que el agua lo que permitió
coger la fase orgánica con siloxanos más fácilmente (Figura 4.17). De esta vez,
se optó hacer la inyección manual de las muestras de agua residual.
Figura 4.17. Soluciones preparadas con agua residual después de microextracción
líquido-líquido dispersiva.
51
4.8 Análisis de Agua Residual
El agua residual utilizado para la microextracción líquido-líquido
dispersiva de siloxanos, fue analizada directamente por la técnica GC/MS para
verificación de la presencia o no de siloxanos.
4.9 Repetibilidad para Análisis de Siloxanos en una Muestra de Agua Residual
La muestra de agua residual analizada por cromatografía gaseosa,
después de haber sido sometida a una microextracción líquido-líquido
dispersiva de siloxanos, fue utilizada para la preparación de una solución con
1 mg L-1 de estos compuestos.
Esta solución de siloxanos en agua residual fue transferida a un tubo de
ensayo de fondo cónico y se añadieron 50 µL del disolvente dispersante. La
agitación procedió en baño de ultrasonido por un período de 2 minutos. Se
centrifugó el tubo durante 5 minutos a 320 rpm. Se analizó la fase orgánica
retirada de la parte superior del tubo y se hicieron 4 inyecciones manuales en el
cromatógrafo de gases.
Se verificó la desviación estándar muestral y el coeficiente de variación
para cada siloxano identificado.
52
5. RESULTADOS Y DISCUSIÓN
5.1 Rectas de Calibrado
Como se describió en el apartado 4.3, se construyeron curvas de
calibrado para cada siloxano en 7 concentraciones: 0,1; 0,5; 1; 2; 5; 10 y
20 mg L-1. Las rectas de calibrado de cada siloxano se presentan a
continuación, junto con las ecuaciones correspondientes a cada una y su
coeficiente de correlación. En algunas curvas se quitaron puntos para la
obtención de un coeficiente de correlación que reflejase mayor precisión.
Figura 5.1. Curva de calibrado del trimetilsilanol.
Calibration Curve ReportFile: c:\varianws\data\2012\siloxanos\pruebascal0.1mgl\siloxanos2-8-12.mth
Detector: 2000 Mass Spec, Address: 40
TMSCurve Fit: Linear, Origin: Ignore, Weight: None Resp. Fact. RSD: 18,05%
Coeff. Det.(r2): 0,987776y = +412,219177x +357,777405
Peak
Size
Amount (ppm)
5 10 15 20
0.0
2.5
5.0
7.5
k
Replicates 1 2 1 1 1 1
53
Figura 5.2. Curva de calibrado del hexametildisiloxano.
Calibration Curve ReportFile: c:\varianws\data\2012\siloxanos\pruebascal0.1mgl\siloxanos2-8-12.mth
Detector: 2000 Mass Spec, Address: 40
L2Curve Fit: Linear, Origin: Ignore, Weight: None Resp. Fact. RSD: 37,41%
Coeff. Det.(r2): 0,996488y = +6861,872559x +846,995667
Peak
Size
Amount
5 10 15 20
0
25
50
75
100
125
150
k
Replicates 1 1 1 1 1 1 1
54
Figura 5.3. Curva de calibrado del hexametilciclotrisiloxano.
Calibration Curve ReportFile: c:\varianws\data\2012\siloxanos\pruebascal0.1mgl\siloxanos2-8-12.mth
Detector: 2000 Mass Spec, Address: 40
D3Curve Fit: Linear, Origin: Ignore, Weight: None Resp. Fact. RSD: 69,00%
Coeff. Det.(r2): 0,992049y = +552,217102x -156,911102
Peak
Size
Amount
5 10 15 20 25
0.0
2.5
5.0
7.5
10.0
12.5
k
Replicates 1 1 1 1 1 1 1
55
Figura 5.4. Curva de calibrado del octametiltrisiloxano.
Calibration Curve ReportFile: c:\varianws\data\2012\siloxanos\pruebascal0.1mgl\siloxanos2-8-12.mth
Detector: 2000 Mass Spec, Address: 40
L3Curve Fit: Linear, Origin: Ignore, Weight: None Resp. Fact. RSD: 47,43%
Coeff. Det.(r2): 0,995504y = +5431,739746x -1450,345093
Peak
Size
Amount
5 10 15 20 25
0
25
50
75
100
125
k
Replicates 1 1 1 1 1 1 1
56
Figura 5.5. Curva de calibrado del octametilciclotetrasiloxano.
Calibration Curve ReportFile: c:\varianws\data\2012\siloxanos\pruebascal0.1mgl\siloxanos2-8-12.mth
Detector: 2000 Mass Spec, Address: 40
D4Curve Fit: Linear, Origin: Ignore, Weight: None Resp. Fact. RSD: 49,35%
Coeff. Det.(r2): 0,996397y = +5348,076660x +5742,875488
Peak
Size
Amount
5 10 15 20 25
0
25
50
75
100
125
150
k
Replicates 1 1 1 1 1 1
57
Figura 5.6. Curva de calibrado del decametiltetrasiloxano.
Calibration Curve ReportFile: c:\varianws\data\2012\siloxanos\pruebascal0.1mgl\siloxanos2-8-12.mth
Detector: 2000 Mass Spec, Address: 40
L4Curve Fit: Linear, Origin: Ignore, Weight: None Resp. Fact. RSD: 41,59%
Coeff. Det.(r2): 0,995264y = +4248,095703x -3212,043701
Peak
Size
Amount
5 10 15 20 25
0
25
50
75
100
k
Replicates 1 1 1 1 1 1 1
58
Figura 5.7. Curva de calibrado del decametilciclopentasiloxano.
Calibration Curve ReportFile: c:\varianws\data\2012\siloxanos\pruebascal0.1mgl\siloxanos2-8-12.mth
Detector: 2000 Mass Spec, Address: 40
D5Curve Fit: Quadratic, Origin: Ignore, Weight: None Resp. Fact. RSD: 46,27%
Coeff. Det.(r2): 0,998502y = -1,734068x2 +6233,807129x +2374,386230
Peak
Size
Amount
5 10 15 20 25 30
0
50
100
150
k
Replicates 1 1 1 1 1 1 1
59
Figura 5.8. Curva de calibrado del dodecametilpentasiloxano.
Calibration Curve ReportFile: c:\varianws\data\2012\siloxanos\pruebascal0.1mgl\siloxanos2-8-12.mth
Detector: 2000 Mass Spec, Address: 40
L5Curve Fit: Linear, Origin: Ignore, Weight: None Resp. Fact. RSD: 52,26%
Coeff. Det.(r2): 0,988911y = +4586,031250x +3434,374268
Peak
Size
Amount
5 10 15 20 25
0
25
50
75
100
k
Replicates 1 1 1 1 1 1 1
60
Figura 5.9. Curva de calibrado del dodecametilciclohexasiloxano.
Calibration Curve ReportFile: c:\varianws\data\2012\siloxanos\pruebascal0.1mgl\siloxanos2-8-12.mth
Detector: 2000 Mass Spec, Address: 40
D6Curve Fit: Quadratic, Origin: Ignore, Weight: None Resp. Fact. RSD: 55,06%
Coeff. Det.(r2): 0,986734y = +0,109698x2 +22,361710x +131,483322
Peak
Size
Amount
5 10 15 20 25
0
100
200
300
400
500
600
700
800
Replicates 1 1 1 1 1
61
Con excepción de las curvas de los siloxanos L5 y D6 y del
trimetilsilanol, los coeficientes de correlación fueron de 0,99 lo que indica buena
precisión en la separación por la columna cromatográfica e identificación por el
espectrómetro de masas.
En las tablas siguientes están los valores de área de cada pico y su
respectiva concentración, correspondientes a cada siloxano. La ecuación de la
recta de calibrado expresa por y = ax + b, resulta en la concentración x
equivalente al área y. Aunque en las gráficas se encuentran las alturas de los
picos en la ordenada, las ecuaciones de las rectas están construidas con las
áreas de los picos cromatográficos. Los datos expresos en la Tablas 5.1-5.8
son generados por el Software.
Tabla 5.1. Área y concentración del TMS en cada solución madre de calibrado.
Concentración solución madre
(mg L-1)
Área del pico
cromatográfico
Concentración del TMS
(mg L-1)
0,5 755 0,634
1 611 0,557
2 1295 0,921
5 3187 1,926
10 6138 3,494
20 9438 5,246
Tabla 5.2. Área y concentración del L2 en cada solución madre de calibrado.
Concentración solución madre
(mg L-1)
Área del pico cromatográfico
Concentración del L2 (mg L-1)
0,5 6510 0,628
1 7432 0,747
2 16202 1,877
5 43465 5,391
10 71186 8,963
20 155324 19,806
62
Tabla 5.3. Área y concentración del D3 en cada solución madre de calibrado.
Concentración solución madre
(mg L-1)
Área del pico cromatográfico
Concentración del D3 (mg L-1)
0,5 593 0,984
1 546 0,931
2 1018 1,453
5 3000 3,648
10 5872 6,828
20 13947 15,769
Tabla 5.4. Área y concentración del L3 en cada solución madre de calibrado.
Concentración solución madre
(mg L-1)
Área del pico cromatográfico
Concentración del L3 (mg L-1)
0,5 6078 1,181
1 5057 1,043
2 11151 1,865
5 32364 4,725
10 61401 8,641
20 139789 19,210
Tabla 5.5. Área y concentración del D4 en cada solución madre de calibrado.
Concentración solución madre
(mg L-1)
Área del pico cromatográfico
Concentración del D4 (mg L-1)
0,5 10724 0,829
1 8887 0,564
2 18626 1,969
5 48039 6,211
10 79443 10,740
20 150669 21,013
63
Tabla 5.6. Área y concentración del L4 en cada solución madre de calibrado.
Concentración solución madre
(mg L-1)
Área del pico cromatográfico
Concentración del L4 (mg L-1)
0,5 2482 1,437
1 2110 1,368
2 4780 1,862
5 10393 2,901
10 47859 9,835
20 106178 20,629
Tabla 5.7. Área y concentración del D5 en cada solución madre de calibrado.
Concentración solución madre
(mg L-1)
Área del pico cromatográfico
Concentración del D5 (mg L-1)
0,5 12138 1,506
1 9840 1,250
2 19809 2,363
5 52219 6,020
10 95827 11,041
20 191231 22,464
Tabla 5.8. Área y concentración del L5 en cada solución madre de calibrado.
Concentración solución madre
(mg L-1)
Área del pico cromatográfico
Concentración del L5 (mg L-1)
0,5 8041 1,009
1 5686 0,600
2 12548 1,792
5 37059 6,050
10 66355 11,140
20 112847 19,217
64
Para comprobar la validez de los datos, considerando, por ejemplo, el
siloxano L3, se hace el cálculo utilizando su ecuación de calibrado:
Y = 5431,739746*x – 1450,345093
Con un área igual a 5057 (solución madre 1 mg L-1) (Tabla 5.4.),
sustituyendo en la ecuación, x = (5057 + 1450,345093) / 5431,739746 =
1,2 mg L-1.
El valor de concentración obtenido con la ecuación resultó muy cercano
al generado por el Software del equipo GC-MS.
5.2 Comparación Valor Calculado y Valor Experimental
El análisis cromatográfico resultante de las diluciones a 0,5; 1; 2; 5; 10 y
20 mg L-1 preparadas con la solución madre de verificación, generó valores
reales de concentraciones de los siloxanos (valores experimentales). La
cromatografía permite cuantificar compuestos, aunque estén a bajas
concentraciones.
Partiendo de las masas pesadas de cada siloxano en la preparación de
la solución madre de verificación, se calcularon las concentraciones,
comparándolas con las concentraciones experimentales.
En la tabla 5.9 se incluyen los valores de error porcentual relativo para la
concentración del siloxano L3 en cada dilución.
Tabla 5.9. Error porcentual relativo para el siloxano L3 en soluciones a diferentes
diluciones a partir de una solución madre de verificación.
L3
Valor
calculado Valor
experimental Error Porcentual
Relativo 0,5 mg L-1 0,495 1,181 58,08636749 1 mg L-1 0,991 1,043 4,985618408 2 mg L-1 1,982 1,969 0,660233621 5 mg L-1 4,955 4,725 4,867724868 10 mg L-1 9,91 8,641 14,68580025 20 mg L-1 19,82 19,21 3,175429464
El error calculado para la concentración de 0,5 mg.L-1 fue muy alto,
pudiendo haber sido provocado por una mala cuantificación del pico
cromatográfico para esta concentración. Se esperaba un valor más bajo del
siloxano L3 en esta dilución, pues el orden de concentraciones es creciente a
partir de 0,5 mg.L-1. También puede ser que el L3 haya sido acumulado en la
columna de otros análisis y haya salido con un área ampliada en el
cromatograma.
65
5.3 Estudio r&R – Repetibilidad y Reproducibilidad
La validación del método para identificación de siloxanos consistió de un estudio experimental para examinar la significancia de algunas fuentes de variación que inciden en la repetibilidad y reproducibilidad de la técnica analítica GC/MS. 5.3.1 Repetibilidad
Las diluciones de 2 y 10 mg L-1 (partiéndose de la solución madre de calibrado) fueron inyectadas 5 veces seguidas para verificar la repetibilidad del método de identificación de siloxanos. Los valores de desviación estándar muestral y el coeficiente de variación calculados a partir de las cuentas de área para las dos concentraciones están expuestos en la tablas 5.10 y 5.11. Tabla 5.10. Estadística para solución 2 mg L-1 de siloxanos.
Área 1ª
inyección
Área 2ª
inyección
Área 3ª
inyección
Área 4ª
inyección
Área 5ª
inyección
Desviación
estándar
muestral
Coeficiente
de
variación
TMS 1753 1624 1883 1618 1914 139,231 7,918
L2 7040 6761 7086 7103 7617 309,728 4,349
D3 2426 2404 2611 2413 2600 105,070 4,218
L3 5605 5688 5841 5863 6006 157,045 2,707
D4 9841 9699 9941 10086 10175 189,784 1,908
L4 3752 3656 3855 3579 3988 161,609 4,291
D5 7765 7873 7865 8765 8434 437,207 5,371
L5 6316 6533 5735 6043 6384 315,852 5,093
D6 4257 4001 4563 4529 4318 227,782 5,256
66
Tabla 5.11. Estadística para solución 10 mg L-1 de siloxanos. Área 1ª
inyección
Área 2ª
inyección
Área 3ª
inyección
Área 4ª
inyección
Área 5ª
inyección
Desviación
estándar
muestral
Coeficiente
de
variación
TMS 9135 9034 8817 9356 9012 196,651 2,168
L2 41780 41403 43008 42337 41889 614,814 1,461
D3 13787 13802 14257 14102 14230 227,810 1,623
L3 34160 33399 35034 34202 34104 580,072 1,697
D4 45732 45231 46534 45440 47418 901,035 1,956
L4 32751 32784 32542 31567 32887 539,789 1,661
D5 39151 40729 41499 39099 40254 1033,005 2,573
L5 32166 31199 32362 32089 31396 512,042 1,608
D6 21167 21688 22845 21452 21748 637,782 2,928
Según USEPA-Método Estándar para Identificar Compuestos Volátiles
por GC/MS (1996), el coeficiente de variación no debe exceder un 15%.
En este estudio de repetibilidad, se obtuvo valores debajo de 8%, lo que
indica que el método es repetitivo.
5.3.2 Reproducibilidad
Se dispone de valores de concentraciones de 2 y 10 mg L-1 a partir de la
solución de verificación y la solución de calibrado preparadas en días distintos,
lo que permite estudiar la reproducibilidad.
En las tablas 5.12 y 5.13 se encuentran las cuentas de área, desviación
estándar y coeficientes de variación para las soluciones 2 y 10 mg L-1 de
verificación, preparadas e inyectadas en día distinto a las soluciones de
calibrado de las tablas 5.10 y 5.11 del apartado anterior.
67
Tabla 5.12. Estadística para solución de verificación 2 mg.L-1 de siloxanos. Área 1ª
inyección
Área 2ª
inyección
Área 3ª
inyección
Área 4ª
inyección
Área 5ª
inyección
Desviación
estándar
muestral
Coeficiente
de
variación
TMS 422 425 391 388 429 19,812 4,820
L2 5364 5653 5490 5471 5448 104,157 1,899
D3 350 405 374 359 421 30,277 7,930
L3 3888 4080 3946 3747 3966 121,654 3,099
D4 5921 6080 5640 5585 5805 202,915 3,495
L4 1540 1646 1558 1585 1605 41,409 2,610
D5 2552 3134 2992 3086 3167 251,524 8,423
L5 869 918 925 936 1017 53,502 5,734
Tabla 5.13. Estadística para solución de verificación 10 mg L-1 de siloxanos.
Área 1ª
inyección
Área 2ª
inyección
Área 3ª
inyección
Área 4ª
inyección
Área 5ª
inyección
Desviación
estándar
muestral
Coeficiente
de
variación
TMS 2700 2890 2590 2922 2926 152,318 5,429
L2 35448 40209 41323 43852 44105 3511,725 8,568
D3 3080 3226 3349 3647 3605 243,198 7,192
L3 25939 27928 28911 30806 31126 2138,429 7,389
D4 38270 41708 42293 45358 45410 2963,999 6,956
L4 10539 11405 11694 12386 12664 840,803 7,163
D5 22340 23507 24133 20094 24602 1800,457 7,850
L5 20073 25845 25610 28381 26829 2753,872 10,864
Las dos diluciones de verificación proporcionaron coeficientes de
variación por debajo del 15% permitido para técnica GC/MS de volátiles
(USEPA, 1996). De esta manera se concluye que el Método de Análisis de
siloxanos también es reproducible.
5.4 Análisis de Agua Residual
La muestra de agua residual extraída por solvente dispersivo fue
analizada por cromatografía gaseosa en cuanto a presencia de siloxanos.
68
Según los resultados ilustrados en la Figura 5.10, no se detectó ningún
siloxano en el agua residual.
Figura 5.10. Análisis de una muestra de agua residual por GC/MS.
5.5 Análisis Cromatográfico de Muestra de Agua Residual Pre-tratada con LLE
y DLLME
En los estudios para pre-tratamiento de las muestras de agua residual
utilizando extracción líquido-líquido con hexano se obtuvo el siguiente
cromatograma para la muestra que formó mínima emulsión en la fase orgánica:
69
Figura 5.11. Cromatograma agua residual enriquecida con solución 10 mg L-1 de
siloxanos.
La presencia de señal ruido en el cromatograma, además de no haberse
obtenido los 9 picos correspondientes a los siloxanos añadidos al agua
residual, conllevó la búsqueda de otro pre-tratamiento, la microextracción
dispersiva líquido-líquido (DLLME).
5.6 Repetibilidad para Análisis Cromatográfico de Agua Residual
Se decidió hacer una microextracción dispersiva líquido-líquido con la
solución de 1 mg L-1 de siloxanos en agua residual y en seguida se realizaron 4
inyecciones de la fase orgánica en el GC para verificar la repetibilidad del
método.
Los coeficientes de variación se encuentran en la tabla 5.14.
Chromatogram Plot
File: ...rianws\data\2012\siloxanos\matrices\rep7-8-12\blan agua 1589342.sms
Sample: Blan agua 1589342 Operator:
Scan Range: 1 - 2067 Time Range: 0.00 - 32.57 min. Date: 8/8/2012 1:46 PM
5 10 15 20 25 30minutes
0
1
2
3
4
5
6
7
8
kCounts RIC Merged blan agua 1589342.sms 2000 CENTROID RAW
70
Tabla 5.14. Estadística para repetibilidad de análisis de siloxanos en agua residual.
Área 1ª
inyección
Área 2ª
inyección
Área 3ª
inyección
Área 4ª
inyección
Desviación
estándar
muestral
Coeficiente
de
variación
TMS 2836 3126 2617 2871 209 7,3
L2 691472 607906 581317 720364 66232 10,2
D3 29555 26948 22301 27205 3037 11,5
L3 530094 457064 439587 553661 55325 11,2
D4 1060000 852829 853787 917209 97468 10,6
L4 372434 285499 314636 383267 46667 13,8
D5 891728 671981 787114 555157 145264 20,0
L5 883005 608106 765558 698665 115762 15,7
D6 308835 203736 285128 273878 45186 16,9
Según USEPA-Método Estándar para Identificar Compuestos Volátiles
por GC/MS (1996), el coeficiente de variación no debe exceder un 15%. Para
los siloxanos D5 y D6, se obtuvo un coeficiente de variación superior al
admisible. Se puede corregir estos coeficientes haciéndose otro análisis con
más inyecciones, lo que permitiría acercar los valores de cuentas de área,
resultando menores coeficientes de variación.
El método resulta repetitivo para los demás siloxanos: TMS, L2, D3, L3,
D4, L4 y L5.
71
6. CONCLUSIONES
El Método desarrollado para Análisis de Siloxanos en aguas residuales
resultó repetitivo y reproducible, comprobación obtenida por los valores
de coeficientes de variación menores del 15 % en el estudio r&R con
una solución patrón de siloxanos.
La precisión fue buena para la mayoría de los análisis de siloxanos, con
valores de coeficientes de correlación de 0,99 en las curvas de
calibrado.
En la comparación entre las concentraciones calculadas a partir de la
masa pesada de cada siloxano en la solución de verificación y el valor
real encontrado de cada siloxano en los análisis cromatográficos, los
errores porcentuales fueron aceptables en su mayoría.
Con los buenos resultados obtenidos se puede decir que el Programa de
Temperatura elegido para el estudio, la columna cromatográfica DB-624 y los
solventes orgánicos utilizados para la preparación de las muestras se
encuadran perfectamente para el análisis de siloxanos por cromatografía
gaseosa acoplada a espectrometría de masas.
La técnica GC/MS tiene la selectividad necesaria para detectar y cuantificar siloxanos en agua. También los resultados para los límites de detección comprueban que a bajas concentraciones, como 0,1 mg L-1, aún es posible la identificación y cuantificación dentro de un rango de concentraciones que genera buenas curvas de calibrado.
El análisis de agua residual es posible utilizando este método cromatográfico, repetitivo para la gran mayoría de los siloxanos.
7. ACCIONES FUTURAS
El Método de Análisis de Siloxanos puede ser mejorado en relación al
análisis de agua residual, en lo que refiere principalmente a los siloxanos D5 y
D6, cuyos coeficientes de variación impidieron la repetibilidad para su análisis.
Los siloxanos son derivados de algunas industrias, como las de
cosméticos, y sus concentraciones variarán dependiendo del tipo de agua
residual, pudiendo no ser detectados en algunos casos. Deberían realizarse
estudios en distintas EDAR´s para tratar de relacionar la presencia de siloxanos
con el origen del agua residual.
Se hace importante desarrollar un método para la eliminación de los
siloxanos en el agua, antes que se depositen en los lodos y sigan para la
quema del gas producido por la digestión anaerobia de estos lodos.
72
BIBLIOGRAFIA
Accettola, F.; Guebitz, G. M.; Shoeftner, R. Siloxane removal from biogas by biofiltration: biodegration studies. Clean Technology Environment Policy, Springer. 2008. Air Toxics, presented at SWANA 2003 disponible en URL: http://airtoxics.com/literature/papers/Siloxanes_SWANA_03.pdf APHA. “Métodos normalizados para el análisis de aguas potables y residuales”. Editorial Díaz de Santos, S.A. Edición en español (1992). Appels, L.; Baeyens, J. & Dewil, R. Siloxane removal from biosolids by peroxidation. Energy conversion and management 49, pp. 2859-2864, 2008. ASTM E 691. Standard practice for conducting an interlaboratory study to determine the precision of a test method. American Society for Testing and Materials. West Con-shohocken, PA, USA. 1999. Azcárate, F.; Castillo, S.; Benvenuto, R.; Lagier, V.; Giorda, J.; Piotto, F.; Boschetti, C. Uso de microextracción líquido-líquido dispersiva como alternativa rápida y económica para la determinación de pesticidas organoclorados en matrices acuosas. Laboratorio Litoral S.A. Facultad de Ciencias Bioquímicas y Farmacéuticas, Universidad Nacional de Rosario. Rosario. Argentina. 2000. Biron, M. Silicones ou siloxanes applications. Techniques de l’Ingénieur, Doc.N2884-1, 2007. Cabirta Branco, M. S. Avaliação do impacto da presença de silloxanos em sistemas de aproveitamento de biogás. Dissertação de mestrado. Lisboa, Portugal. 2010. Chao, S. Direct measurement and speciation of volatile organosilicons in landfill gas by gas chromatography with atomic emission detection, Proceedings of SWANA, 25ème Annual landfill gas symposium, Monterey, California, 2002. Chary, N. S.; Fernandez-Alba, A. R. Determination of volatile organic compounds in drinking and environmental waters. TrAC- Trends in Analytical Chemistry, vol. 32, pg. 60-75. 2012. Companioni-Damas, E.Y.; Santos, F.J.; Galceran, M.T. Analysis of linear and
cyclic methylsiloxanes in water by headspace-solid phase microextraction
and gas chromatography-mass spectrometry. Elsevier, Talanta. Volume 89.
Pages 63-69. Analytical Chemistry Department, University of Barcelona.
Barcelona, Spain, 2011.
Cortada, C.; Vidal L.; Tejada, S.; Romo, A.; Canals, A. Determination of
organochlorine pesticides in complex matrices by single-drop
73
microextraction coupled to gas chromatography-mass spectrometry.
Elsevier. Labaqua S.A. & Departamento de Química Analítica, Nutrición y
Bromatología, Universidad de Alicante. 2009.
Dewil, R.; Appels, L.; Baeyens, J. Energy use of biogas hampered by presence of siloxanes. Energy Conversion & Management, 47, 1711 – 1722, 2006. Dewil, R; Appels, L.; Baeyens, J.; Buczynska, A. & Van L. The analysis of volatile siloxanes in waste activated sludge. Elsevier, Talanta 74, 2007. Fendinger, N. J.; Mcavoy, D. C.; Eckhoff, W. S.; Price, B. B. Environmental occurrence of polydimethylsiloxane. Environmental Science and Technology, 31, 1555 – 1563. 1997. Graiver, D.; Farminer, K. W.; Narayan, R. A review of the fate and effects of silicones in the environment. Journal of Polymers and the Environment, II, 129 – 136, 2003. Granda, F.; Valencia, S.; Marín, J. M.; Restrepo, G. Revista Colombiana de Química. Volumen 40. 2011. Griessbach, E. F. C.; Lehmann, R. G. Degradation of polydimethylsiloxane fluids in the environment – A review. Pergamon, 38,1461 – 1468. 1999. Gomis Yagües, V. Tema 3 – Cromatografía de Gases – Equipos Disponibles en el Departamento de Ingeniería Química y en los Servicios Técnicos de Investigación de la Universidad de Alicante. 2008. Hagmann, M.; Hesse, E.; Hentschel, P.; Bauer, T. Purification of biogas – removal of volatile silicones. In proceedings of Sardinia 2001, 8th International waste management and landfill symposium, Cagliari, Italy, 1 – 5 October 2001. Hayes, H. C.; Saeed, S.; Graening, G. J.; Kao, S. A summary of available analytical methods for the determination of siloxanes in biogas. Air Toxics, presented at SWANA 2003 disponible en URL: http://airtoxics.com/literature/papers/Siloxanes_SWANA_03.pdf Hielscher-Ultrasound Technology. Biodiesel de algas mediante ultrasonidos. Estudio de Métodos. 2011. Huppmann, R.; Lohoff, H.W. & Schröder, H.F. Cyclic siloxanes in the biologicalwaste water treatment process—determination, quantification and possibilities of elimination, Fr J Anal Chem 354, 1996. ISO 5667-13:1997 – Calidad del agua. Muestreo. Parte 13: Guía para el muestreo de lodos procedentes de aguas residuales y de las instalaciones de tratamiento del agua.
74
ISO 5725-2. Accuracy (trueness and precision) of measurement methods and results. Part 2: Basic method for the determination of repeatability and reproducibility of a standard measurement method. First edition 1994. International Organization for Standardization. Geneve, Switzerland. IUPAC – International Union of Pure and Applied Chemistry. Gold Book, 2012. Disponible en: http://goldbook.iupac.org/S05671.html
Kierkegaard, A.†; Van Egmond,R.; McLachlan, M.†. Cyclic volatile
methylsiloxane bioaccumulation in flounder and ragworm in the Humber
Estuary. Environ. Sci. Technol., 45 (14), pp 5936–5942, 2011.
Lehmann, R. G.; Varaprath, S.; Annelin, R. B.; Arndt, J. L. Degradation of silicon polymer in a variety of soils. Environmental Toxicology and Chemistry, 14, 1299 – 1305. 1995. Lehmann, R. G.; Varaprath, S.; Frye, C. L. Fate of silicone degradation products (silanols) in soil. Environment Toxicology and Chemistry, 13, 1753 – 1759. 1994.
López López, L.; Calleja Sanz, J.; Janeiro Arocas, J. M.; Alonso Tajes, F., Bouzas, M. C. Orígenes de las Siliconas. El Peu, ISSN 0212-7709, Vol. 22, Nº. 1 (enero-marzo), págs. 32-35, 2002.
Marciniec, B.; Guliński, J.; Kopylova, L.; Maciejewski, H.; Grundwald-Wyspiańska, M. & Lewandowski, M. Catalysis of hydrosilylation: Part XXXI. Functionalization of poly(methylhydro)siloxanes via hydrosilylation of allyl derivatives. Appl. Organometal. Chem., 11: 843–849, 1997.
Marigorta, A. M. 1997. Análisis del Equilibrio Liquido-Vapor a 141,3 kPa de Mezclas Binarias que Contienen Metanol con n-Alcanos (C5, C6) y con Esteres Alquílicos. Tesis de Doctorado en Ciencias Químicas de la Escuela Superior de Ingenieros Industriales de la Universidad de Las Palmas de Gran Canaria.
Mason, J.; Derek; Oblon; Spivak; Mcclelland; Maier & Neustadt. P.C. Siloxane Removal Process. Duke Street, Alexandria, Virginia 22314 (US), 2006.
Mc Bean, E.; Mosher, F.; David, A. Energy from landfill gas utilization in Canada. Recovering energy from waste, 2002. Mcbean, E. A. Siloxanes in biogases from landfills and wastewater digesters. Canadian Journal of Civil Engineering, 35, 431 – 436. 2008. Mckim, J. M.; Wilga, P. C.; Breslin, W.J.; Plotzke, K. P.; Gallavan, R. H.; Meeks, R.G. Potential estrogenic and antiestrogenic activity of the cyclic siloxane octamethylcyclotetrasiloxane (D4) and the linear siloxane hexamethyldisiloxane (HMDS) in immature rats using the uterotrophic assay, Toxicological sciences 63 (1), pp. 37-46, 2001.
75
McNair, H. M. & Miller, J. M. Basic Gas Chromatography. Chemical Analysis. CanadaISBN :0-471-17260-X (alk. paper); ISBN 0-471-17261-8 (pbk.: alk. paper). CHEMICAL ANALYSIS (1998).
Mueller, J. A.; Toro, D. M. D.; Maiello, J. A. Fate of octamethylcyclosiloxane (OMCTS) in the atmosphere in sewage treatment plants as an estimation of aquatic exposure. Environmental Toxicology and Chemistry, 14, 1657 – 1666, 1995.
Niemann, M. Characterization of Si compounds in landfill gas. Proceedings from the Solid Waste Association of North America’s 20th Annual Landfill Gas Symposium, 89-114, 1997.
Narros, A.; Del Peso, M.I.; Mele, G.; Vinot, M.; Fernández, E.; Rodríguez, M. E.
Determination of siloxanes in landfill gas by adsorption on tenax tubes
and TD-GC-MS. Cisa Publisher, Italy. 2009.
OFICINA ESPAÑOLA DE PATENTES Y MARCAS. TRADUCCIÓN DE
PATENTE EUROPEA. Número de publicación: 2 245 811. Título: Mezclas de
siloxanos lineales volátiles. Fecha de publicación del folleto de la patente:
16.01.2006.
Ogawa, T. Simplified synthesis of carbohydrate-functional siloxanes via transacetalation. I. Glucose-functional siloxanes. J. Polym. Sci. A Polym. Chem., 41: 3336–3345, 2003.
Ohannessian, A.; Desjardin, V.; Chatain, V.; Germain, P. Volatile organic silicon compounds: the most undesirable contaminants in biogases. Water sciences and technology, 58 (9), pp. 1775-1781, 2008 Parker, W. J.; Shi, J.; Fendinger, N. J.; Monteith, H. D.; Chandra, G. Pilot plant study to assess the fate of two volatile methyl siloxane compounds during municipal wastewater treatment. Environment Toxicology and Chemistry, 18, 172 – 181. 1999. Poulleau J. Caractérisation des biogaz, Bibliographie. Mesures sur sites, Institute national de l’environnement industriel et des risques, INERIS, 2002. R. Huppmann; H.W¸Lohoff; H.F. Schröder; Fresenius J. Anal. Chem. 354, 66–71. 1996. Reina, J. Biogás para la automoción (BPA) o su inyección en la red de gas natural (BPR). InfoEnviro. (Julio/Agosto 2007). Reina, J. From the biogas to vehicle fuel. Study of CO2 absorption in a packed column. 10º Congreso Mediterráneo de Ingeniería Química. Barcelona- Spain. (2005). Relea, F.; Jiménez, E.; González, E.; Haberbauer, M.; Broto, F.; Comellas, L.; Ribas, C.; Gotor, G.; Roig, E.; Vallmitjana, N. Valorización energética de
76
biogás en depósitos controlados mediante microturbinas. Proyecto Microphilox. Febrero 2009. Ricaurte Ortega, D. Étude du Traitement des siloxanes par adsorption sur matériaux poreux: application au traitement des biogaz. Thèse de doctorat. Nantes, France. 2009. Saeed, S.; Kao, S. F.; Graening, G.J. Comparison of impinger and canister methods for the determination of siloxanes in air. Presented at the AWMA Symposium on Air Quality Measurement Methods and Technology San Francisco, CA. 2002. Sánchez-Brunete, C.; Miguel, E.; Albero, B.; Tadeo, J. L. Determination of cyclic and linear siloxanes in soil samples by ultrasonic-assisted extraction and gas chromatography–mass spectrometry. Journal of Chromatography A, 1217, 7024–7030, 2010. Schweigkofler, M. & Niessner, R. Determination of siloxanes and VOC in landfill gas and sewage gas by canister sampling and GC–MS/AES analysis. Environ Sci Technol, pp. 3680–3685, 1999. Schweigkofler, M. & Niessner, R. Removal siloxanes in biogases. Journal of Hazardous Materials. B83:183-196. 2001.
Sparham, C. ; Van Egmond, R.; O'Connor, S.a; Hastie, C.; Whelan, M.; Kanda,
R.; Franklin, O. Determination of decamethylcyclopentasiloxane in river
water and final effluent by headspace gas chromatography/mass
spectrometry. Journal of Chromatography A. Volume 1212, Issue 1-2, 28 ,
Pages 124-129, 2008.
Stevens, C. Environmental degradation pathways for the breakdown of polydimethylsiloxanes. Journal of Inorganic Biochemistry, 69, 203 – 207, 1998. Sudeep, C.; Popat; Deshusses, M. A. Biological removal of siloxanes from landfill and digester gases: opportunities and challenges. Environnemental Sciences Technology, 42, pp. 8510-8515, 2008. Tower, P. M.; Wetzel, J. V. Making power generation make sense by removing siloxanes from digester gas. Applied Filter Technology, Paper presented at CWEA Conference. 2006. Disponible en: http://www.appliedfiltertechnology.com/page4813.asp Tower, P. New technology for removal of siloxanes in digester gas results in lower maintenance costs and air quality benefits in power generation equipment. Applied filter technology, WEFTEC 78th Annual Technical exhibition and conference, 2003.
77
UNITED STATES ENVIROMENTAL PROTECTION AGENCY. USEPA. Air Quality: Revision to Definition of Volatile Organic Compounds - Exclusion of Volatile Methyl Siloxanes and Parachlorobenzotrifluoride. Washington, D.C., 1994. Disponible en: (http://www.epa.gov/ttn/oarpg/t1/fr_notices/expara.pdf). US Environmental Protection Agency. Method 8260B - Volatile Organic Compounds by Gas Chromatography/Mass Spectrometry (GC/MS), Revision 2, CD-ROM, 1996. UKEA, Guidance on gas treatment technologies for landfill gas engines. United Kingdom Environmental agency, Bristol UK, 2002. Varaprath, S.; Stutts, D. H.; Kozerski, G. E. A primer on the analytical aspects of silicones at trace levels – challenges and airfacts – A review. Silicon Chemistry, 3, 79 – 102. 2006. Watts, R.; Kong, S.; Haling, S;, Hearhart, L.; Frye, C.; Vigon, B. Fate and effects of polydimethylsiloxanes on pilot and bench-TOP activated sludge reactors and anaerobic/aerobic digesters. Permagon, 1995. Wheless, E., & Gary, D. Siloxanes in landfill and digester gas, proceedings of SWANA. 25ème Annual landfill gas symposium, Monterey, California, 2002. Wheless, E.; Pierce, J. Siloxanes in landfill and digestor gas update. SWANA 27th LFG Conference. 2004. Disponible en: http://www.scsengineers.com/Papers/Pierce_2004Siloxanes_Update_Pa per.pdf.
Zhang, Z.; Qi, H.; Ren, N.; Li, Y.; Gao, D.; Kannan. Survey of cyclic and linear
siloxanes in sediment from the Songhua River and in sewage sludge from
wastewater treatment plants, Northeastern China. Archives of
Environmental Contamination and Toxicology. Volume 60, Issue 2, Pages 204-
211, 2011.
78
PUBLICACIÓN
Este trabajo de finalización del Máster en Gestión Sostenible y
Tecnologías del Agua realizado en los Laboratorios de Cromatografía de la
empresa AQUALOGY Medio Ambiental, actualmente Labaqua S.A. (Alicante-
España), resultó en la publicación del artículo científico “Determination of cyclic
and linear siloxanes in wastewater samples by ultrasound-assisted dispersive
liquid–liquid microextraction followed by gas chromatography–mass
spectrometry” en la revista Talanta en el año de 2014
(http://dx.doi.org/10.1016/j.talanta.2013.11.042).