Teoría de las repulsiones entre los pares de electrones de...
Transcript of Teoría de las repulsiones entre los pares de electrones de...

1
Teoría de las repulsiones entrelos pares de electrones de lacapa de valencia
Dr. Enrique Ruiz TrejoFacultad de Química UNAM
Teoría de las repulsiones entre lospares de electrones de la capa devalencia
¿Cuál es la geometría de lasmoléculas?
¿para qué queremos conocerla?

2
Moléculas en una exhibición
Este barbitúrico fue la causa dela muerte de Judy Garland, JimiHendrix, Marilyn Monroe yHeath Ledger.
Secobarbital
Moléculas en una exhibición
Una molécula de metano estáencerrado en una caja de moléculasde agua.El metano es probablemente másdañino que el CO2 para la capa deozono. Se encuentran en los sueloscongelados cercanos a los polos.
Si este metano se puediesecosechar, representa una nuevafuente de energía.
Hidrato de metano

3
Moléculas en una exhibición Naltrexona. Este opiato no
adictivo reduce la euforíaasociada con el uso delalcohol y podría usarse paratratar alcoholismo y ladependencia de la heroína.
Moléculas en una exhibición
Epibatidina. Potente veneno en la piel de algunasranas . Funciona como analgésico y podría auxiliaren la dependencia de nicotina.APBT-594: analgésico derivado.

4
Moléculas en una exhibición
El limoneno tienen dosestereoisómeros que danolores distintos.
Moléculas en una exhibiciónAlgunos medicamentos actúanpor unión a una receptor en lasuperficie de la célula. Estapuede preferir a uno de losenantiómeros. Thalidomida.Comercializada en 1957 contrael insomio y mareos matutinoscon consecuenciasteratogénicas.
El enantiómero levógiro es unpotente teratógeno.
El dextrógiro actúa contra lalepra.
Thalidomida

5
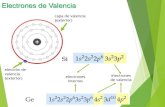
Teoría de repulsiones de electrones de la capade valencia
Cada par de electrones tiene una zona del espacio con alta probabilidad deencontrarlos juntos.Geometría más probable: repulsión mínima entre los pares de electrones dela capa de valencia
http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_4/kap4_1/vsepr1.html
Lineal Trigonal plana Tetraédro
Bipiramide trigonal Octaédro
Moléculas de elementos del segundo periodo:BeCl2 , BeF2 , BeBr2
Pares enlazantes: 2Pares no enlazantes: 0
Geometría: lineal
↑↑Be* [He]
psorbitales
Sólo del átomo central

6
BF3, BCl3, BBr3,
Pares enlazantes: 3Pares no enlazantes: 0
↑↑↑B* He]
psorbitales
Geometría: Trigonal plana
Sólo del átomo central
CH4, CF4, CCl4, CBr4, CI4
Pares enlazantes: 4Pares no enlazantes: 0
↑↑↑↑C* [He]
psorbitales
Geometría: tetraédrica

7
↑↑↑↑↓N [He]
psorbitales
NH3, NF3, NCl3
Pares enlazantes: 3Pares no enlazantes: 1
Los pares electrónicos sedistribuyen en un tetraédro,pero la molécula tieneGeometría: pirámide triangular
H2O, F2O, F2S
Pares enlazantes: 2Pares no enlazantes: 2
↑↑↑↓↑↓O [He]
psorbitales
Electrones: arreglo tetraédricoGeometría molecular: angular

8
Geometría de las moléculas
HFlinealAX31
H2OangularAX222
NH3piramidalAX313
CH4tetraédricaAX404
BCl3Trigonalplana
AX303
BeCl2linealAX202
EjemploGeometríaEstequio-metría
Noenlace
enlace
Tetraédrica4
Trigonal plana3
Lineal2
Distribución de los pareselectrónicos totales
Pares deelectrones totales(átomo central)
Dobles y triples enlaces
Dos o tres pares de enlace nocomparten la misma región pero síestán orientados en la misma dirección.En la TRPECV se comportan como sifueran un enlace simple

9
Geometría molecular
Cl OB•• ••
••
••••Cl SB•• ••
••
••••
O••
••Cl••
••••
N••
lineal lineal
angular Trigonal plana
Geometría molecular

10
Geometría y ángulos de enlace
Existen distorsionesen los ángulos deenlace
Átomos condistintaelectronegatividad
Pares de enlace ≠ pares no enlazantes
Enlaces múltiples ≠enlaces sencillos
Influencia de pares enlazantes ypares no enlazantes
Par libre ocupa mayor volumen que par enlazante
2 pares noenlazante
par enlazantePar no enlazante
2 paresenlazantes> >
Repulsión:

11
Influencia de átomos con distintaelectronegatividad
Par de enlace↑↓
↑↓Más cercaÁtomoelectrone-gativo
Átomo periféricoMás electronegativo
Átomo central máselectronegativo
Menos interaccióncon pares átomocentral
Mayor interacciónrepulsiva con pareselectrónicos
Influencia de los enlaces múltiples
Enlace múltiple haciaenlace sencillo
Enlaces sencillos>Repulsión:
1301.201.84NO2Cl
1361.181.47NO2F
ÁnguloO-N-O
Distancia(N-O) Å
Distancia(N-X) Å
Molecula
N
O
O
Cl••
••••
••
••
••
••
••
N
O
O
F••
••••
••
••
••
••
••

12
Moléculas con 5 pares en el átomocentral
↑↑↑↑↓↑↓Cl* [Ne]
↑↑↑↑↑↓S* [Ne]
↑↑↑↑↑P* [Ne]
dpsorbitales
Moléculas con 5 pares en el átomocentral
1.6561.711AsF5
2.0202.140PCl5
1.5341.577PF5
Distancia (Å)(A-Xec)
Distancia (Å)(A-Aax)
Molécula
FF
F F
FAs

13
Moléculas con 5 pares en el átomocentral
Las posiciones axiales y ecuatorialesno son equivalentes
Cl menos electronegativo que F
Moléculas con 4 pares enlazantes y uno no enlazantealrededor del átomo central
Entre par enlazantey
Par no enlazante>>> Entre 2 pares
enlazantes
Respulsión:
Geometría disfenoidal
100.6169.21.6821.770SeF4
101.6173.11.5451.646SF4
Fec-A-Fec ºFax-A-Fax ºd (A-Xax) Åd (A-Xax) ÅAX4

14
Moléculas con 3 pares enlazantes y dos noenlazantes alrededor del átomo central
ClF3 y BrF3 Geometría: T
85.01.7301.810BrF3
87.01.5801.700ClF3
Fax-A-Fecºd(A-Xec) Åd(A-Xax) ÅAX3
Seis pares de electrones: SF6, SeF6, TeF6.
Octaédro: distribución de mínima energía
Moléculas con 6 pares enlazantes alrededor del átomo central
SF6

15
Seis pares de electrones: ClF5, BrF5, IF5
Pirámide de base cuadrada (distorsionada)
83.01.8711.814IF5
85.11.7681.697BrF5
86.01.6701.570ClF5
Fap-A-Fbasd (A-Xap) °d (A-Xap) °AX5
Moléculas con 4 pares de enlace y doslibres
Geometría: cuadrado plano

16
Precaución
La teoría TRPECV (VSEPR en inglés)sirve para elementos representativosprincipalmente.
Menos eficaz para elementos detransición.
Isolectronicidad Dos moléculas con el mismo número de electrones de
valencia son isoelectrónicas. Las moléculas isoelectrónicastipo AXn son también isoestructurales.
Moléculas AX4 de 32 electrones y estructura tetraédrica:
SnCl4
[PCl4]+[SiO4]4-
ClO3FPOCl3SiF4[AlCl4]-
[ClO4]-[PO4]3-CCl4[BF4]-[BeCl4]2-

17
http://www2.uah.es/edejesus/interactivos/VSEPR/tabla1.htm