ReplicaciReplicacióón y mantenimiento de la informacin y ......Recombinación específica de...
Transcript of ReplicaciReplicacióón y mantenimiento de la informacin y ......Recombinación específica de...

2011 Enrique Castro 1
Replicación y mantenimiento de la informaciónReplicación y mantenimiento de la información
➢ Replicación del DNA Topología de las horquillas de replicación. Etapas genéricas del proceso Química de la polimerización de DNA DNA polimerasas eucarióticas: fidelidad y procesividad Maquinaria molecular en la horquilla replicativa eucariótica. Diferencias importantes en procariotas. Regulación de la replicación: Iniciación, sincronización con el ciclo celular Replicación de telómeros
➢ Recombinación del DNA Modelos topológicos del proceso. Enzimas participantes: RecA, DNA-PK
➢ Reparación del DNA Mutaciones y lesiones química y estructurales en el DNA. Reparación por excisión: MMR, BER, NER. Acoplamiento transcripcional. Bloqueos de polimerasa. Reparación de roturas de doble cadena. NHEJR
Para © Enrique Castro Los trabajos de terceros retienen su licencia original
2011 Enrique Castro 2
Topología de la ReplicaciónTopología de la Replicación
● Semiconservativa● Origen interno, secuencial, bidireccional● Extensión 5' 3', semidiscontinua
Hebras molde intactasHebra nueva complementaria

2011 Enrique Castro 3
Síntesis de la hebra retrasadaSíntesis de la hebra retrasada
2011 Enrique Castro 4
Polimerización de DNA: características generalesPolimerización de DNA: características generales
Hebra molde
Hebra cebadora
3' OH
apareamiento estable
5'
3'
Liberación de PP
i
● Dependiente de molde● Cebador 3'OH● Direccional: 5'→3'● Sustrato dNTPs● Alta fidelidad● Alta procesividad
NTP + H2O NMP+ PPi
ΔG0= –31 kJ/mol
DNAn + NMP DNAn+1 + H20
ΔG0= +25 kJ/mol
DNAn + NTP DNAn+1 + PPi
ΔG0= –6 kJ/mol
PPi + H2O 2 Pi
ΔG0= –31 kJ/mol
sin errores
Continuasin interrupción

2011 Enrique Castro 5
proceso actividad proteína
Reconocimiento del origen ORCcdc45
Dependiente de ciclinas
Desenrollamiento helicasas MCMs Estimulada por cdc45,RPA, DNApol α
unión monohebra RPA Unión polα, RFC
topoisomerasas Topo II
Cebado primasa DNApol α Unión RPA, cdc45
Elongación síntesis DNApol δ DNApol ε Unidas a PCNA
procesividad RFCPCNA
Cargadorandamiaje
MaduraciónEliminación del cebador Exonucleasas
helicasasRnasa H1, FEN1Dna2
Endonucleasa flap
Rellenado de huecos síntesis DNApol δ DNApol ε
Ligamiento DNA ligasa I
Elongación de telómeros telomerasa
Maquinaria de la replicación eucarióticaMaquinaria de la replicación eucariótica
2011 Enrique Castro 6
DNA polimerasas eucarióticasDNA polimerasas eucarióticas
Análogos de nucleótidos2'-3'-didesoxi: AZTDe azúcar: AraC antitumoral AraA antiviral Aciclovir antiviral
aciclovir
DNApol α DNApol β DNApol γ DNApol δ DNApol εNº subunidades 4 hetero 1 4 homo 3 hetero 2 hetero
KM para dNTPs (μM) 2-5 10 0.5 2-4 2-5
Procesividad intrínseca Con PCNA
moderadamoderada
bajabaja
altaalta
bajaalta
altaalta
3' exonuclesa No No Si Si Si
Actividad primasa Si No No No No
Sensibilidad didesoxi-NTP baja alta alta baja moderada
Sensibilidad a AraCTP alta baja baja alta ?
Compartimento Núcleo Núcleo Mitocondria Núcleo Núcleo
Función Replicaciónprimasa
Reparación, BER
Replicación DNA mitocondrial
Rep. (retrasada) Rep. (conductora)Reparación
Homólogo bacteriano Primasa DnaG Pol I --- Pol III Pol III

2011 Enrique Castro 7
DNA polimerasas: fidelidad de copiaDNA polimerasas: fidelidad de copia
Fidelidad ∝ diferencia energética
pol ≈ 10-6-10-7
ΔΔG≈4-15 kJ/mol
DNA pol I de E. ColiBien apareado mal apareado
Fusión local 4-5 pb
molde
Unión surco mayor
Sitio 3' exo
Sitio pol
● Inserción específicaafinidad KM
Error ≫ KMap
● extensión selectivavelocidad kcat
Error ≪ kcatap
● 3' exonucleasa≈1:10 correctos
Fidelidad x 103
Apareamiento deWatson-Crick
mal-apareamiento
Actividad dualDNApolimerasa3'-exonucleasa
Fidelidad replicativa
≈ 10-9
2011 Enrique Castro 8
Fidelidad: Malapareamientos con igual geometríaFidelidad: Malapareamientos con igual geometría

2011 Enrique Castro 9
Etapas de la replicaciónEtapas de la replicación
DNA ligasa
➢Cebado:•Reclutamiento de la primasa• Síntesis del cebador
➢Iniciciación•Reconocimiento del origen•Ensamblaje de la helicasa•Activación de la helicasa
➢Intercambio de polimerasa:•Reclutamiento de RFC•Ensamblaje de la arandela de procesividad•Reclutamiento de DNA polimerasa
➢Procesamiento de F. de Okazaki•Eliminación del cebador•Rellenado de huecos• Ligado
➢Elongación• Síntesis de DNA por polimerasaFEN1
RNasa H
Dna2
DNA pol δ
RFCPCNA
DNA pol α
DNA pol αRPA
Frag. Okazaki previo
RPA
Molde H. retrasada
2011 Enrique Castro 10
Etapas de la replicaciónEtapas de la replicación

2011 Enrique Castro 11
Licenciamiento: reconocimiento del origen y ensamblaje MCMLicenciamiento: reconocimiento del origen y ensamblaje MCM
Origen: secuencias ARS• Repeticiones ricas AT• Fusión fácil• Múltiples: 1 cada 3-300 kpb
ORC• Hexamérico• Unión permanente a ARS• Fosforilable
➢Reconocimiento del origen•Unión MCM
➢Ensamblaje de helicasa• CDT1 presenta MCM• Cdc6 ensambla en DNA
cdc6• Cargador de helicasa• ATPasa
MCM• Helicasa replicativa• Hexamérico toroidal• Desfosfolrilada, Unida a CDT1
Complejopre-replicativolicenciado (inactivo)
ensamblaje• Actividad ATPasa de cdc6• Cambio conformacional MCM• Enhebrado en hebra conductora
➢Activación de helicasa• Fosforilación por CDKs•Reclutamiento de cdc45
cdc45P
P
ADP
Pi
CDKs
2011 Enrique Castro 12
Iniciación de la replicación: Activación de helicasaIniciación de la replicación: Activación de helicasa
Quinasas dependientes de ciclinas, CDKs
Complejo pre-replicativoHelicasa inactiva
Activada en fase Sdel ciclo celular
Fosforilación cdc6 marca para proteolisis
Helicasa 3'5' activaHebra molde conductora
➢Activación de helicasa• Fosforilación MCM por CDKs
•Reclutamiento de cdc45•Cdc45 estimula activ. helicasa
CDKs fosforilan múltiples dianas• ORC • cdc6• cdt1• MCM• otras
➢Sincronización con ciclo celular•Activación única por ciclo•Reconocimiento ORC sólo desfosfo-MCM• fosfo-Cdc-6 ubiquitinizado (degradado)

2011 Enrique Castro 13
Replicación: Desenrollamiento del DNAReplicación: Desenrollamiento del DNA➢Actividad helicasa de MCM
•MCM enhebrado en molde de conductora• Actividad helicasa 3' 5' •Necesita unión de cdc45• Estimulada por RPA• ATPasa: 0,1-0,5 vueltas/ATP
Helicasa 3'5' Montada en molde hebra conductora
RPA• Heterotrimérica (p70, p34, p11)• 4 sitios de unión al DNA (diana 30 pb)• Previene reasociación de monohebras • Estimula helicasa MCM (feedback positivo)
Desenrollados 1-5 nucleótidos por ATP
2011 Enrique Castro 14
Cebado: primasaCebado: primasa
➢Reclutamiento de primasa:•Primasa = DNApolα•Reclutada sobre helicasa/RPA
➢Síntesis del cebador•Cebador mixto RNA/DNA•Baja fidelidad (DNApolα sin correción errores 3' exo)
•Baja procesividad (salida espontánea = terminación cebador)
Interacciones de uniónsinérgicas entre RPA/MCM/DNApolα
DNA pol α
Cebador mixto: ≈30-40 nucleótidos(longitud limitada por baja procesividad)

2011 Enrique Castro 15
Ensamblaje de la arandela de procesividadEnsamblaje de la arandela de procesividad
ATP
RPA
RFC
duplex
5’ 3’
DNA pol α
3’5’
3’
ATP+
PCNA
DNA pol δ / ε
ADP +Pi
Unión a fronteracebador dúplex – monohebra
RFC: •Unión de alta afinidad a DNAdúplex-RPA • ATPasa
Salida de primasaDNA pol α
Polimerasa replicativa
Hebra conductora: >10 kb DNApol ε Hebra retrasada: 0.2-0.5 kb DNApol δ
Baja procesividaddesligado espontáneo
PCNA es sitio de unión de máquinaria
replicativa
Síntesis de fragmentos de Okazaki
Ensamblaje PCNA: • RFC cargador• ATP-dependiente
2011 Enrique Castro 16
Procariotas: DNA pol III β Eucariotas: PCNA
trímero p36
H2Op41
p41
3.5 nm
DNA
┴ a surcos
p21CIP1
Arandelas de procesividadArandelas de procesividad
Inhibidor ciclo celularInhibe replicación, no reparación

2011 Enrique Castro 17
Eliminación del cebadorEliminación del cebador
➢RNasa H1•5' exonucleasa•Ribonucleasa•Elimina PPP
➢FEN 1•Endonucleasa flap•5' exonucleasa•No elimina PPP
terminal5'exo
Vía RNasa H1/ FEN1
Vía Dna2 / FEN1
reconocimiento
corte'flap'
Todas unidas aPCNA y DNApol
Máquina replicativa
Máquina replicativarellenado de huecos
2011 Enrique Castro 18
Ligado de fragmentos de OkazakiLigado de fragmentos de Okazaki
PPi 2 P
i
irreversible
reutilización
• Hidrólisis PP: unidireccional• NMN acumulado en lesiones
DNA ligasa 1 unidaPCNA y DNApol
Máquina replicativa

2011 Enrique Castro 19
Helicasa DnaB
primasa RNA pol
SSB
avance de la horquilla
Duplex parental
arandela β
arandela β
avance dehebra conductora
avance dehebra retrasada
cebador
primer
hebr
a co
nduc
tora
hebr
a re
zaga
da
núcleo pol III
núcleo pol III
DNA ligasa I
DNA pol I
complejo γ
DNA pol α 3’ exo ε
θ
γδδ’χψ
Cargador de β
Helicasa DnaB 5’---3’: hebra retrasada
Primosoma permanente
Cebador RNA
Sin cambio de polimerasa
Ensamblado en máquina molecular dimérica (subunidad τ)
Fragmentos de Okazaki largos
Maduración por DNA pol I
DNA pol 5’---3’exonucleasa 3’ 5’ corrección)exonucleasa 5’ 3’ (Okazaki)
Maquinaria de Replicación en ProcariotasMaquinaria de Replicación en Procariotas
2011 Enrique Castro 20
Maquinarias de replicación: comparaciónMaquinarias de replicación: comparación
Procariotas Eucariotas

2011 Enrique Castro 21
Reorganización de la cromatina en replicaciónReorganización de la cromatina en replicación
➢Detrás:•Re-ensamblaje de nucleosomas•Descarga de PCNA
Topo I humana: camptotecina(antitumoral)
DNA girasa bacteriana:Ác. Nalidíxico (sub A)novobiocina (sub B, ATPasa)
➢Delante: •Desensamblaje de nucleosomas•Tensiones de superenrollamiento positivo
•Alivio de tensión por topoisomerasas•Dianas de fármacos
Hebra conductora
Hebra rezagada
TetrámeroH3/H4
H1H2A/H2B
InteracciónCAF-1 / PCNA
• CAF-1 se une a PCNA• Se añaden H2A/H2B, H1• PCNA es descargado• Histonas desacetiladas
Desensamblaje nucleosómico• 1 Tetrámetro H3/H4• 2 Dímeros H2A/H2B
Ensamblaje cuasi-aleatorio• 1 Tetrámetro + 2 dímeros• Antiguos repartidos• De novo acetilados (y mezclados)
• CAF-1 presenta H3/H4
•re-ensamblaje en ambas hebras
2011 Enrique Castro 22
Mantenimiento de TelómerosMantenimiento de Telómeros
➢Problema telómerico: • Imposible replicar extensión 3' (rezagada) •Acortamiento progresivo (daño en genes)• Senescencia replicativa
5' AGGGTT AGGGTT AGGGTT AGGGTT AGGGTT AGGGTT AGGGTT 3'3' TCCCAA TCCCAA TCCCAA TCCCAA 5' 3' 5'
Stryer 6e Fig. 28-34
Translocación
Translocación
Elongación
Elongación
Ciclo repetido n veces
➢Telomerasa•2 subunidades + RNA•Molde intrínseco RNA (secuencia fija)•Transcriptasa inversa• Sólo embrión/stem, luego inducible
TERT, inducible
TEP1, constitutiva
RNA molde
Telómeros añadidos,no repliclados

2011 Enrique Castro 23
Replicación DNA mitocondrialReplicación DNA mitocondrial
DNA mitocondrial16 kpb, dos hebrassuperenrrollado
Origen hebra H
Nuevahebra H Nueva
hebra H
Bucle de desplazamientoDNApolγ activa en molde L
Origen hebra L
Nuevahebra L
2 orígenes monohebraHorquillas unidireccionales
DNApolγ Alfa fidelidad (3'exo)
2011 Enrique Castro 24
Replicación y mantenimiento de la informaciónReplicación y mantenimiento de la información
➢ Replicación del DNA Topología de las horquillas de replicación. Etapas genéricas del proceso Química de la polimerización de DNA DNA polimerasas eucarióticas: fidelidad y procesividad Maquinaria molecular en la horquilla replicativa eucariótica. Diferencias importantes en procariotas. Regulación de la replicación: Iniciación, sincronización con el ciclo celular Replicación de telómeros
➢ Recombinación del DNA Modelos topológicos del proceso. Enzimas participantes: RecA, DNA-PK
➢ Reparación del DNA Mutaciones y lesiones química y estructurales en el DNA. Reparación por excisión: MMR, BER, NER. Acoplamiento transcripcional. Bloqueos de polimerasa. Reparación de roturas de doble cadena. NHEJR

2011 Enrique Castro 25
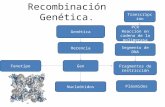
Recombinación Recombinación
Cruce de Holliday
Extremos desapareados disparan recombinación
➢Recombinación específica de sitio: • Secuencia específica / Enzimas específicas• Integración/escisión de virus
➢Transposición•Transposasa y secuencias de inserción• LINES / SINES• Integración/escisión retrovirus
➢Unión de extremos no homólogos • Sin homología secuencial: no recombinación•Reparación de roturas de doble hebra
➢Recombinación homóloga• Secuencia homóloga (complementaria)• Simetría de corte•Cruces de Holliday (4 cadenas)•Reparación (uniones de roturas)•Meiosis: variabilidad de ligamientos génicos
Recombinación: corte y cruce de información
de dos cromosomas
Gen A Gen B
Gen a Gen b
Gen A Gen b
Gen a Gen B
(NHEJ)
Secuencia complementaria
Ku/DNA-PK
2011 Enrique Castro 26
Gen B Gen A
Gen a Gen b
Recombinación homóloga: mecanismo de HollidayRecombinación homóloga: mecanismo de HollidayExisten otros mecanismos• Meselson-Radding• Rotura de doble hebra
Intermediario de Holliday
Corte monohebra• inducido o prexistente
Invasión de hebra• Desenrollamiento local• Apareamiento complementario cruzado
(homología de secuencia)
Migración de rama• Desplazamiento de apareamiento
Religado
Corte de Holliday• Endonuclesa + ligasa
Gen A Gen B
Gen a Gen b
Gen A Gen B
Gen a Gen b
Gen A Gen B
Gen a Gen b
Gen A Gen B
Gen a Gen b
Gen B Gen A
Gen a Gen b
Gen A Gen B
Gen a Gen b
Giro90º Gen A Gen b
Gen a Gen B
Corte 1 (igual)
Corte 2 recombinación
Zonashíbridas

2011 Enrique Castro 27
Mecanismos de recombinaciónMecanismos de recombinaciónRecA cataliza invasión de hebraRecBCD genera monohebras: helicasa+nucleasa
:GCTGGTGG
RecA une monohebrasRecBCD
une extremos
2011 Enrique Castro 28
Recombinación en InmunoglobulinasRecombinación en Inmunoglobulinas
http://scienceblogs.com/webeasties/2011/08/the_god_of_b-cells.phpMatsuda and Hanjo, "Organization of the Human Immunoglobulin Heavy-Chain Locus" Advances in Immunology. Volume 62, 1996, Pages 1-29
The final piece of GoD is what we call "junctional diversity." When the DNA is severed durring V(D)J recombination, it's not always a clean cut, and some extra nucleotides must be added to fill the gap. In addition, there's an enzyme whose only job is to add in random nucleotides to the junction. This randomness can be extreme and it's here that GoD mangages to reach the 10 billion mark. This is also the reason that every individual has their own set of antibodies. The inherent randomness, from the selection of V's, D's and J's, to the jagged cuts to the random inserted nucleotides means that not even identical twins will have the same repertoire, or even similar repertoires.every individual has their own set of antibodies. The inherant randomness, from the selection of V's, D's and J's, to the jagged cuts to the random inserted nucleotides, means that not even identical twins will have the same repertoire.

2011 Enrique Castro 29
Replicación y mantenimiento de la informaciónReplicación y mantenimiento de la información
➢ Replicación del DNA Topología de las horquillas de replicación. Etapas genéricas del proceso Química de la polimerización de DNA DNA polimerasas eucarióticas: fidelidad y procesividad Maquinaria molecular en la horquilla replicativa eucariótica. Diferencias importantes en procariotas. Regulación de la replicación: Iniciación, sincronización con el ciclo celular Replicación de telómeros
➢ Recombinación del DNA Modelos topológicos del proceso. Enzimas participantes: RecA, DNA-PK
➢ Reparación del DNA Mutaciones y lesiones química y estructurales en el DNA. Reparación por excisión: MMR, BER, NER. Acoplamiento transcripcional. Bloqueos de polimerasa. Reparación de roturas de doble cadena. NHEJR
2011 Enrique Castro 30
Errores replicativos Mal-apareamientosinserciones y deleciones(patinado de polimerasa)bloqueo de polimerasa
Agentes intercalantes
Despurinaciónespontánea
Sitios AP (104/genoma/día)
Inducido por ácidos y bases
Desaminación espontánea Mal-apareamientos(100-500/genoma/día)
C→U nitrosaminasG→XA→H
Alquilaciones de bases Mal-apareamientos inducidosimpedimentos estéricos
Mostazas nitrogenadasAlquil sulfonatos
Oxidaciones de bases Mal-apareamientos inducidosentrecruzamientos
Estrés oxidativonitrosaminas
Aductos de bases Impedimentos estéricosentrecruzamientos
Carcinógenos químicosbenzopirenosaflatoxinas
Dímeros de timina Impedimentos estéricosbloqueo de polimerasa
Luz UV
Roturas de hebra Delecionesentrecruzamientostranslocaciones
Radiaciónes ionizantesestrés oxidativo
Mecanismos de daño al DNAMecanismos de daño al DNA

2011 Enrique Castro 31
Daño por malapareamientos inducidosDaño por malapareamientos inducidos➢Tautomerización espontánea ➢Alquilación
➢Desaminación oxidativa➢Oxidación Estrés oxidativo
EspontáneaMuy frecuente
Agentesalquilantes
CU (A)AH (C)G X (A)
2011 Enrique Castro 32
Tautómeros y errores de apareamientoTautómeros y errores de apareamiento
Purine and pyrimidine bases exist in different forms called tautomers.(A) A tautomeric shift occurs when a proton changes its position, resulting in a rare tautomeric form. (B) Standard and anomalous base-pairing arrangements that occur if bases are in the rare tautomeric forms. Base mispairings due to tautomeric shifts were originally thought to be a major source of errors in replication, but such structures have not been detected in DNA, and most evidence now suggests that other types of anomalous pairings are responsible for replication errors.
Pierce, Benjamin. Genetics: A Conceptual Approach, 2nd ed. (New York: W. H. Freeman and Company), 485.DNA Replication and Causes of Mutation. By: Leslie A. Pray, Ph.D. © 2008 Nature Education Citation: Pray, L. (2008) DNA replication and causes of mutation. Nature Education 1(1)

2011 Enrique Castro 33
Agentes mutágenosAgentes mutágenos➢Agentes intercalantes
• Sustituyen pb en apilamiento• Inserciones/deleciones replicativas
➢Radiación UV•UVB, UVC•Radicales oxidantes (8oxoG)•Dímeros de pirimidina
➢Radiación ionizante•Fotones: X, •Partículas: , •Rotural de anillos•Roturas de doble hebra
➢Formadores de aductos•Grupos voluminosos unidos covalentemente•Defromaciones estructurales, impedimentos estéricos• Inserciones, deleciones•Entrecruzamientos de hebra•Bloqueos de polimerasa
Humo de tabaco:benzopireno
Contaminantes biológicos:AflatoxinaMitomicina CPsoraleno
Cancerígenosorgánicos
2011 Enrique Castro 34
Lesión por radiación UV: dímeros de pirimidinaLesión por radiación UV: dímeros de pirimidina
➢Dímeros de pirimidina•Pir-Pir adyacentes (TT más frecuente)•Fotoreacción espontánea (UVA)•Daño estructural (deformación permanente)
Pirimidinas adyacentes
UV 260 nm
Dímero de ciclobutano
Fotoproducto 6-4
Luz solarUVB
Bloqueo de polimerasa
Hueco de ≈1 kpb
Deformaciónestructural

2011 Enrique Castro 35
Mecanismos de Reparación del DNAMecanismos de Reparación del DNA● Nucleótido difosfohidrolasas
● Mantenimiento y control de calidad
MMR Rep. Malapareamientosdependiente de metilaciónpostreplicativo
BER Rep. por escisión de baseDNA-N-glucosilasas/PARP
NER Rep. Por escisión de nucleótidosexcinucleasas
NHEJR Rep. por unión de extremos no homólogosMMEJR Rep. por unión de extremos con microhomología
Ku/DNA-PK/PARP
● Reparación directafotorreactivación: DNA fotoliasa desalquilación: O6-alquil-guanina transferasa
● Mecanismos no específicosRep. Translesión
DNA pol ζ, η, ι
Rep. por recombinaciónIntermedios de Holliday, proteínas Rec
preventivo
Sistemas de detección de daños
especializadosSensores de daño al DNA
Fallosreplicativos
Uracil-DNAbases alteradas
sitios APmalapareamientos
Defectos estéricosdímeros de timinaaductos de base
Mod. voluminosas
Roturas dedoble hebra
Bloqueos de polimerasaRoturas de doble hebra
entrecruzamientos
Bloqueos de polimerasa Sin sistema dedetección dedicado
2011 Enrique Castro 36
Prevención y Reparación directaPrevención y Reparación directa
Fotoliasa
➢Preventivos•Nucleótido difosfohidrolasas•Evitan incorporación incorrecta
dUTP + H2O dUMP + PP
i
d-oxoGTP + H2O d-oxoUMP + PPi
➢Reparación directa• Inversión del daño in situ•Fotoreactivación (no en mamíferos)•Desalquilación
Fotoreactivación: DNA fotoliasa
UV370 nm
dUTPasa
Degradacióntotal
Desalquilación: O6-alquilG transferasa
irreversible
O6mG induce mal-apareamientos

2011 Enrique Castro 37
Reparación por escisión: MMRReparación por escisión: MMRMetilación 5mC, 6mA: marca hebra antigua
MutH•Reconocimiento de hebra•endonucleasa
MutS•Reconocimiento del error
MutL•Asociación ambos
Rellenado de huecosRPA, RFC, PCNADNApol δ/ε
2011 Enrique Castro 38
Reparación por escisión de base: BERReparación por escisión de base: BER
DNA glucosilasas
BER también corrige sitios AP espontáneos
•UDG: uracilo•Malapareamientos G/T(U) A/G (oxoG)
•B. alquiladas 3mA, 06mG
•B. oxidadas 8oxoG
Sensor: PARP
dRPasa
DNApol βN- 8kDa
Reparación BER“hueco corto”
Reparación BER“hueco largo”
HidrólisisN-glucosídico
Sitio AP

2011 Enrique Castro 39
Reparación por escisión de nucleótidos: NERReparación por escisión de nucleótidos: NER
ATP
⑥
2011 Enrique Castro 40
Reparación por escisión de nucleótidos: NERReparación por escisión de nucleótidos: NER

2011 Enrique Castro 41
Reparación de roturas dobles: NHEJR y MMEJRReparación de roturas dobles: NHEJR y MMEJR
➢No-homóloga•Reconoce extremos rotos•Une sin importar secuencia, con deleción• Salvaguardia, propenso a errores•Helicasa Ku / DNA-PK
2011 Enrique Castro 42
Rep. de roturas de doble hebra por recombinaciónRep. de roturas de doble hebra por recombinación
Corte y empalme recombinatorio
Rellenado del hueco
Rellenado del hueco

2011 Enrique Castro 43
Reparación de bloqueos de polimerasaReparación de bloqueos de polimerasa
➢Replicación translesión•Propensa a error: DNApol ζ, ι• Libre de error: DNApol η
Hueco crea rotura en cromosoma hijo
Útil si es zona no codificante
➢Recombinación• Libre de errores
Reparable NER escinucleasa
2011 Enrique Castro 44
Reparación de bloqueos por recombinaciónReparación de bloqueos por recombinación
Corte y empalme recombinatorio
Rellenado del hueco
Reparable NER escinucleasa
Dímero Pir no aparea Pero sus vecinos si: hélice bien alineada