Los bioelementos
-
Upload
wilson-coba-jr -
Category
Education
-
view
1.070 -
download
1
Transcript of Los bioelementos


LOS BIOELEMENTOS

LOS BIOELEMENTOS
Los organismos vivos están constituidos por elementos químicos, a los cuales se les llama Bioelementos.
Estos bioelementos entran a formar parte de la materia viva en cantidades muy variables.
De todos los elementos químicos que se hallan en la corteza terrestre, sólo unos 25 son componentes de los seres vivos

LOS BIOELEMENTOS
Los bioelementos se combinan entre sí, para formar estructuras moleculares de
distinta complejidad. A estas moléculas complejas que forman parte de la materia viva se las denomina
Bio moléculas

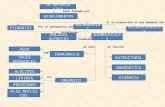
CLASIFICACIÓN DE LOS BIOELEMENTOS
BIOELEMENTOS
PRIMARIOS C, O, H, N, P, S
SECUNDAROSNa, K, Mg, Ca, Cl
GRUPOS
OLIGOELEMENTOS
INDISPENSABLESMn, Fe, Co, Cu, Zn
VARIABLESB, V, Al, Mo, I, Si

CLASIFICACIÓN DELOS BIOELEMENTOS

Clasificación de los biolelementos

CARACTERÍSTICAS DE LOS BIOELEMENTOS PRIMARIOS

LOS BIOELEMENTOS PRIMARIOS
Son los elementos mayoritarios de la materia viva, constituyen el 95% de la masa total.Las propiedades físico-químicas que los hacen idóneos son las siguientes:
1. Forman entre ellos enlaces covalentes, compartiendo electrones 2. El carbono, nitrógeno y oxígeno, pueden compartir más de un par de electrones, formando enlaces dobles y triples, lo cual les dota de una gran versatilidad para el enlace químico 3. Son los elementos más ligeros con capacidad de formar enlace covalente, por lo que dichos enlaces son muy estables.

LOS BIOELEMENTOS PRIMARIOS
4. A causa de la configuración tetraédrica de los enlaces del carbono, los diferentes tipos de moléculas orgánicas tienen estructuras tridimensionales diferentes .
Esta conformación espacial es responsable de la actividad biológica.

LOS BIOELEMENTOS PRIMARIOS
5. Las combinaciones del carbono con otros elementos, como el oxígeno, el hidrógeno, el nitrógeno, etc., permiten la aparición de una gran variedad de grupos funcionales que dan lugar a las diferentes familias de sustancias orgánicas . Estos presentan características físicas y químicas diferentes, y dan a las moléculas orgánicas propiedades específicas, lo que aumenta las posibilidades de creación de nuevas moléculas orgánicas por reacción entre los diferentes grupos.

LOS BIOELEMENTOS PRIMARIOS
6. Los enlaces entre los átomos de carbono pueden ser simples (C - C), dobles (C = C) o triples, lo que permite que puedan formarse cadenas más o menos largas, lineales, ramificadas y anillos.

LOS BIOELEMENTOS SECUNDARIOS
Secundarios son aquellos bioelementos que forman parte de la materia viva en un bajo porcentaje, apenas los están constituyendo en un 4.5%.
No se encuentran presentes en todos los seres vivos.
Entre los bioelementos secundarios más importantes, tenemos los siguientes: Na, K, Mg, Ca, Cl

LOS OLIGOELEMENTOS
Se denominan así al conjunto de elementos químicos que están presentes en los organismos en forma vestigial, pero que son indispensables para el desarrollo armónico del organismo.
A los elementos: hierro, manganeso, cobre, zinc y cobalto se les ha considerado como oligoelementos indispensables, porque son comunes en todos los organismos vivos. Mientras que a los elementos: flúor, iodo, boro, silicio, vanadio, cromo, selenio, molibdeno y estaño se les considera como oligoelementos variables por que no son comunes en los seres vivos

UBICACIÓN Y FUNCIÓN DE ALGUNOS BIOELEMENTOS
AzufreSe encuentra en dos aminoácidos (cisteína y metionina) , presentes en todas las proteínas. También en algunas sustancias como el Coenzima A
FósforoForma parte de los nucleótidos, compuestos que forman los ácidos nucléicos. Forman parte de coenzimas y otras moléculas como fosfolípidos, sustancias fundamentales de las membranas celulares. También forma parte de los fosfatos, sales minerales abundantes en los seres vivos.
MagnesioForma parte de la molécula de clorofila, y en forma iónica actúa como catalizador, junto con las enzimas , en muchas reacciones químicas del organismo

UBICACIÓN Y FUNCIÓN DE ALGUNOS BIOELEMENTOS
CalcioForma parte de los carbonatos de calcio de estructuras esqueléticas. En forma iónica interviene en la contracción muscular, coagulación sanguínea y transmisión del impulso nervioso.
SodioCatión abundante en el medio extracelular; necesario para la conducción nerviosa y la contracción muscular
PotasioCatión más abundante en el interior de las células; necesario para la conducción nerviosa y la contracción muscular
CloroAnión más frecuente; necesario para mantener el balance de agua en la sangre y fluído intersticial

UBICACIÓN Y FUNCIÓN DE ALGUNOS OLIGOELEMENTOS
HierroFundamental para la síntesis de clorofila, catalizador en reacciones químicas y formando parte de citocromos que intervienen en la respiración celular, y en la hemoglobina que interviene en el transporte de oxígeno.ManganesoInterviene en la fotolisis del agua , durante el proceso de fotosíntesis en las plantas.IodoNecesario para la síntesis de la tiroxina, hormona que interviene en el metabolismoFlúorForma parte del esmalte dentario y de los huesos.CobaltoForma parte de la vitamina B12, necesaria para la síntesis de hemoglobina .SilicioProporciona resistencia al tejido conjuntivo, endurece tejidos vegetales como en las gramíneas.

UBICACIÓN Y FUNCIÓN DE ALGUNOS OLIGOELEMENTOS
CromoInterviene junto a la insulina en la regulación de glucosa en sangre.ZincActúa como catalizador en muchas reacciones del organismo.LitioActúa sobre neurotransmisores y la permeabilidad celular. En dosis adecuada puede prevenir estados de depresiones.MolibdenoForma parte de las enzimas vegetales que actúan en la reducción de los nitratos por parte de las plantas.

COMPOSICIÓN QUÍNICA DE LOS SERES VIVOSCOMPOSICIÓN QUÍNICA DE LOS SERES VIVOS
ELEMENTOS BIOGENÉSICOSELEMENTOS BIOGENÉSICOS
PRIMARIOSPRIMARIOS SECUNDARIOSSECUNDARIOS OLIGOELEMENTOSOLIGOELEMENTOS
BIOMOLÉCULAS
INORGÁNICOS ORGÁNICOS
CARBOHIDRATOS LÍPIDOS
PROTEINAS
ÁCIDOS NUCLÉICOS
comprendencomprenden
formanforman
Se clasificanSe clasifican
agua Sales minerales

LAS BIOMOLÉCULAS
Carbohidratos o Glúcidos (CH2O)n
DISACÁRIDOS
POLISACÁRIDOS
Los azúcares son hidratos de carbono generalmente blancos y cristalinos, solubles en agua y con un sabor dulce
azúcares,
almidones, celulosa
MONOSACÁRIDOS Son moléculas simples
Son carbohidratos constituidos de dos azúcares simples
OLIGOSACÁRIDOS
Son carbohidratos constituidos por más de 2 hasta 10 azúcares
Son aquellos que tiene más de 10 moléculas de azúcar

Clasificación de monosacáridos basado en el número de carbonos
Número deCarbonos
Categoría Ejemplos
4 Tetrosa Eritrosa, Treosa
5 PentosaArabinosa, Ribosa, Ribulosa, Xilosa, Xilulosa, Lixosa
6 HexosaAlosa, Altrosa, Fructosa, Galactosa, Glucosa, Gulosa, Idosa, Manosa, Sorbosa, Talosa, Tagatosa
7 Heptosa Sedoheptulosa

Las estructuras de los monosacáridos se distinguen principalmente por la orientación de los grupos hidroxilos (-OH). Esta pequeña diferencia estructural tiene un gran efecto en las propiedades bioquímicas, las características organolépticas, y en las propiedades físicas como el punto de fusión y la rotación específica de la luz polarizada.
CARACTERÍSTICAS DE LOS MONSACÁRIDOS
Ejemplo: LAS TETROSAS
D-Eritrosa D - Treosa

Un monosacárido de forma lineal que tiene un grupo carbonilo (C=O) en el carbono final formando un aldehído (-CHO) se clasifica como una aldosa. Cuando el grupo carbonilo está en un átomo interior formando una cetona, el monosacárido se clasifica como una cetosa.
CARACTERÍSTICAS DE LOS MONSACÁRIDOS
D-RibosaD-Ribosa D-ArabinosaD-Arabinosa D-XilosaD-Xilosa D-LixosaD-Lixosa
Ejemplo: LAS PENTOSAS

CARACTERÍSTICAS DE LOS MONSACÁRIDOS
La forma anular de la ribosa es un componente del ácido ribonucleico (ARN). La desoxirribosa, que se distingue de la ribosa por no tener un oxígeno en la posición 2, es un componente del ácido desoxirribonucleico (ADN). En los ácidos nucleicos, el grupo hidroxilo en el carbono numero 1 se reemplaza con bases nucleótidas.
RibosaRibosa DesoxirribosaDesoxirribosa

HexosasHexosas, como las que están ilustradas aquí, tienen la fórmula molecular C6H12O6. El químico alemán Emil Fischer (1852-1919) identificó los estereoisómeros de estas aldohexosas en 1894. Por este trabajo recibió un Premio Nobel en 1902.
CARACTERÍSTICAS DE LOS MONSACÁRIDOS
D-Manosa D-Alosa D-Altrosa D-Glucosa
La glucosa, también llamada dextrosa, es el azúcar más predominante en las plantas y los animales, y es el azúcar presente en la sangre. La forma lineal de la glucosa es un aldehído polihídrico. En otras palabras, es una cadena de carbonos con varios grupos hidroxilos y un grupo aldehído.

D-Gulosa D-Gulosa D-Idosa D-Idosa D-Galactosa D-Galactosa D-Talosa D-Talosa
Hexosas

CARACTERÍSTICAS DE LOS MONSACÁRIDOS
La fructosa, también llamada levulosa, está ilustrada aquí en forma lineal y anular. La fructosa y la glucosa son los principales hidratos de carbono en la miel.
D-Tagatosa(una cetosa)
D-Fructosa Fructosa Galactosa Manosa

Heptosas
La sedoheptulosa tiene la misma estructura que la fructosa, pero con un carbono adicional
D-Sedoheptulosa
CARACTERÍSTICAS DE LOS MONSACÁRIDOS

Estereoquímica
La estereoquímica es el estudio de la organización de los átomos en un espacio tridimensional. Se les llama estereoisómeros a los compuestos con enlaces químicos idénticos que se distinguen por tener los átomos en una configuración espacial diferente.
Los Sacáridos con grupos funcionales idénticos pero con configuraciones espaciales diferentes tienen propiedades químicas y biológicas distintas
Las estructuras siguientes ilustran la diferencia entre la β-D-Glucosa y la β-L-Glucosa. Moléculas idénticas pueden hacerse corresponder rotándolas.

β-D-Glucosa β-L-Glucosa β-D-Glucosa(forma de silla)
β-D-Glucosa β-L-Glucosa β-D-Glucosa(forma de bote)
Estereoisómeros

OTROS MONOSACÁRIDOSAzúcar-alcoholes, Aminoazúcares, y Ácidos urónicos
Los azúcares pueden ser modificados en el laboratorio o por procesos naturales para producir compuestos que retienen la configuración de los sacáridos, pero con grupos funcionales diferentes. Los azúcar-alcoholes, también llamados polioles, alcoholes polihídricos, o polialcoholes, corresponden a las formas hidrogenadas de las aldosas y cetosas. Por ejemplo, glucitol (sorbitol), tiene la misma forma lineal que la glucosa, pero el grupo aldehído (-CHO) se reemplaza con -CH2OH. Otros azúcar-alcoholes comunes incluyen los monosacáridos eritritol y xilitol, y los disacáridos lactitol y maltitol. Los azúcar-alcoholes tienen aproximadamente la mitad de las calorías que otros carbohidratos y se usan frecuentemente en productos "sin azúcar" o de bajas calorías.

Xilitol, que tiene los grupos hidroxilos con la orientación de la xilosa, es un ingrediente común en dulces y chicles "sin azúcar" porque tiene aproximadamente la dulzura de la sucrosa y solamente el 40% de las calorías. Aunque este azúcar-alcohol parece ser inofensivo para los humanos, una dosis pequeña de xilitol puede causar insuficiencia hepática y muerte en los perros.
OTROS MONOSACÁRIDOSAzúcar-alcoholes, Aminoazúcares, y Ácidos urónicos
Glucitol o Sorbitol (un azúcar alcohol)

OTROS MONOSACÁRIDOSAzúcar-alcoholes, Aminoazúcares, y Ácidos urónicos
Los aminoazúcares o amino-sacáridos reemplazan un grupo hidroxilo con un grupo amino (-NH2). La glucosamina es un aminoazúcar que se usa para regenerar el cartílago y para reducir el dolor y la progresión de la artritis.
Glucosamina (un aminoazúcar)

OTROS MONOSACÁRIDOSAzúcar-alcoholes, Aminoazúcares, y Ácidos urónicos
Los ácidos urónicos tienen un grupo carboxilo (-COOH) en el carbono que no es parte del anillo. Los nombres de los ácidos urónicos retienen la raíz de los monosacáridos, pero el sufijo -osa cambia a -urónico. Por ejemplo, el ácido galacturónico tiene la misma configuración que la galactosa, y la configuración del ácido glucurónico corresponde a la glucosa.
Ácido glucurónico

Los disacáridos son carbohidratos formados por dos azúcares simples.
LOS DISACÁRIDOS
Disacárido Descripción Componentes
sucrosa azúcar común glucosa 1α→2 fructosa
maltosaproducto de la
hidrólisis del almidónglucosa 1α→4 glucosa
trehalosase encuentra en los
hongosglucosa 1α→1 glucosa
lactosael azúcar principal de
la lechegalactosa 1β→4
glucosa
melibiosase encuentra en
plantas leguminosasgalactosa 1α→6
glucosa

SUCROSA LACTOSA
MALTOSA
EJEMPLO DE DISACÁRIDOS

LA SUCROSA (o sacarosa), es el azúcar común refinado de la caña de azúcar y la remolacha azucarera. La sucrosa es el carbohidrato principal del azúcar moreno, del azúcar tamizado, y de la melaza.
EJEMPLO DE DISACÁRIDOS
LA LACTOSA está formada por una molécula de glucosa y otra de galactosa. La intolerancia de lactosa es causada por una deficiencia de enzimas (lactasas) que desdoblan la molécula de lactosa en dos monosacáridos. La inhabilidad de digerir la lactosa resulta en la fermentación de este glúcido por bacterias intestinales que producen ácido láctico y gases que causan flatulencia, meteorismo, cólico abdominal, y diarrea. El yogur no causa estos problemas porque los microorganismos que transforman la leche en yogur consumen la lactosa.

La Maltosa consiste de dos moléculas de α-D-glucosa con el enlace alfa del carbono 1 de una molécula conectado al oxígeno en el carbono 4 de la segunda molécula. Esta unión se llama un enlace glicosídico 1α→4 (también se llama "enlace glucosídico" en muchos textos en español). La trehalosa consiste de dos moléculas de α-D-glucosa conectadas con un enlace 1α→1. La celobiosa es un disacárido formado por dos moléculas de β-D-glucosa conectadas por un enlace 1β→4 como la celulosa. La celobiosa no tiene sabor, mientras que la maltosa y la trehalosa son aproximadamente una tercera parte tan dulces como la sucrosa.
EJEMPLO DE DISACÁRIDOS

Los polisacáridos

LOS POLISACÁRIDOS
Los polisacáridos están formados por la unión de centenares de monosacáridos, unidos por enlaces “O-glucosídicos”. Existen algunos formados por unidades de pentosa, llamados pentosanas, pero los que tienen importancia biológica son los polímeros de unidades de hexosas, llamados también hexosanas, y muy especialmente los polisacáridos formados de glucosa.

PROPIEDADES
Propiedades de los polisacáridos:1. No son cristalinos2. Por lo general insolubles en agua (no poseen poder reductor).3. No tienen sabor dulce.4. Su peso molecular elevado.

Clasificación de los polisacáridos
Los polisacáridos se clasifican en:
Homopolisacáridos, formados por el mismo tipo de monosacáridos. Destacan por su interés biológico el almidón, el glucógeno, la celulosa y la quitina.
Heteropolisacáridos, formados por diferentes monómeros. Entre ellos se encuentran la pectina, la hemicelulosa, el agar-agar y diversas gomas y mucopolisacáridos.

El almidón es el polisacárido de reserva propio de los vegetales, pues sirve como almacén de la glucosa (fabricada por fotosíntesis) en el interior de los plastos, donde se acumula en forma de granos de aspecto característico según la especie. Se halla, sobre todo, en raíces, tubérculos y semillas
EJEMPLOS DE POLISACÁRIDOS
Está formado a su vez por dos componentes, amilosa y amilopectina, en proporciones varia bles, según la especia vegetal de la que se trate.
ALMIDONES

Tiene la misma composición que la amilopectina y una estructura molecular semejante, aunque con mayor número de ramificaciones (cada 8 – 10 glucosas), por lo que el tamaño y el peso molecular son mayores. Su función es también de reserva o almacén de glucosa, pero es exclusivo de las células de los animales. Se acumula en forma de granos, sobre todo en el citoplasma de las células muscula res y hepáticas. El glucógeno muscular proporciona glucosa como combustible para la con tracción muscular, mientras que el del hígado es la reserva general de glucosa que pasa a la san gre y se distribuye a las células.
EJEMPLOS DE POLISACÁRIDOS
Glucógeno.

EJEMPLOS DE POLISACÁRIDOS
Su función es estructural, pues forma la pared de todas las células vegetales, a las que da for ma y consistencia. Es especialmente abundante en los tejidos vegetales de las células muertas, como el leño del interior de los árboles y muchas fibras vegetales (cáñamo, esparto, algodón, etc.). De hecho, se considera que es la molécula orgánica más abundante en la naturaleza.
Celulosa.
Su interés económico es muy grande, pues se emplea en la industria de fabricación de papel, plásticos, explosivos, etc.

LA CELULOSA

QUITINA
Es un polímero de un derivado de la glucosa, la N-acetil-glucosamina, con enlaces beta 1-4, y forma cadenas semejantes a la celulosa que se unen lateralmente, por lo que resultan muy resistentes al ataque de agentes químicos. Las enzimas quitinasas, capaces de degradar la quitina por hidrólisis, son muy escasas en la naturaleza (existen en los caracoles y en ciertos insectos tropicales), por lo que, en general, no es digerible.
Su función es estructural, ya que constituye el componente esencial del exoesqueleto de muchos invertebrados (Artrópodos, algunos Anélidos, etc.). También forma parte de la pared celular de hongos y líquenes.
EJEMPLOS DE POLISACÁRIDOS

EJEMPLO DE QUITINA

LOS LÍPIDOS

CLASIFICACIÓN DE LOS LÍPIDOS

EJEMPLO DE UNA MOLÉCULA DE LÍPIDO

SAPONIFICACIÓN
La saponificación es una reacción química entre un ácido graso (o un lípido saponificable, portador de residuos de ácidos grasos) y una base o alcalino, en la que se obtiene como principal producto la sal de dicho ácido y de dicha base. Estos compuestos tienen la particularidad de ser anfipáticos, es decir tienen una parte polar y otra apolar (o no polar), con lo cual pueden interactuar con sustancias de propiedades dispares. Por ejemplo, los jabones son sales de ácidos grasos y metales alcalinos que se obtienen mediante este proceso.El método de saponificación en el aspecto industrial consiste en hervir la grasa en grandes calderas, añadiendo lentamente sosa cáustica (NaOH), agitándose continuamente la mezcla hasta que comienza esta a ponerse pastosa.La reacción que tiene lugar es la saponificación y los productos son el jabón y la glicerina:Grasa + sosa cáustica → jabón + glicerina

FUNCIONES DE LOS LÍPIDOS
Función de reserva energética. Los triglicéridos son la principal reserva de energía de los animales ya que un gramo de grasa produce 9,4 kilocalorías en las reacciones metabólicas de oxidación, mientras que las proteínas y los glúcidos sólo producen 4,1 kilocalorías por gramo.
Función estructural. Los fosfolípidos, los glucolípidos y el colesterol forman las bicapas lipídicas de las membranas celulares. Los triglicéridos del tejido adiposo recubren y proporcionan consistencia a los órganos y protegen mecánicamente estructuras o son aislantes térmicos.

Función reguladora, hormonal o de comunicación celular. Las vitaminas liposolubles son de naturaleza lipídica (terpenos, esteroides); las hormonas esteroides regulan el metabolismo y las funciones de reproducción; los glucolípidos actúan como receptores de membrana; los eicosanoides poseen un papel destacado en la comunicación celular, inflamación, respuesta inmune, etc.
Función transportadora. El transporte de lípidos desde el intestino hasta su lugar de destino se realiza mediante su emulsión gracias a los ácidos biliares y a las lipoproteínas.
FUNCIONES DE LOS LÍPIDOS

LOS AMINOÁCIDOS
Un aminoácido, como su nombre indica, es una molécula orgánica con un grupo amino (-NH2) y un grupo carboxílico (-COOH; ácido). Los aminoácidos más frecuentes y de mayor interés son aquellos que forman parte de las proteínas. Dos aminoácidos se combinan en una reacción de condensación que libera agua formando un enlace peptídico. Estos dos "residuos" aminoacídicos forman un dipéptido. Si se une un tercer aminoácido se forma un tripéptido y así, sucesivamente, para formar un polipéptido. Esta reacción ocurre de manera natural en los ribosomas, tanto los que están libres en el citosol como los asociados al retículo endoplasmático.

LOS AMINOÁCIDOS
20 aminoácidos diferentes son los componentes esenciales de las proteínas.
. Las plantas pueden sintetizar todos los aminoácidos, nuestro cuerpo solo sintetiza 16, aminoácidos, éstos, que el cuerpo sintetiza reciclando las células muertas a partir del conducto intestinal y catabolizando las proteínas dentro del propio cuerpo.

ESTRUCTURA GENERAL DE UNA MOLÉCULA DE AMINOÁCIDO

Los alimentos que ingerimos nos proveen proteínas. Pero tales proteínas no se absorben normalmente en tal constitución sino que, luego de su desdoblamiento ("hidrólisis" o rotura), causado por el proceso de digestión, atraviesan la pared intestinal en forma de aminoácidos y cadenas cortas de péptidos, según lo que se denomina " circulación entero hepática".Esas sustancias se incorporan inicialmente al torrente sanguíneo y, desde allí, son distribuídas hacia los tejidos que las necesitan para formar las proteínas, consumidas durante el ciclo vital.
DEGRADACIÓN DE LAS PROTEINAS A AMINOÁCIDOS PARA EL APROVECHAMIENTO DEL ORGANISMO

Se sabe que de los 20 aminoácidos proteicos conocidos, 8 resultan indispensables (o esenciales) para la vida humana y 2 resultan "semi indispensables". Son estos 10 aminoácidos los que requieren ser incorporados al organismo en su cotidiana alimentación y, con más razón, en los momentos en que el organismo más los necesita: en la disfunción o enfermedad. Los aminoácidos esenciales más problemáticos son el triptófano, la lisina y la metionina. Es típica su carencia en poblaciones en las que los cereales o los tubérculos constituyen la base de la alimentación. Los déficit de aminoácidos esenciales afectan mucho más a los niños que a los adultos.
Hay que destacar que, si falta uno solo de ellos (Aminoácido esenciales) no será posible sintetizar ninguna de las proteínas en la que sea requerido dicho aminoácido. Esto puede dar lugar a diferentes tipos de desnutrición, según cuál sea el aminoácido limitante.
Se sabe que de los 20 aminoácidos proteicos conocidos, 8 resultan indispensables (o esenciales) para la vida humana y 2 resultan "semi indispensables". Son estos 10 aminoácidos los que requieren ser incorporados al organismo en su cotidiana alimentación y, con más razón, en los momentos en que el organismo más los necesita: en la disfunción o enfermedad. Los aminoácidos esenciales más problemáticos son el triptófano, la lisina y la metionina. Es típica su carencia en poblaciones en las que los cereales o los tubérculos constituyen la base de la alimentación. Los déficit de aminoácidos esenciales afectan mucho más a los niños que a los adultos.
CLASES DE AMINOÁCIDOS


Isoleucina, LeucinaLisinaMetioninaFenilalaninaTriptofano TreoninaValina
Hay que destacar que, si falta uno solo de ellos (Aminoácido esenciales) no será posible sintetizar ninguna de las proteínas en la que sea requerido dicho aminoácido. Esto puede dar lugar a diferentes tipos de desnutrición, según cuál sea el aminoácido limitante.
8 AMINOÁCIDOS ESENCIALES

LOS AMINOÁCIDOS ESENCIALES Y SU FUNCIÓN
Isoleucina: Función: Junto con la L-Leucina y la Hormona del Crecimiento intervienen en la formación y reparación del tejido muscular. Leucina: Función: Junto con la L-Isoleucina y la Hormona del Crecimiento (HGH) interviene con la formación y reparación del tejido muscular. Lisina: Función: Es uno de los más importantes aminoácidos porque, en asociación con varios aminoácidos más, interviene en diversas funciones, incluyendo el crecimiento, reparación de tejidos, anticuerpos del sistema inmunológico y síntesis de hormonas. Metionina: Función: Colabora en la síntesis de proteínas y constituye el principal limitante en las proteínas de la dieta. El aminoácido limitante determina el porcentaje de alimento que va a utilizarse a nivel celular.

LOS AMINOÁCIDOS ESENCIALES Y SU FUNCIÓN
Fenilalanina: Función: Interviene en la producción del Colágeno, fundamentalmente en la estructura de la piel y el tejido conectivo, y también en la formación de diversas neurohormonas. Triptófano: Función: Está inplicado en el crecimiento y en la producción hormonal, especialmente en la función de las glándulas de secreción adrenal. También interviene en la síntesis de la serotonina, neurohormona involucrada en la relajación y el sueño. Treonina: Función: Junto con la L-Metionina y el ácido Aspártico ayuda al hígado en sus funciones generales de desintoxicación. Valina: Función: Estimula el crecimiento y reparación de los tejidos, el mantenimiento de diversos sistemas y balance de nitrógeno.

LOS AMINOÁCIDOS NO ESENCIALES Y SU FUNCIÓN
Alanina: Función: Interviene en el metabolismo de la glucosa. La glucosa es un carbohidrato simple que el organismo utiliza como fuente de energía. Arginina: Función: Está implicada en la conservación del equilibrio de nitrógeno y de dióxido de carbono. También tiene una gran importancia en la producción de la Hormona del Crecimiento, directamente involucrada en el crecimiento de los tejidos y músculos y en el mantenimiento y reparación del sistema inmunologico. Asparagina: Función: Interviene específicamente en los procesos metabólicos del Sistema Nervioso Central (SNC). Acido Aspártico: Función: Es muy importante para la desintoxicación del Hígado y su correcto funcionamiento. El ácido L- Aspártico se combina con otros aminoácidos formando moléculas capases de absorber toxinas del torrente sanguíneo.

LOS AMINOÁCIDOS NO ESENCIALES Y SU FUNCIÓN
Cisteina: Función: Junto con la L- cistina, la L- Cisteina está implicada en la desintoxicación, principalmente como antagonista de los radicales libres. También contribuye a mantener la salud de los cabellos por su elevado contenido de azufre. Glutamina: Función: Nutriente cerebral e interviene específicamente en la utilización de la glucosa por el cerebro. Acido Glutáminico: Función: Tiene gran importancia en el funcionamiento del Sistema Nervioso Central y actúa como estimulante del sistema inmunologico. Glicina: Función: En combinación con muchos otros aminoácidos, es un componente de numerosos tejidos del organismo.

LOS AMINOÁCIDOS NO ESENCIALES Y SU FUNCIÓN
Histidina: Función: En combinación con la hormona de crecimiento (HGH) y algunos aminoácidos asociados, contribuyen al crecimiento y reparación de los tejidos con un papel específicamente relacionado con el sistema cardio-vascular. Serina: Función: Junto con algunos aminoácidos mencionados, interviene en la desintoxicación del organismo, crecimiento muscular, y metabolismo de grasas y ácidos grasos. Tirosina: Función: Es un neurotransmisor directo y puede ser muy eficaz en el tratamiento de la depresión, en combinación con otros aminoácidos necesarios. Prolina: Función: Está involucrada también en la producción de colágeno y tiene gran importancia en la reparación y mantenimiento del músculo y huesos.

Productos naturales que contienen las cantidades medias de aminoácidos que se usan en realidad a
nivel celular
Almendras (1 taza) 1.00 gr. Semillas de girasol crudas (1 taza) 1.28 gr. Arroz Integral (1 taza) 0.47 gr. Cebada (1 taza) 0.90 gr. Guisantes (1 taza) 0.27 gr. Habichuelas rojas (1 taza) 0.85 gr. Semillas de Ajonjolí (1 taza) 0.89 gr. Pan integral (1 rebanada) 0.14 gr. Spaghetti Harina Integral (1 taza) 0.65 gr. Todos los demás vegetales (1 taza) 0.27 gr.
CANTIDADES EN GRAMOS

Productos naturales que contienen las cantidades medias de aminoácidos que se usan en realidad a
nivel celular
Leche (1 taza) 0.29 gr. Una clara de huevo 1.63 gr. Huevo completo (aminoácidos limitantes) 0.70 gr. Pescado (1/4 libra) 0.21 gr. Hígado (1/4 libra) 0.78 gr. Queso blanco (1/4 taza) 0.26 gr. Carne de res (1/2 libra) 1.49 gr. Carne de cerdo (1/4 libra) 0.69 gr. Pavo (1/4 libra) utilización muy limitada de aminoácidos. gr. Pollo (1/4 libra) 0.95 gr. Cordero o Cabro (1/2 libra) 1.54 gr.
CANTIDADES EN GRAMOS

CÁLCULO DE LA CANTIDAD MEDIA DE AMINOÁCIDOS QUE NECESITAMOS LOS SERES HUMANOS
Para saber la cantidad media de aminoácidos que necesitamos al día, se multiplica el peso corporal en kilos (1000 gramos) 0.12 %.La libra americana es de 450 gramos. Si el peso son 146 libras multiplica por 450 gramos y luego los divide por 1000 da el peso en kilos.Ejemplo: una persona que pesa 146 libras americanas, lo multiplicado por 450 gramos es igual a 65700 y lo dividimos por 1000 es igual a 65.70 kilos. 146 x 450 = 65.700 gramos 65.700 - 1000 = 65.70 kilos.

LAS PROTEÍNAS
Las proteínas son macromoléculas formadas por cadenas lineales de aminoácidos. El nombre proteína proviene de la palabra griega πρώτα ("proteios"), que significa "primario" o del dios Proteo, por la cantidad de formas que pueden tomar.Las proteínas desempeñan un papel fundamental para la vida y son las biomoléculas más versátiles y más diversas. Son imprescindibles para el crecimiento del organismo.

LAS PROTEÍNAS
En otras palabras, las proteínas son macromoléculas compuestas por carbono, hidrógeno, oxígeno y nitrógeno. La mayoría también contienen azufre y fósforo. Las mismas están formadas por la unión de varios aminoácidos, unidos mediante enlaces peptídicos. El orden y disposición de los aminoácidos en una proteína depende del código genético, ADN, de la persona.

LAS PROTEÍNAS
El conjunto de los aminoácidos esenciales sólo está presente en las proteínas de origen animal.
En la mayoría de los vegetales siempre hay alguno que no está presente en cantidades suficientes. Se define el valor o calidad biológica de una determinada proteína por su capacidad de aportar todos los aminoácidos necesarios para los seres humanos.

LAS PROTEÍNAS
Las proteínas constituyen alrededor del 50% del peso seco de los tejidos y no existe proceso biológico alguno que no dependa de la participación de este tipo de sustancias.

Ser esenciales para el crecimiento. Las grasas y carbohidratos no las pueden sustituir, por no contener nitrógeno. Proporcionan los aminoácidos esenciales fundamentales para la síntesis tisular. Son materia prima para la formación de los jugos digestivos, hormonas, proteínas plasmáticas, hemoglobina, vitaminas y enzimas. Funcionan como amortiguadores, ayudando a mantener la reacción de diversos medios como el plasma. Actúan como catalizadores biológicos acelerando la velocidad de las reacciones químicas del metabolismo. Son las enzimas.
Las funciones principales de las proteínas

Actúan como transporte de gases como oxígeno y dióxido de carbono en sangre. (hemoglobina). Actúan como defensa, los anticuerpos son proteínas de defensa natural contra infecciones o agentes extraños.Permiten el movimiento celular a través de la miosina y actina (proteínas contráctiles musculares). Resistencia. El colágeno es la principal proteína integrante de los tejidos de sostén.
Las funciones principales de las proteínas
Energéticamente, las proteínas aportan al organismo 4 Kcal de energía por cada gramo
que se ingiere.

CLASIFICACIÓN DE LAS PROTEÍNAS
Proteínas simples: Producen solo aminoácidos al ser hidrolizados.Albúminas y globulinas: Son solubles en agua y soluciones salinas diluidas (ej.: lactoalbumina de la leche).Glutelinas y prolaninas: Son solubles en ácidos y álcalis, se encuentran en cereales fundamentalmente el trigo. El gluten se forma a partir de una mezcla de gluteninas y gliadinas con agua.Albuminoides: Son insolubles en agua, son fibrosas, incluyen la queratina del cabello, el colágeno del tejido conectivo y la fibrina del coagulo sanguíneo.Proteínas conjugadas: Son las que contienen partes no proteicas. Ej.: nucleoproteínas.Proteínas derivadas: Son producto de la hidrólisis.

En el metabolismo, el principal producto final de las proteínas es el amoníaco (NH3) que luego se convierte en urea (NH2)2CO2 en el hígado y se excreta a través de la orina.


SÍNTESIS DE LAS PROTEÍNAS
Se conoce como síntesis de proteínas al proceso por el cual se componen nuevas proteínas a partir de los veinte aminoácidos esenciales. En este proceso, se transcribe el ADN en ARN. La síntesis de proteínas se realiza en los ribosomas situados en el citoplasma celular.
En el proceso de síntesis, los aminoácidos son transportados por ARN de transferencia correspondiente para cada aminoácido hasta el ARN mensajero donde se unen en la posición adecuada para formar las nuevas proteínas. Al finalizar la síntesis de una proteína, se libera el ARN mensajero y puede volver a ser leído, incluso antes de que la síntesis de una proteína termine, ya puede comenzar la siguiente, por lo cual, el mismo ARN mensajero puede utilizarse por varios ribosomas al mismo tiempo.

La realización de la biosíntesis de las proteínas, se divide en las siguientes fases: 1. Fase de activación de los aminoácidos.2. Fase de traducción que comprende:
• Inicio de la síntesis proteica.• Elongación de la cadena polipeptídica.• Finalización de la síntesis de proteínas.
3. Asociación de cadenas polipeptídicas y, en algunos casos, grupos prostésicos para la constitución de las proteínas.
FASES DE LA SÍNTESIS DE PROTEÍNAS

FASES DE LA SÍNTESIS DE PROTEÍNAS

LA RESPIRACIÓN CELULAR
La respiración celular, es la degradación de biomoléculas (glucosa, lípidos, proteínas) para que se produzca la liberación de energía necesaria, y así el organismo pueda cumplir con sus funciones vitales.
Este proceso es utilizado por la mayoría de las células animales y vegetales,

LA RESPIRACIÓN CELULAR
Mediante la degradación de la glucosa (glucólisis) se forma ácido pirúvico. Este ácido se desdobla a dióxido de carbono y agua, generándose 36 moléculas de ATP.

LA GLICÓLISIS
La glucólisis o glicolisis (del griego glycos, azúcar y lysis, ruptura), es la vía metabólica encargada de oxidar la glucosa con la finalidad de obtener energía para la célula. Consiste en 10 reacciones enzimáticas consecutivas que convierten a la glucosa en dos moléculas de piruvato, el cual es capaz de seguir otras vías metabólicas y así continuar entregando energía al organismo.[

LA RESPIRACIÓN CELULAR
LA GLICÓLISIS
Durante la glucólisis se obtiene un rendimiento neto de dos moléculas de ATP y dos moléculas de NADH; el ATP puede ser usado como fuente de energía para realizar trabajo metabólico, mientras que el NADH puede tener diferentes destinos. Puede usarse como fuente de poder reductor en reacciones anabólicas; si hay oxígeno, puede oxidarse en la cadena respiratoria, obteniéndose tres ATPs; si no hay oxígeno, se usa para reducir el piruvato a lactato (fermentación láctica), o a CO2 y etanol (fermentación alcohólica), sin obtención adicional de energía.

LA GLICÓLISIS
Las funciones de la glucólisis son:1.La generación de moléculas de alta energía (ATP y NADH) como fuente de energía celular en procesos de respiración aeróbica (presencia de oxígeno) y fermentación (ausencia de oxígeno). 2.La generación de piruvato que pasará al ciclo de Krebs, como parte de la respiración aeróbica. 3.La producción de intermediarios de 6 y 3 carbonos que pueden ser utilizados en otros procesos celulares.

LA GLICÓLISIS

LA GLICÓLISIS
En la respiración aeróbica, la degradación de glucosa comprende una serie de reacciones. Sin embargo, la ecuación química general se puede representar con la siguiente fórmula, inversa a la de la fotosíntesis:

LA RESPIRACIÓN CELULAR
La respiración celular puede dividirse en dos tipos, según sea la presencia de oxígeno.
Respiración aerobia o aeróbica
Respiración anaerobia o anaeróbica

LA RESPIRACIÓN CELULAR
Respiración aerobia o aeróbica: hace uso del O2 como aceptor último de los electrones desprendidos de las sustancias orgánicas. Es la forma más extendida de respiración, propia de la mayoría de las bacterias y de los organismos eucariotas. Es por ello que a los seres que requieren de oxígeno se los llama aerobios

LA RESPIRACIÓN CELULAR
-Respiración anaerobia o anaeróbica: no interviene el oxígeno, sino que se emplean otros aceptores finales de electrones, generalmente minerales. La respiración anaeróbica está presente en algunos organismos procariotas, en general habitantes de suelos y sedimentos, y de vital importancia en los ciclos biogeoquímicos de los elementos. Al no requerir de oxígeno se los denomina anaerobios.

LA RESPIRACIÓN CELULAR

LA RESPIRACIÓN CELULAR
Mediante la respiración celular, el ácido pirúvico formado en la glucólisis se oxida completamente a CO2 y agua en presencia de oxígeno. Se desarrolla en dos etapas sucesivas: el ciclo de Krebs y la cadena respiratoria de transporte electrónico, asociada a la fosforilación oxidativa.
El ciclo de Krebs

LA RESPIRACIÓN CELULAR
Lo primero que ocurre tras la glucólisis es que el ácido pirúvico pasa desde el citoplasma a la matriz mitocondrial, atravesando las membranas. El ácido pirúvico sufre una oxidación, se libera una molécula de CO2 y se forma un grupo acilo (CH3-CO). En esta reacción se forma una molécula de NADH. Como en la glucólisis el producto final eran dos moléculas de ácido pirúvico, lógicamente se formarán ahora dos de NADH por cada molécula de glucosa. Cada grupo acilo se une a un Coenzima A y se forma acetilCoenzimaA. En este momento empieza el ciclo de Krebs.

LA RESPIRACIÓN CELULAR

LA RESPIRACIÓN CELULAR

LA RESPIRACIÓN CELULAR
En las células eucariotas el ciclo de Krebs tiene lugar en la matriz de la mitocondria en presencia de oxígeno. La membrana mitocondrial externa es permeable a la mayoría de las moléculas de pequeño tamaño, sin embargo la interna tiene una permeabilidad selectiva y controla el movimiento de iones hidrógeno.

LA RESPIRACIÓN CELULAR

LA RESPIRACIÓN CELULAR
CICLO DE KREBS

FASES DE LA SÍNTESIS DE PROTEÍNAS

LA RESPIRACIÓN CELULARCICLO DE KREBS

LA RESPIRACIÓN CELULAR

FASES DE LA SÍNTESIS DE PROTEÍNAS

FASES DE LA SÍNTESIS DE PROTEÍNAS

FASES DE LA SÍNTESIS DE PROTEÍNAS

FASES DE LA SÍNTESIS DE PROTEÍNAS