Enseñanza de la nomenclatura de química inorgánica como ...
Transcript of Enseñanza de la nomenclatura de química inorgánica como ...

Enseñanza de la nomenclatura de
química inorgánica como lenguaje
científico especializado en el área de
química
María Mónica Cabrera Casadiego
Universidad Nacional De Colombia
Facultad De Ciencias
Maestría En Enseñanza De Las Ciencias Exactas Y Naturales
Bogotá
2020


Enseñanza de la nomenclatura de
química inorgánica como lenguaje
científico especializado en el área de
química
María Mónica Cabrera Casadiego
Tesis o trabajo de investigación presentada(o) como requisito parcial para optar al título
de:
Magister en Enseñanza de la Ciencias Exactas y Naturales
Director
Orlando Hernández Fandiño
Magister en Ciencias - Química
Universidad Nacional De Colombia
Facultad De Ciencias
Maestría En Enseñanza De Las Ciencias Exactas Y Naturales
Bogotá
2020


Agradecimientos
A mis padres, que siempre han estado conmigo apoyándome para salir siempre
adelante.
A mis hermanas, Luz y Laura, quienes han sido mi palanca para poder realizar este
trabajo.
Al profesor Orlando, quien con su paciencia y consejo me ayudó a sacar a flote este
proyecto.
A Daniel, quien con su apoyo e insistencia me motivó para poder terminar.
A mis estudiantes y compañeros de trabajo, quienes permitieron que llevara a cabo mi
trabajo de grado.


Resumen
La tesis propone una estrategia didáctica, centrada en la enseñanza-aprendizaje de la
nomenclatura en química inorgánica, el cual es un lenguaje especializado muy propio de
esta disciplina. En el cual es necesario el poder comprender el nombre de los distintos
compuestos en un nivel global, teniendo en cuenta sus reglas de acuerdo con la Unión
Internacional de Química Pura y Aplicada (IUPAC). Se realizó teniendo como contexto el
Centro Educativo Rural San José de Castro, ubicado en el Corregimiento de Castro del
municipio de Arboledas (Norte de Santander).
La estrategia didáctica fue aplicada en 35 estudiantes del grado decimo, en el área de
química, siendo la docente autora de esta tesis. Se trata de pasar de unas formas
pedagógicas memorísticas y mecánicas a otras activas y relacionadas con los entornos
cotidianos y vivenciales de los alumnos. La metodología utilizada fue descriptiva con un
enfoque cualitativo; observándose que, mediante la aplicación de diversos ejercicios de
nomenclatura con los estudiantes, hubo progreso en la apropiación del lenguaje de la
química inorgánica, enfocándose primordialmente en identificar la presencia de
compuestos químicos en su vida cotidiana.
Palabras claves: Nomenclatura, química inorgánica, estrategia didáctica, aprendizaje
activo y aprendizaje situado.


Abstract
The thesis proposes a didactic strategy, focused on the teaching-learning of the
nomenclature in inorganic chemistry, which is a specialized language very typical of this
discipline. In which it is necessary to be able to understand the name of the different
compounds on a global level, taking into account their rules according to the International
Union of Pure and Applied Chemistry (IUPAC). It was carried out with the context of the
San José of Castro Rural Educational Center, located in the Castro District of the
municipality of Arboledas (North of Santander).
The didactic strategy was applied in 35 students of the tenth grade, in the area of chemistry,
being the teacher author of this thesis. It is about moving from a rote learning and
mechanical pedagogical forms to other active and related to the daily and experiential
environments of the students. The methodology used was descriptive with a qualitative
approach; observing that, through the application of various nomenclature exercises with
the students, there was progress in the appropriation of the language of inorganic
chemistry, focusing primarily on identifying the presence of chemical compounds in their
daily lives.
Keywords: Nomenclature, inorganic chemistry, didactic strategy, active learning and
situated learning.


Contenido
Resumen ............................................................................................................................ VII
Contenido ........................................................................................................................... XI
Lista de figuras ................................................................................................................ XIII
Lista de tablas ...................................................................................................................XV
Introducción ........................................................................................................................ 1
1. Aspectos preliminares ................................................................................................... 5 1.1 Identificación del problema ................................................................................. 5
1.1.1 Antecedentes ........................................................................................ 5 1.1.2 Descripción del problema ..................................................................... 6 1.1.3 Formulación de la pregunta problema .................................................. 8
1.2 Justificación ......................................................................................................... 8 1.3 Objetivos .............................................................................................................. 9
1.3.1 Objetivo general .................................................................................... 9 1.3.2 Objetivos específicos ............................................................................ 9
2. Marco referencial .......................................................................................................... 11 2.1 Marco teórico ..................................................................................................... 11
2.1.1 Conceptos preliminares. ..................................................................... 11 2.1.2 Epistemología de la nomenclatura de química inorgánica. ............... 13 2.1.3 Nomenclatura de química inorgánica ................................................. 16 2.1.4 Enseñanza de la nomenclatura química. ........................................... 32 2.1.5 Aprendizaje Activo. ............................................................................. 32 2.1.6 Cognición situada................................................................................ 32 2.1.7 Enseñanza de la química. .................................................................. 33 2.1.8 Estándares de competencias y derechos básicos de aprendizaje ................................................................................................... 33
3. Metodología ................................................................................................................... 35 3.1 Tipo de investigación ......................................................................................... 35 3.2 Población ........................................................................................................... 35 3.3 Etapas del proceso de enseñanza .................................................................... 36
3.3.1 Selección información. ........................................................................ 36 3.3.2 Diseño prueba diagnóstica. ................................................................ 36 3.3.3 Contenido y estructura de la estrategia didáctica. ............................. 36 3.3.4 Desarrollo de la estrategia didáctica. ................................................. 36 3.3.5 Evaluación ........................................................................................... 36

XII Contenido
4. Resultados y análisis de resultados .......................................................................... 39 4.1 Selección información ....................................................................................... 39 4.2 Prueba diagnóstica ............................................................................................ 39 4.3 Contenido y estructura de la estrategia didáctica ............................................. 42 4.4 Evaluación ......................................................................................................... 45
5. Conclusiones y recomendaciones ............................................................................. 52 5.1 Conclusiones ..................................................................................................... 52 5.2 Recomendaciones ............................................................................................. 54
A. Anexo: Guías utilizadas en la enseñanza de la nomenclatura inorgánica ........... 56
B. Anexo: Prueba final ..................................................................................................... 59
Referencias bibliográficas ............................................................................................... 61

Lista de figuras
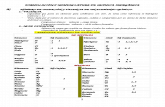
Figura 1. Fórmulas estructurales de algunos compuestos inorgánicos. .................... 13
Figura 2. Símbología planteada por Dalton (1810) ..................................................... 15
Figura 3. Prueba diagnóstica aplicada ........................................................................ 40
Figura 4. Actividad de apropiación .............................................................................. 44
Figura 5. Desarrollo actividad de apropiación ............................................................. 44


Lista de tablas
Tabla 1. Nomenclatura de hidruros metálicos ........................................................... 18
Tabla 2. Nomenclatura Stock óxidos ......................................................................... 20
Tabla 3. Nomenclatura sistemática óxidos ................................................................ 21
Tabla 4. Nomenclatura tradicional óxidos .................................................................. 21
Tabla 5. Nomenclatura Stock hidróxidos ................................................................... 24
Tabla 6. Nomenclatura sistemática hidróxidos .......................................................... 24
Tabla 7. Nomenclatura tradicional hidróxidos ............................................................ 24
Tabla 8. Nomenclatura hidrácidos ............................................................................. 25
Tabla 9. Nombres tradicionales y Stock de los ácidos oxigenados del cloro (oxiácidos) ...................................................................................................................... 27
Tabla 10. Nomenclatura sistemática de oxiácidos del cloro ....................................... 28
Tabla 11. Nomenclatura Stock para las sales binarias ............................................... 29
Tabla 12. Nomenclatura sistemática para las sales binarias ...................................... 29
Tabla 13. Nomenclatura tradicional para las sales binarias ........................................ 29
Tabla 14. Nomenclatura Stock de oxisales ................................................................. 30
Tabla 15. Nomenclatura tradicional oxisales ............................................................... 31
Tabla 16. Resultados obtenidos en la aplicación de la prueba diagnóstica ............... 41
Tabla 17. Resultados obtenidos de relacionar los términos de la izquierda con las definiciones ...................................................................................................................... 45
Tabla 18. Identificación de grupos funcionales (óxidos, hidróxidos, ácidos y sales) .. 46
Tabla 19. Resultados de nombrar los óxidos según la nomenclatura tradicional ....... 46

XVI Contenido
Tabla 20. Resultados de nombrar los óxidos según la nomenclatura sistemática ..... 47
Tabla 21. Resultados de nombrar los óxidos según la nomenclatura Stock .............. 47
Tabla 22. Resultados a la pregunta sobre relacionar el compuesto con su nombre
correspondiente .................................................................................................................. 48
Tabla 23. Resultados identificación de un catión o un anión ...................................... 48
Tabla 24. Resultados identificación de los compuestos inorgánicos estudiados (óxidos, ácidos, hidróxidos y sales), en un producto de uso diario. .................................. 49

Introducción
Durante el desarrollo del plan de área de Ciencias Naturales Química, una de las temáticas
a tratar es la enseñanza de la nomenclatura de química inorgánica. Según Araque y Mazo
(2015): “La nomenclatura química puede considerarse como un lenguaje y desde este
punto de vista está constituida por palabras que obedecen las reglas de la sintaxis.” Es
decir, que para que los estudiantes puedan aplicar estas normas correctamente, deben
aprender el lenguaje de la química, lenguaje que muchas veces, debido a la metodología
empleada por los docentes se vuelve un proceso mecánico y memorístico, sin permitir que
estos sean relacionados por los alumnos en procesos de su entorno y vida cotidiana.
(Hernández Fandiño, 2011)
El aprendizaje de la nomenclatura en la escuela secundaria y en la universidad ha sido
objeto de grandes controversias debido no sólo al fracaso observado en la adquisición de
este lenguaje por parte de los estudiantes sino también al rechazo que los mismos
muestran hacia dicho aprendizaje (Laurella, 2015). Según Triana Beltrán (2016), se
evidencia que en la competencia de lectura y comprensión de cualquier tipo de texto en
los jóvenes de la actualidad se ha visto deteriorada por muchos factores, entre ellos la
limitación que hay en el aprendizaje de conceptos científicos básicos, lo que determina que
los jóvenes no alcanzan niveles de comprensión y explicación de los fenómenos naturales
acordes a los años de formación recibida.
Actualmente los jóvenes son apáticos a desarrollar la lectura de libros, según cifras del
2016 en la encuesta de consumo cultural del DANE, solo un 47,5 % de personas mayores
de 12 años leyeron libros en el último año, lo cual da como resultado un promedio de 4,3
libros leídos en el año (DANE, 2017). Esta apatía se ve reflejada igualmente en la lectura
de textos científicos, haciendo que los conceptos básicos de este lenguaje no sean
comprendidos. Es por ello por lo que, como docente de química, se deben de implementar

2 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
estrategias para que los estudiantes puedan construir un lenguaje científico, especialmente
en la nomenclatura de compuestos inorgánicos.
En el presente trabajo se implementa una estrategia didáctica que permita a los
estudiantes adquirir un lenguaje especializado a partir del aprendizaje de la nomenclatura
de compuestos inorgánicos, a través del aprendizaje activo y la enseñanza situada. Para
lograrlo, este se basa en experiencias previas, y en procesos de investigación que se han
desarrollado en torno al tema. De la misma forma, busca que mediante dicha estrategia
los educandos logren identificar y aplicar las reglas en la nomenclatura inorgánica y
relacionar las sustancias inorgánicas que encuentran en el diario vivir.
Dentro de la revisión bibliográfica se encontraron trabajos previos que abordan la
enseñanza de la nomenclatura química, así como algunas estrategias que permitan
adquirir este lenguaje de forma más práctica para los estudiantes. Según Bernadelli (2015):
“numerosas investigaciones reflejan que algunas dificultades surgen debido a problemas
en la comunicación dentro del aula por desconocimiento del lenguaje específico disciplinar
por parte de los estudiantes”.
Igualmente, se reconoce que la nomenclatura está dada por unas normas establecidas por
la IUPAC (International Union of Pure and Applied Chemistry), la cual ha realizado algunas
recomendaciones para la nomenclatura de la química inorgánica, pero es flexible en el
nombramiento de los ácidos inorgánicos, dado que con frecuencia el estudiante se pude
confundir al utilizar una nomenclatura sistemática (IUPAC) y al mismo tiempo interactuar
en la vida cotidiana con sustancias que se nombran de forma radicalmente diferente
(Araque Marín & Mazo Lopera, 2015).
En cuanto al lenguaje en la química, se refiere a todos los elementos lingüísticos y no
lingüísticos que los químicos utilizan para expresar lo que se quiere decir sobre el mundo
de las sustancias y sus transformaciones, por tanto, es un lenguaje particularmente
diferente de otros lenguajes en ciencias. Incluye, por lo menos, el simbolismo químico
(Dalton, Berzelius) y las fórmulas químicas, y es a partir de estos elementos que se
transforma en un lenguaje especializado.

Introducción 3
Puesto que un lenguaje en general es la forma de comunicar el pensamiento y las
emociones, “Cuando se habla de lenguaje de la ciencia se refiere a un uso sociocultural
específico que permite comunicar las búsquedas, los procesos, los descubrimientos, los
resultados de la actividad científica a una comunidad tanto especializada como no
especializada, el cual es primordialmente escrito y requiere un descentramiento de la
escritura personal para dar paso a la escritura académica que se adecua, generalmente,
a la tipología de texto expositivo-argumentativo” (Cisneros Estupiñan, 2011).


1. Aspectos preliminares
1.1 Identificación del problema
1.1.1 Antecedentes
Las propuestas sobre la enseñanza de la nomenclatura de química inorgánica abundan en
la bibliografía, un ejemplo está el realizado por Cantillo (2016) la cual propone el diseño de
una unidad didáctica integradora como estrategia para mejorar el proceso de enseñanza y
aprendizaje en el tema de nomenclatura de química inorgánica, teniendo en cuenta los
conceptos del modelo didáctico integrador, en la cual presentó resultados positivos por
parte de los estudiantes, con respecto a la identificación de sustancias químicas
inorgánicas en su entorno cotidiano y la importancia de conocer cómo se nombran,
basándose en la estructura del aprendizaje situado. Igualmente, se presenta la ponencia
de Araque y Mazo (2015) en el encuentro internacional de educación en ingeniería, en la
cual se construyó una estrategia didáctica potencialmente significativa, la cual se centró
en el entendimiento de los ácidos oxácidos, orientada en criterios pedagógicos y didácticos
correspondientes para facilitar la comprensión de la nomenclatura inorgánica tradicional
de forma significativa, obteniendo que es posible relacionar la nomenclatura IUPAC y la
nomenclatura tradicional.
En el trabajo de Pinzón (2016), se llevó a cabo un diagnóstico inicial en el cual se pudo
determinar las falencias de los jóvenes, y a su vez se diseñó una estrategia didáctica de
aprendizaje, mediante la elaboración de una cartilla y juegos que permitieron reforzar el
tema de nomenclatura química, y obtener con ello un mayor de parte de los estudiantes
hacia el tema en cuestión.
En cuanto a la enseñanza del lenguaje científico se pueden encontrar diferentes referentes,
según Borsese (2000) el lenguaje químico “es específico, ya que cada símbolo encierra un
número elevado de significados, no sólo da nombres a las transformaciones de la materia

6 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
a nivel macro y microscópico, sino que los registra, codifica y convierte en elementos de
pensamiento y comunicación”. Algunos estudios han mostrado que debido a que el
lenguaje de la química no es un lenguaje basado solo en conceptos, sino que a su vez es
gráfico y algunas veces matemático, es bastante confuso y difícil de entender, gracias a la
polisemia y la sinonimia, que en este se presenta (Montagut Bosque, 2010).
Según Mayeem, et al (2018), el uso de modelos conceptuales construidos localmente en
los colegios de Offinso y Atebubu Ghana, el cual tuvo como objetivo mejorar la
comprensión de los estudiantes de SHS en fórmulas químicas y nomenclatura. Mediante
la aplicación de pruebas diagnostico al inicio y al final en un grupo experimental y de control
con 200 estudiantes como tamaño de muestra. Cuyos resultados han demostrado que el
uso de modelos conceptuales mejora la comprensión de los profesores en prácticas en
fórmulas químicas y nomenclatura. Además, se descubrió que los modelos conceptuales
no tenían influencia sobre el género o la capacidad cognitiva.
1.1.2 Descripción del problema
La sede de secundaria del Centro Educativo Rural San José de Castro está ubicada en el
Corregimiento de Castro, a una distancia de 9 kilómetros del casco urbano del municipio
de Arboledas Departamento Norte de Santander. Ocupa un área de 1.200 m2. Es un
establecimiento educativo no certificado de carácter oficial, adscrita a la secretaría de
educación de Norte de Santander.
De acuerdo con la evaluación de su contexto, cuenta con una población de estudiantes
ubicados en el estrato uno y dos, se estima que el 75 % donde los padres no tienen ningún
grado de escolaridad, afectando en el acompañamiento de sus hijos a nivel educativo. De
igual forma esto conlleva al escaso cumplimiento de las labores escolares reflejándose en
el bajo rendimiento académico.
Los jóvenes especialmente los hombres en ocasiones se retiran del estudio para
colaborarles económicamente a sus padres y en el caso de las niñas para formar nuevas
familias a temprana edad, interrumpiendo su proyecto de vida.
Se presenta inestabilidad económica y emigración de familias debido a la falta de empleo
u ocupación que les permita generar recursos. Igualmente, debido a la situación de la

Aspectos preliminares 7
frontera se ha presentado un aumento de estudiantes procedentes de Venezuela, algunos
de los cuales no han definido su documentación. El contexto socio económico donde se
desenvuelven es muy limitado sin oportunidades de mejoramiento y de progreso. Sin
embargo, las tierras de este corregimiento son fértiles y prósperas.
Unido a estas condiciones, también se presentan cambios frecuentes de docentes, debido
a la búsqueda de mejores condiciones por parte de estos, ya sea en el ámbito familiar o
por cuestiones de salud. Estas situaciones han ocasionado que los jóvenes vean
interrumpidas de manera parcial sus actividades académicas y experimenten un cambio
en la metodología del docente, por lo que afecta los procesos de aprendizaje y formación
en competencias.
La asignatura de química en el centro consiste en una intensidad de cuatro clases de 50
min cada uno, durante la semana. Algunos de los cuales se ven interrumpidos debido a
una diversidad de actividades que se desarrollan en el colegio, como izadas de bandera,
eucaristías, charlas de diversas instituciones, actividades deportivas, culturales, entre
otras, las cuales ocasionan una pérdida en la continuidad del proceso. Igualmente, debido
a las grandes distancias que deben recorrer la mayoría de los estudiantes para poder llegar
al colegio y de regreso a sus casas, algunos de ellos caminando entre dos y tres horas, y
a lo extenuante de la jornada, es complicado el proceso de dejar actividades por fuera del
horario escolar, ya que es poco probable que sean desarrolladas. Así, todos los procesos
de enseñanza-aprendizaje y refuerzo de conocimientos se llevan a cabo en el aula escolar.
Todas estas variables hacen que los conceptos de nomenclatura de química inorgánica
sean considerados difíciles y complicados de entender en los estudiantes del grado
décimo. Según Gómez et al. (2008) son básicamente:
- Confusión de las reglas, aprendizaje memorístico sin comprensión y por tanto a corto
plazo.
- Aislamiento de los conceptos estudiados en distintos capítulos.
- El mito de la dificultad del estudio de la nomenclatura.

8 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
- En secundaria y posiblemente a nivel medio superior, el alumno no comprende las
razones de un lenguaje especial, puesto que no conoce la amplia gama de los compuestos
químicos y la necesidad de ese lenguaje.
- Se evalúan los exámenes por las respuestas correctas, y no se consideran las razones
por las que el alumno llega a una determinada conclusión.
1.1.3 Formulación de la pregunta problema
Como puede verse, hay varios motivos por los que el aprendizaje de los temas
relacionados con nomenclatura de química inorgánica, primeramente, que los estudiantes
debido a las dificultades presentadas en su formación presentan falencias en la
interpretación de las normas que se plantean para la nomenclatura de compuestos
inorgánicos. Igualmente, no relacionan lo visto en las clases con las sustancias que los
rodean en su entorno cotidiano.
Ante esta situación se plantea la siguiente pregunta: ¿Cómo se puede proponer una
estrategia didáctica centrada en el aprendizaje activo y la enseñanza situada para la
enseñanza aprendizaje de la nomenclatura de química inorgánica a los jóvenes del grado
décimo del Centro Educativo Rural San José de Castro?
1.2 Justificación
La mayoría de los eventos que ocurren en el entorno llevan a cabo procesos químicos, por
tanto, es una ciencia inherente al ser humano. Desde las partículas que componen el
cuerpo de los seres vivos y no vivos, hasta los grandes astros que se encuentran en el
universo, todo está conformado por materia. Por este motivo se debe incentivar en los
jóvenes el interés por aprender esta rama del conocimiento. Actualmente se encuentran
diversidad de herramientas que hacen que el proceso de aprendizaje de la química sea
mucho más significativo para los estudiantes.
Por esta razón, cada día se implementan nuevas estrategias que permiten al joven poder
desarrollar procesos de comprensión frente a la materia, haciendo de este un modelo más
dinámico y, por ende, haciendo que los estudiantes interioricen más los conceptos. Esto
da una ventaja al momento de aprender las normas para la nomenclatura de química

Aspectos preliminares 9
inorgánica, ya que puede hacerse de forma más lúdica, lo que facilita el proceso de
aprendizaje.
El planteamiento de una estrategia didáctica está basado en la observación del docente,
al identificarse una situación problema dentro del grupo de trabajo, se permite diseñar
distintas actividades que permitan solucionarlo, de acuerdo con los temas a tratar y el
grupo poblacional. En este caso, se llevó a cabo una serie de actividades pedagógicas que
permitieron a los estudiantes mejorar su aprendizaje y comprensión de la nomenclatura de
química inorgánica.
1.3 Objetivos
1.3.1 Objetivo general
Proponer una estrategia didáctica centrada en el aprendizaje activo y la enseñanza situada
para la enseñanza aprendizaje de la nomenclatura de química inorgánica a los jóvenes del
grado décimo del Centro Educativo Rural San José de Castro (Arboledas, Norte de
Santander)
1.3.2 Objetivos específicos
• Seleccionar los conceptos relacionados con nomenclatura de química inorgánica que
harán parte de la estrategia.
• Diseñar e implementar una prueba diagnóstica para evaluar los conocimientos previos
de los estudiantes.
• Proponer el contenido y la estructura de la estrategia.
• Desarrollar la estrategia didáctica utilizando el método de aprendizaje activo, y valiéndose
de objetos de la vida cotidiana (enseñanza situada) para la enseñanza de la nomenclatura
de química inorgánica.
• Evaluar el proceso cognitivo de los estudiantes sobre nomenclatura de química
inorgánica.


2. Marco referencial
2.1 Marco teórico
2.1.1 Conceptos preliminares.
Dentro de la enseñanza de la nomenclatura de química inorgánica, debemos tener claros
ciertos conceptos, los cuales nos brindan la información suficiente para poder nombrar los
distintos compuestos inorgánicos. Entre ellos están:
- Números de oxidación: Cada átomo de un compuesto se caracteriza por un estado de
oxidación (electrones ganados o perdidos con respecto al átomo aislado). El número que
indica este estado se llama número de oxidación del elemento en dicho compuesto. Es
positivo si se presenta una pérdida de electrones y negativo si hay ganancia de electrones.
El número de oxidación se define como la carga eléctrica formal (puede que no sea real)
que se asigna a un átomo en un compuesto. Para asignar el número de oxidación a cada
átomo en una especie química se emplea un conjunto de reglas, que se pueden resumir
del modo siguiente:
1. El número de oxidación de todos los elementos libres es cero, en cualquiera de las
formas en que se presenten: Ca, He, N2, P4, etc. En moléculas con átomos iguales, N2, H2,
etc., los electrones del enlace están compartidos equitativamente y no se pueden asignar
a ninguno de los átomos.
2. El número de oxidación de cualquier ion monoatómico es igual a su carga eléctrica. Así,
el número de oxidación del 𝑆2– es -2, de 𝐾+ es +1, los cuales coinciden con sus respectivas
cargas eléctricas.
3. El número de oxidación del hidrógeno (H) en sus compuestos es +1, excepto en los
hidruros, que es –1.

12 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
4. El número de oxidación del oxígeno (O) en sus compuestos es –2, excepto en los
peróxidos, que es –1 y superperóxidos -1/2
5. El número de oxidación de los metales alcalinos es siempre +1.
6. El número de oxidación de los metales alcalinotérreos es siempre +2.
7. El número de oxidación del flúor (F) en sus compuestos es siempre –1. El número de
oxidación de los demás halógenos varía desde ±1 a 7, siendo positivo cuando se combina
con el oxígeno o con otro halógeno más electronegativo.
8. La suma algebraica de los números de oxidación de los átomos de una molécula es
cero, y si se trata de un ion, es igual a la carga del ion.
- Número de oxidación y valencia: La valencia es la capacidad de formar enlaces. El
concepto de valencia resulta útil en la formulación de compuestos binarios, mientras que
el número de oxidación lo es en compuestos de tres o más elementos. Es importante
distinguir entre número de oxidación y valencia. Consideremos, por ejemplo, los siguientes
compuestos del carbono:
–4 –2 0 +4
𝐶𝐻4 𝐶𝐻3𝐶𝑙 𝐶𝐻2𝐶𝑙2 𝐶𝐶𝑙4
En todos ellos el carbono presenta invariablemente su valencia de cuatro, mientras que su
número de oxidación es distinto en cada compuesto (se indica encima de la fórmula).
- Fórmulas químicas: La fórmula química es una representación simbólica de la molécula
o unidad estructural de una sustancia en la que se indica la cantidad o proporción de
átomos que intervienen en el compuesto.
Tipos de fórmulas químicas:

Marco referencial 13
a. Fórmula molecular: indica el número y clase de átomos de una molécula. No da apenas
información de cómo están unidos los átomos. H2O, HCl, O2, F2
b. Fórmula estructural: se representa la ordenación de los átomos y cómo se enlazan
para formar moléculas. Ej. ácido sulfúrico, cloruro de hidrógeno, ácido fosfórico.
Figura 1. Fórmulas estructurales de algunos compuestos inorgánicos.
a) b) c)
a) Ácido sulfúrico (H2SO4) b) cloruro de hidrógeno (HCl) c) Ácido fosfórico (H3PO4)
c. Fórmula empírica: indica la proporción de los diferentes átomos que forman dicho
compuesto. Así el peróxido de hidrógeno se representa mediante la fórmula empírica 𝐻𝑂
y molecular 𝐻2𝑂2 El óxido fosfórico empírico 𝑃2𝑂5 molecular 𝑃4𝑂10 .
- Función química y grupo funcional: A excepción de los gases nobles, prácticamente
todos los elementos se combinan entre sí. Se conoce como función química a las
propiedades comunes que caracterizan a un grupo de sustancias que tienen estructura
semejante; es decir, que poseen un determinado grupo funcional. Y el grupo funcional,
determina las propiedades químicas de las sustancias de las cuales hacen parte. Los
compuestos que se clasifican dentro de una función química pueden tener diferentes
propiedades físicas y químicas. (Solís Correa, 2014).
2.1.2 Epistemología de la nomenclatura de química inorgánica.
Se puede hablar de nomenclatura de química inorgánica desde la Edad Antigua. En la
Edad Media con la alquimia y en la Edad Moderna donde se dan los más grandes aportes
generados por diferentes científicos dentro de los que se destacan Lavoisier, Dalton y
Berzelius, para la consolidación de la nomenclatura de química inorgánica y finalmente con
el surgimiento de la IUPAC en la Edad Contemporánea la cual se encarga de unificar por

14 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
medio de reglas los nombres de las sustancias inorgánicas. (Díaz Suarez, Vargas Rojas,
& Pérez Miranda, 2009).
A partir de sus estudios en mineralogía y química analítica, Bergman (1735 – 1784) planteó
que la química debía dividirse en dos partes, la química orgánica y la química inorgánica
(De Jaime Lorén, 2010). Lavoisier propuso los cimientos de la química, a la cual le da
forma, rigurosidad y lógica. Lavoisier y sus colaboradores propusieron entonces un sistema
de nomenclatura que tomó como base las reacciones de oxidación, las cuales los
condujeron a clasificar las sustancias en: Elementos (metales y no metales) y compuestos
(óxidos, ácidos, bases y sales). (Cantillo Maldonado, 2016).
En 1782 Guyton de Morveau (1737 – 1816) postuló un sistema de nomenclatura en el libro
Methode de Nomenclature Chimie en colaboración con Lavoisier y los demás autores,
publicado en 1787, que se convirtió rápidamente en el lenguaje internacional de la química
(Díaz Suarez, Vargas Rojas, & Pérez Miranda, 2009).
Por otro lado, en el lenguaje químico se hizo necesaria la representación gráfica de las
sustancias, es por esto por lo que muchos intentaron crear códigos escritos para tal fin.
Entre ellos se destacan Jean-Henry Hassenfratz (1755 - 1827) y Pierre Adet (1763 - 1832),
quienes plantearon el uso de un conjunto de símbolos (simbolismo) adaptada a la nueva
forma de nombrar y pensar acorde con los nuevos planteamientos hechos por Morveau y
sus colaboradores. (Cantillo Maldonado, 2016)
De igual forma, John Dalton (1766 - 1844) propuso representar los elementos y
compuestos químicos con símbolos (Círculos con un diseño interior para cada elemento),
pero este sistema no tuvo acogida debido a la dificultad de reproducirlos (Figura 1).
Berzelius (1779 - 1848) posteriormente propuso el uso de la primera letra mayúscula del
nombre del elemento para representarlo y, si dos elementos tenían la misma letra propuso
adicionar la segunda letra minúscula para diferenciarlos y así facilitar la escritura, por
ejemplo: carbono C, calcio Ca, cobalto Co. Esta simbología es la que se utiliza en la
actualidad.

Marco referencial 15
Figura 2. Simbología planteada por Dalton (1810)
Fuente. Tomado de SINC ciencias. Recuperado de: https://www.agenciasinc.es/Visual/Ilustraciones/3-de-septiembre-de-1803-primeros-simbolos-para-los-atomos-de-los-elementos

16 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
En el siglo XIX Arrhenius (1859 - 1927) centró su estudio en los iones y las moléculas,
generando la necesidad de nombrar las partículas cargadas y las neutras. Werner propuso
en 1920, un nuevo sistema de nomenclatura aditivo para los compuestos coordinados.
Este sistema fue acogido por la Unión Internacional de Química Pura y Aplicada, conocida
por sus siglas en ingles IUPAC, que agregó al nombre el número de oxidación del metal
ubicándolo al final y entre paréntesis, en número romanos, ejemplo: óxido de hierro(II),
óxido de hierro(III) (IUPAC, 2005). Este sistema es conocido como nomenclatura
Stock, los números romanos con paréntesis van pegados a la última del nombre ej.
Hierro(III) corresponde a Stock
2.1.3 Nomenclatura de química inorgánica
Dentro de los nombres de los compuestos químicos, podemos dividir arbitrariamente su
nomenclatura (más allá de que sean orgánicos o inorgánicos) en dos grandes clases:
- Nombres triviales: Corresponden a pocas sustancias, pero de amplio uso. Se aprenden
de forma memorística. Ejemplo: Agua, gas pimienta, sal de cocina.
- Nombres tradicionales: Sirven para nombrar una amplia gama de sustancias, aunque
no necesariamente conocidas. Dan información sobre la composición y la estructura de los
compuestos a los cuales refieren. Requieren el aprendizaje de reglas para su utilización.
Ej.: nitrato de sodio, trifluoruro de fósforo.
Según el libro rojo para nomenclatura de compuestos inorgánicos de la IUPAC (2005): “La
nomenclatura química debe evolucionar para reflejar las necesidades de la comunidad que
hace uso de ella.” También es necesario hacer una nomenclatura lo más sistemática y
sencilla posible para ayudar a los usuarios menos familiarizados (por ejemplo, porque solo
están en el proceso de estudiar química o son no-químicos que necesitan tratar con
productos químicos en el trabajo o en casa).
Existen tres sistemas de nomenclatura donde se agrupan y nombran los compuestos
inorgánicos, sin embargo, la IUPAC recomienda la nomenclatura Sistemática. Estos tres
sistemas son:

Marco referencial 17
• Stock: propuesta por Alfred Stock en 1919 para uso en la denominación de compuestos
binarios, ternarios y cuaternarios, donde el oxígeno actúa como grupo oxo. Se nombra
primero el anión y luego el catión, teniendo en cuenta el número de oxidación del metal se
ubica al final en número romano y en paréntesis.
• IUPAC (sistemática): se emplean prefijos indicando el número de átomos de cada
elemento de acuerdo con las reglas dadas por la IUPAC.
• Tradicional: Se empieza con el nombre del anión y con los prefijos hipo-, per- y los sufijos
–ico (-ato) e –oso (-ito), cuando hay presencia de oxígeno, y el sufijo -hídrico (-uro) en
ausencia de oxígeno; dependiendo del número de oxidación seguido del catión cuyo sufijo
dependerán de este número. Ico y oso con presencia de oxígeno; hídrico y uro ausencia
de oxígeno.
Algunos conceptos para tener en cuenta definidos por la IUPAC son:
• Cationes: Un catión es una especie monoatómica o poliatómica que tiene carga positiva
(+1, +2, +3).
• Aniones: Un anión es una especie monoatómica o poliatómica que tiene carga negativa
(-1, -2, -3).
• Compuestos binarios: Los compuestos binarios son los que tienen dos elementos
diferentes, por ejemplo:
- El 𝑁𝑎𝐶𝑙, cloruro de sodio, contiene dos elementos, el sodio y el cloro.
- El 𝐻2𝑂, agua, contiene dos elementos, el hidrógeno y el oxígeno.
Se habla de óxido cuando el compuesto está formado por el oxígeno y otro elemento el
cual puede ser metal o no metal. Y de sales binarias (-uro), cuando el compuesto se forma
por la unión de un anión y un catión.

18 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
Hidruros: Son compuestos que contienen hidrógeno y otro elemento. Generalmente se
obtienen por reacción directa entre los dos elementos: El hidrógeno tiene carga -1 porque
está unido a un átomo con menor electronegatividad con respecto al hidrógeno ej., NaH y
no NH3
1
𝑛𝐸𝑛 +
𝑦
2𝐻2 = 𝐸𝐻𝑦
donde 𝐸𝐻𝑦 es la fórmula general de los hidruros. Podemos ver que 𝑦 es el número de
átomos de hidrógeno que hacen falta para completar los octetos de los otros átomos en la
molécula. Habrá dos casos:
Caso 1: Cuando E es un átomo de un metal, los electrones externos de E serán cedidos
al hidrógeno, que adquirirá carga negativa y la configuración del helio (𝐻: )−. Así, el hidruro
de calcio será:
𝐻𝑥° 𝐶𝑎𝑥
° 𝐻 o 𝐶𝑎𝐻2
Todos los elementos que pertenecen a grupos periódicos con un número igual o menor
que 14 actuarán con estado de oxidación formal positivo, siendo 𝑦 este estado de
oxidación. Esto significa que estos elementos tienen mayor capacidad para donar
electrones que el átomo de hidrógeno. En los hidruros metálicos el hidrógeno está unido
al metal en forma atómica.
La nomenclatura de los hidruros metálicos se hace con la palabra hidruro, la preposición
"de", el nombre del elemento y entre paréntesis, su estado de oxidación. Por ejemplo:
Tabla 1. Nomenclatura de hidruros metálicos
Compuesto Nomenclatura
𝐶𝑠𝐻 hidruro de cesio
𝐻𝑔𝐻2 hidruro de mercurio(II)
𝐺𝑎𝐻3 hidruro de galio
𝑃𝑏𝐻4 hidruro de plomo(IV)
Fuente: Solís, Correa (2014)

Marco referencial 19
Cuando el elemento metálico sólo forma un estado de oxidación positivo, como es el caso
del cesio es optativo escribir su estado de oxidación.
Caso 2: Cuando el elemento E es un no-metal, el hidrógeno cederá su electrón al átomo E
para que éste complete su octeto, quedando el hidrógeno con carga formal positiva y el
elemento E quedará invertido respecto al caso anterior. Se forma el nombre del compuesto
con el nombre del no-metal (terminado en "uro"), la preposición "de" y la palabra hidrógeno.
Esto se da porque el hidrógeno se combina con un átomo más electronegativo ej. NH3. Por
ejemplo, para el sulfuro de hidrógeno la fórmula es 𝐻2𝑆. Nótese que en todas las fórmulas
se escribe primero el símbolo del átomo que tiene estado de oxidación positivo. Cuando el
compuesto se encuentra en estado acuoso, se utiliza el sufijo –hídrico.
Este caso ocurre con los elementos de los grupos 16 y 17.
La ecuación estequiométrica cambia sólo en que los elementos de los grupos 16 y 17
forman moléculas con un número de átomos pequeño y conocido. El azufre forma
moléculas 𝑆8 por lo que la ecuación química para la obtención de su hidruro es:
1
8𝑆8 + (
2
2) 𝐻2 ⇆ 𝐻2𝑆
o
1
8𝑆8 + 𝐻2 ⇆ 𝐻2𝑆 (Solís Correa, 2014)
La composición química de muchos hidruros (carga negativa del hidrógeno) se conoce
desde antes de la sistematización de la nomenclatura química, y la IUPAC acepta que se
sigan utilizando sus nombres tradicionales. Por ejemplo, se utiliza el nombre metano en
lugar de hidruro de carbono para el 𝐶𝐻4. (Solís Correa, 2014)
• Óxidos: Las combinaciones de los elementos con el oxígeno producen compuestos
llamados óxidos. Prácticamente cualquier óxido puede obtenerse de la reacción directa
con el oxígeno y el elemento, aunque esta reacción no es la única forma para obtenerlos:

20 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
𝑥
𝑛𝐸𝑛 +
𝑦
2𝑂2 = 𝐸𝑥𝑂𝑦
por ejemplo,
1
𝑛𝐶𝑎𝑛 +
1
2𝑂2 = 𝐶𝑎𝑂
2
𝑛𝐹𝑒𝑛 +
3
2𝑂2 = 𝐹𝑒2𝑂3
1
8𝑆8 + 𝑂2 = 𝑆𝑂2
2
2𝐼2 +
7
2𝑂2 = 𝐼2𝑂7
En los ejemplos anteriores, el valor de 𝑛 en Ca y Fe es de 1.
La fórmula general de los óxidos es 𝐸𝑥𝑂𝑦. Hay varias formas de nombrar a los óxidos.
Stock La más sencilla es iniciar con la palabra óxido, seguida de la preposición "de", el
nombre del elemento que forma el óxido, y el estado de oxidación que presenta, escrito en
número romano y entre paréntesis (Tabla 2).
Tabla 2. Nomenclatura Stock óxidos
Compuesto Nomenclatura Stock
𝐾2𝑂 óxido de potasio
𝐹𝑒𝑂 óxido de hierro(II)
𝐵𝑖2𝑂3 óxido de bismuto(III)
𝐶𝑂2 óxido de carbono(IV)
𝑉2𝑂5 óxido de vanadio(V)
Fuente: Solís, Correa (2014)

Marco referencial 21
Cuando un elemento presenta sólo un estado de oxidación, como ocurre entre los que
están en los grupos 1 y 2, se omite el número romano del estado de oxidación. El estado
de oxidación del elemento será el valor de "𝑦”, excepto cuando este número se ha
simplificado. Considerando que el estado de oxidación del oxígeno es -2, todas las
fórmulas 𝐸𝑂 indican que el estado de oxidación de E es +2, todas las fórmulas 𝐸𝑂2 indican
que el estado de oxidación de E es +4, y todas las fórmulas 𝐸𝑂3 indican que el estado de
oxidación de E es +6.
Sistemática. Otra nomenclatura consiste en "leer" la fórmula: indicar con un prefijo el
número de átomos de oxígeno, seguido de la palabra óxido, luego la preposición "de", y
con otro prefijo el número de átomos del otro elemento, con su nombre, el cual se lee de
derecha a izquierda vea la tabla 3.
Tabla 3. Nomenclatura sistemática óxidos
Compuestos Nomenclatura sistemática
𝐾2𝑂 óxido de potasio
𝐹𝑒𝑂 monóxido de monohierro
𝐵𝑖2𝑂3 trióxido de dibismuto
𝐶𝑂2 dióxido de carbono
𝑉2𝑂5 pentóxido de divanadio
Fuente: Solís, Correa (2014)
Tradicional. Otra nomenclatura, ya casi en desuso en binarios porque exige memorizar los
diferentes estados de oxidación de los elementos, consiste en decir la palabra óxido
seguida del nombre del ion en su estado de oxidación correspondiente (Tabla 4).
Tabla 4. Nomenclatura tradicional óxidos
Compuesto Nomenclatura tradicional
𝐾2𝑂 óxido potásico
𝐹𝑒𝑂 óxido ferroso
𝐵𝑖2𝑂3 óxido bismutoso
𝐶𝑂2 óxido carbónico
𝑉2𝑂5 óxido pervanádico
Fuente: Solís, Correa (2014)

22 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
• Peróxidos: El átomo estable del oxígeno en la naturaleza es el 𝑂2, que también se
escribe como <∶ �̈� = 𝑂 ∶̈ >. Algunos elementos donadores de electrones logran estabilizar
un ion dioxígeno dinegativo, llamado peróxido con fórmula — 𝑂— 𝑂—. En realidad, son
pocos los peróxidos importantes en química inorgánica: el peróxido de hidrógeno, 𝐻202
llamado comercialmente agua oxigenada (es una disolución de peróxido de hidrógeno con
agua), es muy poco estable y tiende a liberar oxígeno gaseoso:
2 𝐻202(𝑙) ⇒ 2𝐻20(𝑙) + 02(𝑔)
el peróxido de sodio, 𝑁𝑎202, comercialmente llamado "oxilita", y el peróxido de bario, 𝐵𝑎02,
que fue una de las principales materias primas para la preparación del 𝐻2𝑂2.
En todos los casos en los que aparezca la raíz peroxi o la palabra peróxido, ello indica que
existe el grupo 022−, y los oxígenos estructuralmente están unidos -O-O-. Los anteriores
son los más importantes como compuestos puros, pero el grupo aparece frecuentemente
en otros compuestos. (Solís Correa, 2014)
• Hidróxidos metálicos: Son compuestos de fórmula general 𝑀(𝑂𝐻)𝑦, donde 𝑦 es el
estado de oxidación del ion metálico. Son ternarios porque contienen tres elementos: un
elemento metálico, oxígeno e hidrógeno.
Algunos hidróxidos pueden obtenerse por la reacción de óxidos con agua, como en los
ejemplos siguientes:
𝑁𝑎2𝑂(𝑠) + 𝐻2𝑂(𝑙) ⟶ 2 𝑁𝑎𝑂𝐻(𝑎𝑐)
ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑠𝑜𝑑𝑖𝑜 + 𝑎𝑔𝑢𝑎 = 2 ℎ𝑖𝑑𝑟ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑠𝑜𝑑𝑖𝑜
o 𝐶𝑎𝑂(𝑠) + 𝐻20(𝑙) ⟶ 𝐶𝑎(𝑂𝐻)2(𝑎𝑐)
ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑐𝑎𝑙𝑐𝑖𝑜 + 𝑎𝑔𝑢𝑎 = ℎ𝑖𝑑𝑟ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑐𝑎𝑙𝑐𝑖𝑜.
Una expresión general para las reacciones anteriores es:
𝑀𝑥𝑂𝑦 + 𝑦𝐻20 ⟶ 𝑥𝑀(𝑂𝐻)𝑦

Marco referencial 23
ó𝑥𝑖𝑑𝑜 𝑚𝑒𝑡á𝑙𝑖𝑐𝑜 + 𝑎𝑔𝑢𝑎 = ℎ𝑖𝑑𝑟ó𝑥𝑖𝑑𝑜 𝑚𝑒𝑡á𝑙𝑖𝑐𝑜
Los índices 𝑥 y 𝑦 provienen de la fórmula del óxido.
La reacción de un óxido con agua no es una forma general de obtención de hidróxidos.
Algunas veces el óxido es más estable que el hidróxido y la reacción que se presenta es
la opuesta a la anterior:
𝑥𝑀(𝑂𝐻)𝑦 ⟶ 𝑀𝑥𝑂𝑦 + 𝑦𝐻20
que ocurre regularmente cuando 𝑦 es un valor alto, igual o mayor que 3, como en los casos
siguientes:
2 𝐴𝑙(𝑂𝐻)3(𝑎𝑐) ⟶ 𝐴𝑙2𝑂3(𝑠) + 3𝐻2𝑂(𝑙)
2 ℎ𝑖𝑑𝑟ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑎𝑙𝑢𝑚𝑖𝑛𝑖𝑜 = ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑎𝑙𝑢𝑚𝑖𝑛𝑖𝑜 + 3 𝑎𝑔𝑢𝑎.
2 𝐴𝑢(𝑂𝐻)3(𝑎𝑐) ⟶ 𝐴𝑢2𝑂3(𝑠) + 3𝐻2𝑂(𝑙)
2 𝑡𝑟𝑖ℎ𝑖𝑑𝑟ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑜𝑟𝑜 = 𝑡𝑟𝑖ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑜𝑟𝑜 + 3 𝑎𝑔𝑢𝑎
𝑇𝑖(𝑂𝐻)4(𝑎𝑐) ⟶ 𝑇𝑖𝑂2(𝑠) + 2𝐻2𝑂(𝑙)
𝑡𝑒𝑡𝑟𝑎ℎ𝑖𝑑𝑟ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑡𝑖𝑡𝑎𝑛𝑖𝑜 = 𝑑𝑖ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑡𝑖𝑡𝑎𝑛𝑖𝑜 + 2 𝑎𝑔𝑢𝑎
𝑃𝑡(𝑂𝐻)4(𝑎𝑐) ⟶ 𝑃𝑡𝑂2(𝑠) + 2𝐻2𝑂(𝑙)
𝑡𝑒𝑡𝑟𝑎ℎ𝑖𝑑𝑟ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑝𝑙𝑎𝑡𝑖𝑛𝑜 = 𝑑𝑖ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑝𝑙𝑎𝑡𝑖𝑛𝑜 + 2 𝑎𝑔𝑢𝑎
La nomenclatura de estos compuestos se da de forma similar a la de los óxidos.
Stock: con la palabra hidróxido, la preposición “de”, el nombre del ion metálico y el estado
de oxidación en número romanos entre paréntesis (Tabla 5).

24 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
Tabla 5. Nomenclatura Stock hidróxidos
Compuesto Nomenclatura Stock
𝐹𝑒(𝑂𝐻)2 hidróxido de hierro(II).
𝐹𝑒(𝑂𝐻)3 hidróxido de hierro(III).
𝐻𝑔𝑂𝐻 hidróxido de mercurio(I).
𝐻𝑔(𝑂𝐻)2 hidróxido de mercurio(II).
Fuente: Solís, Correa (2014)
Sistemática: con la palabra hidróxido, la preposición "de" y el nombre del ion metálico
(Tabla 6).
Tabla 6. Nomenclatura sistemática hidróxidos
Compuesto Nomenclatura sistemática
𝐿𝑖𝑂𝐻 hidróxido de litio
𝑀𝑔(𝑂𝐻)2 hidróxido de magnesio
𝑇𝑙(𝑂𝐻)3 hidróxido de tritalio
Fuente: Solís, Correa (2014)
Tradicional: cuando el metal puede presentar varios estados de oxidación es posible utilizar
la nomenclatura tradicional, en la cual el nombre del ion metálico termina en -ico o en –oso
(Tabla 7).
Tabla 7. Nomenclatura tradicional hidróxidos
𝐹𝑒(𝑂𝐻)2 hidróxido ferroso.
𝐹𝑒(𝑂𝐻)3 hidróxido férrico.
𝐻𝑔𝑂𝐻 hidróxido mercurioso.
𝐻𝑔(𝑂𝐻)2 hidróxido mercúrico.
Fuente: Solís, Correa (2014)
Sólo los hidróxidos de los elementos alcalinos son solubles en el agua. Además, éstos
pueden formar iones con facilidad:
𝑀𝑂𝐻 + 𝐻2𝑂 ⟶ 𝑀+ + 𝑂𝐻− 𝑒𝑛 𝑎𝑔𝑢𝑎 M+(ac)

Marco referencial 25
como el 𝐾𝑂𝐻 ⟶ 𝐾(𝑎𝑐)+ + 𝑂𝐻(𝑎𝑐)
−
El ion 𝑂𝐻(𝑎𝑐)− recibe el nombre de hidroxilo u oxhidrilo, que resulta de extraer un hidrógeno
a la molécula del agua.
Toda sustancia que esté formada por metal y el hidróxido no importa que sea soluble o
insoluble en agua, es considera una base o hidróxido, por ejemplo, 𝑇𝑖(𝑂𝐻)4 es un hidróxido
y es insoluble en agua. Los hidróxidos de los metales alcalinos son bases fuertes y los de
los metales alcalinotérreos (los de Mg, Ca, Sr y Ba) son bases débiles, pues casi no se
disocian; además son poco solubles en agua. Los demás hidróxidos metálicos son casi
totalmente insolubles, o se comportan como bases demasiado débiles. (Solís Correa,
2014)
• Hidrácidos: Los hidruros de los grupos 16 y 17 reaccionan con el agua para producir
iones hidronio y son, por tanto, ácidos. Tomando como ejemplo al cloruro de hidrógeno:
𝐻𝐶𝑙(𝑔) + 𝐻2𝑂(𝑙)(𝑙) ⟶ 𝐻3𝑂(𝑎𝑐)+ + 𝐶𝑙(𝑎𝑐)
−
Las soluciones acuosas de los hidruros ácidos se denominan "ácidos hidrácidos" o
simplemente "hidrácidos", y en su nomenclatura se incluye la palabra ácido, el nombre
apocopado del no metal y la terminación "hídrico" si está en agua. Su fórmula debe estar
acompañada por la palabra "acuoso" (ac) (Tabla 8).
Tabla 8. Nomenclatura hidrácidos
Compuesto Nomenclatura
𝐻𝐹(𝑎𝑐) acido fluorhídrico
𝐻𝐶𝑙(𝑎𝑐) ácido clorhídrico
𝐻𝐵𝑟(𝑎𝑐) ácido bromhídrico
𝐻𝐼(𝑎𝑐) acido yodhídrico
𝐻2𝑆(𝑎𝑐) ácido sulfhídrico
𝐻2𝑆𝑒(𝑎𝑐) ácido selenhídrico
𝐻2𝑇𝑒(𝑎𝑐) ácido telurhídrico
Fuente: Solís, Correa (2014)

26 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
• Oxiácidos: Otro tipo de óxidos reactivos con el agua son los óxidos de los no metales.
Por ejemplo: trióxido de azufre es un líquido
𝑆𝑂3(𝑙) + 𝐻2𝑂(𝑙) ⇄ 𝐻2𝑆𝑂4(𝑎𝑐)
Una diferencia importante entre esta reacción y las anteriores es que cuando se trata de
los óxidos metálicos, el producto siempre contiene uniones simples 𝑀— 𝑂𝐻. En este caso
no siempre se obtienen estas uniones, sino también enlaces 𝑀 = 𝑂 o 𝑀 ⟶ 𝑂. Este hecho
hace que la fórmula general de los compuestos sea 𝐻𝑟𝑀𝑂𝑞, donde 𝑟 y 𝑞 no siempre son
iguales. Generalmente 𝑟 (el número de átomos de hidrógeno) es menor que 𝑞 (el número
de átomos de oxígeno). Es muy difícil generalizar fórmulas para estos compuestos. Es
posible, al mirar la tabla periódica, escoger el número de oxidación más pequeño en valor
absoluto del no metal y este corresponde al número de hidrógenos del oxácido, este
método no aplica para el nitrógeno.
La mayor parte de los oxiácidos son solubles en agua y al disolverse forman iones. A
diferencia de los hidróxidos que dan iones 𝑀𝑌+ y 𝑂𝐻−, la ruptura de las moléculas de
oxiácidos ocurre en el enlace oxígeno-hidrógeno, por su alta diferencia de
electronegatividad: En los hidróxidos la ruptura se da por la alta diferencia de
electronegatividad entre el no metal y el oxígeno ej. NaOH electronegatividad Na 0,9; O
3,5 y H 2,1, hay mayor diferencia de electronegatividad entre el sodio y el oxígeno.
𝑂𝑏𝑀(𝑂𝐻)𝑟 ⟶ 𝑟𝐻+ + 𝑂𝑏𝑀𝑂𝑟𝑟−ó 𝑀𝑂𝑞
𝑟−
como en el siguiente caso:
H2O(𝑙) + HNO3(𝑙) → 𝐻3𝑂(𝑎𝑐)+ + NO3(𝑎𝑐)
−
Observe que 𝑞 = 𝑟 + 𝑏.
Por lo anterior la molécula se representa como 𝐻𝑟𝑀𝑂𝑞, con los átomos de hidrógeno
separados de los de oxígeno, pues en la disociación en solución acuosa los hidrógenos
actuarán como iones positivos. Esta representación es un convenio para los ácidos,

Marco referencial 27
siguiendo la diferencia de electronegatividad, aunque estructuralmente el hidrógeno va
unido al oxígeno.
Las sustancias que producen iones 𝐻+ al ser disueltas en el agua se llaman ácidos (𝐻3𝑂)+.
Las sustancias que contienen oxígeno en sus moléculas y producen iones 𝐻+ al quedar
disueltas en el agua se denominan ácidos oxigenados u oxiácidos.
Como la mayoría de los oxiácidos fueron preparados antes del desarrollo de la
nomenclatura sistemática, recibieron el nombre del óxido no metálico correspondiente
terminado en -oso o en -ico, y éste es el nombre tradicional con que se les denomina. El
nombre Stock, poco empleado, se forma con la palabra "ácido", la raíz griega del número
de oxígenos por molécula seguido de la partícula -oxo-, el nombre del elemento central
terminado en -ico y su estado de oxidación encerrado en paréntesis. Por ejemplo, el ácido
sulfúrico 𝐻2𝑆𝑂4 debería denominarse ácido tetraoxosulfúrico(VI).
Los ácidos oxigenados del cloro son 𝐻𝐶𝑙𝑂, 𝐻𝐶𝑙𝑂2, y 𝐻𝐶𝑙𝑂3 y 𝐻𝐶𝑙𝑂4. En la tabla 9
observamos los nombres tradicionales y Stock de ellos.
Tabla 9. Nombres tradicionales y Stock de los ácidos oxigenados del cloro
(oxiácidos)
Compuesto Nombre tradicional Nombre Stock
𝐻𝐶𝑙𝑂 ácido hipocloroso ácido monoxoclórico(I)
𝐻𝐶𝑙𝑂2 ácido cloroso ácido dioxoclórico(III)
𝐻𝐶𝑙𝑂3 ácido clórico ácido trioxoclórico(V)
𝐻𝐶𝑙𝑂4 ácido perclórico ácido tetraoxoclórico(VII)
Fuente: Solís, Correa (2014)
Hay una forma muy rápida para reconocer el estado de oxidación del elemento central en
un ácido oxigenado con fórmula general 𝐻𝑟𝑀𝑂𝑞. Esta consiste en realizar la operación
2𝑞 − 𝑟 = 𝑀.
Por ejemplo, en el ácido ortobórico 𝐻3𝐵𝑂3, el estado de oxidación del boro es
(2 × 3) − 3 = 3, y el nombre Stock será: ácido trioxobórico(III). (Solís Correa, 2014).

28 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
En la nomenclatura sistemática primero se escribe un prefijo que indica el número de
oxígenos, la palabra "oxo", otro prefijo para el número de átomos no metálicos, la raíz de
ese átomo acabado en "-ato". Por último, las palabras "de hidrógeno", no se cuenta su
número se lee de derecha a izquierda.
Tabla 10. Nomenclatura sistemática de oxiácidos del cloro
Acido Nombre sistemático
𝐻𝐶𝑙𝑂 oxoclorato de hidrógeno
𝐻𝐶𝑙𝑂2 dioxoclorato de hidrógeno
𝐻𝐶𝑙𝑂3 trioxoclorato de hidrógeno
𝐻𝐶𝑙𝑂4 tetraoxoclorato de hidrógeno
Fuente: Solís, Correa (2014)
• Sales binarias: La mayor parte de los elementos situados del lado izquierdo de la tabla
periódica se combinan directamente con los elementos situados en el lado derecho. Los
del lado derecho producen iones negativos en estas combinaciones y los del izquierdo,
iones positivos:
𝑥
𝑛𝐴𝑛 +
𝑦
𝑚𝐵𝑚 = 𝐴𝑥𝐵𝑦
Los compuestos así formados se llaman sales binarias. Un ejemplo clásico es el cloruro
de sodio:
1
𝑛𝑁𝑎𝑛 +
1
2𝐶𝑙2 = 𝑁𝑎𝐶𝑙
La mayoría de los compuestos así formados son sólidos, cristalinos, blancos y parecidos
a la sal de cocina o cloruro de sodio (sistemático) o cloruro sódico (tradicional). Por esta
razón las sales binarias se llaman también sales halógenas (el cloro es un elemento de los
halógenos) o sales haloideas (porque las formas minerales de la sal común se llaman
halitas), aunque no todas tengan elementos del grupo de los halógenos ej.: sulfuro de
sodio.

Marco referencial 29
Los valores 𝑥 y 𝑦 de la fórmula general 𝐴𝑥𝐵𝑦 se obtienen de la regla de intercambios de
estado de oxidación. La nomenclatura Stock de las sales generalmente se forma
enunciando el nombre del ion negativo, terminado en -uro, la preposición "de", y el nombre
del metal seguida del estado de oxidación del mismo entre paréntesis (Tabla 11).
Tabla 11. Nomenclatura Stock para las sales binarias
Compuesto Nomenclatura Stock
𝐺𝑎𝐴𝑠 arseniuro de galio(III)
𝐶𝑑𝑇𝑒 telururo de cadmio
𝐶𝑢2𝑆 sulfuro de cobre(I)
𝐹𝑒𝐶𝑙3 cloruro de hierro(III)
𝐴𝑔𝐵𝑟 bromuro de plata
Fuente: Solís, Correa (2014)
Las otras dos nomenclaturas, mencionadas para los óxidos, también son comunes para
las sales. Los compuestos anteriores pueden tener los siguientes nombres:
Tabla 12. Nomenclatura sistemática para las sales binarias
Compuesto Nomenclatura sistemática
𝐺𝑎𝐴𝑠 arseniuro de galio
𝐶𝑑𝑇𝑒 telururo de cadmio
𝐶𝑢2𝑆 sulfuro de dicobre
𝐹𝑒𝐶𝑙3 tricloruro de hierro
𝐴𝑔𝐵𝑟 bromuro de plata
Fuente: Solís, Correa (2014)
Tabla 13. Nomenclatura tradicional para las sales binarias
Compuesto Nomenclatura tradicional
𝐺𝑎𝐴𝑠 arseniuro gálico
𝐶𝑑𝑇𝑒 telururo cádmico
𝐶𝑢2𝑆 sulfuro cuproso
𝐹𝑒𝐶𝑙3 cloruro férrico
Fuente: Solís, Correa (2014)

30 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
• Oxisales: Las oxisales son las que resultan de combinar iones metálicos (cationes) con
aniones oxigenados. La fórmula general que les corresponde es:
𝑀𝑝(𝑀′𝑂𝑞)𝑦
donde 𝑦 es el estado de oxidación del catión metálico 𝑀, y 𝑝 es la carga formal del
oxoanión, cuyo átomo central es 𝑀′. Los valores de 𝑝 y de 𝑦, como estados de oxidación
de 𝑀𝑦+ y 𝑀𝑂𝑞𝑝−
, se intercambian siguiendo la regla del intercambio de los estados de
oxidación.
Para indicar el nombre de una oxisal en nomenclatura Stock se enuncia el nombre del
oxianión, la preposición "de" y el nombre del catión, poniendo su estado de oxidación entre
paréntesis, cuando proceda (Tabla 14).
Tabla 14. Nomenclatura Stock de oxisales
Nomenclatura Stock Compuesto
yodato de potasio 𝐾𝐼𝑂3
nitrato de calcio 𝐶𝑎(𝑁𝑂3)2
sulfato de sodio 𝑁𝑎2𝑆𝑂4
metasilicato de magnesio 𝑀𝑔𝑆𝑖𝑂3
fosfato de hierro(II) u ortofosfato de hierro(II) 𝐹𝑒3(𝑃𝑂4)2
carbonato de cobalto(III) 𝐶𝑜2(𝐶𝑂3)3
Fuente: Solís, Correa (2014)
En la nomenclatura tradicional el anión se nombra igual que el ácido oxácido del que
procede, sustituyendo las terminaciones –oso e –ico por –ito y –ato respectivamente; y el
catión añadiendo hipo-, -oso, -ico, hiper-, de acuerdo al número de valencias que posea
(Tabla 15).

Marco referencial 31
Tabla 15. Nomenclatura tradicional oxisales
Compuesto Nomenclatura tradicional
𝑁𝑎𝐶𝑙𝑂2 clorito sódico
𝐹𝑒𝑆𝑂4 sulfato ferroso
𝐹𝑒2(𝑆𝑂4)3 sulfato férrico
𝑀𝑔𝑆𝑖𝑂3 metasilicato magnésico
Fuente: Solís, Correa (2014)
El método de obtención generalizado de las oxisales consiste en hacer reaccionar al ácido
que da origen al oxoanión con el hidróxido metálico que corresponde. La ecuación química
general es:
𝑦𝐻𝑝𝑀′𝑂𝑞 + 𝑝𝑀(𝑂𝐻)𝑦 ⟶ 𝑀𝑝(𝑀′𝑂𝑞)𝑦
+ (𝑝 × 𝑦)𝐻2𝑂
oxiácido hidróxido oxisal agua
Ejemplo:
𝐻2𝑆𝑂4(𝑎𝑐) + 2𝑁𝑎𝑂𝐻(𝑎𝑐) ⟶ 𝑁𝑎2𝑆𝑂4(𝑎𝑐) + 2𝐻2𝑂(𝑙)
á𝑐𝑖𝑑𝑜 𝑠𝑢𝑙𝑓ú𝑟𝑖𝑐𝑜 + 2ℎ𝑖𝑑𝑟ó𝑥𝑖𝑑𝑜 𝑑𝑒 𝑠𝑜𝑑𝑖𝑜 = 𝑠𝑢𝑙𝑓𝑎𝑡𝑜 𝑑𝑒 𝑠𝑜𝑑𝑖𝑜 + 2𝑎𝑔𝑢𝑎
A este método de preparación se le conoce como neutralización, pues consiste en igualar
las cantidades de iones 𝐻+ que provienen del ácido con las cantidades de iones 𝑂𝐻− que
provienen de las bases. La neutralización ocurre cuando la cantidad de ácido reacciona
con una cantidad igual de base y el producto final es neutro, ya que
𝐻+ + 𝑂𝐻− = 𝐻2𝑂 (Solís Correa, 2014)
Las funciones químicas inorgánicas de mayor relevancia son: óxidos, hidróxidos, ácidos y
sales; cada una de las cuales se rige por los sistemas de nomenclatura mencionados
anteriormente.

32 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
2.1.4 Enseñanza de la nomenclatura química.
Respecto de la práctica áulica de la enseñanza de la nomenclatura, se observan varias
modalidades generales, cada una con sus matices y variantes:
- Enseñanza tradicional.
- Enseñanza por medio del juego.
- Enseñanza dentro de un paradigma ciencia-tecnología-sociedad (CTS). (Laurella, 2015)
2.1.5 Aprendizaje Activo.
Este se basa en la concepción que el aprendizaje se da de mejor forma a medida que el
estudiante interactúa y elabora el mismo sus procesos de generación de nuevos
conocimientos, contando con la orientación del docente. En este se logra una educación
horizontal, en la que el estudiante tiene un papel activo. El aprendizaje activo puede ser
entendido como aquel basado en el alumno que se consigue no solo con la motivación,
sino también con implicación, atención y trabajo constante (Esteba Ramos, 2013).
Según Jerez (2015) el aprendizaje “ocurre” porque el estudiante hizo algo más que
escuchar una clase, y el docente se enfocó en que lo anterior ocurriera, teniendo en vista
el aprendizaje que deseaba lograr en ellos. A esto se le llama formación orientada hacia
los estudiantes y su participación activa. No es necesario que se diseñen estrategias tan
elaboradas, pero sí que tengan una significancia para los estudiantes, y que les permita
desarrollar sus propios conceptos a través de distintas actividades pedagógicas.
2.1.6 Cognición situada.
En este el aprendizaje se entiende como los cambios en las formas de comprensión y
participación de los sujetos en una actividad conjunta. Debe comprenderse como un
proceso multidimensional de apropiación cultural, ya que se trata de una experiencia que
involucra el pensamiento, la afectividad y la acción (Díaz Barriga, 2003).

Marco referencial 33
2.1.7 Enseñanza de la química.
Si hay una ciencia que ha de contribuir a la alfabetización científica de nuestros estudiantes
es precisamente la química. Los cambios producidos en las estrategias de enseñanza y
aprendizaje de las ciencias, al responder a las nuevas necesidades formativas generadas
por la sociedad, tienen como meta el "aprender a aprender", con el consecuente desarrollo
en todas las áreas y niveles de educación (Sandoval, Mandolesi, & Cura, 2013)
2.1.8 Estándares de competencias y derechos básicos de aprendizaje.
Los estándares básicos de competencias constituyen uno de los parámetros de lo que todo
niño, niña y joven debe saber y saber hacer para lograr el nivel de calidad esperado a su
paso por el sistema educativo (Ministerio de Educación Nacional, 2006).
Un estándar es un criterio claro y público que permite juzgar si un estudiante, una
institución o el sistema educativo en su conjunto cumplen con unas expectativas comunes
de calidad; expresa una situación deseada en cuanto a lo que se espera que todos los
estudiantes aprendan en cada una de las áreas a lo largo de su paso por la Educación
Básica y Media, especificando por grupos de grados (1 a 3, 4 a 5, 6 a 7, 8 a 9, y 10 a 11)
el nivel de calidad que se aspira alcanzar. (Ministerio de Educación Nacional, 2006).
Una de las metas fundamentales de la formación en ciencias es procurar que los y las
estudiantes se aproximen progresivamente al conocimiento científico, tomando como
punto de partida su conocimiento “natural” del mundo y fomentando en ellos una postura
crítica que responda a un proceso de análisis y reflexión (Ministerio de Educación Nacional,
2006)
Para el grado décimo y undécimo, el estándar básico de competencias relacionado con la
nomenclatura química es: “Relaciono la estructura de las moléculas orgánicas e
inorgánicas con sus propiedades físicas y químicas y su capacidad de cambio químico”
(Ministerio de Educación Nacional, 2006).
Los Derechos Básicos de Aprendizaje (DBA), corresponde a un conjunto de aprendizajes
estructurantes que han de aprender los estudiantes en cada uno de los grados de
educación escolar, desde transición hasta once. Los DBA se organizan guardando

34 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
coherencia con los Lineamientos Curriculares y los Estándares Básicos de Competencias
(EBC). Su importancia radica en que plantean elementos para construir rutas de
enseñanza que promueven la consecución de aprendizajes año a año para que, como
resultado de un proceso, los estudiantes alcancen los EBC propuestos por cada grupo de
grados (Ministerio de Educación Nacional, 2016).
Es importante tener en cuenta que los DBA por sí solos no constituyen una propuesta
curricular y estos deben ser articulados con los enfoques, metodologías, estrategias y
contextos definidos en cada establecimiento educativo, en el marco de los Proyectos
Educativos Institucionales (PEI) materializados en los planes de área y de aula. Los DBA
también constituyen un conjunto de conocimientos y habilidades que se pueden movilizar
de un grado a otro, en función de los procesos de aprendizaje de los estudiantes. Si bien
los DBA se formulan para cada grado, el maestro puede trasladarlos de uno a otro en
función de las especificidades de los procesos de aprendizaje de los estudiantes. De esta
manera, los DBA son una estrategia para promover la flexibilidad curricular puesto que
definen aprendizajes amplios que requieren de procesos a lo largo del año y no son
alcanzables con una o unas actividades. (Ministerio de Educación Nacional, 2016).
Para la enseñanza de la nomenclatura química inorgánica, el DBA correspondiente es:
“Comprende que los diferentes mecanismos de reacción química (oxido-reducción,
descomposición, neutralización y precipitación) posibilitan la formación de compuestos
inorgánicos.” (Ministerio de Educación Nacional, 2016)

3. Metodología
3.1 Tipo de investigación
La presente investigación es descriptiva, de tipo cualitativo, enmarcada en el enfoque de
aprendizaje activo. La investigación descriptiva tiene como meta construir y reconstruir en
forma colaborativa el conocimiento pedagógico en pro del mejoramiento de los procesos
educativos.
En el estudio de Sierra (2013), se describe al aprendizaje activo como una estrategia que
propicia una actitud activa del estudiante en clase. Es el proceso que compenetra a los
estudiantes a realizar cosas y pensar en esas cosas que realizan. En esta estrategia los
estudiantes desarrollan distintas habilidades, que les permitirán resolver problemas, así
como adquirir una serie de competencias con las que el joven podrá desenvolverse en la
sociedad.
3.2 Población
Estudiantes del grado décimo del Centro Educativo Rural San José de Castro, ubicado en
el Corregimiento de Castro, en el municipio de Arboledas, Norte de Santander, cuyas
edades oscilan entre los 15 y los 19 años, los cuales provienen de veredas aledañas (zona
rural), con muchas dificultades en el desplazamiento desde y hacia sus hogares. Sus
condiciones familiares son muy diversas, encontrándose desde familias nucleares, hasta
grupos familiares extensos con varios parientes en la misma vivienda. Algunos con padres
con problemas de alcoholismo, y con un nivel de formación bajo; muy pocos padres
culminaron sus estudios básicos, y ninguno tiene formación universitaria.
Igualmente presentan un bajo interés en el estudio, ya que muy pocos aspiran a salir del
campo a estudiar a una institución de educación superior.

36 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
3.3 Etapas del proceso de enseñanza
Para dar cumplimiento a los objetivos del trabajo de grado se llevaron a cabo las siguientes
acciones:
3.3.1 Selección información.
Se hizo un barrido de la información encontrada, para seleccionar los conceptos idóneos
que harán parte de la estrategia didáctica implementada.
3.3.2 Diseño prueba diagnóstica.
Se diseñó una prueba donde se evalúen los conocimientos previos que los estudiantes
deben tener con respecto a la temática de nomenclatura inorgánica, como lo es la
identificación de los tipos de enlaces, iones y fórmulas químicas. Con el fin de determinar
la cantidad de jóvenes que se encuentran apropiados de los presaberes necesarios para
poder comprender la temática de nomenclatura química inorgánica, o en caso contrario,
realizar un refuerzo sobre los mismos.
3.3.3 Contenido y estructura de la estrategia didáctica.
Después del análisis de las pruebas diagnósticas, se realizará la planeación del contenido
y estructura de la estrategia, para que esté acorde a los pre-saberes de los estudiantes y
al contexto en que se desenvuelven.
3.3.4 Desarrollo de la estrategia didáctica.
Luego de aplicada la prueba diagnóstica, se realizará una estrategia didáctica mediante el
desarrollo del aprendizaje activo, utilizando diversas herramientas lúdicas y tecnológicas,
con el fin de despertar en los jóvenes la curiosidad por nombrar los distintos compuestos
químicos inorgánicos. Igualmente, se familiarizará a los estudiantes con las diversas
sustancias inorgánicas que rodean su vida cotidiana, para que se acerquen al lenguaje
científico sin sentirse cohibido por el uso de términos técnicos.
3.3.5 Evaluación
Se llevó un registro a manera de diario de las actividades de los estudiantes y sus logros
cognitivos.

Metodología 37
Mediante las charlas permanentes con los estudiantes se irá evaluando su proceso de
apropiación del lenguaje de la química inorgánica.
Finalmente se realizará una prueba donde se evalúen los conocimientos adquiridos
durante la implementación de la estrategia didáctica.


4. Resultados y análisis de resultados
4.1 Selección información
Luego de realizada la lectura de la bibliografía consultada, así como los estándares básicos
correspondientes a la nomenclatura inorgánica, se pudo establecer la temática que se
debe tratar en el desarrollo de este módulo.
Así el primer contenido a tratar será valencia y número de oxidación, seguido de la historia
de la nomenclatura de química inorgánica, con el fin de conocer como ha sido el proceso
para llegar hasta la nomenclatura utilizada actualmente, después el concepto de función
química y grupo funcional y finalmente los distintos grupos funcionales en química
inorgánica y cómo es su nomenclatura en los tres sistemas más comúnmente utilizados:
stock, tradicional y sistemático.
4.2 Prueba diagnóstica
Se aplicó a 35 estudiantes de grado décimo una prueba diagnóstica (Figura 3) la cual tuvo
como objetivo el conocer los pre-saberes que los jóvenes tienen con respecto a la
configuración electrónica, enlaces y tipos de enlaces. El manejo de la configuración
electrónica y tipos de enlaces, les permite a los jóvenes entender más fácilmente los tipos
de compuestos que se forman, así como el comportamiento de los átomos presentes en
los mismos, y podrán identificar más fácilmente los iones que pueden derivar de dichos
compuestos al disociarse. Los resultados obtenidos en la prueba diagnóstica sirvieron para
poder desarrollar la planeación que les permitió comprender la temática tratada.
Es necesario dentro de los pre-saberes de los estudiantes, el concepto de átomo y
partículas subatómicas, molécula y cómo se forma la misma, enlace y los tipos de enlace;
ya que con estos temas se pueden afianzar los conocimientos de la nomenclatura química.
Igualmente, el conocer la configuración electrónica, le permitirá al estudiante determinar
las propiedades periódicas de los elementos que se presenten, y será más fácil aplicar las

40 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
reglas al momento de nombrar un compuesto inorgánico, además de poder predecir el
comportamiento de los elementos en una fórmula química. Igualmente, el conocer los tipos
de enlace, le permitirá al educando el poder determinar si puede haber formación de iones
o no al momento de una reacción química.
Figura 3. Prueba diagnóstica aplicada
Fuente: Elaboración propia
A partir de la aplicación de la prueba se pudo apreciar los resultados consignados en la
tabla 16.

Resultados y análisis de resultados 41
Tabla 16. Resultados obtenidos en la aplicación de la prueba diagnóstica
Pregunta Correcto Incorrecto No responde
Total Cant. % Cant % Cant. %
1. Realiza la configuración electrónica del azufre (S), que tiene 16 electrones
30 85,71 5 14,29 0 0 35
2. Realiza la configuración electrónica del calcio (Ca), que tiene 20 electrones
25 71,43 10 28,57 0 0 35
3. Realiza la configuración electrónica del ion calcio (Ca2+)
23 65,71 7 20,00 5 14 35
4. Realiza la configuración electrónica del ion sulfuro (S2-)
22 62,86 7 20,00 6 17 35
5. ¿Por qué el azufre tiene menos electrones que el ion sulfuro?
9 25,71 21 60,00 5 14 35
6. ¿Por qué el calcio tiene más electrones que el ion calcio?
6 17,14 21 60,00 8 23 35
7. ¿Qué es un enlace iónico?
8 22,86 22 62,86 5 14 35
8. ¿Qué es un enlace covalente?
14 40,00 16 45,71 5 14 35
9. ¿Qué tipo de enlace tiene el compuesto CO2?
12 34,29 12 34,29 11 31 35
10. ¿Qué tipo de enlace tiene el compuesto CaCl2?
12 34,29 13 37,14 10 29 35
Fuente: Elaboración propia
Para las preguntas 1 a 4, se puede concluir que los jóvenes tienen facilidad para realizar
la configuración electrónica en elementos sin carga (85,71 % y 71,43 % de respuestas
correctas), sin embargo, presentan una mayor dificultad a la hora de representar la
cantidad de electrones presente en iones (65,71 % y 62,86 % de aciertos). Sin embargo,
más del 50 % de los estudiantes son capaces de realizar la configuración electrónica de
los elementos dados.
Con base a las respuestas de las preguntas 5 y 6, se puede apreciar que los jóvenes no
tienen claridad a la hora de explicar la razón por la que ion cargado positivamente tiene
una menor cantidad de electrones en su configuración electrónica, o porqué un ion

42 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
negativo tiene una mayor cantidad de electrones (con un 60,00 % incorrecto en ambas
respuestas).
Con respecto a las respuestas dadas en las preguntas 7 a 10, se pudieron observar
dificultades al dar el concepto de tipos de enlace iónico o covalente (62,86 % y 45,71 %
incorrecto), así como en identificar el tipo de enlace de una molécula, teniendo un mayor
porcentaje de incorrecto, o no responde en estas preguntas (34,29 % de aciertos en las
preguntas 9 y 10).
A partir del diagnóstico se pudo determinar que, los estudiantes muestran falencias y
vacíos conceptuales. Por lo que se hizo necesario realizar un refuerzo en los jóvenes antes
de abordar la temática de nomenclatura de química inorgánica, a partir del desarrollo de
una clase magistral, en la cual se socializaron los conceptos de ion, enlaces, tipos de
enlaces y la forma de identificar los tipos de enlaces químicos. Así como un refuerzo en
configuración electrónica, la cual permite determinar algunas propiedades químicas y la
ubicación de los elementos en la tabla periódica.
Después del desarrollo de la clase magistral, a partir del desarrollo de actividades
individuales y grupales, se pudo observar que los jóvenes eran capaces de distinguir los
tipos de enlaces, así como la formación de iones por disociación de los mismos.
4.3 Contenido y estructura de la estrategia didáctica
Para llevar a cabo la estrategia didáctica, fue necesario realizar una planeación de los
distintos contenidos a tratar.
Primeramente, se comenzó con la historia y el origen de los nombres y representación de
los elementos, partiendo de los alquimistas, los símbolos de Dalton y finalmente llegando
a Berzelius, quien fue el que postuló la simbología que se utiliza hoy. Seguidamente se
basa en el sistema de Berzelius para la representación de los compuestos.
Se continuó con los conceptos de número de oxidación y valencia. Los cuales guardan una
relación, pero a su vez son completamente distintos. Después se habla sobre la
nomenclatura de los compuestos, que hay dos grandes grupos de sustancias, las

Resultados y análisis de resultados 43
inorgánicas y las orgánicas, y cada uno de ellos tienen formas distintas de nombrarlas. A
su vez los compuestos inorgánicos se dividen en grupos funcionales, y se dan a conocer
los grupos funcionales inorgánicos, y los tipos de nomenclatura utilizados para cada uno
(Anexo A).
A partir de una dinámica de identificación de grupo funciónales, en la cual la docente
escribía una fórmula química, y en trabajo de grupo los estudiantes intentaban nombrarlo
en las tres formas (Stock, Sistemática y Tradicional); y el primer grupo que terminara
pasaba al tablero y procedía a nombrar el compuesto. Se hacía retroalimentación con los
compañeros, si había errores se corregían de forma grupal y si se realizaba el ejercicio de
forma correcta, los estudiantes del grupo recibían un punto. Los grupos recibían una nota
apreciativa de acuerdo a la cantidad de aciertos que tuvieran.
Otra actividad realizada para la identificación de los distintos grupos funcionales, y su uso,
es lograr ubicar estos compuestos en los elementos que los estudiantes encuentren a su
alrededor; para ello se les pide a los jóvenes que traigan diversos empaques de productos
que usen en la casa (empaques de alimentos, alimento de mascotas, productos de aseo,
entre otros) y se realiza una actividad en la cual ellos deben anotar las sustancias que
crean que correspondan a compuestos inorgánicos, según la nomenclatura vista. Hecho
esto, se socializó con los compañeros el listado, para realizar un consolidado de estos, y
entre todos se trató de ubicarlos en los distintos grupos funcionales vistos (óxidos, ácidos,
hidróxidos, sales) y se trató de plantear su fórmula química. Para finalizar esta actividad
se realizó una investigación de los compuestos listados, en la cual se incluía su función o
uso, y la fórmula molecular, con la cual se hizo un cotejo para determinar si hubo
coincidencia o no con respecto a la planteada en el salón (Figuras 4 y 5).

44 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
Figura 4. Actividad de apropiación
Fuente: Elaboración propia
Figura 5. Desarrollo actividad de apropiación
Fuente: Elaboración propia

Resultados y análisis de resultados 45
A partir del desarrollo de esta actividad, los jóvenes demostraron su capacidad de
reconocer compuestos inorgánicos, al observar las etiquetas de diversos productos de uso
cotidiano, así como intentaron escribir las fórmulas químicas correspondientes.
Finalmente se evaluó a los estudiantes mediante una prueba escrita en la cual se midió el
nivel de apropiación de los conceptos referentes a la nomenclatura química y la
identificación de las distintas funciones químicas inorgánicas estudiadas.
4.4 Evaluación
A través del desarrollo de la temática sobre nomenclatura de química inorgánica, se realizó
un registro a manera de diario de las actividades de los estudiantes y sus logros.
Igualmente, mediante la formulación de distintos ejercicios de nomenclatura con los
estudiantes se evaluó el progreso de estos en la apropiación del lenguaje de la química
inorgánica.
Finalmente se realizó una prueba (Anexo B) donde se evidencien los conocimientos
adquiridos durante la implementación de la estrategia didáctica.
A partir de la prueba, se pudieron observar los siguientes resultados:
Tabla 17. Resultados obtenidos de relacionar los términos de la izquierda con las
definiciones
Número de respuestas acertadas
Cantidad de estudiantes Porcentaje (%)
0/6 9 26
1/6 8 23
2/6 5 14
3/6 3 9
4/6 4 11
5/6 0 0
6/6 6 17
Total 35 100
Fuente: Elaboración propia
En esta pregunta, en la cual se pedía que se relacionaran términos con su función química
correspondiente, se obtuvo que un 26 % no resolvió ninguna de las seis opciones dadas,

46 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
un 23 % tuvo una respuesta acertada; un 14 %, dos respuestas acertadas; un 9 %, tres
respuestas correctas; un 11 % obtuvieron cuatro aciertos y un 17 % tuvo seis respuestas
afirmativas. Esto quiere decir que los jóvenes presentan dificultad en relacionar los
conceptos con las funciones químicas correspondientes.
Tabla 18. Identificación de grupos funcionales (óxidos, hidróxidos, ácidos y sales)
Número de respuestas acertadas
Cantidad de estudiantes Porcentaje (%)
0/10 1 3
1/10 4 11,5
2/10 5 14
3/10 2 6
4/10 6 17
5/10 4 11,5
6/10 1 3
7/10 6 17
8/10 1 3
9/10 5 14
10/10 0 0
Total 35 100
Fuente: Elaboración propia
De acuerdo a la información recolectada, puede apreciarse que un 3 % no tuvo ninguna
respuesta acertada, un 11,5 % solo una respuesta de diez, un 14 %, dos de diez, un 6 %,
tres de diez, un 17 %, cuatro respuestas acertadas, un 11,5 %, cinco respuestas acertadas;
un 3 % con seis respuestas correctas; un 17 % con siete respuestas acertadas; un 3 %
con ocho aciertos y 14 % con nueve respuestas correctas, y ningún estudiante respondió
afirmativamente las diez opciones de respuesta. Esto muestra una falencia a la hora de
reconocer funciones químicas inorgánicas.
Tabla 19. Resultados de nombrar los óxidos según la nomenclatura tradicional
Número de respuestas acertadas
Cantidad de estudiantes Porcentaje (%)
0/4 20 57
¼ 1 3
2/4 0 0
¾ 6 17
4/4 8 23
Total 35 100
Fuente: Elaboración propia

Resultados y análisis de resultados 47
Un 57 % de los estudiantes no tuvo ningún acierto en nombrar óxidos por la nomenclatura
tradicional, un 3 % presentó una respuesta acertada, un 17 %, tres respuestas y un 23 %
cuatro respuestas, de cuatro opciones de respuesta. Esto muestra cierta dificultad en el
manejo de la nomenclatura tradicional de los óxidos.
Tabla 20. Resultados de nombrar los óxidos según la nomenclatura sistemática
Número de respuestas acertadas
Cantidad de estudiantes Porcentaje (%)
0/5 17 49
1/5 3 8,5
2/5 3 8,5
3/5 6 17
4/5 5 14
5/5 1 3
Total 35 100
Fuente: Elaboración propia
Un 49 % no respondió ninguna de las opciones de nomenclatura sistemática dada, un
8,5 % tuvo una respuesta acertada de cinco posibles, un 8,5 % tuvo dos respuestas
correctas, un 17 % presentó tres respuestas correctas, un 14 %, cuatro respuestas
acertadas y solo un 3 % obtuvo cinco de cinco respuestas acertadas. Esto evidencia
falencias en el manejo de la nomenclatura sistemática.
Tabla 21. Resultados de nombrar los óxidos según la nomenclatura Stock
Número de respuestas acertadas
Cantidad de estudiantes Porcentaje (%)
0/5 24 68
1/5 2 6
2/5 0 0
3/5 2 6
4/5 1 3
5/5 6 17
Total 35 100
Fuente: Elaboración propia
Un 68 % no respondió acertadamente a ninguna de las opciones de respuesta, un 6 %
resolvió una opción acertadamente, un 6 %, tres opciones acertadamente, un 3 %, cuatro
respuestas acertadas y un 17 %, cinco respuestas acertadas de cinco opciones de

48 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
respuesta. Esto evidencia una dificultad en la formulación de los nombres utilizando el
sistema Stock de nomenclatura.
Tabla 22. Resultados a la pregunta sobre relacionar el compuesto con su nombre
correspondiente
Número de respuestas acertadas
Cantidad de estudiantes Porcentaje(%)
0/10 0 0
1/10 0 0
2/10 0 0
3/10 3 8,5
4/10 2 6
5/10 0 0
6/10 3 8,5
7/10 2 6
8/10 6 17
9/10 1 3
10/10 18 51
Total 35 100
Fuente: Elaboración propia
Un 8,5 % de los estudiantes dieron tres respuestas acertadas de diez posibles; un 6 %,
cuatro respuestas de diez; un 8,5 %, seis aciertos de diez; un 6 %, siete respuestas
correctas; un 17 %, ocho respuestas acertadas; un 3 %, presentaron nueve respuestas de
diez posibles y un 51 % presentaron diez respuestas correctas de diez posibles. Esto indica
que más de la mitad de los jóvenes son capaces de relacionar el nombre del compuesto
con la fórmula química correspondiente, demostrando que, aunque tienen dificultad a la
hora de recordar las reglas para nombrar compuestos inorgánicos, si son capaces de
reconocer los mismos y sus nombres cuando los tienen al frente.
Tabla 23. Resultados identificación de un catión o un anión
Número de respuestas acertadas
Cantidad de estudiantes Porcentaje(%)
0/10 13 37
1/10 0 0
2/10 0 0
3/10 0 0
4/10 0 0
5/10 0 0

Resultados y análisis de resultados 49
6/10 0 0
7/10 1 3
8/10 1 3
9/10 1 3
10/10 19 54
Total 35 100
Fuente: Elaboración propia
Un 37 % de los estudiantes no respondió correctamente ninguna de las diez opciones de
respuesta, presentaron siete, ocho y nueve respuestas correctas en un 3 % cada una, y
un 54 % de los estudiantes presentaron diez respuestas correctas de diez opciones. Esto
indica que más de la mitad de los estudiantes son capaces de identificar si un ion es
positivo (catión) o negativo (anión).
Tabla 24. Resultados identificación de los compuestos inorgánicos estudiados
(óxidos, ácidos, hidróxidos y sales), en un producto de uso diario.
Número de respuestas acertadas
Cantidad de estudiantes Porcentaje (%)
0/10 2 6
1/10 0 0
2/10 2 6
3/10 2 6
4/10 0 0
5/10 5 14
6/10 5 14
7/10 1 3
8/10 0 0
9/10 9 25,5
10/10 9 25,5
Total 35 100
Fuente: Elaboración propia
A partir de la descripción de una etiqueta de la comida para perros Nutrecan Croquetas de
la marca Nutrecan, se les requirió a los estudiantes que subrayaran los compuestos
inorgánicos que lograran identificar, obteniendo los siguientes resultados: un 6 % no
presentó ningún acierto; un 6 % tuvo dos respuestas acertadas; un 6 % seleccionó tres
compuestos de diez posibles; un 14 % presentó cinco respuestas acertadas; un 14 %
obtuvo seis aciertos; un 3 % tuvo un total de siete respuestas correctas; un 25,5 % presentó

50 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
un total de nueve respuestas acertadas y un 25,5 % tuvo diez aciertos con respecto a esta
pregunta. Esto indica que más de la mitad de los estudiantes son capaces de identificar
distintos compuestos inorgánicos que se presentan en las etiquetas.


5. Conclusiones y recomendaciones
5.1 Conclusiones
A partir del desarrollo del trabajo de grado, se formuló una estrategia didáctica centrada en
el aprendizaje activo y la enseñanza situada para la enseñanza aprendizaje de la
nomenclatura de química inorgánica a los jóvenes del grado décimo del Centro Educativo
Rural San José de Castro (Arboledas, Norte de Santander), que se encuentre
contextualizada al nivel educativo de los estudiantes, así como al ritmo de aprendizaje de
los mismos.
En el desarrollo de la estrategia didáctica se utilizaron varias herramientas que se
encontraban disponibles en el Centro Educativo. Sin embargo, no se pudieron desarrollar
prácticas de laboratorio debido a que el salón que se utiliza para las mismas se encontraba
lleno de material de construcción y fue imposible acceder a los materiales que se
necesitaban pues representaba un riesgo para la seguridad del docente y los estudiantes.
A pesar de esta dificultad, se permitió que los estudiantes interactuaran con algunas
sustancias que podían encontrar en su entorno diario y se le explicó que uso tenían algunos
compuestos que encontraban en las etiquetas de dichos productos, esto con el fin que
entendieran que los compuestos inorgánicos no se encuentran solo en el laboratorio, sino
que están a nuestro alrededor y tienen muchos usos.
A partir de los resultados obtenidos durante el desarrollo del trabajo de grado, se pudo
determinar que, aunque los estudiantes de grado décimo no lograron apropiarse de las
normas de nomenclatura de los compuestos inorgánicos, si fueron capaces de identificar
compuestos inorgánicos a partir de la fórmula química y relacionar dicha fórmula con su
nombre dado. Sin embargo, presentan cierta dificultad al momento de nombrar un
compuesto inorgánico a partir de una fórmula dada por medio de cualquiera de los tres
sistemas de nomenclatura (Stock, sistemática y tradicional).

Resultados y análisis de resultados 53
Se pudo presenciar la capacidad de identificar los compuestos inorgánicos presentes en
los productos que se consumen de forma cotidiana, haciendo que estos sean asimilados
como una parte fundamental de la vida diaria.
Uno de los principales factores que incide sobre los bajos resultados en el aprendizaje del
lenguaje científico, ha sido la pobre formación en ciencias en la infancia, debido
principalmente a la escasa formación científica inicial de los maestros. Igualmente, el
modelo educativo flexible modalidad “Escuela Nueva”, implementado en el Centro
Educativo, hace que la formación de los estudiantes sea dada de forma incompleta, puesto
que se cuenta con un solo docente para atender a 5 o 6 grados diferentes en las escuelas
(grado transición a quinto).
Esta falta de docentes en la formación primaria, aunada a la falta de acompañamiento que
brindan los padres de familia a sus hijos; muchos de los cuales tuvieron una educación
bastante básica, que incluye algunos grados de primaria, y algunos de ellos ni siquiera
asistieron a una escuela. Una mala formación en la infancia, hace que las competencias
básicas sean deficientes, por lo que la interpretación, argumentación y proposición de los
estudiantes en las distintas áreas es bastante básica.
Finalmente, el hecho de provenir de familias campesinas, la mayoría de ellas con bajos
recursos económicos, hace que el interés por las actividades académicas sea realmente
poco. Ya que muchos no aspiran continuar con la educación superior, debido a las
condiciones económicas que se presentan en sus hogares. La aspiración de los
estudiantes es lograrse graduar de bachiller y poder comenzar a trabajar para suplir sus
necesidades básicas o para ayudar a su familia.
Todos estos factores, hacen que la apropiación de las normas de nomenclatura de
compuestos inorgánicos, sean bastantes complejas de asimilar por los estudiantes, y por
tanto no hayan sido comprendidas por los mismos. A pesar de habérseles enseñando de
una forma bastante gráfica e ilustrativa.

54 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
5.2 Recomendaciones
Con la elaboración del presente trabajo se recomienda:
- Habilitar un espacio destinado al desarrollo de prácticas experimentales, en el cual los
jóvenes cuenten con los equipos básicos de seguridad y los lugares apropiados para la
manipulación de sustancias químicas.
- Mejorar en los jóvenes el proceso de comprensión lectora, para que de esta forma puedan
interpretar y poder aplicar de forma correcta las normas para la nomenclatura de los
compuestos inorgánicos en los distintos modelos.
- Desarrollar con los estudiantes espacios de conversación, en los cuales ellos puedan
manifestar sus dudas e inquietudes con respecto a los temas vistos en la práctica
educativa.


A. Anexo: Guías utilizadas en la enseñanza de la nomenclatura inorgánica
Centro Educativo Rural San José de Castro REPÚBLICA DE COLOMBIA
SECRETARÍA DE EDUCACIÓN DEPARTAMENTAL NORTE DE SANTANDER
Código DANE: 254051000821
Decreto de Creación 000252 del 12 de Abril de 2005
Resolución 001715 del 03 de Noviembre de 2006
Corregimiento San José de Castro, Arboledas (N. de S.)
ÁREA: QUÍMICA DOCENTE: MARÍA MÓNICA CABRERA GRADO: UNDÉCIMO AÑO: 2018
NOMBRE:
GUÍA No. 2. NOMENCLATURA QUÍMICA
Todos los días, podemos relacionarnos con las personas que nos rodean, gracias a que utilizamos el mismo idioma o lenguaje. De la misma manera, los químicos, sin importar qué idioma hablen en su lugar de origen, necesitan comunicarse entre sí, de manera muy específica. Para ello, han creado un lenguaje propio. Te invitamos a que lo conozcas. LOS SÍMBOLOS Y LAS FÓRMULAS QUÍMICAS A TRAVÉS DE LA HISTORIA El desarrollo de la química como ciencia hizo necesario dar a cada sustancia conocida un nombre que pudiera representarse de forma abreviada, pero que al mismo tiempo incluyera información acerca de la composición molecular de las sustancias y de su naturaleza elemental. Los alquimistas habían empleado ya símbolos para representar los elementos y compuestos hasta entonces conocidos.
Muchos de estos símbolos y fórmulas representaban cuerpos celestes, pues, los primeros químicos pensaban
que las sustancias materiales estaban íntimamente relacionadas con el cosmos. Dalton fue el primero en utilizar un sistema de signos, desprovisto de misticismo, para los diferentes elementos y con base en estos, para algunos compuestos.
Los símbolos modernos para representar los elementos químicos se deben a Berzelius, quien propuso utilizar, en vez de signos arbitrarios, la primera letra del nombre latino del elemento. Cuando varios elementos tuvieran la misma inicial, se representaban añadiendo la segunda letra del nombre. Así, por ejemplo, el carbono, el cobre y el calcio se

A. Anexo: Guías utilizadas en la enseñanza de la nomenclatura inorgánica 57 representan: C, Cu y Ca, respectivamente. Observa que la primera letra del nombre se escribe siempre en mayúscula, mientras que la segunda, cuando está presente, se escribe en minúscula.
De la misma manera como estos símbolos representan elementos, las fórmulas indican la composición molecular de las sustancias, mediante la yuxtaposición de los símbolos de los elementos constituyentes. Para indicar el número de átomos presentes de cada elemento integrante de la molécula, se escribe tal cantidad como un subíndice al lado del correspondiente elemento. Por ejemplo, la fórmula del agua H2O, indica que está constituida por dos átomos de hidrógeno y uno de oxígeno. Las fórmulas químicas se clasifican en: fórmula empírica, fórmula estructural, fórmula electrónica y fórmula molecular. - La fórmula empírica llamada también fórmula mínima o condensada, indica la relación proporcional entre el número de átomos de cada elemento presentes en la molécula, sin que esta relación señale exactamente la cantidad de átomos. Esta fórmula se puede determinar a partir del porcentaje en peso correspondiente a cada elemento. Por ejemplo, CH2O corresponde a la fórmula empírica o mínima de la glucosa, pero su fórmula molecular es C6H12O6. - La fórmula estructural indica la proporción de átomos y la posición o estructura de la molécula. Por ejemplo, la fórmula para la molécula de agua es
- La fórmula electrónica (Lewis) indica los electrones de valencia de cada átomo y la unión o enlace que se presenta. Por ejemplo, la fórmula electrónica del cloruro de bario es
- La fórmula molecular muestra con exactitud la relación entre los átomos que forman la molécula. Es múltiplo de la fórmula empírica, por lo tanto, se puede determinar conociendo la masa molar del compuesto y el peso de la fórmula mínima. Por ejemplo, si la masa molar de la glucosa es 180 g y el peso de la fórmula mínima CH2O es de 30 g, entonces,
𝑛 = 𝑃𝑒𝑠𝑜 𝑑𝑒 𝑙𝑎 𝑓ó𝑟𝑚𝑢𝑙𝑎 𝑚𝑜𝑙𝑒𝑐𝑢𝑙𝑎𝑟
𝑃𝑒𝑠𝑜 𝑑𝑒 𝑙𝑎 𝑓ó𝑟𝑚𝑢𝑙𝑎 𝑚í𝑛𝑖𝑚𝑎=
180 𝑔
30 𝑔= 6
Como la fórmula mínima es CH2O, al multiplicarla por 6 da como resultado C6H12O6 que es la fórmula molecular. VALENCIA Y NÚMERO DE OXIDACIÓN VALENCIA: La valencia es la capacidad de formar enlaces. El concepto de valencia resulta útil en la formulación de compuestos binarios, mientras que el número de oxidación lo es en compuestos de tres o más elementos. Se denomina capa de valencia de un átomo a su capa más externa de electrones. Los electrones de esta capa reciben el nombre de electrones de valencia y determinan la capacidad que tienen los átomos para formar enlaces. Existen dos tipos de valencia: - Valencia iónica: es el número de electrones que un átomo gana o pierde al combinarse con otro átomo mediante un enlace iónico. Así, por ejemplo, cada átomo de calcio pierde dos electrones al formar enlaces iónicos, y por eso la valencia iónica del calcio es dos. Así mismo, cada átomo de oxígeno gana dos electrones al combinarse iónicamente con otro átomo, por lo tanto, su valencia iónica es dos. - Valencia covalente: es el número de pares de electrones que un átomo comparte con otro al combinarse mediante un enlace covalente. Por ejemplo, cada átomo de carbono comparte cuatro pares de electrones al formar enlaces covalentes con otros átomos, y por eso su valencia covalente es cuatro. Algunos elementos poseen más de un número de valencia, lo cual quiere decir que pueden formar más de un compuesto. NÚMERO DE OXIDACIÓN: Se conoce como número de oxidación de un elemento a la carga que posee un átomo de dicho elemento, cuando se encuentra en forma de ion. Los números de oxidación pueden ser positivos o negativos según la tendencia del átomo a perder o ganar electrones. Los elementos metálicos siempre tienen números de oxidación positivos, mientras que los elementos no-metálicos pueden tenerlos positivos o negativos. Similar a lo

58 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
que ocurre con la valencia, un mismo átomo puede tener uno o varios números de oxidación para formar compuestos.
Elemento Símbolo Números de oxidación
Hidrógeno H +1
Oxígeno O -2
Sodio Na +1
Potasio K +1
Calcio Ca +2
Zinc Zn +2
Aluminio Al +3
Hierro Fe +2, +3
Cobre Cu +2, +1
Carbono C +4, +2
Nitrógeno N ±3, +5, +4, +2
Azufre S +2, +4, +6
Cloro Cl ±1, +3, +5, +7
Yodo I ±1, +5, +7
Normas Para Calcular El Número De Oxidación En Compuestos: En la formulación de un compuesto conviene tener en cuenta las siguientes normas: - El número de oxidación de cualquier elemento en estado libre (no combinado) siempre es cero, no importa cuán complicada sea su molécula. - Un compuesto siempre está formado por unos elementos que actúan con número de oxidación positivo y otros con número de oxidación negativo. - Al escribir la fórmula del compuesto se coloca primero el o los elementos que actúen con número de oxidación positivo. - En todo compuesto, la suma algebraica de los números de oxidación de sus elementos multiplicados por los subíndices correspondientes de los mismos, debe ser igual a cero. Por ejemplo, en la fórmula del óxido de aluminio: Al2O3 el aluminio tiene número de oxidación +3 y el oxígeno -2, de manera que: 2 (+3) + 3 (-2) = 0. - Cuando todos los subíndices de una fórmula son múltiplos de un mismo número, se pueden dividir entre este número, obteniéndose así la fórmula simplificada compuesto. Por ejemplo, H2N2O6 se debe escribir HNO3 - La suma algebraica de los números de oxidación de los elementos en un ion debe ser igual a la carga del ion. Por
ejemplo, en el ion carbonato, 𝐶𝑂32−, llamamos X al número
de oxidación del carbono. Como el oxígeno actúa con número de oxidación -2, se debe cumplir que (+X) + 3(-2) = -2, donde X debe ser igual a 4; así, el carbono actúa con +4 Número de oxidación de algunos elementos comunes: - El oxígeno actúa con número de oxidación -2, excepto en los peróxidos donde presenta -1 y en el fluoruro de oxígeno (F2O) donde tiene un número de oxidación atípico de +1, debido a la gran electronegatividad del flúor (4,0). - El hidrógeno actúa con número de oxidación +1, excepto en los hidruros, donde presenta un número de oxidación de -1 - Los metales de los grupos I, II y III siempre tienen números de oxidación de +1, +2 y +3, respectivamente.
- Los metales de transición presentan, por lo regular dos o más números de oxidación positivos, según el número de electrones que entreguen. Por ejemplo, el cobre tiene dos números de oxidación +1 y +2, mientras que el cromo tiene tres números de oxidación: +6, +3 y +2. FUNCIÓN QUÍMICA Y GRUPO FUNCIONAL Se llama función química a un conjunto de compuestos o sustancias con características y comportamiento comunes. Las funciones químicas se describen a través de grupos funcionales que las identifican. Un grupo funcional es un átomo o grupo de átomos que le confieren a los compuestos pertenecientes a una función química, sus propiedades principales. Por ejemplo, la función ácido se reconoce porque en su estructura está presente el grupo funcional H+ (hidrogenión) y la función hidróxido se caracteriza por la presencia del grupo funcional OH- (hidroxilo). Así, la fórmula del ácido clorhídrico es HCI y la del hidróxido de sodio NaOH. En la química inorgánica las funciones más importantes son: óxido, ácido, base y sal.


Centro Educativo Rural San José de Castro REPÚBLICA DE COLOMBIA
SECRETARÍA DE EDUCACIÓN DEPARTAMENTAL NORTE DE SANTANDER
Código DANE: 254051000821
Decreto de Creación 000252 del 12 de Abril de 2005
Resolución 001715 del 03 de Noviembre de 2006
Corregimiento San José de Castro, Arboledas (N. de S.)
ÁREA: QUÍMICA DOCENTE: MARÍA MÓNICA CABRERA GRADO: UNDÉCIMO AÑO: 2018
NOMBRE:
GUÍA No. 3. FUNCIONES INORGÁNICAS
Se llama función química a un conjunto de compuestos o sustancias con características y comportamientos comunes. Las funciones químicas se describen a través de grupos funcionales que las identifican. Un grupo funcional es un átomo o grupo de átomos que le confieren a los compuestos pertenecientes a una función química, sus propiedades principales. En la química inorgánica las funciones más importantes son: óxido, ácido, base y sal. FUNCIÓN ÓXIDO Los óxidos son compuestos inorgánicos binarios (constituidos por dos elementos), que resultan de la combinación entre el oxígeno y cualquier otro elemento. Cuando el elemento unido al oxígeno es un metal, el compuesto se llama óxido básico, mientras que, si se trata de un no metal, se le denomina óxido ácido. Para nombrar este tipo de compuestos basta recordar las siguientes reglas: - El oxígeno en la gran mayoría de sus compuestos actúa con número de oxidación -2. - En todo compuesto la suma algebraica de los números de oxidación de sus elementos debe ser igual a cero. Al nombrar o escribir las fórmulas de los óxidos se pueden presentar tres situaciones: - Elementos con un único número de oxidación: Se incluyen en esta categoría los elementos de los grupos 1, 2 y 3. En este caso para expresarla fórmula del compuesto basta con escribir los símbolos de los elementos involucrados dejando un espacio entre ellos para anotar los subíndices numéricos que permiten equilibrar el número de cargas positivas y negativas del compuesto de tal manera que se cumpla la segunda regla. Ejemplos: 1. Tomemos un elemento del grupo 1, como el sodio. - Número de oxidación del sodio, Na: +1 - Número de oxidación del oxígeno, O: -2 - Fórmula del óxido: Na2O - Nombre del óxido: Óxido de sodio Se puede decir entonces que la proporción en que se combinan estos elementos con el oxígeno es de 2:1. 2. Tomemos un elemento del grupo 2, como el calcio.
- Número de oxidación del sodio, Ca: +2 - Número de oxidación del oxígeno, O: -2 - Fórmula del óxido: CaO - Nombre del óxido: Óxido de calcio De lo anterior podemos deducir que los elementos del grupo 2 se combinan con el oxígeno en la proporción 1:1. - Elementos que presentan dos números de oxidación: En este caso, estos elementos pueden combinarse con el oxígeno para dar lugar a dos tipos de óxidos, con propiedades químicas y físicas propias y que de igual forma reciben nombres y fórmulas distintos. Dentro de la nomenclatura tradicional se emplean sufijos que permiten diferenciar las dos clases de óxidos. Ejemplo: - Números de oxidación del Hierro, Fe: +2, +3 - Número de oxidación del oxígeno, O: -2 - Fórmulas de los óxidos: FeO (+2), Fe2O3 (+3). Nótese que en la primera fórmula la proporción es 1:1, mientas que en la segunda es 2:3. De esta manera las cargas positivas y negativas se equilibran y se cumple la segunda regla. Nomenclatura tradicional: Para diferenciar el primer óxido del segundo se emplea el sufijo -oso para el óxido formado con el menor número de oxidación (+2), e -ico para el óxido formado con el mayor número de oxidación (+3). Los nombres serán entonces óxido ferroso (FeO) y óxido férrico (Fe2O3). Nomenclatura stock: En este sistema se nombra el óxido incluyendo en el nombre el número de oxidación del elemento. Dicho número se escribe dentro de un paréntesis en números romanos. Por ejemplo, el FeO es óxido de hierro(II) y el Fe2O3, óxido de hierro(III). Nomenclatura sistemática: Empleado para nombrar óxidos ácidos (no metal y oxígeno). Según este sistema los óxidos se nombran con la palabra genérica óxido anteponiéndole prefijos de origen griego, como mono-, di-, tri-, tetra-, penta-, etc., para indicar la cantidad de átomos de oxígeno presentes en la molécula. Algunos ejemplos son: CO: monóxido de carbono, NO2: dióxido de nitrógeno y SO3: trióxido de azufre. - Elementos con tres o cuatro números de oxidación: En este caso se forman tres o cuatro óxidos con fórmulas, nombre y propiedades distintas, según el caso. Ejemplo:

A. Anexo: Guías utilizadas en la enseñanza de la nomenclatura inorgánica 61 1. Elemento con tres números de oxidación: Azufre (S) - Números de oxidación del Azufre, S: +2, +4, +6 - Número de oxidación del oxígeno, O: -2 - Fórmulas de los óxidos: SO (+2), SO2 (+4), SO3 (+6). Para nombrar el segundo y el tercer óxido basta con aplicar la misma norma del caso anterior. Es decir, el SO2 recibirá el nombre de óxido sulfuroso, mientras que el SO3 se llamará óxido sulfúrico. Para nombrar el óxido que tiene el menor número de oxidación de los tres, es decir, S+2, es necesario anteponer al nombre del óxido el prefijo hipo (“por debajo de”), seguido de la raíz del nombre del elemento con la terminación oso. En este caso el nombre del SO será óxido hiposulfuroso. 2. Elemento con cuatro números de oxidación: Cloro (Cl). - Números de oxidación del Cloro, Cl: +1, +3, +5, +7 - Número de oxidación del oxígeno, O: -2 - Fórmulas de los óxidos: Cl2O (+1), Cl2O3 (+3), Cl2O5 (+5), Cl2O7 (+7). Para nombrar estos óxidos empleamos la misma regla del caso anterior, pero añadimos el prefijo per o hiper (“por encima de”) para el óxido formado cuando el cloro actúa con el mayor número de oxidación, en este caso, +7. Los nombres son: óxido hipocloroso (Cl2O), óxido cloroso (Cl2O3), óxido clórico (Cl2O5) y óxido perclórico (Cl2O7). FUNCIÓN HIDRÓXIDO Los hidróxidos, también llamados bases, se caracterizan por liberar iones OH-, en solución acuosa. Esto les confiere pH alcalino a las soluciones. Se caracterizan por tener un sabor amargo. Son compuestos ternarios formados por un metal, hidrógeno y oxígeno. Todos los hidróxidos se ajustan a la fórmula general M(OH)x, donde M es el símbolo del metal y x corresponde al valor absoluto de su número de oxidación, ya que el ion OH tiene una carga negativa. Se denominan con la palabra hidróxido seguida del elemento correspondiente. Si se trata de un metal con más de un número de oxidación, se adiciona el sufijo -oso al nombre, para el menor, e -ico para el mayor. Empleando la nomenclatura stock se escribe el número de oxidación entre paréntesis como en el caso de los óxidos. Ejemplo: - Hidróxido de sodio
𝑁𝑎2𝑂(𝑠) + 𝐻2𝑂(𝑙) ⟶ 2𝑁𝑎𝑂𝐻(𝑎𝑐)
- Hidróxidos de cromo: dado que el cromo puede formar dos hidróxidos, se tienen las siguientes reacciones que dan lugar a los correspondientes hidróxidos:
𝐶𝑟𝑂(𝑠) + 𝐻2𝑂(𝑙) → 𝐶𝑟(𝑂𝐻)2(𝑎𝑐)
Hidróxido de cromo (II)
𝐶𝑟2𝑂3(𝑠) + 3𝐻2𝑂(𝑙) → 2𝐶𝑟(𝑂𝐻)3(𝑎𝑐)
Hidróxido de cromo (III)
Las bases son importantes para la industria puesto que son reactivos indispensables en la fabricación de jabones, detergentes y cosméticos. FUNCIÓN ÁCIDO Los ácidos son sustancias que se caracterizan por liberar iones H+ cuando se encuentran en solución acuosa. Además, presentan sabor agrio. Existen dos clases de ácidos inorgánicos: - Ácidos hidrácidos: son compuestos binarios que contienen solamente hidrógeno y un no-metal, en estado gaseoso se nombran como haluros. En solución acuosa se comportan como ácidos y para nombrarlos se antepone la palabra ácido seguida de la raíz del elemento con la terminación hídrico. Por ejemplo: F2(g) + H2(g) 2HF(g) fluoruro de hidrógeno HF(ac) se llama ácido fluorhídrico cuando se encuentra en disolución acuosa. El hidrógeno trabaja con número de oxidación positivo +1, en estos ácidos el no metal debe tener número de oxidación negativo. Ejemplo: H+1CI-1 - Ácidos oxácidos: son compuestos ternarios que contienen hidrógeno, oxígeno y un no-metal en su molécula. Se obtienen de la reacción entre un óxido ácido, es decir, formado por un no-metal y el agua. En la fórmula se coloca en primer lugar el hidrógeno, luego el no-metal y por último el oxígeno. En la nomenclatura de los ácidos oxácidos se utilizan los mismos prefijos y sufijos empleados con los óxidos. Veamos. - Del óxido hipocloroso:
𝐶𝑙2𝑂(𝑠) + 𝐻2𝑂(𝑙) → 𝐻2𝐶𝑙2𝑂2(𝑎𝑐) → 2𝐻𝐶𝐼𝑂(𝑎𝑐)
Ácido hipocloroso - Del óxido sulfúrico:
𝑆𝑂3(𝑠) + 𝐻2𝑂(𝑙) → 𝐻2𝑆𝑂4(𝑎𝑐)
Ácido sulfúrico Cuando reaccionan el óxido bórico, el óxido hipofosforoso, el óxido fosforoso y el óxido fosfórico con el agua, se obtienen varios ácidos dependiendo del número de moléculas de agua que se añadan al óxido. Sin embargo, la forma más estable de los ácidos obtenidos, corresponde a la reacción del óxido con tres moléculas de agua: - Del óxido fosforoso:
𝑃2𝑂3(𝑔) + 3𝐻2𝑂(𝑙) 𝐻6𝑃2𝑂6(𝑎𝑐) → 𝐻3𝑃𝑂3(𝑎𝑐)
Ácido fosforoso — Del óxido fosfórico:
𝑃2𝑂5(𝑠) + 3𝐻2𝑂(𝑙) 𝐻8𝑃2𝑂8(𝑎𝑐) → 𝐻4𝑃𝑂4(𝑎𝑐)
Ácido fosfórico

62 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
FUNCIÓN SAL Las sales se definen como las sustancias resultantes de la reacción entre los ácidos y las bases. También pueden resultar de combinaciones entre un metal y un no-metal, con el oxígeno. Las sales son compuestos binarios, ternarios o cuaternarios, que resultan de la unión de una especie catiónica con una especie aniónica, las cuales provienen del ácido y la base involucradas. El catión es, por lo general, un ion metálico, aunque también existen sales de iones como el amonio
(𝑁𝐻4+1). El anión proviene normalmente del ácido. En
consecuencia, puede ser un anión simple o monoatómico
(Cl-1, S-2, etc.) o un ion poliatómico (𝑆𝑂42−, 𝑁𝑂3
1−, 𝐶𝑙𝑂1−, etc.). Por ejemplo: el ácido clorhídrico y el hidróxido de sodio reaccionan para formar el cloruro de sodio o sal común, según la ecuación: HCl + NaOH NaCl + H2O Ácido Hidróxido Cloruro Agua clorhídrico de sodio de sodio Para nombrar las sales es necesario saber qué catión y qué anión intervienen en su formación. Veamos. - Los cationes: reciben el nombre del elemento del cual provienen. Por ejemplo, el ion sodio es Na+1 y el ion aluminio es Al+3. Si se trata de un metal, con capacidad para formar dos iones, éstos se distinguen por las terminaciones -oso, para el menor, e -ico, para el mayor. Si se usa el sistema stock, la valencia del metal se indica entre paréntesis. Por ejemplo: — Fe+2 es el ion ferroso o hierro (II). — Fe+3 es el ion férrico o hierro (III).
Símbolo Nombre Símbolo Nombre
𝑁𝐻4+ Ion amonio 𝑁𝑖+3
Ion níquel (III) o ion niquélico
𝐴𝑔+ Ion plata 𝑃𝑑+2
Ion paladio (II) o ion paladioso
𝐶𝑢+1 Ion cobre (I) o ion cuproso
𝑃𝑑+4 Ion paladio (IV) o ion paládico
Símbolo Nombre Símbolo Nombre
𝐶𝑢+2
Ion cobre (II) o ion cúprico
𝐶𝑜+2
Ion cobalto (II) o ion cobatoso
𝐻𝑔+1
Ion mercurio (I) o ion mercurioso
𝐶𝑜+3
Ion cobalto (III) o ion cobáltico
𝐻𝑔+2
Ion mercurio (II) o ion mercúrico
𝑆𝑛+2
Ion estaño (II) o ion estannoso
𝐴𝑢+1 Ion oro (I) o ion auroso
𝑆𝑛+3
Ion estaño (III) o ion estánnico
𝐴𝑢+3 Ion oro (III) o oin aúrico
𝑃𝑏+2 Ion plomo (II) o ion plumboso
𝐹𝑒+2
Ion hierro (II) o ion ferroso
𝑃𝑏+4
Ion plomo (IV) o ion plúmbico
𝐹𝑒+3 Ion hierro (III) o ion férrico
𝑃𝑡+2 Ion platino (II) o ion platinoso
𝑁𝑖+2
Ion níquel (II) o ion niqueloso
𝑃𝑡+4
Ion platino (IV) o ion platínico
Cationes más comunes - Los aniones: cuando los ácidos se encuentran en solución acuosa, se disocian o separan, en iones con carga positiva y negativa, en razón a la fuerte atracción que ejercen las moléculas del agua sobre las del ácido. Como vimos, los ácidos se caracterizan porque siempre presentan hidrógeno, así, al disociarse, se forman iones H+, además de iones negativos, cuya composición depende de los demás elementos presentes. Por ejemplo:
− 𝐻𝐶𝑙 𝐻+ + 𝐶𝑙− − 𝐻𝑁𝑂3 𝐻+ + 𝑁𝑂3
1− − 𝐻2𝑆𝑂4 ⇋ 2𝐻+ + 𝑆𝑂4
2− Para nombrar los aniones se considera el nombre del ácido del cual provienen y se procede de la siguiente manera: Si el ácido termina en -hídrico, el anión terminará en -uro. Si el ácido termina en -oso, el anión terminará en -ito. Si el ácido termina en -ico, el anión terminará en -ato. Para los ejemplos anteriores tenemos: - Del ácido clorhídrico, según la reacción
𝐻𝐶𝑙 ⇌ 𝐻+ + 𝐶𝐼1−, se obtiene el anión cloruro.
- Del ácido nítrico, 𝐻𝑁𝑂3 ⇌ 𝐻+ + 𝑁𝑂31−, se obtiene el anión
nitrato.
- Del ácido sulfúrico, 𝐻2𝑆𝑂4 ⇌ 2𝐻+ + 𝑆𝑂42−, se forma el
anión sulfato.

A. Anexo: Guías utilizadas en la enseñanza de la nomenclatura inorgánica 63
Nombre del ácido Nombre de la sal
_________hídrico __________uro
Hipo________oso Hipo_______ito
____________oso ___________ito
____________ico ___________ato
Per_________ico Per________ato
Nomenclatura de las sales oxácidas
Símbolo Nombre
𝐹− Ion fluoruro
𝐶𝑙− Ion cloruro
𝐵𝑟− Ion bromuro
𝐼− Ion yoduro
𝑆2− Ion sulfuro
𝐶𝑁− Ion cianuro
𝐶𝑙𝑂− Ion hipoclorito
𝐶𝑙𝑂2− Ion clorito
𝐶𝑙𝑂3− Ion clorato
𝐶𝑙𝑂4− Ion perclorato
𝑀𝑛𝑂4− Ion permanganato
𝐻𝐶𝑂3− Ion bicarbonato
𝑁𝑂2− Ion nitrito
𝑁𝑂3− Ion nitrato
𝑆𝑂32− Ion sulfito
𝑆𝑂42− Ion sulfato
𝐶𝑂22− Ion carbonito
𝐶𝑂32− Ion carbonato
𝑃𝑂33− Ion fosfito
𝑃𝑂43− Ion fosfato
𝐶𝑟𝑂42− Ion cromato
𝐶𝑟2𝑂72− Ion dicromato
Aniones más comunes




B. Anexo: Prueba final
Centro Educativo Rural San José de Castro REPÚBLICA DE COLOMBIA
SECRETARÍA DE EDUCACIÓN DEPARTAMENTAL NORTE DE SANTANDER
Código DANE: 254051000821
Decreto de Creación 000252 del 12 de Abril de 2005
Resolución 001715 del 03 de Noviembre de 2006
Corregimiento San José de Castro, Arboledas (N. de S.)
ÁREA: QUÍMICA DOCENTE: MARÍA MÓNICA CABRERA GRADO: UNDÉCIMO AÑO: 2018 Nombre: __________________________________________ Fecha: ____________
BIMESTRAL CUARTO PERIODO
1. Relaciona los términos de la izquierda con las definiciones
a. Función ácido
Son sustancias que se caracterizan por liberar iones OH- cuando se encuentran en solución acuosa
b. Función óxido
A veces el oxígeno puede presentar estado de oxidación -1. Estos compuestos muestran un alto poder oxidante.
c. Función sal
Son compuestos binarios formados por hidrógeno y cualquier otro elemento menos electronegativo que el hidrógeno. Son una excepción, en la cual el hidrógeno actúa con número de oxidación 1- .
d. Función hidróxido
Son sustancias que se caracterizan por liberar iones H+ cuando se encuentran en solución acuosa
e. Función hidruro
Se definen como las sustancias resultantes de la reacción entre los ácidos y las bases. También pueden resultar de combinaciones entre un metal y un no-metal, con el oxígeno.
f. Función peróxido
Son compuestos inorgánicos binarios formados por la combinación de un elemento más el oxígeno.
2. Identifica si son óxidos (O), hidróxidos (H), ácidos (A) o sales (S).
___ NaOH ___ TiO2
___ CaCO3 ___ NaHCO3
___ H2SO4 ___ HNO3
___ KNaSO4 ___ Ca(OH)2
___ SO3 ___ AlOH(NO3)2
3. Nombra los siguientes óxidos según la nomenclatura tradicional: Cl2O ____________________________________ Cl2O3 ____________________________________ Cl2O5 ____________________________________ Cl2O7 ____________________________________ 4. Nombra los siguientes óxidos según la nomenclatura sistemática: Fe2O3 ____________________________________ Cu2O ____________________________________ SO2 ____________________________________ CuO ____________________________________ Br2O5 ____________________________________ 5. Nombra los siguientes óxidos según la nomenclatura stock: FeO ____________________________________ Cu2O ____________________________________ SO3 ____________________________________

60 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
CO2 ____________________________________ NO2 ____________________________________ 6. Relaciona el compuesto con su nombre correspondiente:
a. NaOH
Bicarbonato de sodio
b. CaCO3
Hidróxido de calcio
c. H2SO4
Óxido de azufre
d. KNaSO4
Hidróxido de sodio
e. SO3
Nitrato básico de aluminio
f. TiO2
Ácido sulfúrico
g. NaHCO3
Carbonato de calcio
h. HNO3
Sulfato de sodio y potasio
i. Ca(OH)2
Dióxido de titanio
j. AlOH(NO3)2
Ácido nítrico
7. Identifica si es un anión o un catión
Fe2+
CN-
ClO4-
Pt4+
Pd4+
CrO42-
Au3+
MnO4-
Cu2+
NH4+
8. La comida para perros Nutrecan Croquetas tiene los siguientes ingredientes: Maíz y/o sorgo
Torta de soya
Harina de carne y/o harina de pescado
Harina de trigo
Harina de maíz
Mogolla de trigo
Grasa animal
Carbonato de calcio
Fosfatos mono o dicálcicos
Cloruro de sodio
Cloruro de potasio
Vitamina A
Vitamina D3
Vitamina E
Vitamina K
Vitamina B1
Vitamina B2
Vitamina B6
Pantotenato de calcio
Biotina
Ácido fólico
Niacina
Vitamina B12
Cloruro de colina
Sulfato de cobre
Sulfato de zinc
EEDI
Selenito de sodio
Óxido de manganeso
Óxido de magnesio
Sulfato ferroso
Antioxidante (BHT, etoxiquina)
Aminoácidos sintéticos (lisina, metionina)
A partir de la temática vista, subraya los compuestos inorgánicos estudiados (óxidos, ácidos, hidróxidos y sales)

Referencias bibliográficas
Araque Marín, P., & Mazo Lopera, M. A. (2015). Estrategia didáctica para la enseñanza y
aprendizaje de la nomenclatura inorgánica en estudiantes de primer semestre de la escuela de ingeniería de Antioquia. Encuentro Internacional de Educación en Ingeniería. Cartagena. Recuperado el 16 de Noviembre de 2017, de https://www.acofipapers.org/index.php/eiei2015/2015/paper/viewFile/1012/362
Bernadelli, C. (2015). Diseño de Taller para la Enseñanza de Nomenclatura Química. (E. e. Universitaria, Ed.) La Plata, Argentina: Universidad Nacional de La Plata. Recuperado el 16 de Noviembre de 2017, de http://sedici.unlp.edu.ar/bitstream/handle/10915/52795/Documento_completo.pdf-PDFA.pdf?sequence=3
Borsese, A. (2000). Comunicación, lenguaje y enseñanza. Educación química, 11(2), 220-227. doi:http://dx.doi.org/10.22201/fq.18708404e.2000.2.66456
Cantillo Maldonado, I. I. (2016). Enseñanza-aprendizaje de la nomenclatura química inorgánica a través de un modelo didáctico integrador. Valledupar, Colombia: Universidad Nacional de Colombia. Recuperado el 16 de Noviembre de 2017, de http://www.bdigital.unal.edu.co/54119/1/49798125.2016.pdf
Cisneros Estupiñan, M. (2011). Ciencia y lenguaje en el contexto académico. Lenguaje, 36 (1), 117-137. Recuperado el 16 de Noviembre de 2017, de https://media.utp.edu.co/referencias-bibliograficas/uploads/referencias/articulo/634-ciencia-y-lenguaje-en-el-contexto-academicopdf-RO72h-articulo.pdf
DANE, D. A. (2017). Encuesta de Consumo Cultural (ECC) 2016. Bogotá. Recuperado el 16 de Noviembre de 2017, de https://www.las2orillas.co/wp-content/uploads/2017/05/CIFRAS-LIBROS-LEIDOS-COLOMBIANOS-Y-EL-MUNDO.pdf
De Jaime Lorén, J. M. (2010). Torbern Olof Bergman. Epónimos Científicos. Recuperado el 16 de Noviembre de 2017, de https://blog.uchceu.es/eponimos-cientificos/wp-content/uploads/sites/24/2011/10/epo-BERGMAN.pdf
Díaz Barriga, F. (2003). Cognición situada y estrategias para el aprendizaje significativo. Revista Electrónica de Investigación Educativa, 5(2). Recuperado el 16 de Noviembre de 2017, de http://redie.ens.uabc.mx/vol5no2/contenido-arceo.html
Díaz Suarez, P., Vargas Rojas, D., & Pérez Miranda, R. (2009). Análisis histórico – epistemológico de nomenclatura Química Inorgánica. Tecné, Episteme y Didaxis: TEA. Recuperado el 16 de Noviembre de 2017, de http://revistas.pedagogica.edu.co/index.php/TED/article/viewFile/187/175
Esteba Ramos, D. (2013). Recursos y estrategias para un aprendizaje activo del alumno en el aula ELE. Actas del I Congreso Internacional de Didáctica de Español como Lengua Extranjera del Instituto Cervantes de Budapest. Budapest. Recuperado el 16 de Noviembre de 2017,

62 Enseñanza de la nomenclatura de química inorgánica como lenguaje científico especializado en el área de química
de https://cvc.cervantes.es/ensenanza/biblioteca_ele/publicaciones_centros/PDF/budapest_2013/43_esteba.pdf
Gómez - Moliné, M., Morales, M. L., & Reyes-Sánchez, L. B. (2008). Obstáculos detectados en el aprendizaje de la nomenclatura química. Educación química, 19(3), 201-206. Obtenido de http://www.scielo.org.mx/pdf/eq/v19n3/v19n3a7.pdf
Hernández Fandiño, O. (Diciembre de 2011). Estrategia para aprender la nomenclatura de ácidos, sales e iones monoatómicos y poliatómicos inorgánicos. (U. T. Pereira, Ed.) Scientia et Technica. Recuperado el 18 de Octubre de 2017, de https://mail.google.com/mail/u/0/#search/orlando/15f1bb310c1333b8
IUPAC. (2005). Nomenclature of inorganic chemistry. RSC Publishing. Obtenido de https://www.iupac.org/cms/wp-content/uploads/2016/07/Red_Book_2005.pdf
Jerez Y., O. (2015). Aprendizaje Activo, Diversidad e Inclusión. Chile: Universidad de Chile. Recuperado el 03 de Noviembre de 2017, de http://www.plataforma.uchile.cl/libros/MANUAL_AA_01_dic_2014.pdf
Laurella, S. L. (2015). Nomenclatura: Enseñanza en contexto. Actas IV Jornadas de Enseñanza e Investigación Educativa en el campo de las Ciencias Exactas y Naturales. Facultad de Humanidades y Ciencias de la Educación. Universidad Nacional de La Plata. La Plata. Recuperado el 03 de Noviembre de 2017, de http://jornadasceyn.fahce.unlp.edu.ar/convocatoria
Mayeem, B. P. (2018). Understanding of Chemicai Formulae And Nomenclature Of Inorganic Compounds Using Improvised Conceptual Models Among Teacher-Trainees In Offinso And Atebubu Colleges Of Education In Ghana. International Journal of Scientific Research and Management, 6(10). Obtenido de https://ijsrm.in/index.php/ijsrm/article/view/1814/1623
Ministerio de Educación Nacional. (2006). Estándares Básicos de Competencias en Lenguaje, Matemáticas, Ciencias y Ciudadanas.
Ministerio de Educación Nacional, M. (2016). Derechos Básicos de Aprendizaje Ciencias Naturales (Vol. 1).
Montagut Bosque, P. (2010). Los procesos de enseñanza y aprendizaje del lenguaje de la química en estudiantes universitarios. Educación química, 21(2), 126-138. Obtenido de http://www.scielo.org.mx/pdf/eq/v21n2/v21n2a4.pdf
Pinzón Martín, C. P. (2016). Estrategia didáctica para la enseñanza de la nomenclatura de los compuestos inorgánicos. Bogotá, Colombia: Universidad Nacional de Colombia. Obtenido de http://bdigital.unal.edu.co/56614/7/CindyP.Pinz%C3%B3nMart%C3%ADn.2016.pdf
Sandoval, M., Mandolesi, M., & Cura, R. (2013). strategias didácticas para la enseñanza de la química en la educación superior. Educación y Educadores, 16 (1). Recuperado el 14 de Noviembre de 2017, de http://educacionyeducadores.unisabana.edu.co/index.php/eye/article/view/2283/3078
Sierra Gómez, H. (2013). El aprendizaje activo como mejora de las actitudes de los estudiantes hacia el aprendizaje. Recuperado el 16 de Noviembre de 2017, de https://academica-e.unavarra.es/bitstream/handle/2454/9834/TFM%20HELENA%20SIERRA.pdf
Solís Correa, H. E. (2014). Nomenclatura Química. México, D.F.: Grupo Editorial Patria. Triana Beltrán, G. (2016). El problema del lenguaje y la enseñanza de las ciencias. Revista Digital
Perfiles Libertadores, 1, 116-124. Recuperado el 16 de Noviembre de 2017, de http://publicaciones.libertadores.edu.co/index.php/perfiles_libertadores/article/view/612/580