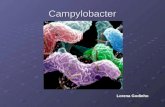
CAMPYLOBACTER
-
Upload
rosa-karina-vasquez-reyes -
Category
Documents
-
view
1.446 -
download
3
Transcript of CAMPYLOBACTER

UNIVERSIDAD NACIONAL
PEDRO RUIZ GALLO
“ FACULTAD DE CIENCIAS BIOLOGICAS”
TEMA: FAMILIA CAMPYLOBACTERIACEAE
CURSO: BACTERIOLOGIA.
DOCENTE: M.Sc. OLGA FRANCIA ARANA.
ALUMNA: LLANOS OLIVERA CINTHYA J.
CODIGO: 055507- K
Lambayeque, AGOSTO del 2009.
Familia: Campylobacteriaceae 1/14

INDICE
FAMILIA CAMPYLOBACTERIACEAEI.INTRODUCCION------------------------------------------------------------------------------
II. IMPORTANCIA--------------------------------------------------------------------------------
III. CARACTERIS TICAS
GENERALES----------------------------------------------------
IV. CLASIFICACION TAXONOMICA ------------------------------------------------------
V. GÉNERO Campylobacter
-----------------------------------------------------------------
1. MORFOLOGIA -------------------------------------------------------------------
-
2. FISIOLOGIA -----------------------------------------------------------------------
3. ESTRUCTURA ANTIGENICA
-------------------------------------------------
4. DETERMINANTES DE PATOGENICIDAD--------------------------------
5. INMUNIDAD --------------------------------------
---------------------------------
6. IDENTIFICACION EN EL LABORATORIO
---------
-----------------------
ANEXOSa. Tratamiento:-----------------------------------------------------------------------
b. Pruebas de Aglutinación del Latex para la identificación de
especies de Campylobacter. -------------------------------------------------
c. Sondas de Ácidos Nucleicos--------------------------------------------------
d. Prueba de ureasa en Biopsia (CLOTEST) --------------------------------
BIBLIOGRAFIA
Familia: Campylobacteriaceae 2/14

FAMILIA CAMPYLOBACTERIACEAE
I. INTRODUCCION
El aislamiento inicial del género Campylobacter en 1909 se clasificó como
Vibrio fetus, debido a su morfología.
Se creo un nuevo género el Campylobacter cuando se reconoció que no
estaba relacionado con la familia Vibrionaceae sobre la base de su diferente
composición de bases nucleotídicas, así como la incapacidad para utilizar
los azúcares de forma oxidativa o fermentativa.
En 1947, se reconoció el primer caso de infección humana y luego se aisló
C. fetus y otros microorganismos del género Campylobacter de: la sangre,
líquido cefalorraquídeo y las heces.
II. IMPORTANCIA
Las infecciones causadas por campilobacterias tienen gran interés debido a
las serias perdidas económicas que se experimentan como resultado de los
abortos y la infertilidad de los bovinos y los ovinos infectados.
Reservorios de los cuales se aislan:
C. jejuni aves de corral, perros,
gatos, ovinos, bovinos Reservorios de
C. coli porcinos infección humana
C. fetus ovinos y bovinos
C. lari gaviotas
III. CARACTERISTICAS GENERALES
a. Forma: son bacterias Gram – negativas, de forma helicoidal o de
vibriode. Sin esporas.
b. Metabolismo respiratorio: son microaerófila; requieren menor
cantidad de oxígeno y capnófilas; requieren mayor cantidad de
CO2.
c. Movilidad: son móviles por medio de un flagelo no envainado
único, polar.
Familia: Campylobacteriaceae 3/14

d. Hábitat: la mayoría de las especies se hallan como comensales
en el tracto intestinal, órganos reproductores y cavidad bucal de
gran cantidad de animales salvajes y domésticos.
e. Contenido de G + C(%mol): 30 - 38
f. Hidratos de carbono: no fermentados ni oxidados.
g. Oxidasa y catalasa: positivas y Ureasa: negativa.
h. Obtienen la energía de la utilización de aminoácidos e
intermediarios de cuatro y seis carbonos del ciclo de Krebs.
i. Existe gran diversidad fenotípica y genotípica aun dentro de las
especies actualmente reconocidas como Campylobacter.
IV. CLASIFICACION TAXONOMICA:
Según El Manual Determinativo de Bacteriología de Bergey
( 9 na edición)
CATEGORIA 1: EUBACTERIAS GRAM - NEGATIVAS QUE TIENEN
PARED CELULAR.
GRUPO 2: BACTERIAS GRAM NEGATIVAS AEROBIAS O
MICROAEROFILAS, HELICOIDALES O VIBRIODES
MOVILES
Según EL Manual Sistemático de Bacteriología de Bergey
Se encuentra en el Volumen II: Proteobacterias
Sección XIX: - Proteobacterias
• Dominio : Bacteria
• Phylum : Proteobacteria.
• Clase : Epsilonproteobacteria class. nov.
• Orden : Campylobacteriales ord. nov.
• Familia : Campylobacteriaceae
• Género : Campylobacter
• Especie : Campylobacter jejuni
Campylobacter fetus
Campylobacter coli
Familia: Campylobacteriaceae 4/14

Campylobacter lari
V. GÉNERO Campylobacter
1. MORFOLOGIA
El nombre del género Campylobacter deriva de la palabra Campylo, que
significa curvado.
Son bacilos gram negativos helicoidalmente curvados y delgados; miden
0,2 a 0,5 µm de ancho y de 0,5 a 5 µm de longitud.
Se han informado diversas formas morfológicas de Campylobacter:
Formas en espiral: abundantes en tejidos jóvenes.
Formas en S
Forma en ala de gaviota: bacilos típicos en frotis de heces
teñidas con tinción de Gram.
Forma de coma: cuando se ven en los tejidos infectados.
Formas cocoides o filamentosas: después del aislamiento
en el laboratorio. Predominan en cultivos viejos. En
paricular después de que las colonias fueran expuestas al
aire ambiental.
La mayoría de especies presenta flagelo unipolar o bipolar; sin vaina; los
microorganismos tienen un tipo de motilidad distintivo en sacacorchos
rápido; con un solo flagelo polar.
2. FISIOLOGIA
Las bacterias son microaerófilas requieren baja tensión de O2 (3 a 15%)
y un nivel aumentado de CO2 (3 a 5%) para su proliferación.
Son sensibles al peroxido de hidrogeno y a los iones superoxido que
aparecen en los medios de cultivo cuando se exponen al aire y a la luz.
Las campilobacterias son incapaces de utilizar los azucares de forma
oxidativa o fermentativa.
3. ESTRUCTURA ANTIGENICA
Los estudios acerca de la configuración antigénica del genero
Campylobacter se han encontrado en estructuras de superficie de
Familia: Campylobacteriaceae 5/14

C jejuni. Esta especie es antigénicamente diversa como lo indica
la demostración de:
o 50 serotipos termoestables sobre la base del LPS.
o 36 serotipos sobre la base de los antígenos flagelares.
Candidatos para inclusión de vacunas contra campilobacterias.
o Proteína de superficie en cepas de variedad de
serotipos termolábiles.
o OMP principal relación antigénica con OMP principales
de diversos serotipos de campilobacterias; es probable
que esta proteína sea una molécula de porina ya que es
una proteína transmembrana y se asocia con el
peptidoglucano.
Diferencias entre la estructura de superficie de C. fetus y
C. jejuni.
C. fetus C. jejuni.
Microcápsula o capa S
Antígeno proteico compuesto por
formaciones proteicas irregulares
tienen forma de enrejado
cristalino, curen la superficie
celular.
La capa es antifagocítica y
desempeña un papel central en la
patogenia de C. fetus.
Puede sobrevivir a ingestión por fagotitos mononucleares, lo que representa mecanismo de supervivencia.
Proteína S
Da resistencia al efecto del suero
humano o de conejo normal o
inmune.
Es una proteína de APM
constituyente de la capsula
Es sensible
Familia: Campylobacteriaceae 6/14

bacteriana y de las proteínas de
superficie.
Impide fijación del C3b,
conduciendo a una opsonización
defectuosa.
Lipopolisacárido
De tipo liso en general se asocia
resistencia al suero.
Antígeno O
Posee cadenas constituidas por el
polisacárido y tienen y tienen
longitud intermedia, todas son
homogéneas a diferencia de las
enterobacterias que son
heterogéneas.
El LPS es del tipo LOS de BPM y parece antigénicamente diferente lo cual explicará el gran numero de serotipos.
Flagelos
El análisis inmunoquímico de la
flagelina revela la presencia de
epítopes en la superficie
Los flagelos
son
importantes
antígenos de
superficie, la
flagelina de C.
jejuni se
diferencia de
C. fetus.
Tipificacion
La serotipificación del C. jejuni y el C. coli es útil para estudios de
epidemiología. Dos métodos:
o Método de Penner Antígenos termoestables solubles
Técnica de hemoaglutinación indirecta.
Familia: Campylobacteriaceae 7/14

o Método de Lior Antígenos termolábiles
Técnica de aglutinación en portaobjetos.
4. DETERMINANTES DE PATOGENICIDAD
Se han identificado tres propiedades potencialmente patogénicas del C.
jejuni.
4.1.La invasividad
Para la colonización son cruciales los flagelos que incrementan la
adherencia y que en virtud de su motilidad permiten que los
microorganismos atraviesen la capa mucosa que cubre la superficie del
intestino.
4.2.La producción de enterotoxina
Las cepas de Campylobacter aisladas de pacientes con diarrea acuosa
producen una enterotoxina termolábil.
La toxina causa una diarrea secretora por la estimulación de la actividad
de la adenilato ciclasa en la mucosa intestinal y por la alteración del
transporte normal de los iones en los enterocitos.
4.3.La producción de citotoxina.
Por algunas cepas de C. jejuni y C. coli, esta citotoxina lesiona una
variedad de células de los mamíferos.
5. INMUNIDAD
5.1.Los pacientes con deficiencia de Ig A pueden experimentar
recurrencias de la enfermedad causada por C. jejuni.
5.2.Después del episodio agudo, las personas normales presenta títulos
en aumento de los anticuerpos de IgG, IgM e IgA, medidos por el
inmunoensayo (ELISA).
6. IDENTIFICACION EN EL LABORATORIO
CULTIVO
6.1.Especie: Campylobacter jejuni
6.1.1. Aislamiento: muestra material obtenido del recto y materia
fecal.
6.1.2. Medios selectivos apropiados: medios de plaqueo de
Butzler, de Skirrow (contiene Vancomicina, polimixinaB,
Familia: Campylobacteriaceae 8/14

trimetropim para inhibir el crecimiento de otras bacterias) y
Campy – BAP.
Los medios selectivos son adecuados para el aislamiento de C.
jejuni a 42º C; cuando el medio Skirrow se incuba de 36 a 37º C se
puede aislar otras campilobacterias.
Se crearon varios medios selectivos que permiten el aislamiento de
C. jejuni a partir de muestras de materia fecal.
Formulas de medios selectivos para el aislamiento de Campylobacter jejuniMedio Base Aditivos
Medio Selectivo de Butzler
Medio tioglicolato
líquido
Agar(3%)Sangre de carnero(10%)Bacitracina(25,000UI/L)Novobiocina(5mg/L)Colistina(10,000UI/L)Cefalotina(15mg/L)Actidiona(50mg/L)
Agar Sangre de Skirrow Agar sangre
Sangre lisada de caballo(7%)Vancomicina(10mg/L)Polomixina B(2,500UI/L)Trimetropina(5mg/L)
Medio de BlaserAgar base Brucella
Sangre de carnero(10%)Vancomicina(10mg/L)Trimetropina(5mg/L)Polomixina B(2,500UI/L)Cefalotina(15mg/L)AnfotericinaB(2mg/L)
Medio Selectivo para
Campylobacterde Preston Caldo nutritivo
5% de sangre de caballo lisada con saponinaTrimetropina(10µg/mL)Polomixina B(5UI/mL)Rifampicina(10µg/mL)Cicloheximida(100µg/mL)
Medio libre de sangrepara
Campylobacter de Preston Caldo nutritivo
Carbón bacteriológicoDesoxicolato de sodioSulfato ferrosoPiruvato de sodioHidrolizado de caseínaCefoperazona(32mg/L)
Mediopara vibriones
de ButzlerAgar base Columbia
Sangre de carnero desfibrinadaCefoperazona(15mg/L)Rifampicina(10mg/mL)Colistina(10,000UI/L)AnfotericinaB(2mg/L)
Medio de Preston
modificado Caldo nutritivo
7% de sangre desfibrinada de caballoCefoperazona(32mg/L)AnfotericinaB(2mg/L)Suplemento para desarrollo de Campylobacter
Familia: Campylobacteriaceae 9/14

Medio selectivoa base de carbon,
libre de sangre.Agar base Columbia
Carbón activadoHematina(0,032g/L)Piruvato de sodio(0,1g/L)Vancomicina(20mg/L)Cefoperazona(32mg/L)Cicloheximida(100mg/L)
Merino y col. Encontraron que el medio para Campylobacter de Preston,
libre de sangre y con cefaperazona, proporcionaba la mayor cantidad de
aislamientos de C jejuni.
Karmali y col. Hallaron que un medio selectivo libre de sangre basado
en carbón (CSM), con una base de agar Columbia, con carbón activado,
hematina, piruvato de sodio, cefoperazona, vancomicina y
cicloheximida, es mas selectivo que el medio Skirrow.
El carbón activado, la hematina, el sulfato ferroso y el piruvato de sodio
funcionan como sustitutos de la sangre en los medios de desarrollo para
campilobacterias.
La caseína se agrega para estimular a ciertas cepas de
campilobacterias termófilas resistentes al ácido nalidíxico que se
encuentran como microorganismos ambientales.
6.1.3. Incubación de placas inoculadas: a temperaturas elevadas
de 42ºC (C. jejuni puede proliferar a 37ºC pero a temperaturas
elevadas puede inhibir la flora intestinal). El desarrollo de
colonias es de 24 a 48 horas.
6.1.4. Atmósfera de incubación adecuada, con 5% de O2 , 10%
CO2 y 85% de N2.
No se recomienda el uso de estufas de CO2 para el cultivo de
campilobacterias debido a que en la atmósfera resultante sólo
se desarrollan las cepas muy aerotolerantes.
Tampoco son adecuadas las jarras con extinción de vela, debido
a que el nivel de oxígeno(12% al 17%) es demasiado alto para
el desarrollo óptimo de las campilobacterias.
Familia: Campylobacteriaceae 10/14

6.1.5. Las Colonias: tienden a ser incoloras o de color gris; pueden
ser acuosas y extenderse o redondas y convexas, y ambos tipos
de colonias pueden aparecer en las placas de agar.
6.1.6. Características del crecimiento: C. jejuni y otras
campilobacterias patógenas para humanos son:
o Oxidasa y catalasa positivas
o No oxidan ni fermentan carbohidratos
Para clasificación de especies se emplea:
o Reducción del nitrato
o Producción de H2S
o Prueba de hipurato (hidrolizan el hipurato a
acido benzoico y glicina)
o Sensibilidad a antimicrobianos
(Prueba de resistencia al ácido nalidíxico diferencia al C. jejuni del C. laridis).
6.2.Especie: Campylobacter fetus
6.2.1. Es un patógeno oportunista involucrado con infecciones
gastrointestinales.
6.2.2. Los cultivos de sangre o líquidos corporales deben hacerse en
placas de agar sangre no selectivas o medios de cultivo liquidos
con sangre.
6.2.3. Incubar en condiciones microaerófilas, a temperatura de 25º C
porque alguna cepas de C. fetus no proliferan a 42º C.
6.2.4. El cultivo debe hacerse en medio de cultivo sin cefalosporinas
en pacientes con síntomas diarreicos.
6.2.5. Otros medios selectivos tienen Cefalotina, cefoperazona y
compuestos inhibidores, debido a su contenido de cefalosprina
C.fetus y otras especies de campilobacterias no crecerán en
estos medios, por lo tanto deben emplearse medios sin
cefalotina incubar entre 36 a 37º C.
Familia: Campylobacteriaceae 11/14

Propiedades de las especies de Campylobacter
que son patógenas humanas impotantes
C. jejuni
C. coli
C. fetus
Ureasa - - -Oxidasa + + +Catalasa + + +Proliferación a: 25ºC - - +37ºC + + +42ºC + + -
Sensibilidad a la cefalotina R R S
Sensibilidad al ácido nalidíxico S S RHidrólisis de hipurato + - -
Proliferación anaeróbica a 37ºC + + +Reducción de nitrato + + +
Motilidad en la placade agar. + + +
ANEXOS
e. Tratamiento:
i. casi todas la cepas de C. jejuni son sensibles in Vitro a la
eritromicina, los aminoglucosidos, tetraciclina y el
cloramfenicol. El tratamiento con eritromicina acorta la
excreción fecal.
f. Pruebas de Aglutinación del Latex para la identificación de
especies de Campylobacter. Meritec – Campy (jcl) (Meridian
Diagnostics, Cincinnati, OH) es una prueba de aglutinación de
látex utilizada para la identificación de de aislamientos en cultivo,
Familia: Campylobacteriaceae 12/14

de los cuatro Campylobacter patógenos principales, es decir C.
jejuni, C coli, C. lari y C. fetus.
g. Sondas de Acidos Nucleicos: para la identificación de especies
de Campylobacter. El Accu- Probe Campylobacter Culture
Identification Test; es una prueba basada en sondas de DNA para
la identificación rapida de C. jejuni, C coli y C. lari, directamente
de las colonias. La sonda no es radiometrica y está marcada con
un éster de acridina quimioluminiscente. Las reacciones se leen
en un fotómetro.
H. pylori Campylobacter
Tienen ramillete de flagelos
polares que están envainados.
No se observan filamentos axiales.
Tienen un solo flagelo polar
desenvainado.
Pared celular es lisa y contiene
acidos grasos inusuales.
Pared celular en C. jejuni tiene
aspecto arrugado.
Muy alta actividad de ureasa y
catalasa
Ausencia de la quinona
respiratoria menaquinona 6 -
metilada
BIBLIOGRAFIA
JOKLIK, W. H. WILLETT, D. AMOS. 1,994.Microbiología de Zinsser.
20a. ed. Edit. Panamericana. Buenos Aires.
KONEMAN, E. S. ALLENS, W. JANDA, W. WINN 1997. Diagnóstico
Microbiológico. 5ª. ed. Edit. Médica Panamericana. Madrid – España.
PRESCOTT, L. J. HARLEY, D. KLEIN 2004. Microbiología. 5a. ed.
Edit. McGRAW – HILL- INTERAMERICANA DE ESPAÑA, S.A.U.
Madrid.
MADIGAN, M, J. MARTINKO, P. PACK. 2003. Brock. Biología de los
Microorganismos 8a. ed. Edit. Prentice Hall. Madrid. 1011.
Familia: Campylobacteriaceae 13/14

Familia: Campylobacteriaceae 14/14