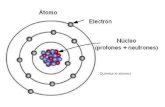
Atomos y particulas subatomicas
-
Upload
yanely-lucia-perez-romero -
Category
Education
-
view
23.110 -
download
5
description
Transcript of Atomos y particulas subatomicas

INTRODUCCIÓN: MATERIA Y MEDICIÓN

¿Por qué estudiar Química?
La química es básica para la comprensión de muchos campos:
- Agricultura- Astronomía
- Ciencia animal- Geología
etc.
Todos utilizamos química en
nuestra vida diaria
Aprender los beneficios y los
riesgos asociados a los productos
químicos

Relación de la Química con otras ciencias y la industria

Aspectos Positivos y Negativos
Ejemplo: Gasolina Potencia Gases de combustión. Daño al ambiente.
Fertilizantes y Plaguicidas:
Ayudan a la Agricultura Daño al medio Ambiente .
Industrias en general: Negocios que hacen o venden productos Tienen que ver con las sustancias químicas.

Química
Parte de la ciencia que se ocupa del estudio de la composición, estructura, propiedades y
transformaciones de la materia.
Materia es cualquier cosa que tenga masa y
ocupa espacio
Ejemplos:•Aire•Alimentos •Rocas•Vidrio

CLASIFICACIÓN DE LA MATERIA
DE ACUERDO A LA COMPOSICIÓN

CompuestoCompuesto es cualquier sustancia pura que se pueden descomponer por medios químicos en
dos o más sustancias diferentes y más simples.
ElementoElemento es cualquier sustancia pura que no se puede descomponer en algo más simple. Tiene
un solo tipo de átomo
Sustancia pura Sustancia pura materia con composición física materia con composición física y propiedades características. y propiedades características.
Átomo de hidrógeno
Átomo de hidrógeno

Mezclas: son combinaciones de dos o más sustancias en las que cada una conserva su propia identidad química y sus
propiedades.
La composición de la mezcla puede variar. Ejemplo Taza de café con azúcar
Mezclas homogéneas: conservan su composición en todas sus partes y se forman por dos o más sustancias puras. Uniformes en todos sus puntos.
Ejemplo: aire, solución de azúcar en agua, agua carbonatada y vinagre.
Mezclas Heterogéneas: .no tienen las misma composición, propiedades y aspecto en todos sus puntos.
Ejemplo: una mezcla de azufre y hierro

Para obtener una sustancia pura es necesario separar de una mezcla.
Está separación se basa en las diferencias de las propiedades físicas y químicas de los componentes de la mezcla.
Existen distintas separaciones:- Decantación- Filtración- Destilación- Tamizado
Separación de mezclas

Tipos de separación:
Tamizado Destilación Decantación
Filtración

ESTADOS DE LA MATERIA

CLASIFICACIÓN DE LA MATERIA
ESTADOS FÍSICOS DE LA MATERIA
Estado Forma Volumen Partículas Compresibilidad
Sólido Definida Definido
Unidas rígidamente;
muy empacadas
Muy pequeña
Líquido Indefinida DefinidoMóviles, unidas
Pequeña
Gaseoso Indefinida Indefinido
Independientes y
relativamente lejanas entre sí
Alta

ESTADOS DE LA MATERIA
Oxigeno
Vapor de agua
Cera de vela
Alcohol
Gas
Gas
Sólido
Líquido

CAMBIOS FISICOS Y CAMBIOS QUÍMICOS
CAMBIOS FISICOS- No varia composición química de la materia - Lo que se tiene al principio se tiene al final- No se forman nuevas sustancias.
Ejemplo:
hielo agua vapor

CAMBIOS FISICOS
Fusión Vaporización
Solidificación Condensación
Sublimación
Sólido Líquido Gaseoso

CAMBIOS FISICOS Y CAMBIOS QUÍMICOS
CAMBIOS QUÍMICOS- Alteran la composición química de la materia. - Origen a otras sustancias.
Ejemplo:
Cl + Na (NaCl)

Cambios químicos o reacciones químicas:
*Se forman nuevas sustancias.
Las propiedades de las nuevas sustancias son diferentes de las sustancias
anteriores. En un cambio químico - puede producirse un gas, - puede haber desprendimiento de calor, - puede ocurrir un cambio de color o - puede aparecer una sustancia insoluble.
Los elementos pueden sufrir cambio químico para producir compuestos nuevos:
Ejemplo: Cl + Na (NaCl)
Son modificaciones que se pueden observar solo cuando se presenta un cambio en la
composición de una sustancia

PROPIEDADES FISICAS Y QUÍMICAS
Nos permiten identificar o caracterizar una sustancia de otras

Propiedades de la materia. Propiedades físicas: se pueden
observar sin cambiar la composición de la sustancia
- color, olor, sabor, densidad, punto de fusión y punto de ebullición.

Propiedades químicas: se observan sólo cuando la sustancia sufre un cambio en su composición. - Cuando el hierro se oxida, al quemar un papel.

MEDICIONES
FUNDAMENTALES

PRIMEROS PATRONES DE MEDIDA
Cerca - lejos
RápidoLento
Pesado Liviano
Grande- Pequeño Frío - caliente

Un valor de medición se compone la cantidad métrica y la unidad. ejemplo
Las unidades empleadas en mediciones científicas son las del sistema internacional (SI).
UNIDADES DE MEDICIÓN

MEDICIONES FUNDAMENTALES
24

SISTEMA INTERNACIONAL (S.I)
Sistema de unidades que utilizan la mayoría de países actualmente.
Se basa en el sistema decimal, distinto del Sistema anglosajón que utiliza fracciones.
Las magnitudes o unidades pueden ser de dos clases: Fundamentales y Derivadas.

SISTEMA INTERNACIONAL (S.I)
Magnitudes (Unidades) Fundamentales: aquellas que no dependen de otras unidades como masa en Kilogramos o longitud en metros.
Magnitudes (Unidades) Derivadas: dependen de la intervención de dos o más unidades como: d, F.

UNIDADES FUNDAMENTALES
MAGNITUD NOMBRE SIMBOLO
Longitud metro m
Masa kilogramo kg
Tiempo segundo s
Intensidad de corriente eléctrica
ampere A
Temperatura termodinámica
kelvin K
Cantidad de sustancia mol mol
Intensidad luminosa candela cd

UNIDADES DERIVADAS
MAGNITUD NOMBRE SIMBOLO
Superficie metro cuadrado m2
Volumen metro cúbico m3
Velocidad metro por segundo m/s
Aceleraciónmetro por segundo
cuadrado
m/s2
Velocidad angular radián por segundo rad/s
Fuerza Newton N (Kg.m/s2)
Presión Pascal Pa (N/m)

PREFIJOS - MULTIPLOS
Prefijo Símbolo Factor de multiplicación
Tera T 1 000 000 000 000 1012
Giga G 1 000 000 000 109
Mega M 1 000 000 106
Hecto h 100 102
Deca Da 10 101
_ _ 1 100

PREFIJOS - SUBMULTIPLOS
Prefijo Símbolo Factor de multiplicación
Deci d 1 / 10 10 -1
Centi c 1 / 100 10 -2
Mili m 1 / 1 000 10 -3
Micro µ 1 / 1 000 000 10 -6
Nano n 1 / 1 000 000 000 10 -9
Pico p 1 / 1 000 000 000 000 10 -12

MEDICIÓN METRICA DE LONGITUD
NOMBRE SIMBOLO EQUIVALENCIA
Kilometro Km 1.000 m
hectómetro hm 100 m
decámetro dam 10 m
METRO m 1m
decímetro dm 0.1m
centímetro cm 0.01m
milímetro Mm 0.001m

Ejemplos
a) 5 cm = _____a m
5 × 0,01 m = 0,05 m
b) 1.5 Km ----------------- m
1 Km----------------103 m
1.5Km----------------- x
x= 1.5 x 103 m /1km
x= 1500 m

Ejemplos
45 kilómetros = 45 x 1000 metros
= 45 000 m
640 µA = 640 x 1A = 0,00064 A
1 000 000µ
357,29 milimetros = 357,29 x 1m = 0,357 m
1 000mm

MEDICIÓN METRICA DE MASA
NOMBRE SIMBOLO EQUIVALENCIA
Kilogramo Kg 1.000 g
hectogramo hg 100 g
decagramo dag 10 g
gramo g 1 g
decigramo dg 0.1 g
centigramo cg 0.01 g
milígramo mg 0.001 g

Ejemplo
kg
gkg
1
10.120 3
g
dggx
1
3
10
1*10.120
Trasformar : 120 k g------------ dg
1 kg-----------103 g
120 Kg-----------x
Luego, 1 dg-----------------10-1g
X----------------- 120.103g
x=120.103g
x= 120.104 dg

UNIDADES DE MEDICIÓN
K= °C + 273.15
°C= 5/9 (°F – 32)
°F= 9/5 (°C + 32)

VOLUMEN Y DENSIDAD
¿? VOLUMEN DE UN CUBO?
Instrumentos para medir volúmenes
D = m/v (g/ml) (g/cc) (g/cm3)

INCERTIDUMBRE AL MEDIR
Números exactos: tienen valores por definición. Ejemplo. 1 Kg tiene 1000 gramos, 60 minutos en una hora. No tienen incertidumbre.
Números inexactos: los números que se obtienen midiendo, debido a errores de equipo o errores humanos

Ninguna medición es exacta al 100%
Precisión se refiere a la cercanía de una serie de medidas entre si.
Exactitud se refiere a que tan cerca del valor real se encuentra el valor medido. Dicho de otra manera exactitud tiene que ver con el grado de coincidencia de las mediciones con el valor verdadero.
INCERTIDUMBRE AL MEDIR

PRECISIÓN
1

EXACTITUDEXACTITUD
1

PRECISIÓN Y EXACTITUD
Supongase que solicitamos a tres estudiantes determinar la masa de un cilindro de aluminio cuya masa real es de 3.00 g. ( ver la gráfica siguiente)

MEDICIONES FUNDAMENTALES
ESTUDIANTE # 1 ESTUDIANTE # 2 ESTUDIANTE # 3
2.65 2.87 3.01
2.76 2.86 3.00
2.68 2.87 2.99

CIFRAS SIGNIFICATIVAS Son todos los dígitos de una cantidad medida, incluido el dígito incierto
1. Todos los enteros diferentes de cero son significativos.
2. Todos los ceros a la izquierda del (o que preceden al) primer dígito diferente de cero no son significativos.
0,00567 (3) 0,0089 (2)
3. Todos los ceros situados entre dígitos diferentes de cero son significativos.
207,08 (5) 0,0401 (3)

CIFRAS SIGNIFICATIVAS (REGLAS)4. Todos los ceros al final de un número con punto decimal
son significativos 0,0670 (3)
400,00 (3)5. En la multiplicación y división el número resultante no
tiene más cifras significativas que el número menor de cifras significativas usadas en la operación.
Ejemplo: ¿Cuál es el área de un rectángulo de 1,23 cm de ancho por
12,34cm de largo?. La calculadora nos da 15,1783 cm2 pero como el ancho sólo tiene tres cifras significativas escribiremos 15,2cm2.