1. ENCUADRE DEL SISTEMA DE PRÁCTICAS
Transcript of 1. ENCUADRE DEL SISTEMA DE PRÁCTICAS

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 1
1. ENCUADRE DEL SISTEMA DE PRÁCTICAS
1.1 INTRODUCCIÓN
La bioquímica es una ciencia que estudia la química de la vida; es decir, pretende
describir la estructura, la organización y las funciones de la materia viva en
términos moleculares. Esta ciencia es una rama de la Química y de la Biología.
Puede dividirse en tres áreas principales: 1) la química estructural de los
componentes de la materia viva y la relación de la función biológica con la
estructura química; 2) el metabolismo, la totalidad de las reacciones químicas que
se producen en la materia viva; y 3) la química de los procesos y las sustancias
que almacenan y transmiten la información biológica. Esta última también es el área
de la genética molecular.
En sus inicios, la bioquímica estuvo ligada a la medicina. En el siglo XVII, las raíces
de la bioquímica descriptiva las encontramos en las investigaciones de Scheele y
las de la bioquímica dinámica en los trabajos de Lavoisier, éste aclaró la naturaleza
de la respiración animal y la relación de este fenómeno fisiológico con la producción
de calor corporal, dando inicio al metabolismo energético. Pasteur al estudiar la
fermentación sentó las bases de la química biológica moderna especialmente de la
enzimología. Los trabajos de Mayer y sus continuadores sentaron las bases de la
termodinámica esencial para comprender las relaciones energéticas en los
sistemas biológicos Emil Fisher utilizando las técnicas de la química orgánica,
estableció sus estructuras por degradación y síntesis posterior y con esto la
bioquímica se consolida definitivamente como disciplina científica. En 1903
Takamine y Aldrich obtuvieron la primera hormona en estado puro; la adrenalina,
entre 1905 y 1906 Pekelharing y Hopkins descubrieron la existencias de las
vitaminas como factores esenciales para la nutrición en pequeñas cantidades y
cuya carencia produce enfermedades específicas conocidas desde la antigüedad.
Hoy en día, los avances de la bioquímica son usados en cientos de áreas, desde la
genética hasta la biología molecular, de la agricultura a la medicina. Por ejemplo la
bioquímica de los ácidos nucléicos es el corazón de la genética; a su vez, el uso de

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 2
las directrices genéticas ha sido fundamental para dilucidar numerosas áreas de la
bioquímica. La fisiología, que es el estudio de la función corporal, se traslapa con la
bioquímica casi por completo. La inmunología emplea buena parte de las técnicas
bioquímicas y muchos de los planteamientos inmunológicos han encontrado amplio
uso entre los bioquímicos. La farmacología y la farmacia descansan en un
conocimiento sólido de la bioquímica y fisiología; como ejemplo, la mayor parte de
los medicamentos son metabolizados por reacciones catalizadas por enzimas. Los
venenos alteran las reacciones o procesos bioquímicos; este es el tema de la
toxicología. Todas las enfermedades son de naturaleza química; por tanto, en
forma creciente, la bioquímica se está utilizando en el estudio de aspectos básicos
de la patología, como inflamación, la lesión celular y cáncer. Muchos zoólogos y
botánicos emplean casi de manera exclusiva planteamientos bioquímicos. Sus
interrelaciones no sorprenden, dado que la vida como la conocemos depende de
las reacciones y procesos bioquímicos. De hecho, las antiguas barreras entre las
biociencias se han roto y cada vez más, la bioquímica se está convirtiendo en su
lenguaje común.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 3
1.2 UBICACIÓN DE LA ASIGNATURA DENTRO DEL MAPA
CURRICULAR
La materia de Bioquímica Aplicada está considerada en el sexto semestre del Plan
de Estudios de la Carrera de Químico Biotecnólogo correspondiendo al eje de
formación disciplinaria.
Contexto Social
de la Profesión
Lectura y
Redacción
Computación
Introducción al
Método
Experimental
Genética
General
Calculo
Diferencial
Física I
Química
Inorgánica
Química
Orgánica I
Química
Orgánica II
Química
Analítica
Biología Celular
Microbiología
General
Química
Orgánica III
Bioquímica
Bioseguridad
Toxicología
Parasitología
Molecular Vegetal
Op
tativ
as
de Á
rea
Ind
us
trial y
Am
bie
nta
l
Probabilidad y
Estadística
Diseño
Estadístico de
Experimentos
Bioinformática
Química
Analítica
Instrumental II
Biología
Molecular
Bioquímica
Aplicada
Bionegocios IBionegocios II
Ecología
Microbiana
Fisiología
Vegetal
Bioprocesos I
Ingeniería
Genética
Bromatología
Evaluación de
Proyectos
Legislación e
Impacto
Ambiental
Inmunología
Microbiología
de Alimentos
Química
Ambiental
Biotecnología
Vegetal I
Genómica
Gestión de la
Calidad Seminario de
Investigación
II
Op
tativ
as
de Á
rea B
iom
éd
ica
y
Fa
rma
cé
utic
a
Op
tativ
as
de
Áre
a V
eg
eta
l y
Alim
en
taria
Eje Disciplinario y Electivo I-disciplinario Eje Terminal y electiva II-optativas
Eje
s In
teg
rad
ore
s
Inn
ova
do
r y de
valo
res
Ejes teórico-epistemológicos
Diagrama de secuencia académica de Químico Biotecnólogo
Educación
Ambiental
Hab. Pensam.
Crítico y
Creativo
Química
Analítica
Instrumental I
Operaciones
Unitarias
Ob
liga
toria
s
Tópicos de
Desarrollo
Humano
Termodinánica
Tópicos Selectos
Farmacogenómica
Biotecnología
Médica
Biotecnología
Vegetal II
Biotecnología
Farmacéutica
Biprocesos II
Proteínas con
Aplicación
Industrial
BioformulacionesInocuidad
Alimentaria
Alimentos
TrasgénicosTópicos Selectos
Bioenergéticos
Ecomateriales Bioprocesos II
Tópicos Selectos IIBiorreactores
Birremediación
Anatomía y
Fisiología
Farmacología
Bacteriología
Parasitología y
Virología
Cultivo de Tejidos
Seminario de
Investigación I
Tópicos Selectos I
Diagnóstico
Molecular
Calculo Integral
Física II
Eje Básico
FORMACIÓN INTEGRAL SERVICIO SOCIAL
Proteínas con
Aplicación
Industrial
Figura. 1. Secuencia de niveles académicos del QFB

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 4
2. PROPÓSITO DEL SISTEMA DE PRÁCTICAS
2.1. ENCUADRE DEL SISTEMA DE PRÁCTICAS DENTRO DE LA
PROFESIÓN
En el curso de Bioquímica aplicada, se pretende dejar bases sólidas sobre las
principales rutas metabólicas y su integración así como fomentar la discusión y
aplicación de los temas tratados esperando que los alumnos comprendan cómo
estos conocimientos son básicos, ya que esta materia lleva cadena e interrelación
con otras asignaturas y pueda los alumnos tener una mejor comprensión de ellas.
2.2 REDACCIÓN DE LAS COMPETENCIAS PROFESIONALES
Explicar el metabolismo de las biomoléculas en los organismos vivos para
identificar las vías metabólicas que se llevan a cabo en éstos.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 5
2.3 NIVELES DE DESEMPEÑO
_________________________________________________________________
Nivel 1. Se realizan funciones rutinarias de baja complejidad. Se reciben
instrucciones. Se requiere baja autonomía.
Nivel 2. Se realizan un conjunto significativo de actividades de trabajo, variadas y
aplicadas en diversos contextos. Algunas actividades son complejas y no
rutinarias. Presenta un bajo grado de responsabilidad y autonomía en las
decisiones. A menudo requiere colaboración con otros y trabajo en equipo.
Nivel 3. Se requiere un importante nivel de toma de decisiones. Tiene baja
responsabilidad de recursos materiales con los que opera su área. Así como,
control de recursos financieros para adquisición de insumos.
Nivel 4. Se desarrolla un conjunto de actividades de naturaleza diversa, en las
que se tiene que mostrar creatividad y recursos para conciliar intereses. Se debe
tener habilidad para motivar y dirigir grupos de trabajo.
Nivel 5. Se desarrollan un conjunto de actividades de naturaleza diversa, en las
que se tiene que mostrar un alto nivel de creatividad, así como buscar y lograr la
cooperación entre grupos e individuos que participan en la implantación de un
problema de magnitud institucional.
Las prácticas del Laboratorio de Bioquímica Aplicada tendrán un nivel de
desempeño del Conocer planteado en el NIVEL 2.
a. Los contextos son varios:
1. Aula: con los conocimientos aprendidos en su unidad de aprendizaje de
Bioquímica Aplicada.
2. Prácticas de laboratorio de Bioquímica Aplicada: aplicar los conocimientos
teóricos para la compresión de los procesos metabólicos.
3. Otros ambientes de aprendizaje: cuando desarrolle trabajos de
investigación que tendrá que realizar en cada práctica. La finalidad es
buscar el fundamento de cada una de las técnicas usadas en el laboratorio.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 6
4. Su grado de responsabilidad y autonomía será determinado por su
compromiso de aprender.
5. Se requiere trabajo en equipo para el desarrollo de cada práctica señalada.
6. Se requiere asesoría del maestro.
3. DESCRIPCIÓN DEL SISTEMA DE PRÁCTICAS
3.1 ESTRUCTURA Y PROGRAMA DEL SISTEMA DE PRÁCTICAS
Las prácticas en el Laboratorio de Bioquímica Aplicada se harán a través de
experimentos, que le permite integrar los conocimientos teóricos aprendidos en el
aula.
Se propone que el estudiante desarrolle habilidades en el desarrollo de la práctica
así como la comprensión de ciertos procesos metabólicos.
El programa de prácticas del Laboratorio de Bioquímica Aplicada tiene una duración
total de 32 horas; las prácticas serán secuenciales y coordinadas con la parte
teórica revisada en el aula.
CUADRO. 1 ESTRUCTURA Y PROGRAMA DEL SISTEMA DE PRÁCTICAS
Competencia o unidad de
Competencia a ser abordada Semana Prácticas Pre requisitos
Conoce e interpreta las leyes
de la termodinámica y los
sistemas abiertos
2ª semana
del curso
1ª práctica
Bioenergética y
generación de
calor
Realiza la determinación de
vitamina C en alimentos y
compara el contenido de esta
vitamina en los diferentes
3ª semana
del curso
2ª práctica
Determinación
de vitamina C
en alimentos

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 7
alimentos ensayados. Haber leído el
procedimiento para
la práctica y realizar
un diagrama de
flujo.
Haber investigado
sobre las hojas de
seguridad de los
reactivos a emplear
Haber realizado los
cálculos
correspondientes
para preparar las
soluciones de
trabajo.
Comprende la acción de las
enzimas sobre los
polisacáridos.
4ª semana
del curso 3ª práctica
Degradación
enzimática de
polisacáridos
Conoce y aplicar
correctamente los
conocimientos de la
respiración celular.
5ª semana
del curso
4ª práctica
Productos de la
respiración
anaerobia
Realiza determinación de
triglicéridos en suero
sanguíneo.
6ª semana
del curso
5ª práctica
Determinación
de Triglicéridos.
Realiza determinación de
colesterol en suero
sanguíneo.
7ª semana
del curso
6ª práctica
Determinación
de colesterol
Realiza determinación de
urea en suero sanguíneo.
8ª semana
del curso
7ª práctica
Excreción del
nitrógeno
proteico
Diseña experimento
integrador de conocimientos
9ª semana
del curso
8ª práctica
Integración de
conocimientos

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 8
4. PRÁCTICAS GENERALES DE SEGURIDAD.
REGLAMENTOS
4.1 REGLAMENTO APLICABLE A LA PRÁCTICA Y EL ÁMBITO
DONDE SE DESEMPEÑAN
El Laboratorio de Alimentos debe seguir reglas generales de seguridad basadas en
la Normas Oficiales Mexicanas (Cuadro 2) de las cuales, se han seleccionado
algunas que determinan el buen funcionamiento del mismo y estas son:
CUADRO 2. NORMAS OFICIALES MEXICANAS
ESPECIFICACIONES NORMAS OFICIALES
MEXICANAS
CONDICIONES DEL MEDIO AMBIENTE
--El laboratorio cuenta con las condiciones y niveles de
iluminación suficiente y adecuada para el tipo de
actividad que realiza.
NOM-025-STPS-1999
--Se cuenta con normas de Seguridad e Higiene que
permitan reducir el riesgo de accidentes en el área de
trabajo.
NOM-017-STP-2001
--En los contenedores se indica el tipo de desecho
para el cual están destinados y están señalizados
NOM-087-ECOL-1995
-- Se establecen las características, el procedimiento
de identificación, clasificación y los listados de los
residuos peligrosos.
NOM-052-SEMARNAT-
2005
SISTEMA CONTRA INCENDIOS
--Se instalarán equipos contra incendio de acuerdo al
grado de riesgo de incendio, a la clase de fuego que
se pueda presentar en el laboratorio y a la cantidad de
materiales en el almacén y proceso.
NOM-002-STPS-2000

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 9
ESPECIFICACIONES NORMAS OFICIALES
MEXICANAS
SISTEMA CONTRA INCENDIOS
--De las salidas normales y de emergencia, la
distancia a recorrer desde el punto más lejano del
interior de una edificación a un área de salida no debe
ser mayor de 40 m.
NOM-002-STPS-2000
--En caso que la distancia sea mayor a la señalada por
el punto anterior, el tiempo máximo en la que debe
evacuarse al personal a un lugar seguro es de 3
minutos. Lo anterior, deberá comprobarse en los
registros de simulacros de evacuación.
NOM-002-STPS-2000
--La puertas de salida normales, de las rutas de
evacuación y de las salidas de emergencia, deberán
estar libres de obstáculos, candados, picaportes o
cerraduras con seguros puestos, durante las horas
laborales
NOM-002-STPS-2000
--Las puertas de salida normales, de ruta de
evacuación y de salida de emergencia, deben ser de
materiales resistentes al fuego y capaces de impedir el
paso del humo entre área de trabajo.
NOM-002-STPS-2000
--Las instalaciones de sistemas fijos contra incendios,
se deben colocar en sitios visibles y de fácil acceso,
libres de obstáculos, protegidas de la intemperie y
señalar su ubicación.
NOM-002-STPS-2000
--Los extintores deben ser revisados al momento de su
instalación y, posteriormente, a intervalos no mayores
de un mes.
NOM-002-STPS-2000

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 10
ESPECIFICACIONES NORMAS OFICIALES
MEXICANAS
EQUIPOS DE PROTECCIÓN
--Se obtiene el conocimiento con capacitación del
personal, para el uso, limpieza, mantenimiento,
limitaciones y almacenamiento del equipo de
protección personal.
Reglamento Federal de
Higiene y Medio Ambien
te del Trabajo (RFHYMA).
Cap. 5º. Art. 135 al 141
INSTALACIONES ELÉCTRICAS
--Las instalaciones eléctricas deben tener protecciones
de seguridad y señalarse de acuerdo al voltaje y
corriente eléctrica de la carga instalada.
NOM-OO1-SEDE-1999,
ART. 1 – 34
--El bloqueo de energía para el control de riesgos,
estará en tableros, controles y equipos, a fin de des
energizar, desactivar y/o impedir la operación normal
de la maquinaria y equipo.
NOM-OO1-SEDE-1999,
ART. DEL 384
SEÑALES, AVISOS DE SEGURIDAD Y CÓDIGO DE COLORES
--Se utiliza el código de colores en el sistema de
tuberías conforme a lo que establece la norma
correspondiente.
NOM-026-STPS-1998
Apdo. 9 y 9.1
--Se ubican las señales de seguridad e higiene de tal
manera que pueden ser observadas e interpretadas
por los trabajadores a los que están destinados y se
evita que sean obstruidos.
NOM-026-STPS-1998
Apdo. 5 y 5.4
Se garantiza que la aplicación del color, señalización y
la identificación en la cubierta están sujetas a un
mantenimiento que asegure en todo momento su
visibilidad y legibilidad.
NOM-026-STPS-1998
Apdo. 5 y 5.3
PLANTA FÍSICA
--Se realizan verificaciones oculares periódicas a las
instalaciones y elementos estructurales.
NOM-001-STPS-1999.
Apdo. 11. RFHYMAH.
Título 2do. Cap. 1º.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 11
ESPECIFICACIONES NORMAS OFICIALES
MEXICANAS
PLANTA FÍSICA
--Se conservan las áreas limpias y en orden,
permitiendo el desarrollo de las actividades para las
que fueron destinadas, asimismo, se les da
mantenimiento preventivo y correctivo.
NOM-025-STPS-1999,
apdo. 7
-Los resultados de dichas verificaciones son anotados
en un registro, siempre y cuando se detecten signos
de ruptura, agrietamiento, pandeo, fatiga de material,
deformación, hundimiento u otra condición similar, se
deben solicitar las reparaciones correspondientes.
Reglamento Federal de
Higiene y Medio
Ambiental del Trabajo.
Título 2do. Cap. 1º.
--Se establecen lugares limpios, adecuados y seguros
destinados al personal, para sanitarios, consumo de
alimentos y en su caso, regaderas y vestidores.
Reglamento Federal de
Higiene y Medio
Ambiental del Trabajo.
Título 2do. Cap.1º y 7º.
--Se mantienen las áreas de trabajo libres de
obstáculos y el suelo limpio. Así como objetos no
deberán obstaculizar la iluminación y ventilación en las
zonas en que éstas se requieran.
Reglamento Federal de
Higiene y Medio
Ambiental del Trabajo.
Cap. 8º y 12º.
--Las áreas de trabajo deben delimitarse mediante
franjas amarillas de al menos 5 cm. De ancho de tal
manera que se disponga de espacios seguros para la
realización de actividades.
NOM-001-STPS-1999
--Los techos del centro de trabajo, cuentan con un
sistema que evite el estancamiento de agua.
NOM-001-STPS-1999,
apdo.11
--Las paredes del centro de trabajo, se mantienen con
colores que no afecten la visión del trabajador.
NOM-026-STPS-1998
--Los pisos del centro de trabajo, se mantienen limpios
y cuentan con un sistema que evite los
estancamientos de líquidos.
NOM-026-STPS-1998

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 12
ESPECIFICACIONES NORMAS OFICIALES
MEXICANAS
ORDEN, LIMPIEZA Y SERVICIOS
--De los laboratorios/talleres, el equipo y las
instalaciones deben mantenerse limpias. La limpieza
debe hacerse por lo menos al término de cada turno.
NOM-001-STPS-1999,
fracc. 7.1 NOM-005-
STPS-1998 NOM-087-
ECOL-SSA1-2002
--Los servicios sanitarios destinados a los
trabajadores, deberán conservarse permanentemente
en condiciones de uso higiénicos.
Reglamento Federal de
Higiene y Medio
Ambiental del Trabajo.
Cap. 12, Art. 108
--Deberán existir excusados y mingitorios con agua
corriente, separados los hombres de los de las
mujeres.
Reg. Federal de Higiene
y Medio Ambiental del
Trabajo. Cap. 12, Art. 103
CONDICIONES GENERALES
--Se cuenta con un manual de primeros auxilios en el
que se definen los medicamentos y materiales de
curación, que requiera el centro de trabajo, así como
los procedimientos para la atención de emergencias
médicas.
NOM-005-STPS-1998
--Se cuenta con un botiquín de primeros auxilios, en el
área, laboratorio ó taller, en la que se deban incluir los
materiales de curación que se requieran de
conformidad con el análisis de riesgos.
NOM-005-STPS-1998
--Se capacita al personal para prestar los primeros
auxilios, por lo menos una vez al año.
NOM-005-STPS-1998
--Se proporciona a todos los trabajadores,
capacitación y adiestramiento para la prevención y,
protección de incendios y combate de conato de
incendios.
NOM-002-STPS-2000,
CAP. 5.8

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 13
ESPECIFICACIONES NORMAS OFICIALES
MEXICANAS
CONDICIONES GENERALES
--Se realizan simulacros una vez al año. NOM-002-STPS-2000,
CAP. 5.9
--Se organizan y capacitan simulacros de evacuación
del personal y de atención de primeros auxilios.
NOM-002-STPS-2000,
CAP. 5.9
--Se efectúa y registra el reconocimiento, evaluación y
control de los niveles de iluminación del área de
trabajo.
NOM-025-STPS-1999,
CAP. 8, 9, 10
El laboratorio de Alimentos, también cuenta con un Reglamento Interno, que
pretende guiar su conducta dentro del mismo, las normas ahí señaladas son
actitudes que el alumno debe conocer, aprender y acatar para un mejor desempeño
y desarrollo de competencias.
4.2 REGLAMENTO INTERNO DEL LABORATORIO DE ALIMENTOS
El laboratorio de alimentos contará con un encargado de laboratorio para
cada turno, el cual debe estar presente durante la realización de las
prácticas.
Las instalaciones pueden ser usadas por alumnos, maestros, egresados y
otros solicitantes que así lo hagan saber.
Todos los usuarios del laboratorio están sujetos al reglamento básico del
laboratorio, así como lo que establece el reglamento interno de la Facultad
de Ciencias Químicas.
Es obligatorio para los usuarios el uso de bata blanca.
En la realización de prácticas de alto riesgo es obligatorio el uso de anteojos
y guantes de seguridad.
Esta prohibido fumar dentro del laboratorio.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 14
Esta prohibido el consumo de alimentos y bebidas dentro del laboratorio.
El usuario debe mantener una conducta adecuada a fin de evitar accidentes
y debe mantener la voz baja dentro del laboratorio.
Para solicitar material existente, deberá firmarse un vale por dicho material.
El mal funcionamiento de los equipos del laboratorio que no se detecten al
solicitarse, deben reportarse inmediatamente al encargado de laboratorio.
El material solicitado será entregado limpio y seco por el laboratorista,
debiéndose devolver por el usuario, al final de la práctica, en las mismas
condiciones.
No se permite sacar material o equipo del laboratorio sin autorización del
laboratorista.
En caso que el usuario requiera retener todo o parte del material solicitado,
el encargado de laboratorio retendrá el vale tachando el material devuelto y
se le entregará éste, solo hasta que se devuelva todo el material.
Si es necesario dejar material con reactivos dentro del laboratorio, este
deberá ser etiquetado adecuadamente para su identificación y deberá
notificarse al encargado de laboratorio.
El encargado de laboratorio no se hace responsable de material olvidado sin
etiquetar.
El usuario será responsable de los desperfectos que pudiesen presentarse
en los equipos debido al mal manejo de los mismos, debiendo cubrir el
importe de su reparación o la restitución del mismo antes de que termine el
semestre. En caso de que el usuario no cumpla con esta disposición:
Los alumnos no serán inscritos al siguiente semestre, hasta que liquiden
su adeudo.
Los alumnos de último semestre, no recibirán su carta de pasante y no
podrán efectuar ningún trámite en la Facultad hasta que no liquiden su
adeudo.
Los maestros recibirán un escrito de los adeudos y de no liquidarse se
descontará de su pago.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 15
Los ex–alumnos y otros usuarios externos deberán depositar en garantía
una cantidad que ampare el costo del material y equipo facilitados, la cual
serà rembolsada si no hay desperfectos o daños de lo contrario se
liquidarán sus adeudos al hacerse efectiva la garantía que ampara el
importe de los equipos.
El usuario será responsable de quebraduras y desperfectos del material,
cuando estos sean ocasionados por el mal manejo de los mismos, debiendo
restituirlos antes de que termine el semestre. En caso de que el usuario no
cumpla con esta disposición:
Los alumnos no serán inscritos al siguiente semestre, hasta que liquiden
su adeudo.
Los alumnos de último semestre, no recibirán su carta de pasante y no
podrán efectuar ningún trámite en la escuela hasta que no liquiden su
adeudo.
Los maestros recibirán un escrito de los adeudos y de no liquidarse se
descontará de su pago.
Los ex –alumnos y otros usuarios liquidarán sus adeudos al hacerse
efectiva la garantía que ampara el importe de los equipos.
Es obligatorio la presencia del catedrático en el laboratorio durante toda la
práctica, para orientar, asesorar y supervisar a los alumnos. En caso de que
por algún motivo el maestro se tenga que retirar, la práctica se tendrá que
suspender en forma inmediata a menos que el responsable de laboratorio a
criterio personal dé su consentimiento para continuar. Cuando suceda lo
anteriormente expuesto deberá hacerse la anotación correspondiente en la
bitácora.
Los maestros registraran la práctica en la bitácora.
Para solicitar la preparación, por el encargado de laboratorio, de reactivos
especiales, debe hacerse por escrito a él mismo y con una semana de
anticipación al menos.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 16
Para usar equipos del laboratorio debe contarse con la autorización del
maestro y/o encargado de laboratorio.
La solicitud de material o equipo no existente deberá hacerse por escrito al
coordinador de laboratorios.
Si se trabaja con material biológico infeccioso, al finalizar la práctica, este
deberá depositarse en los recipientes adecuados.
5. SISTEMA DE EVALUACIÓN DE LAS PRÁCTICAS
5.1. LINEAMIENTOS GENERALES PARA LA EVALUACIÓN
En éste apartado se refiere a la observación que el docente responsable hace a su
desempeño de la práctica. La evaluación de las prácticas será a través de los
siguientes parámetros:
Reporte Escrito: El cual deberá contener al menos:
Titulo y número de la práctica.
Introducción
Objetivo de la práctica.
Fundamentos de la práctica.
Materiales y Método
Resultado de la práctica.
Discusiones personales.
Conclusiones personales.
Desempeño dentro del laboratorio.
Asistencia a las prácticas.
5.2 MÉTODO DE ASIGNACIÓN DE CALIFICACIONES DE LAS
PRÁCTICAS

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 17
La calificación y ponderación de las prácticas de Bioquímica Aplicada es la
siguiente:
ACTIVIDAD A CALIFICAR PONDERACIÓN
Actividades previas 0 – 10
Reporte Escrito. 30 – 50
Desempeño dentro del laboratorio. 30 - 35
Asistencia al laboratorio. 5 – 10

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 18
UNIVERSIDAD JUÁREZ DEL ESTADO DE DURANGO
FACULTAD DE CIENCIAS QUÍMICAS
PRIMERA PRÁCTICA
BIOENERGÉTICA Y GENERACIÓN DE CALOR

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 19
1. NÚMERO DE ALUMNOS POR UNIDAD DE
PRÁCTICA
Para un buen desarrollo de la actividad académica, considerando el espacio, el
número ideal es de 30-35 alumnos en equipos de 3 alumnos.
2. INTRODUCCIÓN DE LA PRIMERA PRÁCTICA
Todo organismo viviente al hacer algún tipo de movimiento consume energía, y en
el ser humano se ha demostrado un alto consumo de energía asociado con el
ejercicio, conocido como bioenergía. Esta bioenergía es en forma de ATP, el que es
consumido en el músculo estriado para provocar el deslizamiento de las bandas de
actina y miosina.
Al iniciar el ejercicio o actividad física, a nivel celular, aumenta la utilización de ATP
para el subsidio energético, lo que trae simultáneamente un aumento con la
producción de calor, que se traduce en aumento de la temperatura corporal.
El aumento de utilización de ATP lleva a un aumento en el consumo de oxígeno por
la célula, para producir más ATP dentro de la cadena respiratoria o cadena de
transporte de electrones, proceso conocido como respiración aeróbica y como
consecuencia hay un aumento en la producción de CO2.
3. PROPÓSITO ESPECÍFICO DE LA PRIMERA
PRÁCTICA
3.1 CRITERIOS DE DESEMPEÑO
1ª PRÁCTICA: BIOENERGÉTICA Y GENERACIÓN DE CALOR

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 20
Que el estudiante observe las manifestaciones de transformación de la energía en
los seres vivos.
Que el estudiante evidencie el consumo de ATP y oxígeno, así como la producción
de CO2.
3.2 RESULTADO FINAL DE LA PRIMERA PRÁCTICA
El estudiante observará la manifestación de transformación de energía en el
organismo humano hará algunas mediciones y relacionará lo anterior con la
bioenergética y leyes de la termodinámica.
4. NORMAS DE SEGURIDAD ESPECÍFICAS DE LA
PRÁCTICA
Sin riesgo particular, seguir las normas de seguridad generales.
5. DESARROLLO DE LA PRIMERA PRÁCTICA
ACTIVIDADES TIEMPO
REQUERIDO
RESULTADO DE LA
ACTIVIDAD
A) Actividad guiada por el
docente responsable de la
práctica
10
min.
El docente realizará una
explicación de la metodología de
la práctica.
ACTIVIDADES TIEMPO
REQUERIDO
RESULTADO DE LA
ACTIVIDAD
B) Actividad realizada por
los equipos de estudiantes
45
Min
Cada equipo desarrollará el
procedimiento señalado en la
práctica
C) Aplicación de la práctica Final de la práctica Reporte de laboratorio para la

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 21
en el desempeño
profesional
30 min siguiente sesión.
Investigación bibliográfica sobre:
Bioenergética
Leyes de la termodinámica
Sistemas
Transformación de la energía
A) PRÁCTICA DIRIGIDA POR EL DOCENTE RESPONSABLE DE LA
PRÁCTICA:
En ésta etapa el docente explicará la metodología de la práctica.
B) ACTIVIDAD REALIZADA POR EL ALUMNO EN GRUPOS DE
TRABAJO.
Al concluir la explicación guiada por el docente, se dividirá al grupo en equipos de
trabajo, máximo de 3 estudiantes. Los equipos se organizarán en mesas de trabajo
para iniciar la práctica.
El desarrollo de ésta parte de la práctica se realizará de la manera siguiente:
1ª PRÁCTICA. PROCEDIMIENTO
REQUERIMIENTOS:
Dos estudiantes por grupo quienes tienen que traer ropa deportiva y tenis.
Dos relojes con cronómetro
Dos termómetros orales
PROCEDIMIENTO:
1. Antes de iniciar la prueba, al estudiante que va ha hacer el ejercicio, se le debe
tomar la temperatura (oral y axilar), así como la frecuencia respiratoria, datos

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 22
que deben estar en la tabla. El sujeto debe estar en reposo y no debe haber
hecho ningún tipo de trabajo o ejercicio en los 15 minutos previos a la práctica.
2. El estudiante debe hacer marcha estacionaria, subiendo las rodillas a la altura
de la cadera durante 10 minutos. Es importante mantener el ritmo durante la
prueba y no debe detenerse a menos que el sujeto esté realmente exhausto.
3. Inmediatamente después de los 10 minutos, debe tomarse la temperatura axilar
y oral así como la frecuencia respiratoria y cardíaca, anotando los resultados en
la casilla correspondiente a 0 minutos, repita las mediciones al haber pasado 5,
10 y 15 minutos después de finalizado el ejercicio.
4. Analice los resultados y discuta los mismos.
RESULTADOS
TABLA DE RESULTADOS
CARACTERISTICAS
CONDICIONES
TEMPERATURA
ORAL
TEMPERATURA
AXILAR
FRECUENCIA
RESPIRATORIA
FRECUENCIA
CARDIACA
Al inicio de de la prueba
Al final del
ejercicio
(minutos)
0
5
10
15
C) APLICACIÓN DE LOS CONOCIMIENTOS , HABILIDADES Y
ACTITUDES ADQUIRIDOS EN LA PRÁCTICA, EN EL DESEMPEÑO
PROFESIONAL Y REPORTE DE LABORATORIO PARA LA SIGUIENTE
SESIÓN.
Reporte de laboratorio para la próxima práctica:
Una actividad académica importante en el modelo educativo es que el alumno
desarrolle habilidades y actitudes para la investigación. La investigación
bibliográfica por ejemplo, le permite ampliar más el acervo de conocimientos

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 23
adquiridos y no conformarse con lo aprendido en el aula, el encontrar una utilidad
práctica a los conocimientos adquiridos le facilitan el aprendizaje.
6. SISTEMA DE EVALUACIÓN DE LA PRIMERA
PRÁCTICA
6.1 LINEAMIENTOS GENERALES PARA LA EVALUACIÓN
La evaluación será a través de los siguientes parámetros:
Reporte Escrito: El cual deberá tener la estructura descrita en el apartado: 5.1.
Lineamientos Generales para la Evaluación (pag 17)
Desempeño dentro del laboratorio.
Asistencia a las prácticas.
6.2 MÉTODO DE ASIGNACIÓN DE CALIFICACIONES DE LA
PRIMERA PRÁCTICA
La calificación y ponderación de ésta primera práctica es la siguiente:
ACTIVIDAD A CALIFICAR PONDERACIÓN
Actividades previas 10
Reporte Escrito. 50
Desempeño dentro del laboratorio. 30
Asistencia al laboratorio 10
7. BIBLIOGRAFÍA:
Harper Bioquímica ilustrada, Robert K. Murray, Peter A. Mayes, Daryl K.
Granner y Victor. W. Rodwell; 28ª. ed, Ed. Mc Graw Hill ,2010.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 24
Fundamentos de Bioquímica, Voet D., Voet JG., Pratt CW. 2ª. ed. Editorial
Médica Panamericana. 2007
Bioquímica, A. L. Lehninger, 3ª edición, Editorial Omega, S. A. 2001
Bioquímica: La base molecular de la vida. Trudy McKee y James R. McKee.
4ª ed., Ed. McGraw-Hill Interamericana. 2009
8. PARA SABER MÁS
Explique cómo se aplican las leyes de la termodinámica a la presente
práctica.
Explique como el organismo humano intercambia energía para considerarlo
un sistema abierto.
9. GLOSARIO DE TÉRMINOS
Investigue sobre los siguientes términos: Bioenergética, leyes de la
termodinámica, compuestos de fosfato de alta energía (ATP),
sistema abierto sistema cerrado, entropía, entalpia, energía
libre.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 25
UNIVERSIDAD JUÁREZ DEL ESTADO DE DURANGO
FACULTAD DE CIENCIAS QUÍMICAS
SEGUNDA PRÁCTICA
DETERMINACIÓN DE VITAMINA C EN ALIMENTOS

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 26
1. NÚMERO DE ALUMNOS POR UNIDAD DE
PRÁCTICA
Para un buen desarrollo de la actividad académica considerando el espacio, el
número ideal es de 30-35 alumnos en equipos de 3 alumnos.
2. INTRODUCCIÓN DE LA SEGUNDA PRÁCTICA
Desde los tiempos de Hipócrates (400 A de C), algunas enfermedades se
atribuían a deficiencias dietéticas, debido a que podían curarse mediante el
consumo de ciertos alimentos. Los factores que originaban estas deficiencias
fueron designados como factores alimenticios complementarios, vitaminas o
aminas vitales, por la creencia errónea de que tales sustancias eran todas de
una estructura química, parecidas a las aminas.
Las vitaminas son moléculas orgánicas complejas, indispensables para el
funcionamiento adecuado de los seres vivos, componentes esenciales de la dieta,
que intervienen a concentraciones mínimas sin tener funciones estructurales ni
energéticas; sin embargo, muchas actúan como coenzimas en reacciones
enzimáticas y otras tienen actividades específicas en el funcionamiento celular. En
general no son sintetizadas por los animales, en la naturaleza las vitaminas son
producidas por las bacterias y los vegetales.
Las vitaminas se clasifican en liposolubles que comprenden las vitaminas A, D, E,
y K; y en hidrosolubles que constituyen las del llamado complejo B y además el
ácido ascórbico.
El ácido ascórbico o vitamina C es un compuesto cuya estructura semeja a la de
un monosacárido de 6 carbonos, se encuentra abundantemente en las frutas y
vegetales, especialmente en las partes en crecimiento activo de las plantas, como
las hojas tiernas y las flores; ocurre en menor proporción en tejidos animales; en la
leche de vaca hay cerca de 20 mg por litro. Los vegetales más ricos en ácido

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 27
ascórbico son los chícharos y los vegetales con hojas, las papas, los nabos, los
tomates y las frutas cítricas como las naranjas, el limón, la toronja, así como la col
cruda.
El contenido de vitamina C en las frutas y verduras varía dependiendo del grado de
madurez, es menor cuando están verdes, aumenta su cantidad cuando están en su
punto y luego vuelve a disminuir; por lo que la fruta madura ha perdido parte de su
contenido de vitamina C. Lo más recomendable es comer las frutas y verduras
frescas puesto que la acción del calor destruye a la vitamina C, también el contacto
con el aire la oxida y pierde su actividad, esto hay que recordarlo cuando se
prepara un jugo de fruta como el de naranja, de no tomárselo rápidamente habrá
perdido una gran cantidad de vitamina C. La otra forma de destrucción de la
vitamina C, es al tener contacto con alcohol etílico, por ejemplo con la cerveza o el
tequila.
El hombre no es capaz de sintetizar el ácido ascórbico, por lo tanto si no lo
adquiere por medio de la dieta presenta signos de su deficiencia, llegando a
desarrollarse el cuadro del escorbuto, el que se caracteriza por tumefacción de
las encías, movilidad de los dientes, hemorragias numerosas y pequeñas en piel
y mucosas y fragilidad ósea, al igual que trastornos en la cicatrización, debido a
que el ácido ascórbico es necesario para la síntesis de hidroxiprolina y la
producción de osteoblastos.
Cualquier cantidad de vitamina C que se ingiera ó se inyecte en concentraciones
por encima de las necesidades, será excretada cuantitativamente por la orina, por
lo que no se justifica el empleo indiscriminado de vitamínicos en la práctica clínica.
Los requerimientos diarios de vitamina C para el adulto son de 75 a 100 mg por
día aumentando durante el embarazo y la lactancia a 150 mg; en niños son de 20
a 60 mg dependiendo de la edad. La excreción urinaria del ácido ascórbico por 24
horas normalmente es de 100 a 400 g por kg de peso.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 28
3. PROPÓSITO ESPECÍFICO DE LA SEGUNDA
PRÁCTICA:
3.1 CRITERIOS DE DESEMPEÑO
2ª PRÁCTICA: Determinación de la vitamina C en alimentos
EL ALUMNO SERÁ COMPETENTE PARA DETERMINAR VITAMINA C EN
ALIMENTOS:
Sea capaz de realizar la determinación de vitamina C al aplicar los fundamentos
teórico – prácticos en la preparación de las soluciones a utilizar y en el
procedimiento para la determinación de la vitamina C en zumos diferentes frutas.
Para lo cual tendrá que:
Antes de usar un reactivo o cualquier sustancia química asegurarse de
conocer la Ficha de Datos de Seguridad, así como las Reglas básicas para el
manejo adecuado de reactivos y soluciones.
Seleccionar el mejor grado de sustancia disponible para el trabajo analítico.
Realizar cálculos para determinar la concentración y el volumen de la solución
a preparar
Conservar el área de trabajo, los materiales y los equipos limpios
Usar el material de vidrio adecuado para cada solución y conocer su método
de limpieza
Establecer y aplicar todas las operaciones requeridas para obtener la solución
(secado, pulverizado, enfriamiento, disolución en frío o con calentamiento,
transvasado, aforo, almacenamiento en un envase adecuado y etiquetado)
Operar adecuadamente el equipo empleado
Realizar cuidadosamente el procedimiento de determinación de la vitamina C
en los zumos de frutas a utilizar.
Comprender las reacciones que se llevan a cabo para el fin de determinar
vitamina C.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 29
3.2 RESULTADO FINAL DE LA SEGUNDA PRÁCTICA
El alumno será capaz de realizar la determinación de vitamina C en alimentos y
comparar el contenido de esta vitamina en los diferentes alimentos ensayados.
4. NORMAS DE SEGURIDAD ESPECÍFICAS DE LA
PRÁCTICA
4.1 CUADRO 4. DETECCIÓN DE RIESGOS PARTICULARES DE LA
SEGUNDA PRÁCTICA
Sin riesgo particular, seguir las normas de seguridad generales
4.2. DISPOSICIÓN DE DESECHOS
Los desechos de sustancias ácidas o básicas deben neutralizarse antes de verter al
drenaje y se deben vaciar cuando el agua de la llave este corriendo.
5. DESARROLLO DE LA SEGUNDA PRÁCTICA
El desarrollo de la segunda práctica será manejado en 3 etapas:
ACTIVIDADES TIEMPO
REQUERIDO
RESULTADO DE LA
ACTIVIDAD
A) Actividad guiada por el
docente responsable de la
práctica
20
min.
El docente realizara una
explicación de la metodología de
la práctica.
B) Actividad realizada por
los equipos de estudiantes
60
min
Cada equipo desarrollará el
proceso analítico para preparar
las soluciones a la concentración
requerida y realizar el

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 30
procedimiento para determinar
vitamina C en los zumos de
diferentes frutas.
C) Aplicación de la práctica
en el desempeño
profesional
Final de la práctica
40 min
Reporte de laboratorio para la
siguiente sesión.
A) Primera etapa de la práctica: PRÁCTICA DIRIGIDA POR EL
DOCENTE RESPONSABLE DE LA PRÁCTICA:
En ésta etapa el docente explicará la metodología de la práctica.
B) Segunda etapa de la práctica: ACTIVIDAD REALIZADA POR EL
ALUMNO EN GRUPOS DE TRABAJO.
Al concluir la explicación guiada por el docente, se dividirá al grupo en equipos de
trabajo máximo de 3 estudiantes. Los equipos se organizan en mesas de trabajo
para iniciar la práctica, con su procedimiento disponible.
El desarrollo de ésta parte de la práctica se realizará de la manera siguiente:
2ª PRÁCTICA. PROCEDIMIENTO
o Reactivos
Almidón
Reactivo de lugol
Jugos de naranja, limón, tomate, zanahoria y durazno
Tabletas de vitamina C 500 mg
o Materiales
Gradilla
Tubos de ensayo
Pipeta
Tapones de caucho

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 31
PROCEDIMIENTO:
1. Disuelva 0.5 g de almidón en 10.0 mL de agua.
2. En un tubo de ensayo adicione 2.0 mL de la solución de almidón y 1.0 mL de
lugol. Adicione media tableta de vitamina C. Registre sus observaciones.
3. La decoloración de la mezcla es una indicación de la presencia de vitamina C;
tenga en cuenta este resultado como patrón de referencia.
4. Identifica cinco tubos de ensayo como A, B, C, D y E y coloca en cada uno de
ellos 1.0 mL de la solución de almidón y 1.0 mL de lugol. Añada unas gotas de
jugo de naranja al tubo A; unas gotas de jugo de limón al tubo B; 1.0 mL de jugo
de tomate al tubo C; 1.0 mL de jugo de zanahoria al tubo D; y 1.0 mL de jugo de
durazno al tubo E. Tape cada tubo con un tapón de caucho y agítelos. Registre
sus observaciones para cada tubo.
5. Analice los resultados y discuta los mismos.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 32
RESULTADOS
Identifique cual de los alimentos empleados contiene mayor cantidad de
vitamina C.
Consulte un método sencillo de laboratorio para identificar otras vitaminas
diferentes a la C.
C) Tercera etapa de la práctica: APLICACIÓN DE LOS CONOCIMIENTOS
, HABILIDADES Y ACTITUDES ADQUIRIDOS EN LA PRÁCTICA, EN EL
DESEMPEÑO PROFESIONAL Y REPORTE DE LABORATORIO PARA
LA SIGUIENTE SESIÓN.
Reporte de laboratorio para la próxima práctica de acuerdo al formato establecido:
6. SISTEMA DE EVALUACIÓN DE LA SEGUNDA
PRÁCTICA
6.1 LINEAMIENTOS GENERALES PARA LA EVALUACIÓN
La evaluación será a través de los siguientes parámetros:
Actividades previas: Cálculos realizados previamente y diagrama de flujo de la
práctica realizados en su bitácora de practicas.
Reporte Escrito: El cual deberá tener la estructura descrita en el apartado: 5.1.
Lineamientos Generales para la Evaluación (pag 17)
Desempeño dentro del laboratorio.
Asistencia a las prácticas.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 33
6.2 MÉTODO DE ASIGNACIÓN DE CALIFICACIONES DE LA
SEGUNDA PRÁCTICA
La calificación y ponderación de ésta segunda práctica es la siguiente:
ACTIVIDAD A CALIFICAR PONDERACIÓN
Actividades previas 10
Reporte Escrito. 35
Desempeño dentro del laboratorio. 45
Asistencia al laboratorio 10
7. BIBLIOGRAFÍA:
Harper Bioquímica ilustrada, Robert K. Murray, Peter A. Mayes, Daryl K.
Granner y Victor. W. Rodwell; 28ª. ed, Ed. Mc Graw Hill ,2010.
Fundamentos de Bioquímica, Voet D., Voet JG., Pratt CW. 2ª. ed. Editorial
Médica Panamericana. 2007
Bioquímica, A. L. Lehninger, 3ª edición, Editorial Omega, S. A. 2001
Bioquímica: La base molecular de la vida. Trudy McKee y James R. McKee.
4ª ed., Ed. McGraw-Hill Interamericana. 2009
8. PARA SABER MÁS
Realizar una búsqueda bibliográfica o en internet sobre los temas de:
Vitaminas, antioxidantes y coenzimas.
Determinación de vitamina C:
El ácido ascórbico o vitamina C (C6H8O6) se puede determinar por medio
de una titulación yodométrica. La vitamina C es un agente reductor suave

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 34
que reacciona rápidamente con el ión triyoduro, en esta práctica se genera
un exceso conocido de ion triyoduro (I3- ) por reacción de
yodato con yoduro, se deja reaccionar y luego el exceso de I3- se titula por
retroceso con una
solución de tiosulfato. El método se basa en las siguientes reacciones:
8I- + IO3- + 6H+____ 3I3- + 3H2O
C6H8O6 + I3- + H2O _______ C6H8O7 + 2H+ + 3I
Ácido
ascórbico ácido deshidroascórbico
I3- + 2(S2O3)-2 ______ 3I- + (S4O6)-2
Tiosulfato tetrationato
9. GLOSARIO DE TÉRMINOS
Investigue sobre los siguientes términos: Vitaminas hidrosolubles,
vitaminas liposolubles, hipervitaminosis, deficiencia de vitaminas
escorbuto.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 35
UNIVERSIDAD JUÁREZ DEL ESTADO DE DURANGO
FACULTAD DE CIENCIAS QUÍMICAS
TERCERA PRÁCTICA
DEGRADACIÓN ENZIMÁTICA DE POLISACÁRIDOS

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 36
1. NÚMERO DE ALUMNOS POR UNIDAD DE
PRÁCTICA
Para un buen desarrollo de la actividad académica considerando el espacio, el
número ideal es de 30-35 alumnos en equipos de 3 alumnos.
2. INTRODUCCIÓN DE LA TERCERA PRÁCTICA
Una de las funciones fundamentales del aparto digestivo es transformar los
alimentos ingeridos en estructuras sencillas capaces de ser absorbidas a nivel
intestinal. La digestión de carbohidratos ingeridos (como es el caso del almidón)
comienza en la boca a través de la ptialina. Esta enzima es una α-amilasa que
hidroliza enlaces α (1,4) internos, pero no los α(1,6) próximos a las ramificaciones.
Los productos de esta digestión en la boca son maltosa e isomaltosa y otros
polímeros que contienen de 3 a 9 moléculas de glucosa. Aunque el alimento
permanece en la boca un corto período de tiempo, la acción de la amilasa salival
continúa hasta que el pH ácido del contenido estomacal la inactiva, de manera que
hasta ese momento la enzima hidroliza de un 30 a un 40% de los almidones de la
dieta. A nivel intestinal actúa otra α-amilasa de origen pancreático y con una
actividad semejante a la salival, rindiendo productos de degradación similares.
Estos productos sufren finalmente la acción de otras carbohidrolasas (maltasa,
lactasa, isomaltasa) liberando los monosacáridos que posteriormente son
absorbidos. El almidón es el polisacárido de reserva más abundante en los
vegetales. Está formado por α-amilosa (lineal de unas 200 unidades de D-glucosa
unidas por enlaces α-(1,4) glucosídicos) y por amilopectina (lineal de glucosa con
enlaces α- (1,4) y con ramificaciones mediante enlaces α-(1,6)-glucosídicos). La α-
amilosa en agua presenta una ordenación espiral característica, con 6 ó 7 residuos
de glucosa por vuelta. En esta hélice los grupos hidroxilos quedan hacia fuera,
mientras que en el interior se disponen los grupos hidrofóbicos. En este interior es

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 37
donde se incluye el yodo, formando un complejo de intenso color azul que permite
la identificación positiva de trazas de almidón. La amilasa salival actúa sobre el
almidón de los alimentos liberando azúcares reductores, estos azúcares en medio
alcalino, son capaces de reducir el ion Cu2+ de color azul a Cu+ de color rojo. Por
otro lado, en medio fuertemente básico, el ión Cu2+ formaría Cu(OH)2 insoluble, por
ello se añade tartrato sódico potásico que actúa como estabilizador al formar un
complejo con el Cu2+.
3. PROPÓSITO ESPECÍFICO DE LA TERCERA
PRÁCTICA
3.1 CRITERIOS DE DESEMPEÑO
3ª PRÁCTICA: DEGRADACIÓN ENZIMÁTICA DE POLISACÁRIDOS
EL ALUMNO SERÁ COMPETENTE PARA REALIZAR UNA DEGRADACIÓN
ENZIMÁTICA DE POLISACÁRIDOS CUANDO:
Sea capaz de: comprender la acción de las enzimas sobre los polisacáridos y las
condiciones en que se llevan a cabo.
3.2 RESULTADO FINAL DE LA TERCERA PRÁCTICA
El alumno será capaz de comprender bajo qué condiciones experimentales se
realiza la degradación enzimática de los polisacáridos

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 38
4. NORMAS DE SEGURIDAD ESPECÍFICAS DE LA
PRÁCTICA
4.1 CUADRO 5. DETECCIÓN DE RIESGOS PARTICULARES DE LA
TERCERA PRÁCTICA.
Tipo de peligro Como evitarlo Como proceder en caso
de accidente…
Contacto de la piel con
ácido clorhídrico
Manejo adecuado del
reactivo.
Usar bata manga larga
El acido diluido pueden
causar quemaduras leves.
Lavar con agua corriente
durante 15 min., quitarse la
ropa contaminada y
calzado.
Contacto de los ojos
con ácido clorhídrico
Manejo adecuado del
reactivo.
Usar lentes.
A baja concentración causa
irritación. Lave rápidamen
te con agua en un lavaojos,
unos 15 min., separando
los párpados. De
mantenerse el daño, acudir
a una asistencia médica.
Ingestión de ácido
clorhídrico
Manejo adecuado del
reactivo.
Usar pipetores
manuales o
automáticos.
El producto causa quema
duras y ulceraciones del
tracto gastrointestinal. No
provocar vomito. Lavar la
boca con agua. Dar de 240
a 300 mL de agua y leche.
Proporcionar atención
médica inmediatamente.
Contacto de hidróxido Manejo adecuado del Lavarse rápidamente con

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 39
de sodio con los ojos reactivo.
Usar lentes.
abundante agua en un
lavaojos, entre 15 y 30
min., mínimo, separando
los párpados. De seguir el
daño, acudir al médico.
Tipo de peligro Como evitarlo Como proceder en caso de
accidente
Contacto de la piel
con hidróxido de
sodio
Manejo adecuado del
reactivo.
Usar bata manga larga
Lavar rápidamente con
abundante agua, por lo menos
de 15 a 20 minutos en una
ducha de emergencia. Quitar
la ropa contaminada. Si
persiste el daño, acudir al
médico.
Ingestión de
hidróxido de sodio
Manejo adecuado del
reactivo.
Usar pipetores
automáticos o
manuales
Este producto produce quema
duras y ulceraciones. Lavar la
boca con bastante agua. Dar a
beber 250 a 300 mL de Agua
para diluir. No inducir al
vómito. Acudir al medico
rápidamente.
4.2. DISPOSICIÓN DE DESECHOS
Los desechos de sustancias ácidas o básicas deben neutralizarse antes de verter al
drenaje y se deben vaciar cuando el agua de la llave este corriendo.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 40
5. DESARROLLO DE LA TERCERA PRÁCTICA
El desarrollo de la tercera práctica será manejado en 3 etapas:
ACTIVIDADES TIEMPO
REQUERIDO
RESULTADO DE LA
ACTIVIDAD
A) Actividad guiada por el
docente responsable de la
práctica
15
min.
El docente realizara una
explicación de la metodología de
la práctica.
B) Actividad realizada por
los equipos de estudiantes
75
min
Cada equipo desarrollará el
proceso para la degradación
enzimática de polisacáridos.
C) Aplicación de la práctica
en el desempeño
profesional
Final de la práctica
30 min
Reporte de laboratorio para la
siguiente sesión.
A) Primera etapa de la práctica: PRÁCTICA DIRIGIDA POR EL DOCENTE
RESPONSABLE DE LA PRÁCTICA:
En ésta etapa el docente explicará la metodología de la práctica y revisará el
procedimiento a desarrollar por los estudiantes.
B) Segunda etapa de la práctica: ACTIVIDAD REALIZADA POR EL
ALUMNO EN GRUPOS DE TRABAJO.
Al concluir la explicación guiada por el docente, se dividirá al grupo en equipos de
trabajo máximo de 3 estudiantes. Los equipos se organizan en mesas de trabajo
para iniciar la práctica.
El desarrollo de ésta parte de la práctica se realizará de la manera siguiente:

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 41
3° PRÁCTICA: PROCEDIMIENTO
MATERIAL:
1 Gradilla
6 tubos de ensayo
1 Termómetro
Papel indicador universal o pHmetro
1 Gotero
1 Vaso de precipitado
1 Mechero
1 Trípode
1 Malla de asbesto
REACTIVOS:
Saliva
Solución de almidón al 5%
Lugol
Solución de HCl al 5%
Solución de NaOH al 5%
Hielo
Agua caliente
PROCEDIMIENTO:
1. Coloque 3.0 mL de solución de almidón y 2 gotas de saliva en tres tubos de
ensayo previamente marcados A, B y C.
2. Determine el pH en cada tubo, utilizando un pHmetro o papel indicador
universal. Registre los resultados.
3. Agregue al tubo A 1.0 mL de ácido clorhídrico al 5%; al tubo B 1.0 mL de NaOH
al 5%; y al tubo C 1.0 mL de agua.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 42
4. Prepara un baño María con una temperatura de 37 ºC y coloque los tres tubos
de ensayo durante 10 minutos.
5. Retire los tubos de ensayo del baño maría y añada cinco gotas de lugol a cada
uno. Registre los cambios de color, olor, temperatura, etc.
6. En otros tres tubos de ensayo, previamente marcados como D, E y F, adicione
tres mL de almidón y dos gotas de saliva, a cada uno.
7. Durante diez minutos coloque el tubo D en hielo, el tubo E en el baño María a 37
ºC y el tubo F en agua hirviendo.
8. Retire los tubos de ensayo D, E y F de las anteriores condiciones y agregue
cinco gotas de lugol a cada uno.
RESULTADOS
Registre todos los cambios que observe.
Análisis
¿En qué situación se registró la mayor actividad enzimática y como la
evidencia?
C) Tercera etapa de la práctica: APLICACIÓN DE LOS CONOCIMIENTOS ,
HABILIDADES Y ACTITUDES ADQUIRIDOS EN LA PRÁCTICA, EN EL
DESEMPEÑO PROFESIONAL Y REPORTE DE LABORATORIO PARA
LA SIGUIENTE SESIÓN.
Reporte de laboratorio para la próxima práctica de acuerdo al formato establecido:

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 43
6. SISTEMA DE EVALUACIÓN DE LA TERCERA
PRÁCTICA
6.1 LINEAMIENTOS GENERALES PARA LA EVALUACIÓN
La evaluación será a través de los siguientes parámetros:
Actividades previas: Cálculos realizados previamente, preparación de
soluciones (Practica 2) y diagrama de flujo de la práctica realizados en su
bitácora de prácticas.
Reporte Escrito: El cual deberá tener la estructura descrita en el apartado: 5.1.
Lineamientos Generales para la Evaluación (pag 17)
Desempeño dentro del laboratorio.
Asistencia a las prácticas.
6.2 MÉTODO DE ASIGNACIÓN DE CALIFICACIONES DE LA
TERCERA PRÁCTICA
La calificación y ponderación de ésta primera práctica es la siguiente:
ACTIVIDAD A CALIFICAR PONDERACIÓN
Actividades previas 10
Reporte Escrito. 50
Desempeño dentro del laboratorio. 30
Asistencia al laboratorio 10
7. BIBLIOGRAFÍA:
Harper Bioquímica ilustrada, Robert K. Murray, Peter A. Mayes, Daryl K.
Granner y Victor. W. Rodwell; 28ª. ed, Ed. Mc Graw Hill ,2010.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 44
Fundamentos de Bioquímica, Voet D., Voet JG., Pratt CW. 2ª. ed. Editorial
Médica Panamericana. 2007
Bioquímica, A. L. Lehninger, 3ª edición, Editorial Omega, S. A. 2001
Bioquímica: La base molecular de la vida. Trudy McKee y James R. McKee.
4ª ed., Ed. McGraw-Hill Interamericana. 2009
9. PARA SABER MÁS
Realizar una búsqueda bibliográfica o en internet sobre los temas de:
titulación volumétrica, valoración de soluciones, modo de acción de una
sustancia indicadora.
Conteste las siguientes preguntas:
9. GLOSARIO DE TÉRMINOS
Investigue sobre los siguientes términos: Enzimas, Polisacáridos,
digestión, Hidrólisis y amilasa

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 45
UNIVERSIDAD JUÁREZ DEL ESTADO DE DURANGO
FACULTAD DE CIENCIAS QUÍMICAS
CUARTA PRÁCTICA
LOS PRODUCTOS DE LA RESPIRACIÓN ANAEROBIA

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 46
1. NÚMERO DE ALUMNOS POR UNIDAD DE
PRÁCTICA
Para un buen desarrollo de la actividad académica considerando el espacio, el
número ideal es de 30-35 alumnos en equipos de 3 alumnos.
2. INTRODUCCIÓN DE LA CUARTA PRÁCTICA
Clásicamente se ha considerado que las levaduras son los microorganismos mas
vinculados al progreso y bienestar humano, por su participación en proceso de
fermentación. Se ha dicho que la levadura es la “planta” más antigua que ha sido
cultivada. Se sabe que la fabricación del pan y la cerveza ya se practicaban en
Tebas durante la IX dinastía 2000 años antes de Cristo. Tales procesos se han
venido desarrollando hasta nuestros días. La levadura Saccharomyces cerevisiae y
algunas especies próximas han sido microorganismos muy utilizados tanto en
microbiología industrial (pan, bebidas fermentadas, y, ocasionalmente glicerina y
grasa) como en todo el desarrollo de la bioquímica. Probablemente el primero que
vio una célula de levadura fue A. Vaan Leewenhoek, en 1680.
En el siglo XVIII Linneo se interesó en la fermentación alcohólica, pero hubo que
esperar hasta mediados del siglo XIX los primeros avances importantes en el
conocimiento de la fisiología y bioquímica de las levaduras. En 1897 los hermanos
Buchner obtuvieron el primer extracto de levadura con el que fermentaron glucosa.
Por este motivo esta fecha se considera como la del nacimiento de la bioquímica.
La fermentación fue descubierta por Pasteur, que la describió como la vie sans l´air
(la vida sin el aire) y el proceso químico de la fermentación alcohólica fue
establecido por Gay-Lussac a principios del siglo XIX. El término fermentación, en
su acepción estricta, se refiere a la obtención de energía en ausencia de oxígeno y
generalmente lleva agregado el nombre del producto final de la reacción.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 47
Las fermentaciones pueden ser: naturales, cuando las condiciones ambientales
permiten la interacción de los microorganismos y los sustratos orgánicos
susceptibles; o artificiales, cuando el hombre propicia condiciones adecuadas.
La fermentación alcohólica (denominada también como fermentación del etanol o
incluso fermentación etílica) es un proceso biológico de fermentación en plena
ausencia de aire (oxígeno) anaerobico, originado por la actividad de algunos
microorganismos que procesan los hidratos de carbono (por regla general
azúcares: como pueden ser por ejemplo la glucosa, la fructosa, la sacarosa, el
almidón, etc.) para obtener como productos finales: un alcohol en forma de etanol
(cuya fórmula química es: CH3-CH2-OH), dióxido de carbono (CO2) en forma de gas
y unas moléculas de ATP que consumen los propios microorganismos en su
metabolismo celular energético anaeróbico. El etanol resultante se emplea en la
elaboración de algunas bebidas alcohólicas, tales como el vino, la cerveza, la sidra,
etc. Aunque en la actualidad se empieza a sintetizar también etanol mediante la
fermentación a nivel industrial a gran escala para ser empleado como
biocombustible.
También se produce la fermentación en la mayoría de las células de los animales
(incluido el hombre), excepto en las neuronas que mueren rápidamente si no
pueden realizar la respiración celular; algunas células, como los eritrocitos, carecen
de mitocondrias y se ven obligadas a fermentar; el tejido muscular de los animales
realiza la fermentación láctica cuando el aporte de oxígeno a las células musculares
no es suficiente para el metabolismo aerobio y la contracción muscular. Desde el
punto de vista energético, las fermentaciones son muy poco rentables si se
comparan con la respiración aerobia, ya que a partir de una molécula de glucosa
sólo se obtienen 2 moléculas de ATP, mientras que en la respiración se producen
38. Esto se debe a que la oxidación del NADH producido en la glucolisis, en lugar
de penetrar en la cadena respiratoria, cede sus electrones a compuestos orgánicos
que se reducirán para poder reoxidar el NADH a NAD+. Ello significa que el aceptor
final de los electrones del NADH no es el oxígeno.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 48
La glucólisis es la primera etapa de la fermentación, lo mismo que en la respiración
celular, y al igual que ésta necesita de enzimas para su completo funcionamiento.
El balance final de la fermentación alcohólica es el siguiente:
Glucosa + 2 ADP + 2 Pi =====> 2 etanol + 2 CO2 + 2 ATP + 2 H2O
La molécula de glucosa (de 6 C) se escinde y rinde dos moléculas de etanol (de 2
C cada una) y dos moléculas de CO2. En las levaduras, el piruvato se descarboxila
para formar acetaldheído, que posteriormente se reduce por el NADH para formar
etanol.
3. PROPÓSITO ESPECÍFICO DE LA CUARTA
PRÁCTICA:
3.1 CRITERIOS DE DESEMPEÑO
4ª PRÁCTICA: LOS PRODUCTOS DE LA RESPIRACIÓN ANAEROBIA
EL ALUMNO SERÁ COMPETENTE PARA MONTAR UN DISPOSITIVO PARA
REALIZAR UN EXPERIMENTO QUE GENERE PRODUCTOS DE RESPIRACIÓN
ANAEROBIA.
Sea capaz de conocer y aplicar correctamente los conocimientos de la respiración
celular. Tenga habilidad para obtener conteo de levaduras.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 49
3.2 RESULTADO FINAL DE LA CUARTA PRÁCTICA
El alumno será capaz de establecer un dispositivo en que se generen productos de
la respiración anaerobia mediante un cultivo de levaduras.
4. NORMAS DE SEGURIDAD ESPECÍFICAS DE LA
PRÁCTICA
4.1DETECCIÓN DE RIESGOS PARTICULARES DE LA CUARTA
PRÁCTICA.
Sin riesgo particular, seguir los lineamientos generales de seguridad del
laboratorio.
4.2. DISPOSICIÓN DE DESECHOS
Los desechos de sustancias ácidas o básicas deben neutralizarse antes de verter al
drenaje y se deben vaciar cuando el agua de la llave este corriendo.
5. DESARROLLO DE LA CUARTA PRÁCTICA
El desarrollo de la cuarta práctica será manejado en 3 etapas.
ACTIVIDADES TIEMPO
REQUERIDO
RESULTADO DE LA
ACTIVIDAD
A) Actividad guiada por el
docente responsable de la
práctica
10 min.
El docente realizara una
explicación de la metodología
de la práctica.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 50
B) Actividad realizada por
los equipos de estudiantes
El dispositivo con el
cultivo de levaduras
requiere de 48 horas,
el alumno realizará
mediciones al tiempo
0, 24 y 48 hrs.
Cada equipo montará el
dispositivo indicado en el
procedimiento de la práctica y
pondrá en marcha el
experimento.
C) Aplicación de la
práctica en el desempeño
profesional
Final de la práctica
20 min
Reporte de laboratorio para la
siguiente sesión.
A) Primera etapa de la práctica: PRÁCTICA DIRIGIDA POR EL
DOCENTE RESPONSABLE DE LA PRÁCTICA:
En ésta etapa el docente explicará la metodología de la práctica.
B) Segunda etapa de la práctica: ACTIVIDAD REALIZADA POR EL
ALUMNO EN GRUPOS DE TRABAJO.
Al concluir la explicación guiada por el docente, se dividirá al grupo en equipos de
trabajo máximo de 3 estudiantes. Los equipos se organizan en mesas de trabajo
para iniciar la práctica.
El desarrollo de ésta parte de la práctica se realizará de la manera siguiente:
4ª PRÁCTICA: PROCEDIMIENTO
MATERIAL:
1 probeta de 100 ml 1 Soporte universal con pinzas
1 vaso de precipitado de 250 ml 1 Manguera
1 Tubo de ensaye con tapón monohoradado 1 gotero

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 51
3 Tubos de vidrio 1 Globo pequeño
1 Matraz Erlemeyer con tapón bihoradado 1 litro de Jugo de cualquier fruta (uva, manzana, piña, caña, excepto cítricos)
EQUIPO:
1 balanza
1 microscopio
1 cámara de Neubauer
REACTIVOS:
1 paquete pequeño de Levadura fresca de panadería, puede ser levadura seca o en pastilla
20 gr. de hidróxido de calcio (Cal)
PROCEDIMIENTO Se procede a medir en la probeta, 100 ml del jugo de fruta, éste debe ser de
preferencia natural y se coloca en el matraz erlemeyer. Pesar 5 g, de levadura y
disolverla en 50 ml de agua tibia, mezclarla con el jugo del matraz.
En el vaso de precipitado se coloca la cal y se le pone agua destilada, hasta hacer
una solución saturada, (cuando se incorpora más cal esta se precipita, es decir ya
no se disuelve) se deja reposar y se utiliza esta agua para llenar el tubo de ensaye
en ¾ partes. Se procede a montar con el material un dispositivo como: el de la
figura.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 52
El matraz con la solución de fruta y levadura se tapa con el tapón bihoradado. En
una de las aberturas del tapón, se coloca un tubo de vidrio pequeño, que en el
extremo contenga el globo y en la otra abertura un tubo de vidrio que se conecta a
la manguera. La manguera va conectada a un tubo de vidrio que penetra por el
tapón monohoradado en el tubo de ensaye que contiene el agua de cal.
Una vez hecha la solución de levadura, toma una gota y colócala en un
portaobjetos de cámara de Neubauer pon el cubreobjetos. Coloca la preparación en
el microscopio y enfócala Encontraras una rejilla, selecciona un cuadro y cuenta
cuantas levaduras encuentras, realiza la operación en 10 cuadros al azar. Anota en
tu cuaderno en una tabla las cantidades encontradas. Deja tu dispositivo durante 24
h, y haz tus primeras observaciones. Realiza un nuevo conteo de levaduras. A las
48 h harás tus observaciones finales. Anota en tu cuaderno lo que está sucediendo,
y realiza el último conteo de levaduras. Gráfica las cantidades obtenidas.
RESULTADOS
Tabla de Datos para el conteo de levaduras
Conteo inicial (0 h) Conteo
No. de levaduras
1
2
3
4
5
6
7
8
9
10
Total
Graficar el número de levaduras de los conteos.
Los resultados obtenidos serán un aumento en el número de levaduras, el globo se
va a inflar y el tubo de cal se enturbiará por la presencia de carbonato de calcio. El
Tabla final de datos
Conteo
No. de
levaduras
globo sol. cal
1 (0 h)
2 (24 h)
3 (48 h)

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 53
profesor debe discutir con los alumnos los resultados obtenidos y compararlos con
las predicciones de cada equipo para definir si la aceptan o rechazan.
C) Tercera etapa de la práctica: APLICACIÓN DE LOS CONOCIMIENTOS,
HABILIDADES Y ACTITUDES ADQUIRIDOS EN LA PRÁCTICA, EN EL
DESEMPEÑO PROFESIONAL Y REPORTE DE LABORATORIO PARA LA
SIGUIENTE SESIÓN.
La práctica culmina cuando se han resuelto todas las actividades de aplicación y
se ha respondido a cada una de las preguntas de la evaluación del aprendizaje
En esta etapa el alumno desarrolla la habilidad de argumentar los resultados
obtenidos.
Reporte de laboratorio para la próxima práctica de acuerdo al formato
establecido:
6. SISTEMA DE EVALUACIÓN DE LA CUARTA
PRÁCTICA
6.1 LINEAMIENTOS GENERALES PARA LA EVALUACIÓN
La evaluación será a través de los siguientes parámetros:
Actividades previas: Cálculos realizados previamente y diagrama de flujo de la
práctica realizados en su bitácora de practicas.
Reporte Escrito: El cual deberá tener la estructura descrita en el apartado: 5.1.
Lineamientos Generales para la Evaluación (pag 17)
Desempeño dentro del laboratorio.
Asistencia a las prácticas.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 54
6.2 MÉTODO DE ASIGNACIÓN DE CALIFICACIONES DE LA
CUARTA PRÁCTICA
La calificación y ponderación de ésta cuarta práctica es la siguiente:
ACTIVIDAD A CALIFICAR PONDERACIÓN
Actividades previas 10
Reporte Escrito. 50
Desempeño dentro del laboratorio. 30
Asistencia al laboratorio 10
7. BIBLIOGRAFÍA:
Harper Bioquímica ilustrada, Robert K. Murray, Peter A. Mayes, Daryl K.
Granner y Victor. W. Rodwell; 28ª. ed, Ed. Mc Graw Hill ,2010.
Fundamentos de Bioquímica, Voet D., Voet JG., Pratt CW. 2ª. ed. Editorial
Médica Panamericana. 2007
Bioquímica, A. L. Lehninger, 3ª edición, Editorial Omega, S. A. 2001
Bioquímica: La base molecular de la vida. Trudy McKee y James R. McKee.
4ª ed., Ed. McGraw-Hill Interamericana. 2009
10. PARA SABER MÁS
Realizar una búsqueda bibliográfica o en internet sobre los temas de:
Investiga con que industrias relacionarías este proceso.
Describe que aportan estas industrias a la Biotecnología.
¿Qué otros organismos se utilizan actualmente en Biotecnología?
Contesta las siguientes preguntas
1. - ¿Por qué se infló el globo?
2. - ¿Qué gas piensas que se acumuló en el globo?

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 55
3. - ¿Cómo probarías que gas es?
4. -¿Qué le sucedió al jugo de frutas?
5. - ¿Cómo identificarías el líquido que se obtuvo?
6. - ¿Qué papel tiene la levadura en este proceso?
7. ¿Con qué función de los seres vivos relacionarías este proceso?
8. - ¿Qué sucedió con la cantidad de levaduras, aumentó disminuyó?
9. - ¿Por qué piensas que sucedió eso con la cantidad de levaduras?
9. GLOSARIO DE TÉRMINOS
Investiga los siguientes términos:
Levadura, oxidación, glucosa, ATP, anaerobia, aerobia, ácido láctico,
metabolismo, ciclo de Krebs, cadena respiratoria.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 56
UNIVERSIDAD JUÁREZ DEL ESTADO DE DURANGO
FACULTAD DE CIENCIAS QUÍMICAS
QUINTA PRÁCTICA
DETERMINACION DE TRIGLICÉRIDOS EN SUERO

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 57
1. NÚMERO DE ALUMNOS POR UNIDAD DE
PRÁCTICA
Para un buen desarrollo de la actividad académica considerando el espacio, el
número ideal es de 30-35 alumnos en equipos de 3 alumnos.
2. INTRODUCCIÓN DE LA QUINTA PRÁCTICA
3. PROPÓSITO ESPECÍFICO DE LA QUINTA
PRÁCTICA
Los triacilgliceroles (triglicéridos) son lípidos formados por la esterificación de tres
moléculas de ácidos grasos con una molécula de glicerol. Se encuentran presentes
en los aceites y las grasas que forman parte de las dietas comunes. En el tejido
adiposo, donde constituyen la principal forma de almacenamiento energético. Los
triacilgliceroles dietarios se dirigen por acción de la lipasa pancreática, generando
principalmente monoacilgliceroles y ácidos grasos, productos capaces de ser
absorbidos por el intestino.
En los enterocitos se reesterifican los monoacilgliceroles con los ácidos grasos, y
los triacilgliceroles resultantes se asocian con otros componentes para estructurar
las lipoproteínas conocidas como quilomicrones, los cuales son secretados hacia la
linfa, a través de la cual son llevados a la circulación general.
En los capilares sanguíneos de diversos tejidos, principalmente del adiposo y del
muscular, la lipoproteína lipasa (LP) hidroliza más del 80% de los triacilgliceroles
de los quilomicrones, la mayor parte de los ácidos grasos liberados penetran a las
células del tejido correspondiente, mientras que el glicerol es captado y
metabolizado por el hígado. Después de que actúa la LP sobre los quilimicrones,
estos quedan convertidos en lipoproteínas pequeñas de alto contenido relativo de

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 58
colesterol, llamadas remanentes de quilimicrones cuyo destino es ser endocitadas
por los hepatocitos.
El hígado forma triacilgliceroles a partir de los carbohidratos dietarios cuando estos
se hayan en exceso. Debido a que el hígado no almacena normalmente grasa, sus
triacilgliceroles se asocian con otros componentes lipídicos y proteínicos para
estructurar por ejemplo, las lipoproteínas de muy baja densidad (LVDL), las cuales
secretan a la sangre.
De manera similar a lo que ocurre con los quilimicrones, la LP hidroliza la mayor
parte de los triacilgliceroles presentes en las LVDL, penetrando los ácidos grasos
liberados, a las células de tejido correspondiente. En la fase de ayuno las LVDL
llegan solamente a tejidos de utilización (p.ej. músculo) mientras que en la fase
postrandial llega preferentemente al tejido adiposo para su almacenamiento.
Por otra parte la elevación de la concentración plasmática de triacilgliceroles
constituye un factor de riesgo aterogénico la concentración normal es menor a 200
mg/dL, aunque se considera sospechosa de hipertriacilgliceridemia en 350 y 200
mg/dL. Aquellos países con dietas altas en grasas animales contienen elevada
prevalencia de aterosclerosis y sus complicaciones por el contrario, en países con
ingesta baja de grasas saturadas, como es el caso de Japón y algunos países
mediterráneos, la prevalencia de aterosclerosis es baja.
Se ha documentado que las campañas exitosas para disminuir la ingesta de grasa
animal en países con alta prevalencia de aterosclerosis y cardiopatía isquémica,
logran reducir la mortalidad por esta causa, lo cual tiene gran importancia clínica.
El hombre primitivo requería el almacenamiento de grasas en su cuerpo debido a lo
incierto de cuando podría tomar su próximo alimento, sin embargo, en la mayoría
de la sociedades actuales es innecesario el almacenamiento de grasas, dada la
disponibilidad de alimentos a cualquier hora del día y a que el esfuerzo físico cada
vez es menor.
En general, las grasas insaturadas son de origen vegetal y por lo tanto su ingesta
no se haya asociada por si misma a la ingesta de colesterol. Además, dicha grasa
proporciona ácidos grasos insaturados como el linoléico, el linolénico y el
araquidónico, conocidos como ácidos grasos esenciales, aunque en la realidad el

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 59
único verdaderamente esencial es el linoéico ya que el organismo no lo puede
sintetizar, pero si se encuentra disponible, el organismo sintetiza a partir de él los
otros dos.
3.1 CRITERIOS DE DESEMPEÑO
5ª PRÁCTICA: DETERMINACION DE TRIGLICÉRIDOS EN SUERO
EL ALUMNO SERÁ COMPETENTE PARA:
1. Determinar la concentración de triacilgliceroles por un método enzimático
colorimétrico
2. Enunciar la importancia clínica de la determinación los triacilgliceroles.
3. Describir los sistemas de absorción y transporte de triacilgliceroles
3.2 RESULTADO FINAL DE LA QUINTA PRÁCTICA
El estudiante determinará la concentración de triglicéridos en suero sanguíneo
y comprenderá las reacciones que se llevan a cabo en el procedimiento.
Además establecerá por comparación de los valores normales si las cifras de
triglicéridos son normales.
4. NORMAS DE SEGURIDAD ESPECÍFICAS DE LA
PRÁCTICA
4.1 DETECCIÓN DE RIESGOS PARTICULARES DE LA QUINTA
PRÁCTICA.
Sin riesgo particular, seguir las normas de seguridad generales.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 60
4.2. DISPOSICIÓN DE DESECHOS
Los desechos biológicos serán colocados en los depósitos que para tal fin se
encuentran en el laboratorio. Así mismo los objetos punzocortantes serán
confinados al depósito señalado en el laboratorio.
5. DESARROLLO DE LA QUINTA PRÁCTICA
El desarrollo de la quinta práctica será manejado en 3 etapas.
ACTIVIDADES TIEMPO
REQUERIDO
RESULTADO DE LA
ACTIVIDAD
A) Actividad guiada por el
docente responsable de la
práctica
10
min.
El docente realizará una
explicación de la metodología de
la práctica.
B) Actividad realizada por
los equipos de estudiantes
50
min
Cada equipo desarrollará el
procedimiento para la
determinación de los triglicérdios
en suero.
C) Aplicación de la práctica
en el desempeño
profesional
Final de la práctica
20 min
Reporte de laboratorio para la
siguiente sesión.
A) Primera etapa de la práctica: PRÁCTICA DIRIGIDA POR EL DOCENTE
RESPONSABLE DE LA PRÁCTICA:
En ésta etapa el docente explicará la metodología de la práctica.
B) Segunda etapa de la práctica: ACTIVIDAD REALIZADA POR EL
ALUMNO EN GRUPOS DE TRABAJO.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 61
Al concluir la explicación guiada por el docente, se dividirá al grupo en equipos de
trabajo máximo de 3 estudiantes. Los equipos se organizan en mesas de trabajo
para iniciar la práctica con su muestra respectiva.
El desarrollo de ésta parte de la práctica se realizará de la manera siguiente:
5ª PRÁCTICA. PROCEDIMIENTO
Material 3 Tubos de ensaye
1Gradilla
1 Pipeta de 1.0 ml
1 Micropipeta de 20 l
Reactivos Equipo Suero
Patrón de triglicéridos Espectrofotómetro
Reactivo de trabajo
PROCEDIMIENTO: Lleve a cabo el procedimiento como lo indica la siguiente tabla:
Solución Suero Patrón Reactivo de Trabajo
Blanco ------ ------- 1.0 ml
Patrón ------ 10 l 1.0 ml
Muestra 10 l ----- 1.0 ml
Mezclar e incubar a 37°C durante 5 min medir la absorbancia a 505 nm de la muestra y del patrón frente al blanco. El color es estable durante 60 min.
La hidrólisis de los triacilgliceroles produce ácidos grasos y glicerol por acción
de la lipasa. El glicerol formado reacciona con ATP, produciendo glicerolfosfato y ADP
por catálisis de la glicerolcinasa. El glicerol fosfato a su vez reacciona con oxígeno y

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 62
da como productos dihidroxiacetona fosfato y peróxido de hidrógeno, en una reacción
catalizada por la glicerolfosfato oxidasa.
El peróxido de hidrógeno reacciona con 4-aminofenazona y 4-clorofenol,
generando quinoneimina (compuesto colorido), ácido clorhídrico y agua. La
concentración del compuesto colorido es proporcional a la concentración de
triacilgliceroles.
RESULTADOS
Lleve a cabo los cálculos siguientes para obtener la concentración de triacilgliceroles
en la muestra problema.
A muestra __________ X 200 = Trigliacilgliceroles mg/dL A patrón Valores normales:
Sospecha de hipertriacilgliceridemia: a partir de: 150 mg/dL
Hipertriacilgliceridemia: a partir de: 200 mg/dL
C) Tercera etapa de la práctica: APLICACIÓN DE LOS CONOCIMIENTOS ,
HABILIDADES Y ACTITUDES ADQUIRIDOS EN LA PRÁCTICA, EN EL
DESEMPEÑO PROFESIONAL Y REPORTE DE LABORATORIO PARA
LA SIGUIENTE SESIÓN.
Reporte de laboratorio para la próxima práctica de acuerdo al formato establecido:

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 63
6. SISTEMA DE EVALUACIÓN DE LA QUINTA
PRÁCTICA
6.1 LINEAMIENTOS GENERALES PARA LA EVALUACIÓN
La evaluación será a través de los siguientes parámetros:
Actividades previas: Preparación de soluciones (Practica 2) y diagrama de flujo
de la práctica en su bitácora de prácticas.
Reporte Escrito: El cual deberá tener la estructura descrita en el apartado: 5.1.
Lineamientos Generales para la Evaluación (pag 17)
Desempeño dentro del laboratorio
Asistencia a las prácticas.
6.2 MÉTODO DE ASIGNACIÓN DE CALIFICACIONES DE LA
QUINTA PRÁCTICA
La calificación y ponderación de ésta primera práctica es la siguiente:
ACTIVIDAD A CALIFICAR PONDERACIÓN
Actividades previas 10
Reporte Escrito. 50
Desempeño dentro del laboratorio. 30
Asistencia al laboratorio 10
7. BIBLIOGRAFÍA:
Harper Bioquímica ilustrada, Robert K. Murray, Peter A. Mayes, Daryl K.
Granner y Victor. W. Rodwell; 28ª. ed, Ed. Mc Graw Hill ,2010.
Fundamentos de Bioquímica, Voet D., Voet JG., Pratt CW. 2ª. ed. Editorial
Médica Panamericana. 2007

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 64
Bioquímica, A. L. Lehninger, 3ª edición, Editorial Omega, S. A. 2001
Bioquímica: La base molecular de la vida. Trudy McKee y James R. McKee.
4ª ed., Ed. McGraw-Hill Interamericana. 2009
8. PARA SABER MÁS
Realizar una búsqueda bibliográfica o en internet sobre los resultados
obtenidos en la práctica realizada.
Construya un esquema del metabolismo de los triglicéridos en el hígado.
Elabore una tabla que incluya diferentes grasas, aceites y mantecas en las
que se indiquen sus principales características.
Mencione y explique al menos dos fisiopatologías que involucren
alteraciones en el metabolismo de los triglicéridos.
¿De qué se componen las lipoproteínas? ¿Cuál es la función biológica y
clasificación?

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 65
UNIVERSIDAD JUÁREZ DEL ESTADO DE DURANGO
FACULTAD DE CIENCIAS QUÍMICAS
SEXTA PRÁCTICA
DETERMINACIÓN DE COLESTEROL EN SUERO

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 66
1. NÚMERO DE ALUMNOS POR UNIDAD DE
PRÁCTICA
Para un buen desarrollo de la actividad académica considerando el espacio, el
número ideal es de 30-35 alumnos en equipos de 3 alumnos.
2. INTRODUCCIÓN DE LA SEXTA PRÁCTICA
El colesterol es un derivado del ciclopentanoperhidrofenantreno. Es una molécula
insoluble en agua que se encuentra en todos los tejidos corporales, especialmente en
cerebro, hígado, médula osea y piel. El colesterol se encuentra en todas las células
animales formando parte de las membranas y los distintos tipos de lipoproteínas:
además de las sales biliares, es precursor de vitamina D y de toda la familia de
hormonas esteroides.
HO
3
5
COLESTEROL
El colesterol se encuentra en el suero o en plasma en forma libre o esterificada con
ácidos grasos. A través del tiempo el interés clínico por los lípidos sanguíneos ha
oscilado entre el colesterol, las lipoproteínas y los triglicéridos, pero en estudios no
especializados la colesterolemia continua siendo el dato preferido por la sencillez de
su valoración y bajo costo. Para la determinación de colesterol total se utiliza una
serie de reacciones enzimáticas. El experimento que se va a efectuar, consiste en
determinar la colesterolemia en el humano por el método de Bloor, que utiliza la

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 67
reacción de Lieberman Burchard para producir un color verde de intensidad
proporcional a la concentración del colesterol.
3. PROPÓSITO ESPECÍFICO DE LA SEXTA
PRÁCTICA:
3.1 CRITERIOS DE DESEMPEÑO
6ª PRÁCTICA: DETERMINACIÓN DE COLESTEROL EN SUERO
EL ALUMNO SERÁ COMPETENTE PARA:
Determinar el contenido de colesterol total plasmático (método enzimático
colorimétrico).
Comprender las reacciones que se llevan a cabo para la determinación de colesterol.
3.2 RESULTADO FINAL DE LA SEXTA PRÁCTICA
El estudiante determinará la concentración de colesterol en suero sanguíneo y
comprenderá las reacciones que se llevan a cabo en el procedimiento.
Además establecerá por comparación de los valores normales si las cifras de
colesterol son normales.
4. NORMAS DE SEGURIDAD ESPECÍFICAS DE LA
PRÁCTICA
4.1 DETECCIÓN DE RIESGOS PARTICULARES DE LA
SEXTA PRÁCTICA
Sin riesgo particular, seguir las normas de seguridad generales.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 68
4.2. DISPOSICIÓN DE DESECHOS
Los desechos biológicos serán colocados en los depósitos que para tal fin se
encuentran en el laboratorio. Así mismo los objetos punzocortantes serán
confinados al depósito señalado en el laboratorio.
5. DESARROLLO DE LA SEXTA PRÁCTICA
El desarrollo de la cuarta práctica será manejado en 3 etapas.
ACTIVIDADES TIEMPO
REQUERIDO
RESULTADO DE LA
ACTIVIDAD
A) Actividad guiada por el
docente responsable de la
práctica
10
min.
El docente realizará una
explicación de la metodología de
la práctica.
B) Parte experimental
realizada por los equipos
de estudiantes
50
min
Cada equipo desarrollará el
proceso analítico para
determinar de colesterol en suero
sanguíneo.
C) Aplicación de la práctica
en el desempeño
profesional
Final de la práctica
20 min
Reporte de laboratorio para la
siguiente sesión.
A) Primera etapa de la práctica: PRÁCTICA DIRIGIDA POR EL DOCENTE
RESPONSABLE DE LA PRÁCTICA:
En ésta etapa el docente explicará la metodología de la práctica.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 69
B) Segunda etapa de la práctica: ACTIVIDAD REALIZADA POR EL
ALUMNO EN GRUPOS DE TRABAJO.
Al concluir la explicación guiada por el docente, se dividirá al grupo en equipos de
trabajo máximo de 3 estudiantes. Los equipos se organizan en mesas de trabajo
para iniciar la práctica con su muestra respectiva.
El desarrollo de ésta parte de la práctica se realizará de la manera siguiente:
6ª PRÁCTICA. PROCEDIMIENTO
MATERIAL:
3 Tubos de ensaye
2 Vasos de precipitado
3 Pipetas graduadas de 1.0 ml
1 Pipeta graduada de 5 ml
MUESTRA
Suero sanguíneo
REACTIVOS
Ácido sulfúrico concentrado
Mezcla Ácido acético/anhídrido acético 1:1
Estándar de colesterol 250 mg/100ml
Agua destilada
EQUIPO:
Baño de hielo
Espectrofotómetro
PROCEDIMIENTO:
1. Marcar 3 tubos de ensaye con los números 1,2 y 3.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 70
2. Agregar a cada tubo 4.1 ml de la mezcla de ácido acético/anhídrido acético.
3. Colocar los tubos en un recipiente con hielo y agregar 0.8 ml de ácido sulfúrico
concentrado.
4. Agregar al tubo No.1, 0.1 ml de suero sanguíneo.
5. Agregar al tubo No.2, 0.1 ml de la solución estándar de colesterol, 250mg/100ml
6. Agregar al tubo No.3, 0.1 ml de agua destilada.
7. Agitar los tubos PERFECTAMENTE y dejarlos reposar durante 10 min. en la
oscuridad.
8. Leer en el espectrofotómetro a 640 nm usando el tubo No.3 como "blanco".
RESULTADOS
Lleve a cabo los cálculos siguientes para obtener la concentración de colesterol en la
muestra problema.
D.O. de la muestra X [estándar] = mg de colesterol D.O. de la sol. estándar 100 ml de sangre Valores normales:
Deseable: menos de 200 mg/dl
Límite alto: 200-239 mg/dl
Hipocolesterolemia: a partir de 240 mg/dl
C) . Tercera etapa de la práctica: APLICACIÓN DE LOS
CONOCIMIENTOS , HABILIDADES Y ACTITUDES ADQUIRIDOS EN LA
PRÁCTICA EN EL DESEMPEÑO PROFESIONAL Y REPORTE DE
LABORATORIO PARA LA SIGUIENTE SESIÓN.
Reporte de laboratorio para la próxima práctica de acuerdo al formato establecido:

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 71
6. SISTEMA DE EVALUACIÓN DE LA SEXTA
PRÁCTICA
6.1 LINEAMIENTOS GENERALES PARA LA EVALUACIÓN
La evaluación será a través de los siguientes parámetros:
Actividades previas: Cálculos realizados previamente y diagrama de flujo de la
práctica realizados en su bitácora de practicas.
Reporte Escrito: El cual deberá tener la estructura descrita en el apartado: 5.1.
Lineamientos Generales para la Evaluación (pag 17)
Desempeño dentro del laboratorio.
Asistencia a las prácticas.
6.2 MÉTODO DE ASIGNACIÓN DE CALIFICACIONES DE LA SEXTA
PRÁCTICA
La calificación y ponderación de ésta sexta práctica es la siguiente:
ACTIVIDAD A CALIFICAR PONDERACIÓN
Actividades previas 10
Reporte Escrito. 50
Desempeño dentro del laboratorio. 30
Asistencia al laboratorio 10
7. BIBLIOGRAFÍA
Harper Bioquímica ilustrada, Robert K. Murray, Peter A. Mayes, Daryl K.
Granner y Victor. W. Rodwell; 28ª. ed, Ed. Mc Graw Hill ,2010.
Fundamentos de Bioquímica, Voet D., Voet JG., Pratt CW. 2ª. ed. Editorial
Médica Panamericana. 2007
Bioquímica, A. L. Lehninger, 3ª edición, Editorial Omega, S. A. 2001

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 72
Bioquímica: La base molecular de la vida. Trudy McKee y James R. McKee.
4ª ed., Ed. McGraw-Hill Interamericana. 2009
8. PARA SABER MÁS
Realizar una búsqueda bibliográfica o en internet sobre el contenido de
acidez de los vinagres comerciales
Responder las siguientes preguntas:
1. Dé el nombre de cinco alimentos ricos en colesterol.
2. ¿Cuáles son los valores normales de colesterol, HDL colesterol y LDL colesterol
en sangre?
3. ¿Cuál es la enfermedad está relacionada con niveles elevados de colesterol en
sangre?
4. Genere un esquema de la como sería la separación electroforética de las
lipoproteínas plasmáticas:
5. ¿Cuál es la importancia de una dieta rica en ácidos grasos de tipo 3 en el
tratamiento y prevención de la hipercolesterolemia? ¿En qué alimentos se
encuentran esos ácidos grasos?
6. ¿Porque el consumo de dietas ricas en fibra podrían disminuir la
colesterolemia?

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 73
UNIVERSIDAD JUÁREZ DEL ESTADO DE DURANGO
FACULTAD DE CIENCIAS QUÍMICAS
SÉPTIMA PRÁCTICA
EXCRECIÓN DEL NITRÓGENO PROTÉICO

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 74
1. NÚMERO DE ALUMNOS POR UNIDAD DE
PRÁCTICA
Para un buen desarrollo de la actividad académica considerando el espacio, el
número ideal es de 30-35 alumnos en equipos de 3 alumnos.
2. INTRODUCCIÓN DE LA SÉPTIMA PRÁCTICA
Uno de los aspectos nutricionales más importantes, es la adecuada ingestión de
proteínas, ya que estos compuestos van a tomar parte en diferentes eventos
metabólicos del organismo.
En algunas ocasiones la cantidad del nitrógeno contenido en las proteínas ingeridas
es mayor que el excretado (balance nitrogenado positivo), esta situación se
presenta durante el crecimiento, embarazo, convalecencia, etc. Puede presentarse
el caso contrario en el que se excrete una mayor cantidad de nitrógeno que el
ingerido en las proteínas, como en el caso de padecimientos con deficiente
absorción intestinal, inanición, etc. (balance nitrogenado negativo).
El catabolismo de las proteínas es un proceso que ocurre en el organismo por el
desgaste normal de los tejidos. Los productos del catabolismo de las proteínas son
los aminoácidos libres, los cuales mediante el proceso conocido como
transdesaminación se transforman en los cetoácidos correspondientes, con la
liberación concomitante del nitrógeno aminoacídico en forma de ion amonio. El
amonio es una sustancia tóxica para el organismo, especialmente para el sistema
nervioso central, por lo que luego de liberarse en los diversos tejidos, llega al
hígado formando parte de diversas moléculas, fundamentalmente alanita y
glutamina. En este órgano se transforma en urea, producto de desecho
notoriamente menos tóxico que el amonio. Finalmente, la urea se elimina por la vía
renal.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 75
En condiciones normales, la concentración de urea en la sangre se halla
influenciada por la magnitud del aporte dietario de proteínas y por el estado de
hidratación general. En este último caso, la deshidratación se asocia con
hemoconcentración y consecuentemente se registra incremento de la
concentración de urea. El exceso de líquidos por el contrario, se asocia con
hemodilución y baja en la concentración de urea.
El término azoemia o azotemia se utiliza en ocasiones para referirse a la
presencia de nitrógeno de origen proteínico en la sangre.
3. PROPÓSITO ESPECÍFICO DE LA SÉPTIMA
PRÁCTICA
3.1 CRITERIOS DE DESEMPEÑO
7ª PRÁCTICA: EXCRECIÓN DEL NITRÓGENO PROTÉICO
EL ALUMNO SERÁ COMPETENTE PARA DETERMINAR LA EXCRECIÓN DE
NITRÓGENO PROTEICO CUANDO:
Comprenda la relación entre el nitrógeno ingerido en las proteínas y el excretado
como urea y creatinina.
b. La mayor parte del nitrógeno proteico ingerido es excretado en la orina en forma
de urea, pudiendo alcanzar cifras hasta de 30 gr en 24 horas. El nitrógeno que
existe en las heces proviene de productos de descamación intestinal o de la flora
bacteriana y su cantidad de 1-2 gr diarios.
c. La creatinina es considerada como otra forma de excreción del nitrógeno proteico
que es producido en el metabolismo endógeno y se elimina por la orina.
d. Tanto la urea como la creatinina tienen un bajo umbral renal, es decir, son
sustancias que se eliminan muy fácilmente conservando una concentración mínima
en sangre. Cuando por aluna razón su producción aumenta no se mantienen en
torrente circulatorio sino que son eliminados por el riñón.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 76
Esta propiedad les confiere un interés especial en la clínica, ya que el aumento de
estos metabolitos en sangre es índice de deterioro de la función renal.
3.2 RESULTADO FINAL DE LA SÉPTIMA PRÁCTICA
El estudiante determinará la concentración de urea en suero sanguíneo y
creatinina en orina, comprenderá las reacciones que se llevan a cabo en el
procedimiento. Además establecerá por comparación de los valores normales si las
cifras de urea son normales.
4 NORMAS DE SEGURIDAD ESPECÍFICAS DE LA
PRÁCTICA
4.1 DETECCIÓN DE RIESGOS PARTICULARES DE LA
SÉPTIMA PRÁCTICA
Sin riesgo particular, seguir normas generales de seguridad
4.2. DISPOSICIÓN DE DESECHOS
Los desechos biológicos serán colocados en los depósitos que para tal fin se
encuentran en el laboratorio. Así mismo los objetos punzocortantes serán
confinados al depósito señalado en el laboratorio.
5. DESARROLLO DE LA SÉPTIMA PRÁCTICA
El desarrollo de la séptima práctica será manejado en 3 etapas.
ACTIVIDADES
TIEMPO
REQUERIDO
RESULTADO DE LA
ACTIVIDAD
A) Actividad guiada por el 10 El docente realizará una

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 77
docente responsable de la
práctica
min.
explicación de la metodología de
la práctica.
B) Parte experimental
realizada por los equipos
de estudiantes
50
min
Cada equipo desarrollará el
proceso analítico para
determinar la excreción de
nitrógeno proteico.
C) Aplicación de la práctica
en el desempeño
profesional
Final de la práctica
20min
Reporte de laboratorio para la
siguiente sesión.
A) Primera etapa de la práctica: PRÁCTICA DIRIGIDA POR EL DOCENTE
RESPONSABLE DE LA PRÁCTICA:
En ésta etapa el docente explicará la metodología de la práctica.
B) Segunda etapa de la práctica: ACTIVIDAD REALIZADA POR EL
ESTUDIANTE EN GRUPOS DE TRABAJO.
Al concluir la explicación guiada por el docente, se dividirá al grupo en equipos de
trabajo máximo de 3 estudiantes. Los equipos se organizan en mesas de trabajo
para iniciar la práctica con su muestra respectiva.
El desarrollo de ésta parte de la práctica se realizará de la manera siguiente:
7ª PRÁCTICA. PROCEDIMIENTO
MATERIAL:
1 gradilla con 3 tubos
1 pipeta de 1 ml
1 micropipeta de 200L
EQUIPO:

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 78
1 baño maría a 37°C
1 Espectrofotómetro
REACTIVOS Y/O MUESTRAS:
Suero o plasma
Orina
Picrato alcalino
Kit de trabajo para determinación de urea
PROCEDIMIENTO:
En cada grupo del laboratorio serán seleccionados dos estudiantes, uno de los
cuales ingerirá los alimentos ricos en proteínas, y el otro los alimentos pobres en
proteínas, durante un mínimo de 4 días anteriores a la práctica. El último día de la
dieta se procederá a recolectar la orina de 24 horas.
• Alimentos sugeridos:
Alto contenido en proteínas: Bajo contenido en proteínas:
Leche y derivados Pastas y tortillas
Carne de res y aves Frutas y verduras
Pescados y mariscos Cereales y atoles
Huevo y leguminosas (lentejas, soya) Alimentos “chatarra”
DETERMINACIÓN DE UREA.
Se realizará la determinación de urea en suero sanguíneo y de orina de los sujetos
de estudio y llevar a cabo el siguiente procedimiento, considerando la muestra
como el suero o la orina.
Longittud de onda: 340 nm Cubeta: 1 cm de espesor Temperatura: 37°C

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 79
Medición: Frente a reactivo blanco
Pipetear en la cubeta:
Tubos Agua destilada Patrón Muestra Reactivo Blanco 10 µl ----- ----- 1000 µl Patrón ----- 10 µl ----- 1000 µl Muestra ----- ----- 10 µl 1000 µl
Mezclar, leer la absorbancia inicial al cabo de 30 segundos y empezar a cronometrar simultáneamente. Leer de nuevo al cabo de 1 minuto.
CALCULOS
Concentración de urea = A muestra X 13.3 mmol/l (80 mg/dL)
(mmol/l) A Patrón VALORES NORMALES Suero 1.7-8.3 mmol/l 10-50 mg/dL
3. DETERMINACIÓN DE CREATININA. La creatinina cuando reacciona con el picrato alcalino forma un complejo
coloreado cuya intensidad es directamente proporcional a su concentración.
• Utilice la dilución de orina (1:20).
• Prepare una serie de tubos de la siguiente manera:
TUBO (ml) Problema Estándar Blanco
Orina (1:20) 0.2 0.0 0.0
Estándar 0.0 0.2 0.0
Agua destilada 2.0 2.0 2.2
Picrato alcalino 1.0 1.0 1.0
• Deje reposar los tubos durante 15 minutos a temperatura ambiente.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 80
• Mida la absorbancia a 520 nm, ajustando a 0 con el tubo blanco.
RESULTADOS
Hacer los cálculos de las concentraciones de urea y creatinina, verificar si están en
los rangos normales.
C) . Tercera etapa de la práctica: APLICACIÓN DE LOS
CONOCIMIENTOS , HABILIDADES Y ACTITUDES ADQUIRIDOS EN LA
PRÁCTICA EN EL DESEMPEÑO PROFESIONAL Y REPORTE DE
LABORATORIO PARA LA SIGUIENTE SESIÓN.
Reporte de laboratorio para la próxima práctica de acuerdo al formato establecido:
6. SISTEMA DE EVALUACIÓN DE LA SÉPTIMA
PRÁCTICA
6.1 LINEAMIENTOS GENERALES PARA LA EVALUACIÓN
La evaluación será a través de los siguientes parámetros:
Actividades previas: Cálculos realizados previamente y diagrama de flujo de la
práctica realizados en su bitácora de practicas.
Reporte Escrito: El cual deberá tener la estructura descrita en el apartado: 5.1.
Lineamientos Generales para la Evaluación (pag 17)
Desempeño dentro del laboratorio.
Asistencia a las prácticas.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 81
6.2 MÉTODO DE ASIGNACIÓN DE CALIFICACIONES DE LA
SÉPTIMA PRÁCTICA
La calificación y ponderación de ésta séptima práctica es la siguiente:
ACTIVIDAD A CALIFICAR PONDERACIÓN
Actividades previas 10
Reporte Escrito. 50
Desempeño dentro del laboratorio. 30
Asistencia al laboratorio 10
7. BIBLIOGRAFÍA
Harper Bioquímica ilustrada, Robert K. Murray, Peter A. Mayes, Daryl K.
Granner y Victor. W. Rodwell; 28ª. ed, Ed. Mc Graw Hill ,2010.
Fundamentos de Bioquímica, Voet D., Voet JG., Pratt CW. 2ª. ed. Editorial
Médica Panamericana. 2007
Bioquímica, A. L. Lehninger, 3ª edición, Editorial Omega, S. A. 2001
Bioquímica: La base molecular de la vida. Trudy McKee y James R. McKee.
4ª ed., Ed. McGraw-Hill Interamericana. 2009
8. PARA SABER MÁS
Realizar una búsqueda bibliográfica o en internet sobre los resultados
obtenidos en la práctica realizada.
Responder las siguientes preguntas:
1. ¿En qué situaciones los aminoácidos son utilizados como combustible para el
hígado y el músculo?
2. Represente con fórmulas químicas el Ciclo de la Urea.
3. Explicar el por qué a ciertos organismos se les llama ureotélicos, uricotelicos y

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 82
amonotélicos, y ejemplifique cada uno de ellos
4. ¿Por qué la inanición eleva las concentraciones de las enzimas del ciclo de la
urea?
5. Escriba la ruta metabólica de síntesis de creatinina.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 83
UNIVERSIDAD JUÁREZ DEL ESTADO DE DURANGO
FACULTAD DE CIENCIAS QUÍMICAS
OCTAVA PRÁCTICA
INTEGRACIÓN DE CONOCIMIENTOS

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 84
1. NÚMERO DE ALUMNOS POR UNIDAD DE
PRÁCTICA
Para un buen desarrollo de la actividad académica se consideran equipos de 3
alumnos.
2. INTRODUCCIÓN DE LA OCTAVA PRÁCTICA
El diseño de experimentos que involucre a la bioquímica y la biotecnología en sus
diferentes áreas será el interés de esta práctica, es un reto para los alumnos, pues
ellos serán los encargados del diseñó, planeación y ejecución del experimento,
haciendo en todo momento la integración del conocimiento adquirido en el aula, no
solo de bioquímica sino del resto de sus asignaturas o bien mediante búsqueda de
información.
3. PROPÓSITO ESPECÍFICO DE LA OCTAVA
PRÁCTICA
3.1 CRITERIOS DE DESEMPEÑO
8ª PRÁCTICA:
EL ALUMNO SERÁ COMPETENTE PARA INTEGRAR SUS CONOCIMIENTOS
DEL CURSO DE BIOQUÍMICA APLICADA CUANDO:
Mediante el conocimiento adquirido en el curso de Bioquímica Aplicada diseñe un
experimento en el que pueda generar productos de procesos metabólicos.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 85
3.2 RESULTADO FINAL DE LA OCTAVA PRÁCTICA
El estudiante será capaz de diseñar un experimento que genere un producto
mediante procesos metabólicos y explicarlo.
4 NORMAS DE SEGURIDAD ESPECÍFICAS DE LA
PRÁCTICA
4.1 DETECCIÓN DE RIESGOS PARTICULARES DE LA OCTAVA
PRÁCTICA
Sin riesgo particular, seguir las normas generales de seguridad.
4.2. DISPOSICIÓN DE DESECHOS
Los desechos deben confinarse en recipientes para disponer de ellos
posteriormente.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 86
5. DESARROLLO DE LA OCTAVA PRÁCTICA
El desarrollo de la octava práctica será manejado en 3 etapas.
ACTIVIDADES
TIEMPO
REQUERIDO
RESULTADO DE LA
ACTIVIDAD
A) Actividad guiada por el
docente responsable de la
práctica
20
min.
El docente realizará una
explicación de la metodología de
la práctica.
B) Parte experimental
realizada por los equipos
de estudiantes
El tiempo será
establecido según el
protocolo diseñado
por los alumnos.
Puede llevar varios
días.
Cada equipo desarrollará el
proceso establecido en el diseño
de su experimento
C) Aplicación de la
práctica en el desempeño
profesional
Final de la práctica
30 min
Reporte de laboratorio para la
siguiente sesión.
A) Primera etapa de la práctica: PRÁCTICA DIRIGIDA POR EL DOCENTE
RESPONSABLE DE LA PRÁCTICA:
En ésta etapa el docente explicará la metodología de la práctica.
B) Segunda etapa de la práctica: ACTIVIDAD REALIZADA POR EL
ESTUDIANTE EN GRUPOS DE TRABAJO.
Al concluir la explicación guiada por el docente, se asignará el tema a desarrollar
por cada equipo y se les indicará el desarrollo de la práctica de acuerdo al siguiente
procedimiento:

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 87
8ª PRÁCTICA: PROCEDIMIENTO
Los alumnos diseñarán un experimento para generar un producto en alguno de los
siguientes temas (que puede ser por sorteo o por asignación).
TEMA EQUIPO
1. BIOTECNOLOGÍA EN LOS
ALIMENTOS
2. BIOTECNOLOGÍA EN BEBIDAS
3. BIOTECNOLOGÍA COSMÉTICA
4. BIOTECNOLOGÍA DE
DETERGENTES
5. BIOTECNOLOGÍA AGRÍCOLA
6. BIOTECNOLOGÍA EN LA
MEDICINA
Estos son los puntos a desarrollar para sus temas
1. Qué composición química tiene la materia prima a utilizar para la obtención
de su producto
2. Qué microorganismo o microorganismos va a emplear, describa brevemente.
3. Cuáles son las condiciones óptimas bajo las cuales se va ha generar su
producto
4. Qué sucede si se alteran condiciones como temperatura, pH,
concentraciones de sustrato, etc.
5. Cuál es el sustrato inicial del microorganismo y qué tipo de biomolécula es
(carbohidrato, proteína o lípidos). Dependiendo del proceso puede o no
aplicar este punto.
6. Integre en un esquema general todas las vías metabólicas (desarrolladas)
que Usted considere va a transitar el microorganismo, para poder generar el
producto, indique si existirá algún tipo de control o regulación.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 88
7. Planteé un supuesto donde pueda manipular la actividad del microorganismo
con diversas condiciones, materias primas diferentes, o incluso alteraciones
genéticas, para generar un producto diferente de interés para la comunidad.
Para este punto considere que cuenta con todo lo necesario en el laboratorio
para poder lograrlo, es algo hipotético pero fundamente su supuesto.
8. Bibliografía consultada.
RESULTADOS
C) Tercera etapa de la práctica: APLICACIÓN DE LOS CONOCIMIENTOS
, HABILIDADES Y ACTITUDES ADQUIRIDOS EN LA PRÁCTICA EN EL
DESEMPEÑO PROFESIONAL Y REPORTE DE LABORATORIO PARA
LA SIGUIENTE SESIÓN.
Reporte de laboratorio para la próxima práctica de acuerdo al formato establecido:
6. SISTEMA DE EVALUACIÓN DE LA OCTAVA
PRÁCTICA
6.1 LINEAMIENTOS GENERALES PARA LA EVALUACIÓN
La evaluación será a través de los siguientes parámetros:
Se hará un rol de exposiciones por equipo en las que se podrá usar
presentaciones de Power Point, todos los integrantes del equipo deberán
participar y se evaluará esta intervención de manera individual. Se hará especial
énfasis en la exposición de las rutas metabólicas involucradas en el proceso de
su experimento. Se les hará cuestionamiento de su trabajo. Además el trabajo
se entregará por escrito la extensión del mismo serán 6 cuartillas mínimo y 12
máximas, letra arial 11 a espacio y medio con margen normal. Si el esquema
del punto 6 se les complica hacerlo electrónico, lo pueden elaborar manuscrito.

MANUAL DE PRÁCTICAS DE BIOQUÍMICA APLICADA
FACULTAD DE CIENCIAS QUÍMICAS UJED MANUELA DE LA A. CARRERA GRACIA
Página 89
6.2 MÉTODO DE ASIGNACIÓN DE CALIFICACIONES DE LA
OCTAVA PRÁCTICA
La calificación y ponderación de ésta octava práctica es la siguiente:
ACTIVIDAD A CALIFICAR PONDERACIÓN
Actividades previas 15
Reporte Escrito. 40
Desempeño dentro del laboratorio. 35
Asistencia al laboratorio 10
7. BIBLIOGRAFÍA
Harper Bioquímica ilustrada, Robert K. Murray, Peter A. Mayes, Daryl K.
Granner y Victor. W. Rodwell; 28ª. ed, Ed. Mc Graw Hill ,2010.
Fundamentos de Bioquímica, Voet D., Voet JG., Pratt CW. 2ª. ed. Editorial
Médica Panamericana. 2007
Bioquímica, A. L. Lehninger, 3ª edición, Editorial Omega, S. A. 2001
Bioquímica: La base molecular de la vida. Trudy McKee y James R. McKee.
4ª ed., Ed. McGraw-Hill Interamericana. 2009
8. PARA SABER MÁS
Realizar una búsqueda bibliográfica o en internet sobre la biotecnología en
las siguientes áreas. Alimentos, cosmética, detergentes, agrícola, medicina,
etc.






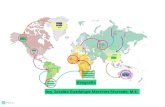
![Encuadre ..[1]](https://static.fdocuments.ec/doc/165x107/5597a7511a28abbc7a8b463c/encuadre-1-559c158b03646.jpg)