01 inflamacion
-
Upload
belen-guzman -
Category
Health & Medicine
-
view
158 -
download
3
Transcript of 01 inflamacion
INFLAMACIÓN
Respuesta fisiológica localizada, dinámica y protectora de los tejidos vascularizados frente a un daño (trauma, infecciones, etc.)
Su objetivo es localizar y aislar el agente agresor, para eliminarlo y reparar el daño producido
Participan:
Mediadores solubles
Componentes celulares
Causas más comunes de inflamación
Trauma Tisular leve (torcedura, contusiones)
Fractura
Cuerpo extraño (sutura)
Enfermedad autoinmune (artritis reumatoidea)
Agentes microbianos (bacterias)
Agentes químicos (ácidos)
Agentes térmicos (quemaduras con fuego o hielo)
Irradiación (UV o radiación)
Reparación de tejidos
Inflamación
Proliferación
Maduración
Prepara la zona para la reparación
Reconstruye y refuerza la zona dañada
Modifica el tejido a su forma madura
Reparación de tejidos
Inflamación
Proliferación
Maduración
1 5 10 15 20 25 30 35 40
Días desde el momento de la lesión
1-6
3-20
9 días-2 años
INFLAMACIÓN AGUDA
Calor
Tumor
Rubor
Dolor
Hiperhemia y vasodilatación
Edema
Presión y mediadores químicos
sobre terminaciones nerviosas
Impotencia
funcional Todos los anteriores
Involucra eventos superpuestos que incluyen procesos vasculares, homeostáticos, celulares e
inmunes.
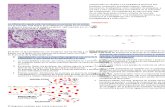
Fase de Inflamación (días 1-3)
Respuesta Vascular • Vasoconstricción transitoria (minimiza la pérdida de sangre - duración de 5 a 10 min-noradrenalina).
• Vasodilatación de Capilares cercanos a la lesión. •La permeabilidad capilar también aumenta debido a la lesión de las paredes capilares y a sustancias químicas liberadas por los tejidos lesionados (se prolonga por mas de 1 hr tras el daño tisular).
Fase de Inflamación (días 1-3)
histamina,
factor hageman, bradiquinina,
prostaglandinas y
fracciones complementarias.
Edema
Acumulación de liquido fuera de los vasos
sanguíneos (espacio extravascular y tejido
intersticiales).
Transudado: casi sin células
ni proteínas
Exudado: con células y proteínas Exudado + Leucocitos = Pus
Electrolitos y agua
Edema = Pº hidrostática capilar + Pº osmótica intersticial +
permeabilidad de los vasos.
Respuesta Hemostática Controla la pérdida de sangre cuando los vasos están dañados o rotos.
Fase de Inflamación (días 1-3)
Fase de Inflamación (días 1-3)
Respuesta Celular
Futuros macrófagos**
Liberan Histamina
Fagocitosis
Transporte de O2
Fagocitosis
Sangre
Plaquetas
Leucocitos
Eritrocitos
Respuesta Celular • Neutrófilos - Limpian la zona para iniciar reparación (fagocitosis)
- Predominan en esta fase (Permanecen en la lesión por solo 24 horas) - Liberan factores quimiotácticos que atraen a otros leucocitos • Macrófagos: - Muy importantes (producen gran cantidad de mediadores químicos que cumplen un rol importante en la fagocitosis y atracción de fibroblastos).
Fase de Inflamación (días 1-3)
Fase de Inflamación (días 1-3)
Respuesta Inmune
Macrófagos: presentan antígenos extraños a los
linfocitos T para activarlos.
Sistema del Complemento: serie de proteínas
plasmáticas enzimáticas que se activan por:
vía clásica (complejo antígeno-anticuerpo)
vía alternativa (sustancias microbianas y celulares)
Aumentan permeabilidad vascular
Estimulan fagocitosis
Estímulo quimiotáctico para leucocitos
MEDIADORES MOLECULARES DE LA
RESPUESTA INFLAMATORIA AGUDA
Mediadores lipídicos
Proteasas plasmáticas
Péptidos y aminas
Óxido nítrico
Citoquinas proinflamatorias
Sistema del complemento
Cininas
Proteínas de la coagulación
RESOLUCIÓN RESPUESTA
INFLAMATORIA AGUDA
Apoptosis de células senescentes
Apoptosis o muerte celular programada
Apoptosis de neutrófilos puede ser regulada por
algunas citoquinas: TNF-α, IL-10, etc.
Mediadores antiinflamatorios:
IL – 4
Transforming Growth Factor – β (TGF – β)
IL – 10
IL – 13
IL – 6
RESOLUCIÓN RESPUESTA
INFLAMATORIA AGUDA
Eje hipotálamo hipófisis suprarrenal
Glucocorticoides suprarrenales son
inmunosupresores y antiinflamatorios y pueden
suprimir la respuesta inflamatoria
Interleuquinas y prostaglandinas estimulan
hipotálamo
↑ ACTH
↑ cortisol
RESOLUCIÓN RESPUESTA
INFLAMATORIA AGUDA
• Objetivo: cubrir y dar fuerza y consistencia al sitio de la lesión.
• Consta de cuatro procesos :
1. Epitelización 2. producción de colágeno 3. contractura de la herida y 4. neovascularización.
Fase Proliferativa (días 3-21)
Epitelización
Es el restablecimiento de la epidermis.
Entrega una barrera protectora para prevenir la pérdida de agua, electrolitos y disminuir el riesgo de infección.
Las células epiteliales no dañadas de los márgenes de la lesión, se reproducen y migran al área dañada cubriendo la superficie de la herida y cerrando el defecto.
Fase Proliferativa (días 3-21)
Fibroplasia
Fibroblastos producen colágeno en el tejido conectivo
Fase Proliferativa (días 3-21)
Fibroblastos
Fibrillas de
colágeno
Procolágeno
Troprocolágeno
Fibras de
colágeno
Filamentos de
colágeno
Tejido de granulación
Colágeno tipo 3 (día 12)
Colágeno tipo 1 (producción máx. día
21)
Consistencia del
tejido sólo 20%
Contracción de la herida Tira los bordes de la lesión para unirlos.
Un anillo de miofibroblastos envuelve los
márgenes de la herida para comenzar la contracción y posteriormente el cierre.
Si la contracción de la herida se hace incontrolable se formará una contractura (tejido muy resistente y de poca elongación).
Durante la cicatrización, la principal intención es evitar las contracturas.
En este proceso la cicatriz aparece roja debido al incremento de la vascularización, fluidos, inervación y relativa inmadurez del tejido.
Cicatrización por
1º intención
Cicatrización por
2º intención
Fase Proliferativa (días 3-21)
Neovascularización
Angiogenesis: desarrollo de nuevos vasos
sanguíneos en el área dañada.
Entregar oxígeno y nutrientesa la zona lesionada.
La cicatrización no podría producirse sin
angiogenesis.
3 mecanismos:
Fase Proliferativa (días 3-21)
Generación de nueva red vascular
Anastomosis de vasos preexistentes
Acoplamiento de vasos en la zona lesionada
• Ocurren cambios en el tamaño, forma y tensión del tejido cicatrizal.
• Es la etapa la mas larga
• La cicatriz se vuelve blanquecina a medida que el colágeno madura y que la vascularización disminuye.
• El objetivo de ésta fase es la restauración de la función primaria del tejido lesionado.
• Durante toda la fase de maduración, la síntesis y lisis del colágeno ocurren de manera balanceada.
• Durante esta fase, el colágeno sintetizado y depositado es predominantemente de tipo 1.
• Como el colágeno de tipo 1 es más fuerte que el colágeno tipo 3 depositado en la etapa proliferativa, la fuerza tensil aumenta.
Fase de Maduración (días 9 en adelante)
•Si el grado de producción de colágeno es mayor que la lisis, se puede producir una cicatriz queloidea o hipertrófica. • Queloides: se extienden mas allá del límite original de una lesión e invaden el tejido circundante • Cicatriz hipertrófica: a pesar de crecer, permanece dentro de los márgenes de la herida original.
Fase de Maduración (días 9 en adelante)
Inflamación Crónica
La inflamación crónica puede responder a dos razones :
1. Persistencia de un agente dañino o alguna otra interferencia con
el proceso normal de cicatrización.
2. Respuesta inmune a algún material extraño o a un tejido huésped
alterado (implantes o suturas) o como respuesta a una
enfermedad autoinmune (AR).
El proceso normal de inflamación
aguda no debe durar mas de dos
semanas.
Si continúa luego de dos semanas,
se le conoce como inflamación
subaguda.
La inflamación se torna crónica
después de meses o años.
Inflamación Crónica
Factores que afectan el proceso de
Reparación
Locales
Tipo, tamaño y
localización de la
lesión
Infección (
producción y lisis de
colágeno)
Aporte vascular
Fuerzas externas
Movimiento
Agentes físicos
Sistémicos
Edad
Enfermedad
Medicamentos
Nutrición
LESIÓN INF. AGUDA PROLIFERACIÓN MADURACIÓN
vasoconstricció
n
vasodilatación
coagulación
fagocitsis
epitelización
fibroplasia
Contr. herida
neovascularizaci
ón
Balance entre
producción y
lisis de colágeno
Orientación de
fibras de
colágeno
LESIÓN
REPARADA
CARTÍLAGO Limitada capacidad para reparar
(carece de vasos sanguíneos, linfáticos
y nervios).
Reacciona diferente cuando:
se lesiona sólo
se lesiona junto al hueso subcondral en el cual se inserta.**
El cartílago por si sólo, es incapaz de formar un coágulo
(limitada capacidad de inducir cicatrización).
Predispuesto a la degeneración por menor contenido de
proteoglicanos
CARTÍLAGO
• En lesiones de cartílago articular +
hueso subcondral, la
vascularización del hueso
subcondral permite una mejor
reparación.
• Un cartílago de apariencia normal
puede verse en dos meses a partir
de la lesión.
• Células madre
TENDONES Y LIGAMENTOS
Los tendones y ligamentos pasan por etapas similares de
curación.
La reparación final depende de varios factores:
Tipo de tendón
Extensión del daño de la vaina tendinoso
Aporte vascular
Duración de la inmovilización
TENDONES Y LIGAMENTOS
Las primeras dos etapas de la cicatrización tendinosa, inflamación y
proliferación, son similares a otros tejidos. La tercera fase, maduración de la cicatriz es única para los tendones
ya que puede ejecutar un estado de reparación cercano a la
regeneración.
El 10º día, las fibras de colágeno comienzan a alinearse
paralelamente, a los 2 meses comienza la transición del
alineamiento, a través de la remodelación y reorientación.
La maduración final del tejido ocurre con carga fisiológica.
MUSCULOESQUELÉTICO
Los músculos pueden lesionarse por:
Trauma (provocando contusión)
Contracción violenta o excesiva tensión
(desgarro)
Enfermedad muscular degenerativa (distrofia)
Células madre
(reserva)
Miositis
Oscificante
HUESO
El hueso es un tejido especializado que está
posibilitado de sanarse a si mismo con su propio
tejido.
Hueso
El hueso pasa por cuatro etapas histológicas en
el proceso de cicatrización:
1. Inflamación: se inicia inmediatamente después
del impacto.
2. Callo débil: se inicia cuando el dolor y el edema
desaparecen. ( vascularización y proliferación
celular)
3. Callo Duro: de 3 semanas a 4 meses. Período de
consolidación clínica y Rx de la Fx.
4. Remodelación del Hueso: puede demorar meses
o años en finalizar. Hueso con disposición
normal.